妊娠期糖尿病合并亚临床甲状腺功能减退的临床特点及妊娠结局研究
2021-09-22朱明慧王婵妮
朱明慧,陈 烨,王婵妮
(广州市番禺区中心医院妇产科,广东 广州 511400)
妊娠期糖尿病(gestational diabetes mellitus,GDM)和亚临床甲状腺功能减退症(subclinical hypothyrodism,SCH)是妊娠期常见的疾病。妊娠期妇女常处于高糖和高代谢负荷状态,可引起糖耐量异常,出现孕妇胰岛素抵抗和甲功紊乱,导致孕妇SCH发生风险增加,主要是通过促进下丘脑促甲状腺激素释放激素的分泌,影响外周血中T4向T3转化[1~3]。目前关于GDM合并SCH的临床特点研究不少,而GDM合并SCH是否加重不良妊娠结局风险及影响因素尚不十分清晰。因此,本研究拟进一步探讨GDM合并SCH的临床特点及妊娠结局,以期为临床治疗该病提供有力的证据。
1 资料与方法
1.1 一般资料选取2017年1月至2019年6月在我院定期产检并分娩的单胎妊娠孕妇GDM患者200例,GDM诊断标准[4]:在孕24~28周及28周后首次行葡萄糖糖耐量试验(oral glucose tolerance test,OGTT),空腹血糖(fasting plasma glucose,FPG)≥5.1 mmol/L、餐后1 h血糖(1 hPBG)≥10.0 mmol/L或餐后2 h血糖(2 hPBG)≥8.5 mmol/L,其中任何一项或多项异常超过正常范围;SCH的诊断标准,血清促甲状腺激素(TSH)≥4 mU/L,游离甲状腺素(FT4)正常范围。入选标准:单胎妊娠,≥18岁,资料齐全配合检查患者。排除标准:存在肝肾肺功能损害、感染性疾病、代谢性疾病史患者、多胎妊娠患者。根据甲状腺功能水平将GDM患者分为单纯GDM患者150例(GDM未合并SCH组)和GDM合并SCH患者50例(GDM合并SCH组),同时选择同期正常健康孕妇150例(NC组)。
1.2 方法及观察指标收集所有孕妇的临床资料,包括年龄、孕前体重指数(BMI)、分娩孕周,口服OGTT、入院即刻血糖、FPG、2 hPBG、糖化血红蛋白(HbA1c)、血脂、白细胞计数(WBC)、红细胞(RBC)、血红蛋白(Hb)、胆固醇(CHO)、甘油三酯(TG)、血小板(PLT)、谷丙转氨酶(ALT)、谷草转氨酶(AST)、尿素氮(BUN)和血肌酐(Scr),甲状腺素水平,包括游离三碘甲状腺原氨酸(FT3)、FT4和TSH,妊娠结局 [新生儿情况、胎膜早破、早产(28周~37周)、死胎、产后出血、感染]。
1.3 统计学方法应用SPSS 21.0统计学软件进行数据分析。计量的资料以均数±标准差表示,多组间比较采用方差分析,组间比较采用LSD法;计数资料以例数(百分比)表示,组间比较采用卡方检验或Fisher精确概率法;采用Logistic回归分析GDM合并SCH患者不良妊娠结局的影响因素。P<0.05为差异有统计学意义。
2 结果
2.1 各组孕妇临床指标、生化指标及甲状腺素比较
与NC组和GDM未合并SCH组比较,GDM合并SCH组患者分娩孕周明显下降,即刻血糖、FBG、2 hPBG、HbA1c、TG、TSH明显升高(P<0.05);各组间在年龄、2 hPBG、WBC、RBC、Hb、PLT、ALT、AST、BUN、SCr、FT3、FT4方面差异无统计学意义(P>0.05),见表1。

表1 各组间临床、生化指标及甲状腺素比较
2.2 不良妊娠结局比较与NC组和GDM未合并SCH组比较,GDM合并SCH组患者胎膜早破、早产、总体不良妊娠结局患者明显增高(P<0.05);两组在死胎、胎儿窘迫、低体重儿方面差异无统计学意义(P>0.05),见表2。

表2 GDM未合并SCH组和GDM合并SCH组不良妊娠结局比较 [n(%)]
2.3 不良妊娠结局多因素Logistic回归分析分娩孕周<35周、HbA1c>6.5%和TSH>5.0 mIU/L是GDM合并SCH患者不良妊娠结局的独立危险因素(P<0.05),见表3。
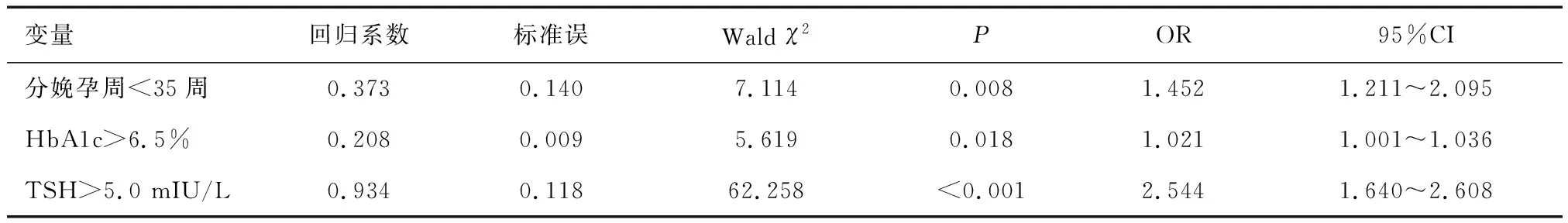
表3 GDM合并SCH患者不良妊娠结局的Logistic回归分析
3 讨论
在全球及我国范围内,GDM的患病率分别为7%和13%左右,妊娠期SCH患病率分别为2%~3%和10%左右,GDM合并SCH在孕妇中患病率可达4.8%~31.4%[3,5]。研究表明,GDM孕妇较非GDM孕妇发生SCH风险明显增加了30%[2,6]。在本研究中,与非GDM孕妇和GDM未合并SCH组比较,GDM患者分娩孕周明显下降,血糖及甲功相关指标明显升高,可能由于孕妇激素水平变化和高代谢状态,更易出现糖耐量异常[7]。外周组织对葡萄糖的利用减少,糖原合成及糖氧化分解增加,同时胰岛素抵抗明显增加,可造成代谢紊乱,引起下丘脑瘦素、葡萄糖转运体4及游离脂肪酸调节障碍有关,主要通过影响下丘脑-垂体-甲状腺素通路而影响甲功能,引起TG和TSH水平升高[5,6]。
既往研究表明,GDM可导致羊水过多或过少、高血压、流产、产后出血、感染、早产及新生儿功能发育迟缓、巨大儿及畸形、血糖异常、呼吸窘迫等不良妊娠结局[7]。而GDM合并SCH患者可导致流产、早产、胎膜早破、低体重儿、胎儿发育迟缓及畸形、贫血及微血管病变等不良妊娠结局[5,6,9,10]。在本研究中,与GMD患者相比,合并SCH的GMD患者出现胎膜早破、早产、产后出血和感染等不良妊娠结局明显增加,考虑可能是血糖异常能够诱发异常氧化应激反应、活性氧水平及自噬功能增强,与滋养细胞的分化相关基因表达下降有关[10]。
本研究还发现分娩孕周<35周、HbA1c>6.5%和TSH>5.0 mIU/L是GDM合并SCH患者不良妊娠结局的独立危险因素,表明分娩孕周越早,影响胎儿成熟度,血糖水平的增高更易体内代谢紊乱,会导致流产、早产、胎膜早破和产后感染等发生率明显增加[11,12]。另外,甲状腺激素的功能主要与调节新陈代谢、胎盘的发育和成熟功能、胎儿的生长、发育及分娩相关的神经肽表达有关[1,6]。甲状腺激素在糖脂代谢中亦发挥了重要作用,主要是通过影响血糖代谢及胰岛素的分泌,更易产生胰岛素抵抗。因此,SCH水平易影响胎儿的智力等神经系统发育,进一步增加甚至加重孕妇的血糖异常,通过影响下丘脑TSH的释放促进外周组织T4转为T3,进而触发一系列不良妊娠结局的发生。总之,本研究进一步探讨了GDM合并SCH患者是否更易产生不良妊娠结局及相关危险因素的分析,对于这类患者应严格控制血糖及L-T4替代治疗,对改善妊娠结局具有重要意义。
综上,GDM合并SCH患者的血糖水平明显升高,不良妊娠结局发生率明显增多,且孕周、HbA1c和TSH水平是GDM合并SCH患者不良妊娠结局的独立危险因素。在临床上,有效管理糖尿病及甲减患者,可减少不良妊娠结局的发生。因此,需对GDM患者进行持续血糖和甲功监测,以期筛选、预防和延缓此类疾病的发生发展。另外,今后需进一步扩大样本量研究及亚组分析,GDM合并SCH患者发生妊娠不良风险结局是否随着血糖异常程度增加而增多,以及探讨GDM合并SCH的不良妊娠结局的具体发病机制。
