术前CTA精准定位胫后动脉穿支皮瓣修复手部创面的应用研究
2021-09-14宗海洋蔡芝军徐永清
宗海洋,王 腾,李 阳,王 静,蔡芝军,林 玮,徐永清
中国人民解放军联勤保障部队第九二〇医院骨科,昆明 650032
手部皮肤缺损常伴有肌腱、骨外露,具有创伤严重、创面复杂,修复困难、易残留功能障碍等特点,常需要皮瓣修复[1]。胫后动脉穿支皮瓣因其不损伤主干血管、血供可靠、供区损伤小的特点,在临床上常用于修复四肢创面[2]。但胫后动脉穿支血管解剖存在变异[3],常规切取方法有一定的失败率。术前皮瓣穿支的精准定位,利于皮瓣的术前设计,可提高皮瓣切取成功率。常用的术前穿支血管定位技术包括手持多普勒、彩色多普勒、磁共振血管成像(magnetic resonance angiography,MRA)、数字减影血管造影(digital subtraction angiography,DSA)、计算机断层扫描血管造影(computed tomography angiography,CTA)等,手持多普勒和彩色多普勒依赖于检查者的经验,特异性低;MRA检查时间长,患者体内有金属植入物对MRA检查结果有干扰,且对小血管的显影效果较CTA差;DSA为有创检查,CTA是目前较为理想的穿支定位技术[4]。本文回顾性分析2017年3月—2019年6月中国人民解放军联勤保障部队第九二〇医院骨科收治的8例手部软组织缺损患者临床资料,以术前下肢CTA观测结果定位胫后动脉穿支,设计胫后动脉穿支皮瓣修复手部创面,效果良好。
临床资料
1 临床资料
纳入标准:(1)18~60岁; (2)术前完善下肢血管CTA检查; (3)手部创面为单一创面伴有深部组织外露。排除标准:(1)下肢血管疾病,如脉管炎、动脉硬化性闭塞、下肢静脉曲张; (2)有麻醉禁忌证或手术禁忌证; (3)无肌腱、血管神经组织外露,可行植皮治疗; (4)肿瘤创面伴局部放疗病史。
本组共8例患者,男性6例,女性2例,年龄20~55岁,平均35.6岁。致伤原因:机器绞伤4例,切割伤3例,电击伤1例。皮肤缺损部位:手背3例,手掌2例,虎口1例,拇指指背1例,中指指背1例。右手5例,左手3例。伴有肌腱损伤4例,掌骨骨折3例。受伤至手术时间7~25d,平均12.5d。皮瓣切取面积2cm×4cm~6cm×10cm。本研究通过笔者医院医学伦理委员会审批[2019-068(科)-01]。
2 术前CTA观测
所有患者术前行下肢血管CTA 检查,以CTA扫描的横断面逐层观察胫后动脉穿支,追踪穿支自胫后动脉发出部位、走形路径,穿支的浅出点,并测量穿支点距内踝的距离。
3 手术方法
受区创面处理:根据术前创面微生物培养及药敏选择敏感抗生素,术中彻底清除感染及坏死组织,肌腱缺损待皮瓣愈合后二期重建,骨折行克氏针固定或接骨板内固定。分离受区动脉及静脉,显微缝线标记。
皮瓣设计、切取及吻合:按照点、线、面的原则,以术前CTA测量的穿支血管穿出点为中心,以胫骨内侧平台后缘与内踝-跟腱中点连线为轴线,根据创面的形状及大小,将创面拓于穿支点周围,设计的皮瓣比创面宽0.5~1cm,下肢不驱血止血带直接充气,先切开皮瓣前缘至深筋膜层,将深筋膜连同皮缘向后掀开,寻找肌间隙穿出的穿支血管,再次根据皮瓣穿支点二次设计皮瓣,于皮瓣后缘切开皮肤、皮下组织及深筋膜,逐步游离皮瓣,结扎穿支血管的骨膜、肌肉分支,游离皮瓣血管蒂,追踪血管蒂至胫后动静脉,气囊止血带放气,确认皮瓣血运良好,于胫后动静脉发出部位结扎穿支血管,保留胫后动、静脉的完整性。将皮瓣移植至手部创面,临时缝合固定皮瓣边缘,显微镜下将皮瓣动脉与受区指动脉或桡动脉腕背支吻合,皮瓣静脉与头静脉或手背静脉吻合。供区处理: 6例直接缝合,2例植皮。
4 术后处理
术后石膏托固定患肢于功能位,1周内常规应用肝素抗凝、罂粟碱解痉、抗生素预防感染等治疗,给予烤灯保暖,常规换药,严密观察皮瓣血运。术后2周,皮瓣成活后拆除皮肤缝线及石膏托,指导患者行手部功能锻炼。
结 果
1 CTA观测结果
下肢CTA横断面观测胫后动脉自比目鱼肌与趾长屈肌间隙发出穿支,穿支浅出点位于小腿内侧。每例患者CTA单侧下肢可观测到胫后动脉皮穿支3~5支,平均左侧3.3支,右侧3.9支。以内踝为标记,测量穿支距内踝的距离,结果见表1。
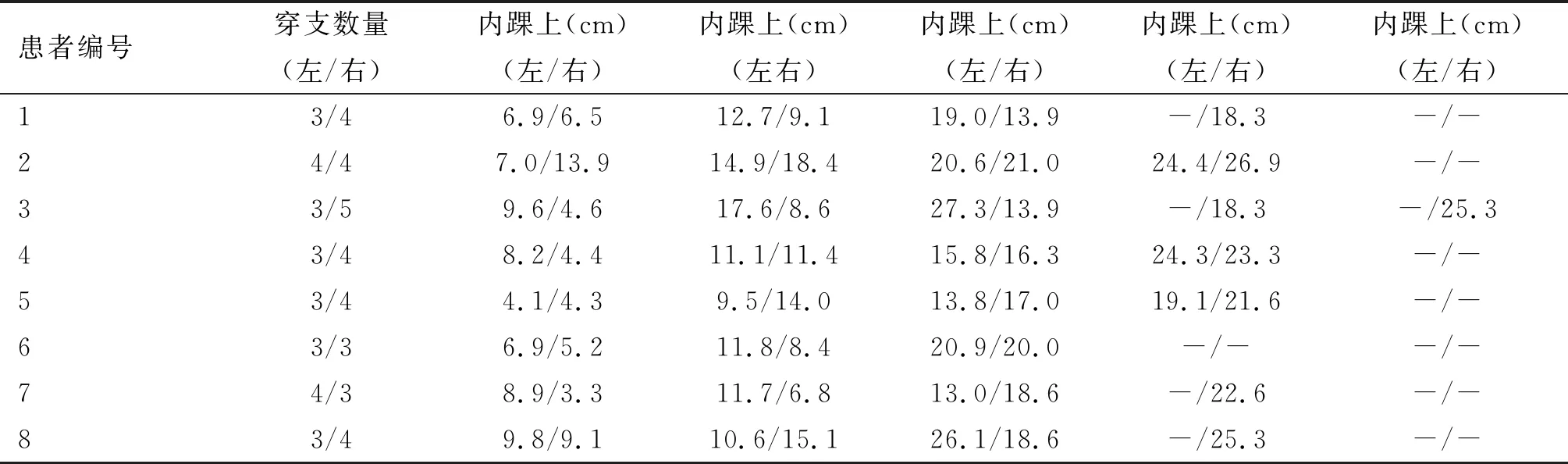
表1 8例患者术前双下肢CTA观测结果
2 临床效果
8例皮瓣完全成活,1例皮瓣边缘感染,经换药及抗感染治疗后顺利愈合,2例患者术后3个月重建伸指肌腱,1例患者术后2个月重建屈指肌腱。患者均获得随访,随访时间6~18个月,皮瓣质地柔软,无瘢痕挛缩,外观良好,以总主动活动度(total active motion,TAM)法评定手功能评分,优6例,良2例,供区均顺利愈合,所有患者对外观及功能满意。典型病例见图1。
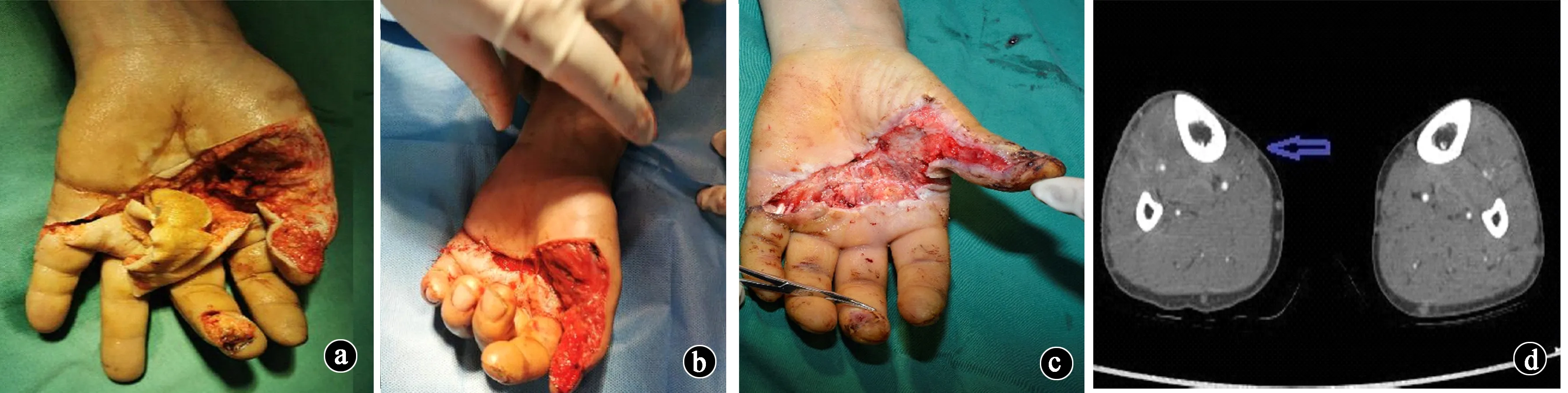
图1 患者男性,53岁,左手掌及拇指、中指尺侧被锐器切割致伤。a.环指、小指指总动脉、指总神经损伤、屈指肌腱3区断裂,环指、小指血运差,中指指腹皮肤缺损,创面污染严重; b.急诊行手部彻底清创,修复屈指肌腱、指总动脉及指总神经,因手掌皮肤脱套,肌腱、血管、神经外露,将手掌屈曲位缝合,部分封闭手掌创面; c.拇指创面油纱布覆盖,经术后抗感染、抗凝及解痉、换药等对症支持治疗,术后2周手掌创面部分坏死伴感染,手指成活。二次手术清创后手掌创面缺损约4cm×8cm; d.术前CTA定位右下肢胫后动脉穿支; e.按照术前设计切取皮瓣,穿支动脉与示指桡侧动脉吻合,伴行静脉与掌背静脉吻合,拇指皮肤缺损取大腿中厚皮片移植。术后抗感染、抗凝、解痉、保暖等对症支持治疗,皮瓣存活; f.术后8个月,皮瓣外形及手功能良好; g.供区仅为线性瘢痕
讨 论
解剖发现胫后动脉平均穿支为(4.17±0.94)支,血管蒂长度1.06~4.87cm,血管直径0.63~1.48mm,在小腿上、中、下段各有1个恒定的穿支发出[5]。邝艺臻等[3]研究发现,胫后动脉90%的穿支浅出点位于内踝上5~26cm,平均有4.8支肌间隙穿支,主要分布在小腿中下段,有3支位置恒定,分别位于内踝上(6.7±1.1)、(15.8±1.8)、(22.6±1.7)cm处。笔者研究发现,术前CTA观察到的胫后动脉皮穿支平均数量为:左侧3.3支,右侧3.9支,穿支大多分布于内踝上4~10cm、11~16cm和18~23cm的位置,与上述研究结果基本一致。CTA 可识别直径0.3~0.5mm以上的穿支血管,CTA识别的穿支,管径可满足显微吻合的要求。本组病例中,术前CTA影像中识别的穿支血管,术中解剖观察均与术前定位一致,且皮瓣均顺利切取,表明CTA识别穿支血管的准确率较高。
选取胫后动脉穿支皮瓣游离移植修复创面,需明确穿支血管蒂长度、穿支位置及直径,为血管吻合做充分准备。术前CTA检查可准确追踪穿支血管于主干血管的起始部位,判断血管蒂长度,计算出穿支浅出点位置,大致判断穿支血管直径[6]。笔者利用术前下肢血管CTA观测穿支血管大致直径、穿支走形及血管蒂长度,选取合适的穿支,以此设计胫后动脉穿支皮瓣,术中均顺利切取,术后皮瓣完全成活。表明术前CTA观测结果准确性高,可用于指导游离胫后动脉穿支皮瓣的设计和切取。但CTA有一定的缺点,如患者会暴露于一定剂量的电离辐射,造影剂有渗漏风险,且可能导致过敏、肾损伤[7-8]。
临床上常用的股前外侧穿支皮瓣、腹壁下动脉穿支皮瓣、旋髂浅动脉穿支皮瓣修复手部创面,因皮瓣角质层及皮下脂肪较厚,修复后手部外观臃肿,或需要在切取皮瓣时行显微削薄,延长了手术时间,皮瓣血运障碍风险增大,或需要在皮瓣成活后多次修整,增加了治疗周期和费用。而局部带蒂转移皮瓣因供区不美观、面积较小等原因限制了其应用。小腿皮瓣因角质层及皮下脂肪层较薄,易于切取,移植至手部外形不臃肿,目前在手部创面中的应用广泛[9-10]。常用的小腿游离皮瓣有腓动脉穿支皮瓣、胫前动脉穿支皮瓣,腓肠外侧浅动脉穿支皮瓣、胫后动脉穿支皮瓣等[11-12]。笔者运用CTA定位胫后动脉穿支皮瓣修复手部创面,主要优点包括:(1)不携主干血管,不影响下肢血供,术前CTA检查可了解下肢血管解剖变异,即使在胫前动脉或腓动脉缺如时仍可应用; (2)术前CTA 精准定位皮瓣穿支,指导皮瓣设计,定位准确,切取成功率高; (3)皮瓣厚度适中,修复手部创面后外观不臃肿,外形比较满意; (4)麻醉状态下,仰卧位下肢自然外旋,皮瓣切取方便,切取及吻合皮瓣不需变换体位; (5)可携带隐神经分支重建受区感觉。缺点有:(1)血管蒂较短,设计皮瓣时需结合穿支血管蒂长度和受区血管的位置和长度,精确设计皮瓣; (2)穿支血管较细,对显微吻合技术要求高。
综上所述,应用胫后动脉穿支皮瓣修复手部创面,具有供区损伤小、皮瓣切取方便、受区外形美观的优点。CTA对胫后动脉穿支血管识别率高,定位准确,术前以CTA检查精准定位胫后动脉穿支,利于术中皮瓣切取,是切取皮瓣较为理想的术前检查。
