化学深度学习的问题驱动创设与实施
2021-09-10邓优华


【摘 要】通过实验探究浓度、温度、压强对平衡移动的影响,利用层层递进的十二个问题,引导学生进行思考和自主学习,探索指向化学学科核心素养的培养。具有探究、体验的深度学习课堂,构建了宏—微—符—曲线的四重表征,较好地解决了它们之间的自由转换。
【关键词】问题情境;深度学习;手持技术;问题驱动
深度学习就是指在教师引领下,学生围绕着具有挑战性的学习主题,全身心积极参与、体验成功、获得发展的有意义的学习过程。深度学习教学研究项目以及深度学习教学实践的理论价值,不仅在于克服机械学习、浅层学习的弊端,让学生学得主动、积极;更重要的是,要克服长期以来的种种二元对立, 使教师、学生、教学内容 (知识) 获得高度的统一, 使教学内容实现其本应有的价值,使教师、学生在教学中获得最大发展,使学生能够形成有助于未来可持续发展的核心素养。新教材正式启用后,各地的教材培训中,都明确强调在深化课堂教学改革过程中要积极探索基于情境、问题导向的互动式、启发式、探究式、体验式等课堂教学。因此笔者在“化学平衡移动”的教学中借助真实的生活情境素材来丰富学生的认知体验,通过设计有梯度的问题来启发学生的自主探究,利用手持技术促进学生的核心素养发展,对深度学习进行有益探索和尝试。
一、教学背景分析
1.教材分析
“化学平衡移动”是人教版选修4《化学反应原理》第二章第三节的内容,本节课为第一课时,《普通高中化学课程标准(2017年版)》对本部分教学内容要求:通过试验探究,了解浓度、压强、温度对平衡状态的影响;认识化学平衡综合调控在生产、生活和科学研究领域中的重要作用。新教材将“化学反应速率”和“影响化学反应速率的因素”合并为一节,整体性更强,教学更连贯;新加入“化学反应的调控”运用勒夏特列原理指导“工业合成氨”生产。内容的呈现发生了变化,“影响化学平衡的因素”和“化学平衡常数”的互换了顺序,以“浓度对化学平衡的影响”引出“化学平衡移动”,形成了“化学平衡状态→化学平衡常数→影响化学平衡的因素→化学平衡移动→勒夏特列原理”的新顺序。以科学认识论为理论基础,抽提出静态本质、动态规律、价值为进阶维度,结合学科本体研究,抽提出限度的表征、限度的改变、限度改变的价值为进阶维度。在浓度对化学平衡移动的影响中增加了控制变量思想,增加了用手持技术验证了压强对化学平衡移动的实验,增加了合成氨工艺流程图等教学资料。
2.学情分析
学生在初中已经学过化学能与能源的关系,在高中化学人教版必修二学习了化学反应速率及其影响因素、化学反应限度,在人教版选修四《化学反应原理》中化学平衡的学习主要是对化学平衡状态的影响因素的探讨。随着化学知识的不断积累和对实验现象的深入观察,学生可能会产生是不是所有的化學反应都能进行完全这样的疑问;学生很多情况下对“化学平衡移动”内容的理解水平处于浅层学习层面,机械地背诵记忆有关的概念和规律,无法建立化学平衡观,不能将化学平衡的相关知识迁移应用到其他的平衡体系,不利于发展学生的“变化观念与平衡思想”的化学核心素养。
二、教学目标
(1)通过观察K2Cr2O7溶液,建构平衡状态的特征;培养宏观辨析和微观探析、变化观念和平衡思想的能力。
(2)通过实验探究,理解浓度、温度、压强对平衡移动的影响规律;增强实验探究水平和证据推理能力(视角水平)。
(3)通过讨论归纳出平衡移动的原理;建立模型认知水平(内涵水平)。
(4)通过平衡移动原理指导工业生产实践;培养问题解决能力(简单化学问题、简单实际问题)和形成正确的化学价值认识水平(学科价值、社会价值、学科和社会价值)。
三、教学重难点
影响化学平衡移动的条件。
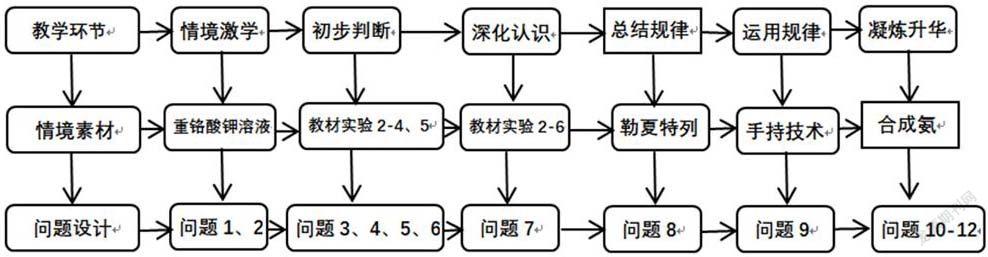
四、教学流程设计
五、教学过程
【情境激学】展示K2Cr2O7溶液
【问题1】 如何判断反应Cr2O72- + H2O⇌2CrO42-+2H+发生了?
【问题2】如何判断该可逆反应达到化学平衡状态?
【学生】积极思考并回答
【过渡】平衡状态是不是永
恒不变的?假如可以改变,哪些因素可以影响化学平衡移动?今天,我们一起探究影响化学平衡移动的因素。
【学习任务一】探究浓度、温度对平衡移动的影响
1.浓度对平衡移动的影响
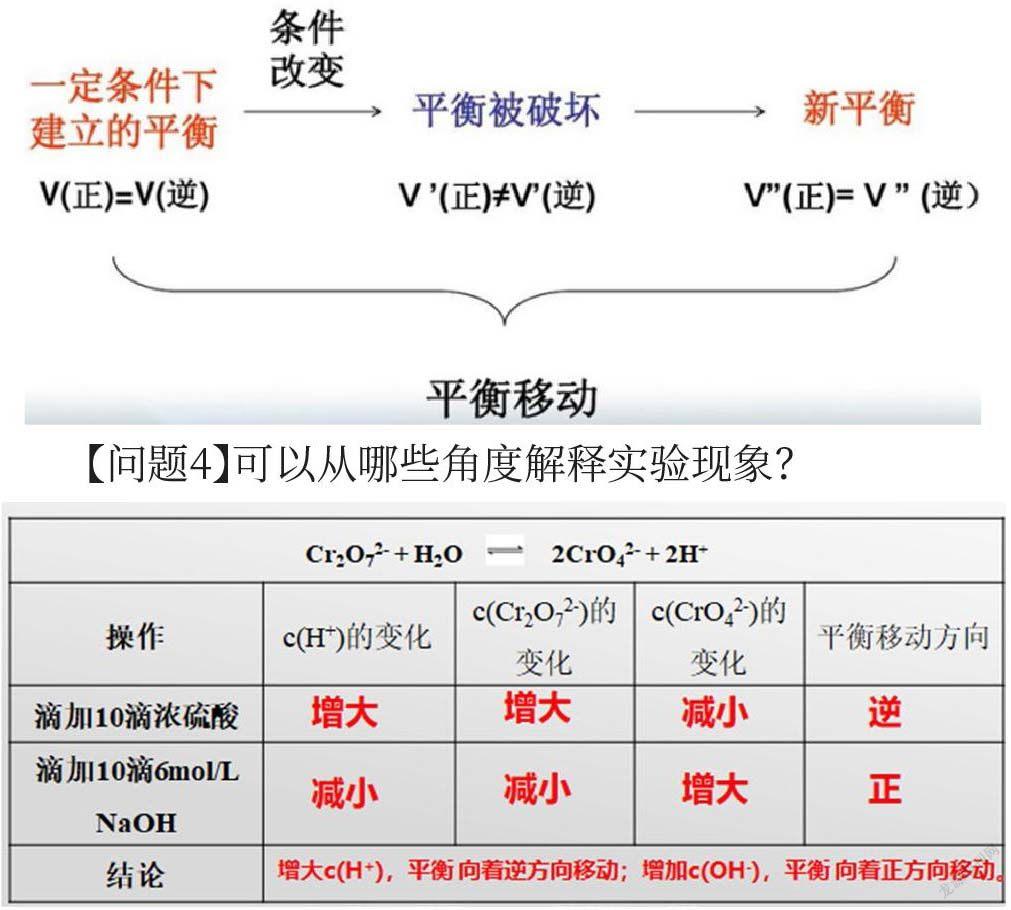
【自主探究】已知在K2Cr2O7的溶液中存在着如下平衡:Cr2O72- + H2O⇌2CrO42- + 2H+ , K2Cr2O7溶液为橙色,K2CrO4溶液为黄色。取三支试管各加入2.5mL(2滴管)0.1 mol/L K2Cr2O7溶液,然后按下表步骤操作,观察并记录。
【学生活动】学生按小组自主实验,记录实验现象。
【问题3】:实验中的现象说明了什么?
【总结】平衡移动的概念
【问题4】可以从哪些角度解释实验现象?
【问题5】实验有没有什么地方有疑问需要改进?
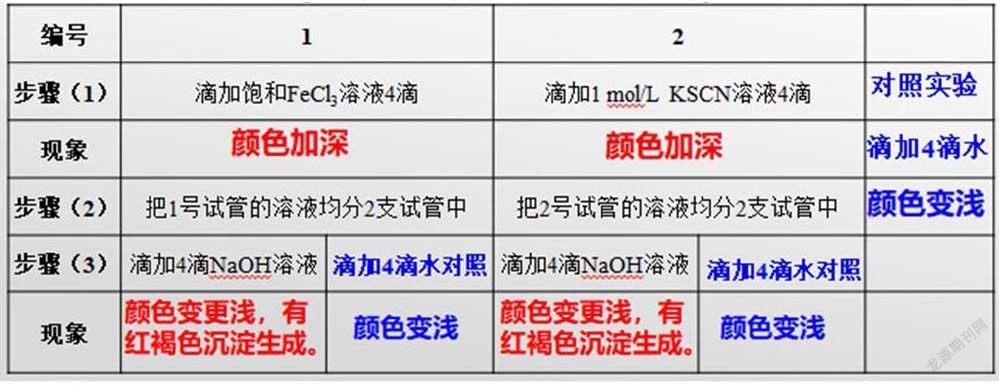
【实验探究】认真阅读以下实验步骤,预测实验现象,预测完后按下列实验操作进行验证。向盛有5mL0.005mol/L FeCl3溶液的试管中加入5mL0.01mol/L KSCN溶液,溶液呈红色,将上述溶液分置二支试管中,然后按下表步骤操作。FeCl3+3KSCN⇌Fe(SCN)3+3KCl
【问题6】往溶液中加入少量氯化钾固态,平衡会移动吗?
【学生活动】请分析,达到平衡的反应体系在t1时刻增大反应物浓度和减小反应物浓度对正、逆反应速率的影响,请用速率—时间图像表示其变化。
【归纳】通过动画解析速率改变移动规律——谁大向谁移。
2.温度对平衡移动的影响
【问题7】温度升高,正逆反应速率都增加,平衡会移动吗?请同学们大胆提出自己的猜想,并设计实验验证。
【探究实验2】已知2NO2(红棕色气体)⇌N2O4(无色气体)△H<0 ,分别将NO2球浸泡在冰水、热水中,观察其变化。
【学生活动】请分析,达到平衡的反应体系在t1时刻升高温度和降低温度对正、逆反应速率的影响,请用速率—时间图像表示其变化。
【学习任务二】建立平衡移动模型——勒夏特列原理
【问题8】回顾以上实验,你能发现什么规律?
【归纳】浓度、温度对平衡移动的影响
【讲授】1984年,法国科学家勒夏特列也对上述问题进行了研究,他发现如果一个体系达到平衡状态时,改变反应条件,化学平衡被破坏,并向减弱改变的方向移动。为了纪念勒夏特列的这个发现,我们将这个有关平衡改变的规律称为勒夏特列原理。回顾、讨论,总结规律在老师的引导下,归纳勒夏特列原理——减弱改变。
【学习任务三】平衡移动模型的完善——利用手持技术探究压强对平衡移动的影响
3.压强对化学平衡移动的影响
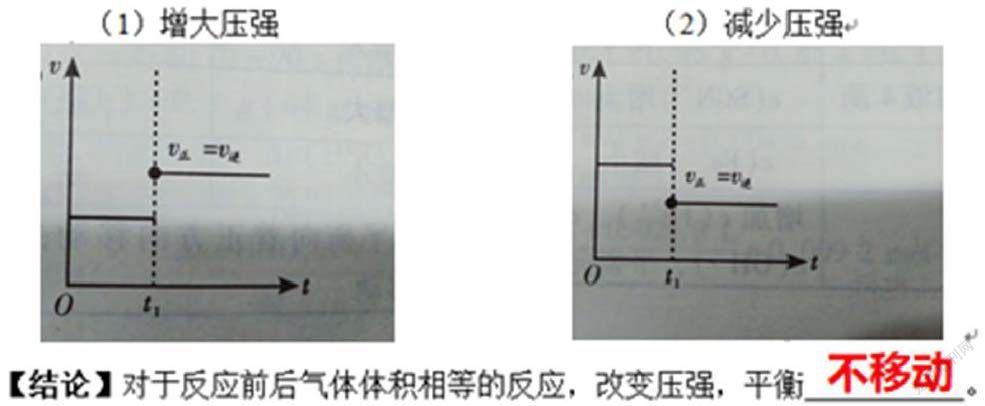
【学生活动】利用勒夏特列原理,分析2NO2⇌N2O4反应体系中增大压强和减少压强。平衡向哪个方向移动?在v-t坐标中画出v(正)与v(逆)的相对变化。
【引导】压强增大,平衡向压强减小的方向移动,即向气体计量数减小的方向移动。增大压强,NO2和N2O4 浓度均增大,反应系数大的NO2浓度增大的倍数更大,平衡向减少NO2浓度的方向移动;减小压强,NO2和N2O4浓度均减小,反应系数大的NO2的浓度减小更多,平衡向着增加 NO2浓度的方向移动。
【学生活动】利用勒夏特列原理,分析H2(g)+I2(g)⇌2HI(g)反应体系中增大压强和减少压强。平衡向哪个方向移动?在v-t坐标中画出v(正)与v(逆)的相对变化。
【图像表征】利用压强传感器表征压強对平衡移动的影响。
4.催化剂对平衡移动的影响
【问题9】催化剂如何影响化学平衡移动?
【引导】催化剂降低反应活化能,有效碰撞增加,化学反应速率提高。对于同一个混合体系中,加入催化剂,v(正)与v(逆)的改变是同等程度的,因此平衡不移动。
【学习任务四】学以致用——讨论优化合成氨反应条件方案
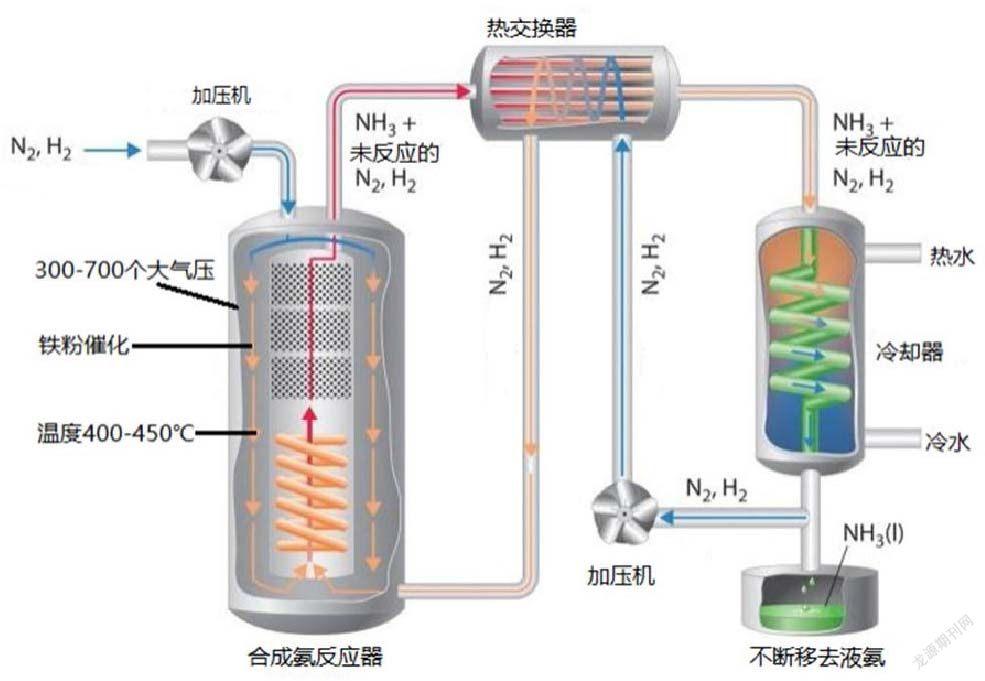
【问题10】为什么合成氨要选择300—700个大气压?
【问题11】为什么要不断地移去液态氨?
【问题12】为什么反应温度要控制在400—450℃?
【引导】选择和调控反应条件时,我们不能单一角度地考虑反应的限度,或反应的速率,而是需要综合考虑诸多因素的影响。既要考虑保障生产的经济效益,也不可忽视了生产对环境资源的影响。
【课堂小结与作业】请一位同学谈谈自己本节课的收获,并要求同学们课后以小组的形式查阅资料和调查了解更多生活、生产中化学平衡的应用。
六、教学思考
1.开发学生学习化学的潜能,激发他们学习化学的兴趣,引导学生自主学习,学会学习,在学习中学会发现问题、提出问题、分析问题、解决问题,从而达到培养学生化学核心素养的目的。
2.用深度学习的课堂教学,到学习中,引导学生深入理解化学平衡的概念,教学设计中采用自主探究实验、问题驱动、迁移应用、四重表征等教学策略使学生能够达到深度学习水平,构建了宏—微—符—曲线的四重表征,较好的解决了它们之间的自由转换,让学生很好的践行了先从特殊到一般,再由一般到特殊的科学研究方法。
【参考文献】
[1]陈义芳.基于深度学习开展高效高中化学教学[J].高考,2021(13):47-48.
[2]陆郁.高中生化学平衡学习进阶的实践研究[J].中学生数理化(教与学),2020(05):72.
[3] 熊茜.基于新课标高一化学教材的比较研究[D].江西师范大学,2020.
[4] 陈静.基于深度学习的化学课堂提问研究[D].南京师范大学,2018.
佛山市顺德区第一中学 邓优华
