牡丹叶的质量标准研究
2021-09-10肖会敏罗定强王四旺
肖会敏,张 妍,杨 旭,李 捷,林 奋,罗定强,王四旺
(1.陕西凤丹正元生物科技有限公司研发部,西安 710077;2.陕西中医药大学,咸阳 712046;3.空军军医大学中药与天然药物教研室,西安 710032;4.陕西省食品药品监督检验研究院,西安 710061;5.西北大学生命科学与医学部,西安 710069)
牡丹叶为毛茛科植物牡丹PaeoniaAndr.的干燥叶,其在历代本草和现代医药著作中均未记载,民间常用于治疗痢疾,主产于陕西、山东、安徽、河南等地,秋季采收[1]。牡丹叶中含有苷类、多酚类、黄酮类、多糖类等成分,苷类如芍药苷、羟基芍药苷等,多酚类如没食子酸、鞣花酸、没食子酸甲酯等[2-6]。现代药理研究表明,牡丹具有抗炎、镇痛、降血糖、降尿酸、抑菌、调节心血管系统、抗肿瘤、清除自由基、抗氧化、缓解痛风性关节炎等多种药理作用[7-13]。牡丹叶中芍药苷对辐射损伤内皮细胞有保护作用,可改善认知功能障碍及抑郁焦虑等[14-16]。牡丹叶中的鞣花酸可改善阿尔茨海默病引起的学习和记忆障碍与肾缺血再灌注引起的大鼠肾损伤[17-18]。现行山东省牡丹叶质量标准缺乏含量检测项,同时药材薄层色谱法 (TLC) 鉴别项目在不同产地实验中难以重现,陕西省是牡丹种植大省,资源丰富。因此,亟需建立一种更加全面、科学的牡丹叶质量标准来评价其质量。本文通过不同产地药材建立定量指标(芍药苷与鞣花酸)与定性指标(芍药苷TLC鉴别)。
1 仪器与试药
1.1仪器 UFLC-20AD-PDA型高效液相色谱仪,日本岛津公司;Kromasil C18色谱柱(250 mm×4.6 mm,5 μm),瑞典NOBEL公司;XPE105型电子分析天平,梅特勒-托利多公司;KQ-5200D型数控超声波发生器,昆山超声仪器有限公司;HWT-6B型恒温水浴箱,天津市恒奥科技发展有限公司。
1.2试药 甲醇、乙腈(HPLC级),美国Fisher公司;超纯水,自制;香草醛和硫酸(分析纯),均购自天津恒兴化学试剂制造有限公司。对照品:芍药苷(批号110736-202044,质量分数为96.8%);鞣花酸(批号111959-201903,质量分数为88.8%),均购自中国食品药品检定研究院。牡丹叶对照药材(批号202105-001),由陕西省食品药品监督研究院提供;牡丹叶(山东菏泽、陕西合阳、陕西蒲城、陕西西安),均由陕西凤丹正元生物科技有限公司提供,经罗定强主任药师鉴定为毛茛科植物牡丹PaeoniaAndr.的干燥叶。
2 方法与结果
2.1牡丹叶中芍药苷的TLC鉴别 取牡丹叶样品粉末1 g,加石油醚(30~60 ℃)50 mL,超声处理30 min,滤过,弃滤液,收集药渣,挥干石油醚,加丙酮50 mL,超声(功率300 W,频率50 kHz)处理30 min,滤过,滤液浓缩至2 mL,作为供试品溶液。另取芍药苷对照品,加丙酮制成质量浓度为1 mg·mL-1的对照品溶液。依据文献方法[1,19-20],吸取上述2种溶液各10 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,展开,取出,晾干,喷以体积分数为5%的香草醛硫酸溶液,加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同蓝紫色斑点。见图1。
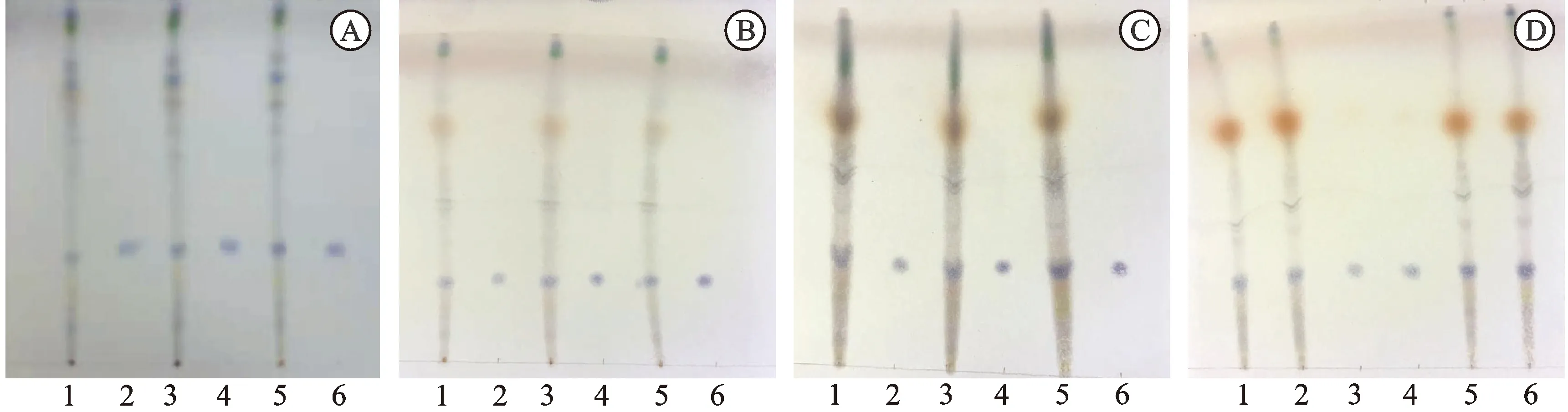
图1 牡丹叶中芍药苷的TLC鉴别
2.2牡丹叶的TLC鉴别 取牡丹叶样品粉末,加石油醚(30~60 ℃)20 mL,超声处理10 min,滤过,弃去滤液,药渣挥去石油醚,加丙酮25 mL,超声处理10 min,滤过,将滤液浓缩至5 mL,作为供试品溶液。另取牡丹叶对照药材1 g,同法制成对照药材溶液。按照TLC法(《中国药典》2020年版四部通则0502)进行实验,吸取上述2种溶液各10 μL,分別点于同一硅胶G 薄层板上,以三氯甲烷-甲酸乙酯-甲酸(5∶5∶1)为展开剂,展开,取出,晾干,用碘蒸气熏蒸2 min。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点[1]。结果见图2。

图2 牡丹叶TLC鉴别
2.3芍药苷与鞣花酸的含量测定
2.3.1色谱条件与系统适用性实验 以十八烷基硅烷键合硅胶为填充剂;以乙腈(A)-0.85 g·L-1磷酸 (B)为流动相进行梯度洗脱,见表1。检测波长为234 nm;柱温为30 ℃;流速为0.8 mL·min-1;理论塔板数按照芍药苷峰计算应不低于4 000。

表1 梯度洗脱程序
2.3.2混合对照品溶液的制备 分别精密称取芍药苷、鞣花酸对照品2.61、4.02 mg,置于5 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得。
2.3.3供试品溶液的制备 取牡丹叶样品粉碎,过4号筛,精密称取1 g,置于具塞锥形瓶中,加入体积分数为70%的甲醇50 mL,密塞,称定质量,超声处理(功率300 W,频率50 kHz)60 min,放冷,再称定质量,用体积分数为70%的甲醇补足减失的质量,摇匀,滤过,精密量取续滤液1 mL,置于10 mL量瓶中,加体积分数为70%的甲醇稀释至刻度,摇匀,即得。
2.3.4标准曲线及线性范围 分别精密量取2.3.2项下制备的混合对照品溶液0.01、0.05、0.10、0.25、0.50 mL,分别置于2 mL的量瓶中,加甲醇定容至刻度,制得系列混合对照品溶液1~5。进样测定,记录峰面积,考察对照品质量浓度(x)与峰面积(y)的线性关系,结果芍药苷、鞣花酸的线性方程分别为y1=9 837.2x1-5 905.7(r1=0.999 8),y2=20 532x2+7 336.2(r2=0.999 8);质量浓度分别在2.53~126.32、3.57~178.49 μg·mL-1范围内线性关系良好。
2.3.5精密度实验 取2.3.4项下制备的混合对照品溶液3,连续测定6次,进样测定峰面积并计算RSD值。结果芍药苷、鞣花酸峰面积的RSD值分别为1.42%、1.09%,表明仪器精密度良好。
2.3.6稳定性实验 取2.3.4项下制备的混合对照品溶液3,分别于0、0.5、1、2、4、8、12、24 h进样测定峰面积,计算RSD值。结果芍药苷与鞣花酸的RSD值分别为1.12%、0.99%,表明供试品溶液在24 h内稳定性良好。
2.3.7重复性实验 精密称取牡丹叶样品(陕西合阳)1 g,按照2.3.3项下方法制备6份供试品溶液,按照2.3.1项下色谱条件进样测定。结果见表2,结果表明实验重复性良好。

表2 重复性实验结果
2.3.8回收率实验 精密称取含量已知的样品(陕西合阳)9份,每份1 g,分别添加混合对照品溶液2.5、5.0、7.5 mL(取芍药苷、鞣花酸对照品77.48、52.93 mg,置于50 mL量瓶中,加甲醇定容至刻度,摇匀即得2种成分质量浓度分别为1.50、0.94 mg·mL-1的混合对照溶液),按照2.3.1项下色谱条件进样测定。结果见表3,结果表明该方法回收率良好。
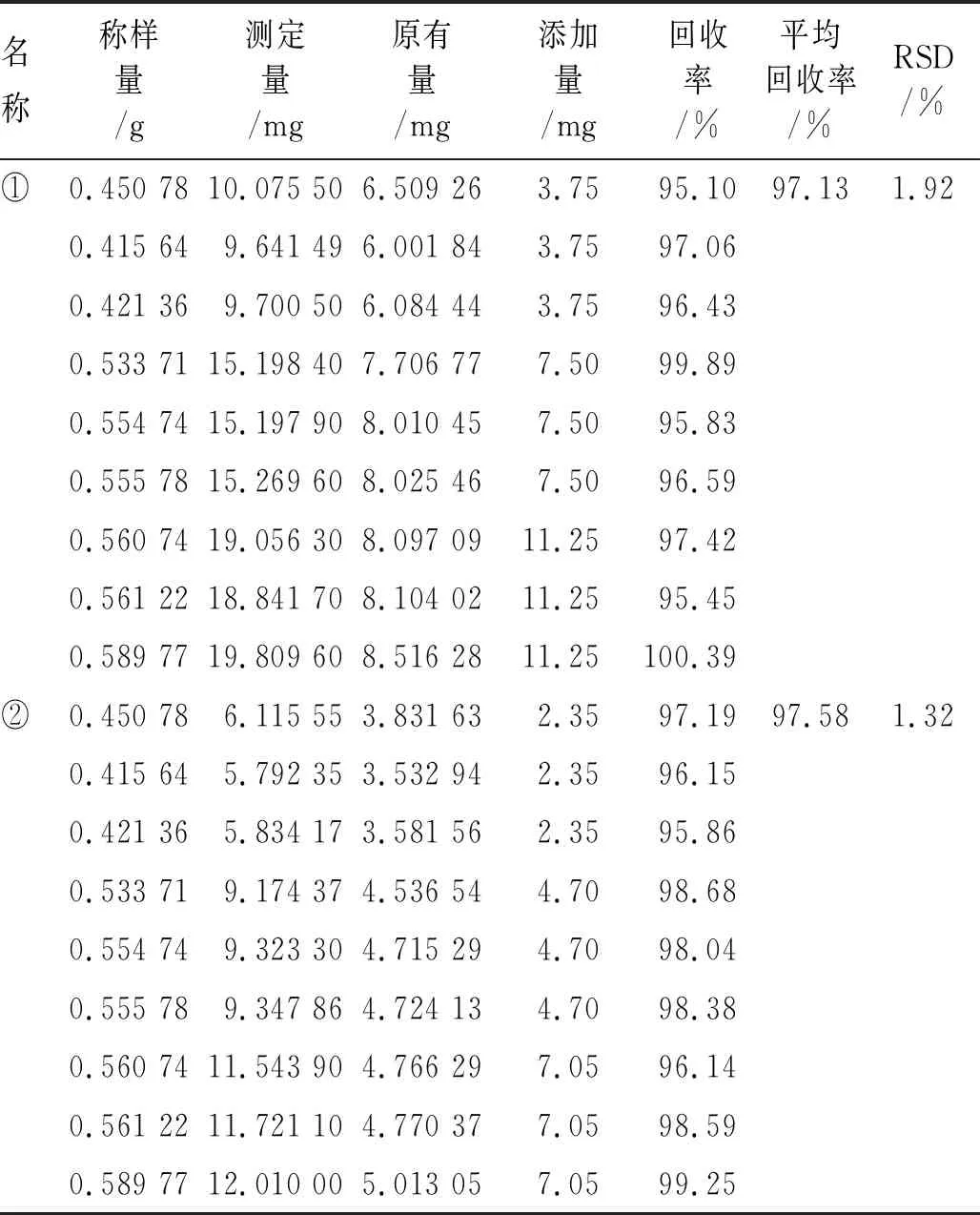
表3 回收率实验结果 (n=9)
2.3.9样品含量测定 测定4个不同产地药材中芍药苷与鞣花酸的含量,按照2.3.3项下方法制备供试品溶液,按照2.3.1项下色谱条件进样测定,结果见表4、图3和图4。

图3 HPLC图
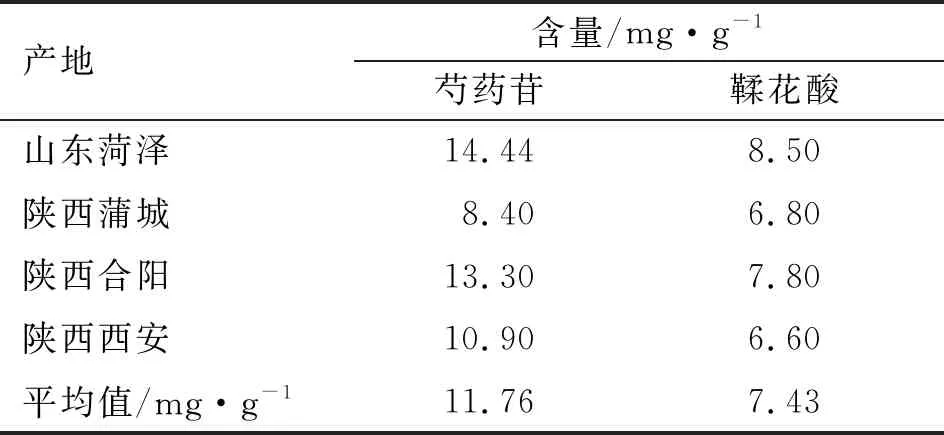
表4 4个不同产地药材中芍药苷与鞣花酸的含量
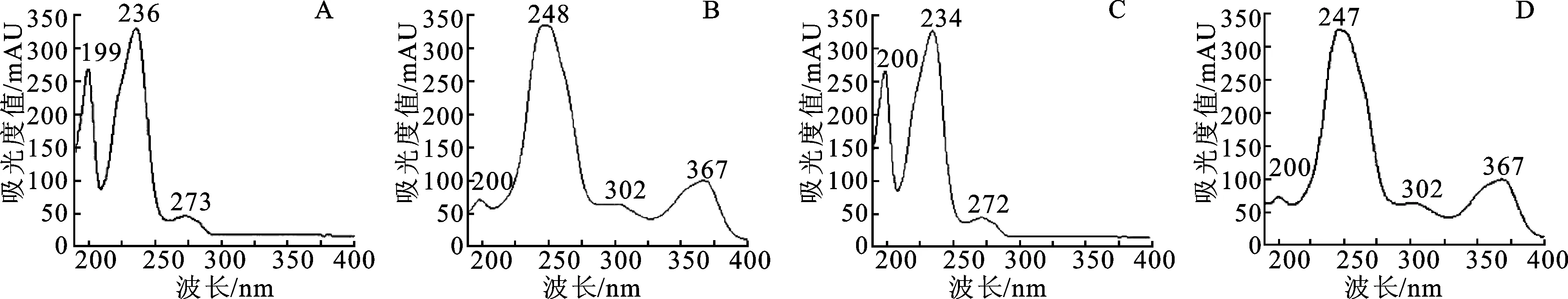
图4 目标物光谱图
3 讨论
3.1TLC鉴别 牡丹为毛茛科芍药属多年生落叶灌木,牡丹叶化学成分复杂,主要成分为苷类、酚类和黄酮类等[3]。本实验参照文献[1]中牡丹叶的TLC鉴别的制样方法、展开方法及显色方法,结果(见图2)与文献结果不一致,即TLC中间斑点未显示或不清晰或不同产地不一致,表明该方法重复性不理想,因此未列入质量标准;再依据文献[19]中白芍的TLC展开系统与显色方法,对制样方法进行改进,结果(见图1)不同产地供试品色谱中,在与对照品色谱相应的位置上,显相同的蓝紫色斑点,斑点清晰明显,操作简便,灵敏度高,重复性较好,故将其列入质量标准。
3.2含量测定 对检测条件进行摸索,比较了不同柱温(40、35、30、25、20 ℃)、不同流速(0.8、1.0、1.2 mL·min-1)、不同色谱洗脱系统[不同质量浓度的磷酸(0、0.85、1.70、3.40、6.80、8.50 g·L-1)-甲醇或乙腈酸]、不同进样量(20、10 μL)、不同制样方法如超声(15、30、45、60 min)、加热回流(15、30、45、60 min)以及不同体积分数的甲醇或乙醇(40%、50%、60%、70%、80%、100%),最终建立了制样简单、灵敏可靠、操作方便、重复性与稳定性良好的HPLC法测定牡丹叶中芍药苷与鞣花酸的含量,可列入标准。
综上所述,把具有良好重复性与稳定性的含量测定项(即芍药苷与鞣花酸的含量测定)以及专属性强、重复性好、操作简便的TLC鉴别项(即芍药苷的鉴别)列入质量标准,可以很好地评价与控制牡丹叶的质量。
