含吡咯里西啶生物碱中成药潜在风险评估
2021-09-06谷丽华熊爱珍宋宗华王峥涛
熊 芬,谷丽华,杨 莉, 2,熊爱珍, 2,宋宗华,王峥涛, 2
含吡咯里西啶生物碱中成药潜在风险评估
熊 芬1,谷丽华1,杨 莉1, 2,熊爱珍1, 2*,宋宗华3,王峥涛1, 2*
1. 上海中医药大学中药研究所,中药标准化教育部重点实验室暨国家中医药管理局中药新资源与质量评价重点实验室,上海 201203 2. 上海中药标准化研究中心,上海 201203 3. 国家药典委员会,北京 100061
吡咯里西啶生物碱(pyrrolizidine alkaloids,PAs)是一种双环吡咯啶生物碱,因多数具有肝毒性,又称肝毒性吡咯里西啶生物碱(hepatotoxic PAs)。PAs广泛存在于菊科、豆科、紫草科的多种药用植物中。《中国药典》2020年版共收载含有PAs的药材8种,包括千里光、款冬花、佩兰、紫草等,涉及成方制剂数十种。此外,《卫生部药品标准》《药品注册标准》等收载含PAs制剂尚有200余种。除千里光药材外,其他含PAs中药及其制剂均没有关于PAs类成分的安全限量标准,其临床用药安全存在极大的风险。对含PAs中成药的研究概况进行了系统总结、分析,以期为此类中成药的临床用药安全提供警示和参考。
吡咯里西啶生物碱;中国药典;中药;中成药;安全性
吡咯里西啶生物碱(pyrrolizidine alkaloids,PAs)是一种天然毒素,广泛分布于全世界6000多种高等有花植物中,特别是菊科(Compositae)、豆科(Leguminosae)、紫草科(Boraginaceae)和兰科(Orchidaceae)植物中[1]。有研究报道,在蜂蜜与牛奶中也检测到PAs,是由于蜜蜂、奶牛采食含PAs植物而造成PAs在其体内积聚[2-4]。PAs结构多样,目前已报道600多种PAs,其中一半具有肝毒性,临床可导致肝窦阻塞综合征(hepatic sinusoidal obstruction syndrome,HSOS)[5-6]。
据报道,在我国有50多种药用植物含PAs[7],其中数种被《中国药典》(以下简称药典)收录,其他种类或收载于地方标准,或作为民间、民族药物使用[8]。通过检索药典2020年版,笔者发现其收录千里光等8种含PAs的中药(不含饮片及蜂蜜);进一步检索药典及其他常用药品标准,包括《卫生部药品标准》《国家中成药标准汇编》《新药转正标准》,共检索到含此8种中药的成药200余种。PAs具有强烈的肝毒性、肺毒性、基因毒性、致癌性等,德国、英国、新西兰等国家均严格控制含PAs的植物药及相关制品中PAs的含量。然而,我国目前仅药典中规定了千里光药材中PAs的限量,其他含PAs的中药以及中成药均无PAs的限量标准,其临床用药安全性值得关注。本文对这些中成药的研究概况进行了系统分析,为其临床用药安全提供警示和参考。
1 PAs的结构类型与毒性
PAs大多数是由具有双稠吡咯啶环的氨基醇和不同的有机酸2部分缩合形成,其醇部分称为裂碱(necine),酸部分称为裂酸(necic acid)[9]。裂碱结构上的C-1、C-2不饱和双键,是PAs具有毒性的关键结构。根据C-1、C-2不饱和双键的有无,PAs分为饱和型与不饱和型;其中不饱和型具有较强的肝毒性,又称肝毒性吡咯里西啶生物碱(hepatotoxic PAs,HPAs)[1]。常见的不饱和型PAs可分为retronecine(RET)型和otonecine(OTO)型(图1),RET型常有氮氧化物及-结构[10];饱和型PAs主要是platynecine(PLA)型。

RET-retronecine OTO-otonecine PLA-platynecine
PAs毒性与代谢活化作用密切相关[11]。大部分PAs本身不具有毒性,需经肝脏细胞色素P450酶(cytochrome P450,CYP450)代谢活化,生成活泼的中间体脱氢吡咯(dehydropyrrolizidine alkaloids,DHPAs),具有极强的亲电活性,可快速与体内大分子如蛋白、酶、DNA、RNA等结合,进一步诱发毒性。而OTO型PAs,如山岗橐吾碱(clivorine),除代谢活化致毒外,本身就有毒性,可诱导细胞凋亡以及氧化损伤[12-14]。PAs氮氧化物除天然存在于植物中,还可由PAs原型生物碱在体内经黄素单加氧酶与CYP450酶代谢生成,由于其极性更大,易于排除体外,曾被认为毒性较原型生物碱更小;但近期亦有研究表明[15],PAs氮氧化物可在体内转化成原型生物碱,与原型生物碱的毒性相当。总的来说,RET型和OTO型PAs具有较强的肝毒性;而PLA型PAs毒性较小,一般被认为无毒。
此外,根据C-7、C-9有无裂酸取代,PAs还可分为无酯取代型、C-7单酯取代型、C-9单酯取代型,以及C-7、C-9大环双酯取代型。在植物中,PAs多以双酯取代型存在,无酯取代型极为少见。不同结构类型的PAs毒性差异较大。研究表明[16],各类型PAs的毒性大小顺序为大环双酯取代型>单酯取代型>无酯取代型。
2 含PAs的中药在药典中收录情况
药典2020年版共收录含PAs的中药8种,6种来源于菊科(Asteraceae)植物:千里光、款冬花、佩兰、返魂草、野马追、一点红,2种来源于紫草科(Boraginaceae)植物:紫草和滇紫草(表1)。其中一点红、滇紫草收载于药典2020年版四部,属于倒挂药材。各中药中所含HPAs的主要结构见图2。
3 含PAs中药在中成药的应用情况
3.1 含千里光的中成药
千里光为菊科植物千里光的干燥地上部分,主要功效为清热解毒,可治疗痈肿疼痛。千里光中主要含有的PAs为阿多尼弗林碱(adonifoline)、千里光碱(senecionine)、千里光菲林碱(seneciphylline)[17-18]。药典2020年版以阿多尼弗林碱作为千里光药材中PAs的限量检查指标成分,规定千里光药材按干燥品计算,含阿多尼弗林碱不得超过0.004%。熊爱珍等[19]检测采集自不同地区千里光全草中阿多尼弗林碱的含量,结果有2批(共检测6批)超过了药典限定含量,提示在使用千里光时应注意其安全性,尤其注意产地的影响。检索得到含千里光的中成药共24种(表2),包括散剂、片剂、丸剂等多种剂型。
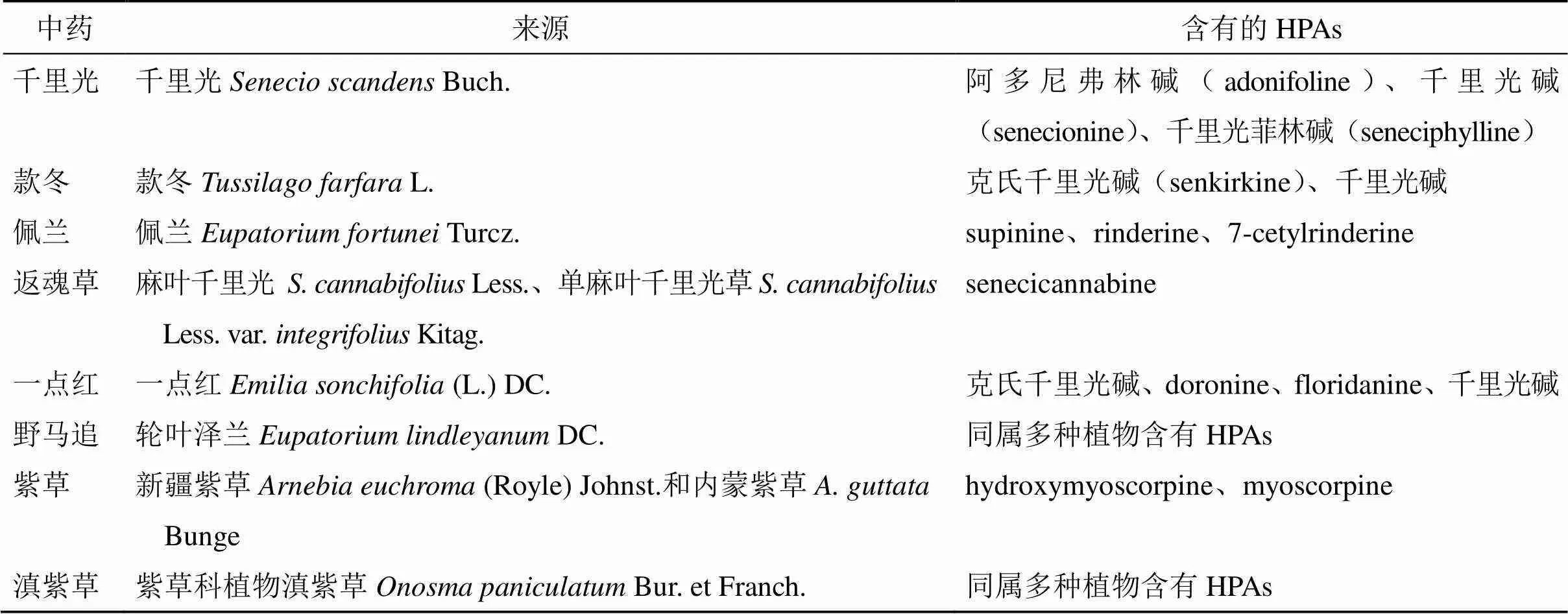
表1 药典中含肝毒性PAs的中药
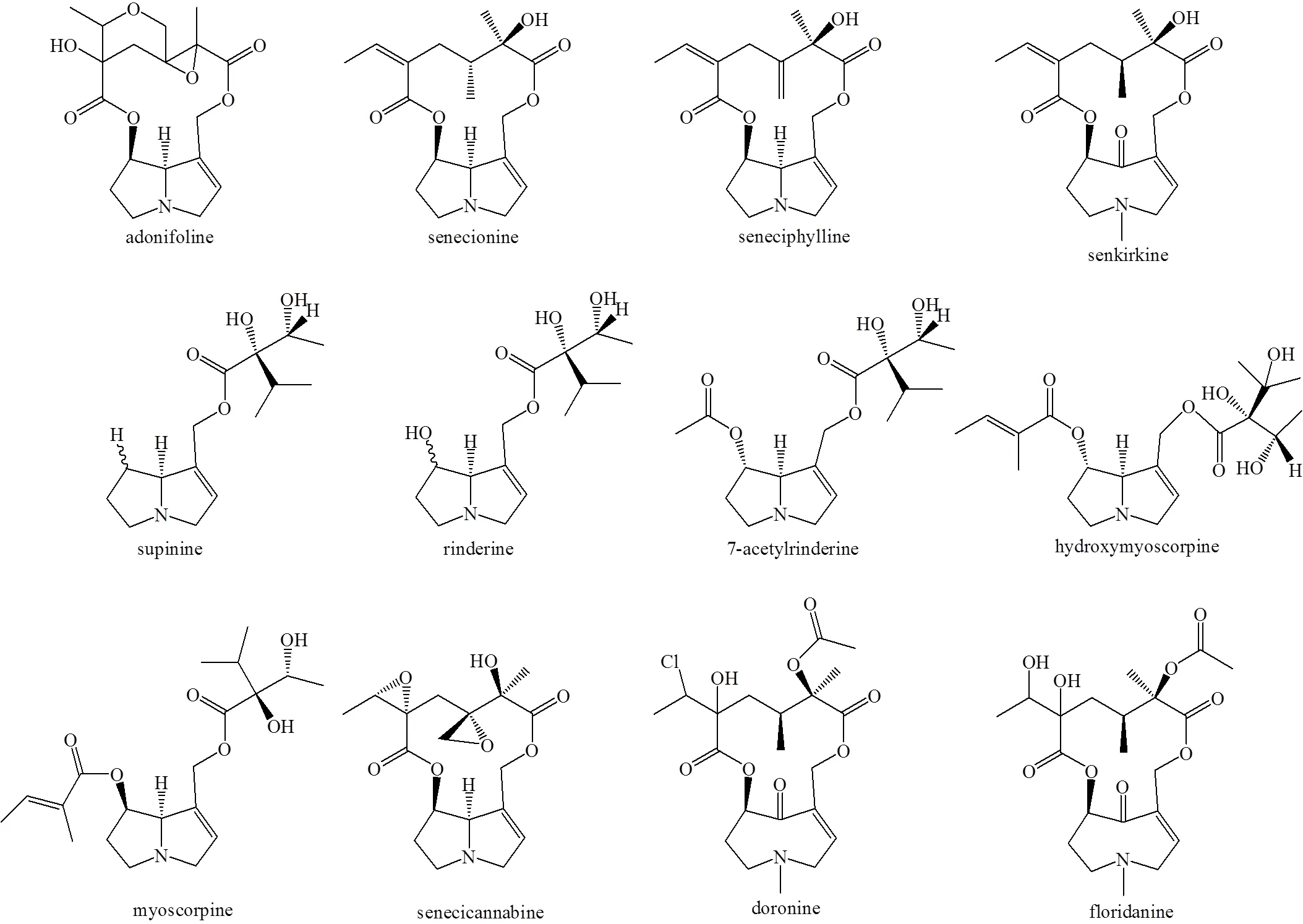
图2 药典收录中药含主要肝毒性PAs的结构
3.2 含款冬花的中成药
款冬花为菊科款冬的花,主要功效为润肺下气、止咳化痰,多与紫菀合用。款冬花主要含有的PAs为克氏千里光碱(senkirkine)和千里光碱[20]。检索发现含款冬花的中成药有66种(表3),处方功效以止咳类为主。药典仅收录含款冬花的中成药14种,《卫生部药品标准(中药成方制剂分册)》收录40种。

表2 含千里光的中成药
药典-《中国药典》 部颁-《卫生部药品标准》 中成药汇编-《国家中成药标准汇编》 转正-《新药转正标准》 “-”表示无明确的处方含量,下表同
Yaodian-Buban-Zhongchengyao Huibian-Zhuanzheng-“-” the composition is unknown, same as below tables
3.3 含佩兰的中成药
佩兰来自于菊科泽兰属佩兰的地上部分,主要功效为芳香化湿、醒胃开脾等。佩兰主要含有的PAs为supinine和rinderine[21]。检索得到含佩兰的中成药共11种(表4),处方功效多为清热解毒。
3.4 含紫草的中成药
紫草为紫草科植物新疆紫草或内蒙紫草的干燥根,其主要功效为清热凉血、活血解毒、透疹消斑。主要含有的PAs为intermedine、myoscorpine、hydroxymyoscorpine[22]。检索到含紫草的中成药共101种(表5),处方功效多以清热、解毒、活血为主。其中药典仅收录含紫草的中成药15种,其余多收录于《卫生部药品标准》(共66种,其中中药成方制剂分册收录30种,藏药分册收录33种,维吾尔药分册收录2种,蒙药分册收录1种)。
3.5 其他中成药
一点红为菊科紫背草属一点红的全草,主要功效为清热解毒、散瘀消肿、凉血;主要含有的PAs为千里光碱和克氏千里光碱[23]。野马追为菊科泽兰属轮叶泽兰(又称林泽兰)的地上部分,主要功效为化痰止咳平喘。返魂草为菊科千里光属宽叶返魂草(又称麻叶千里光)、单叶返魂草(又称单麻叶千里光var)的地上部分,主要功效为润肺下气、消痰止咳。宽叶返魂草主要含有的PAs为seneciphylline、senecicannabine和jacozine[24],单叶返魂草主要含senecicannabine,jacoline,jacobine和jaconine[25]。滇紫草为紫草科滇紫草属滇紫草Bur. et Franch. 的根部栓皮,主要功效为清热解毒。
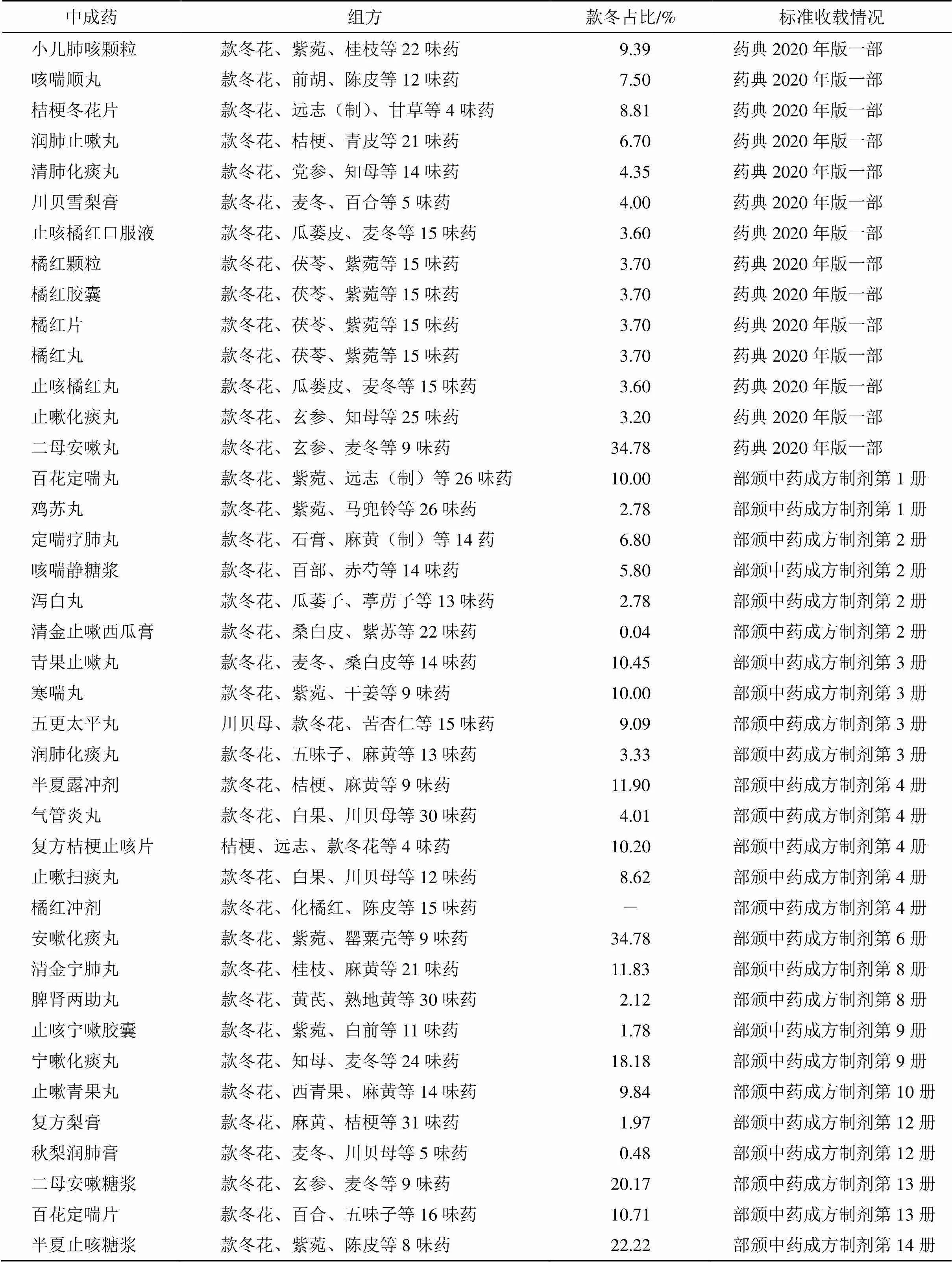
表3 含款冬花的中成药
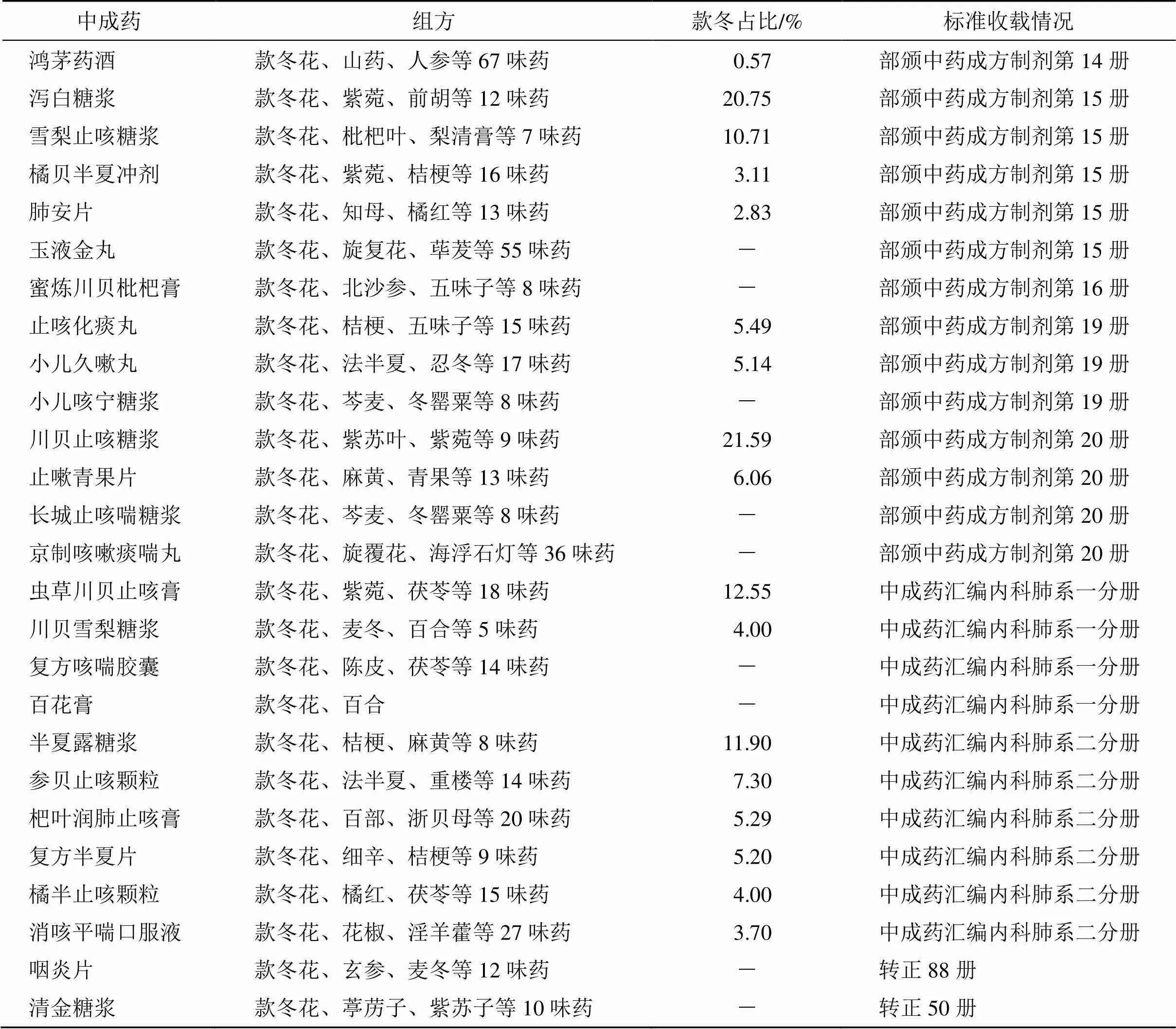
续表3
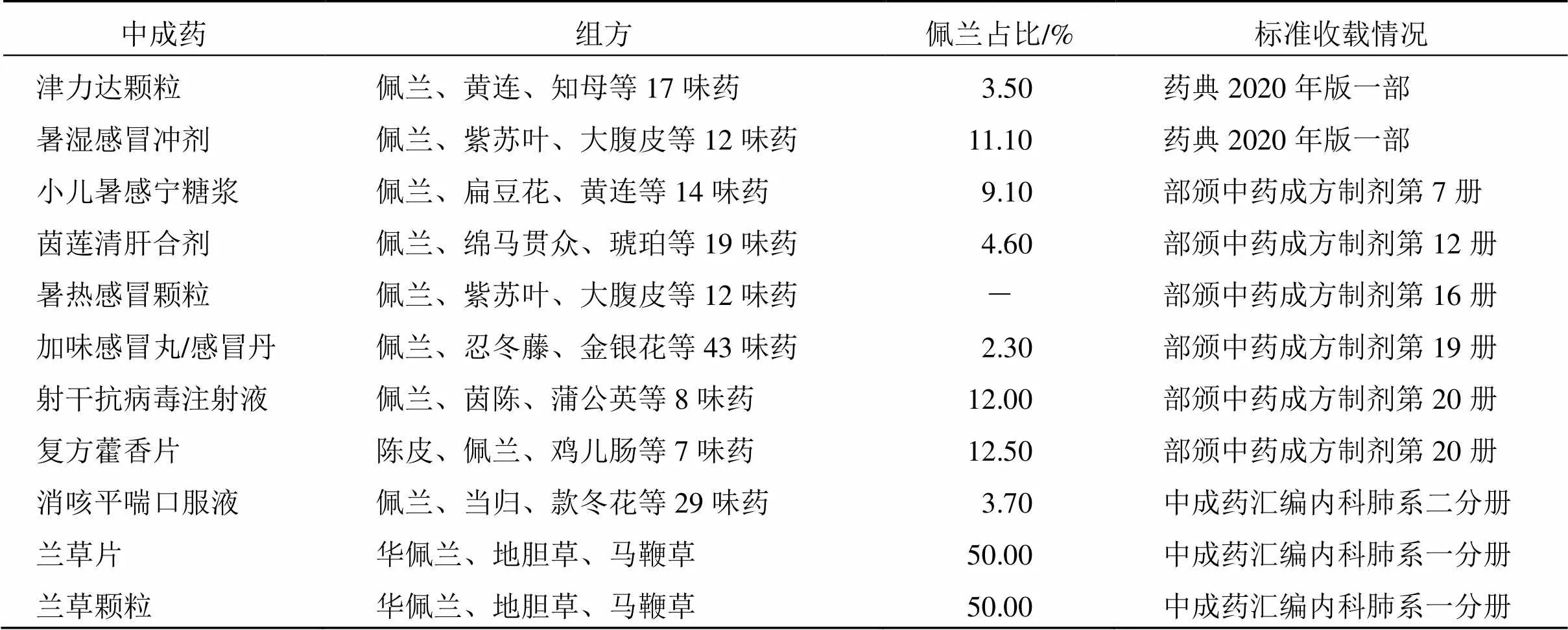
表4 含佩兰的中成药
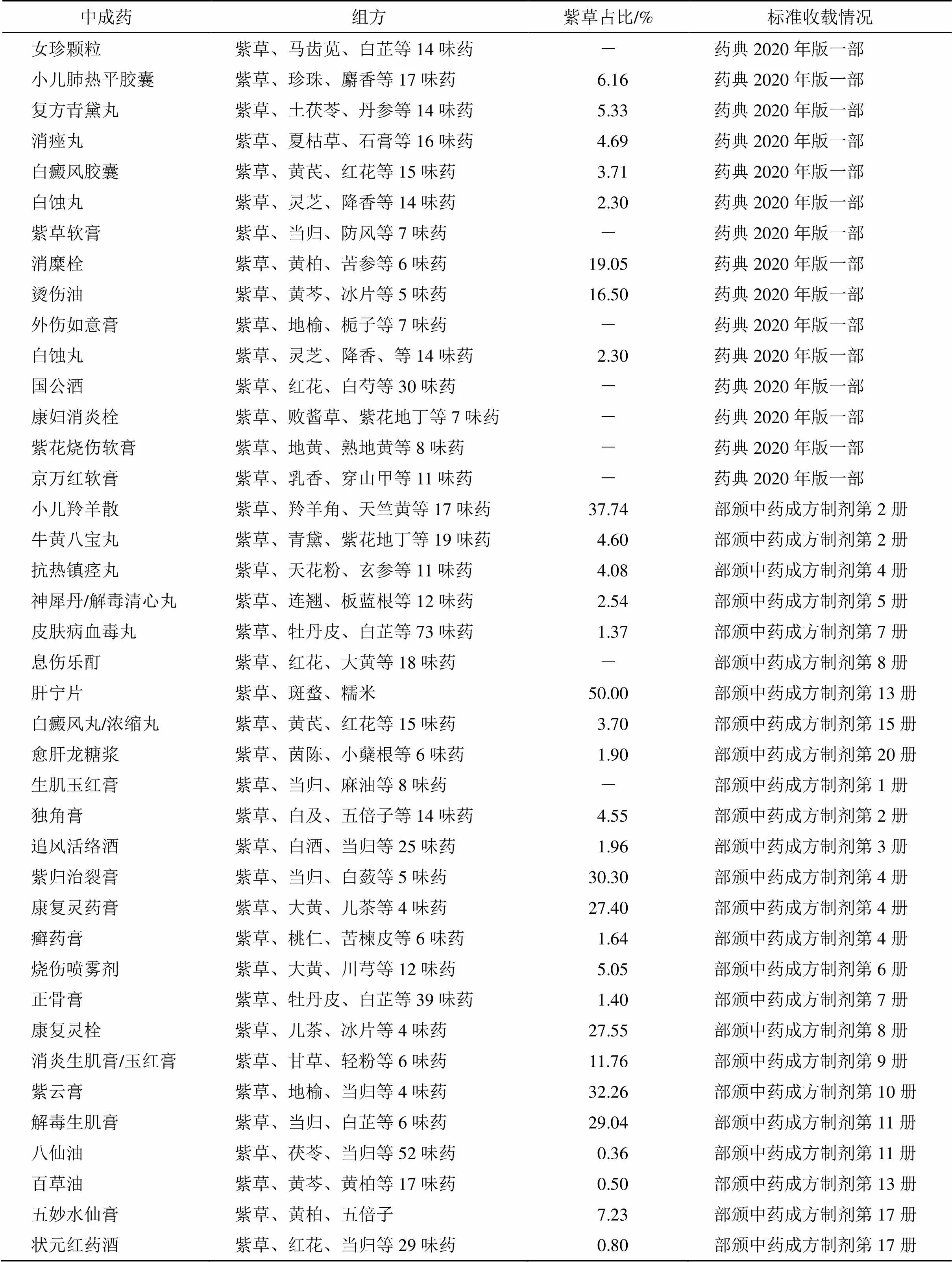
表5 含紫草的中成药
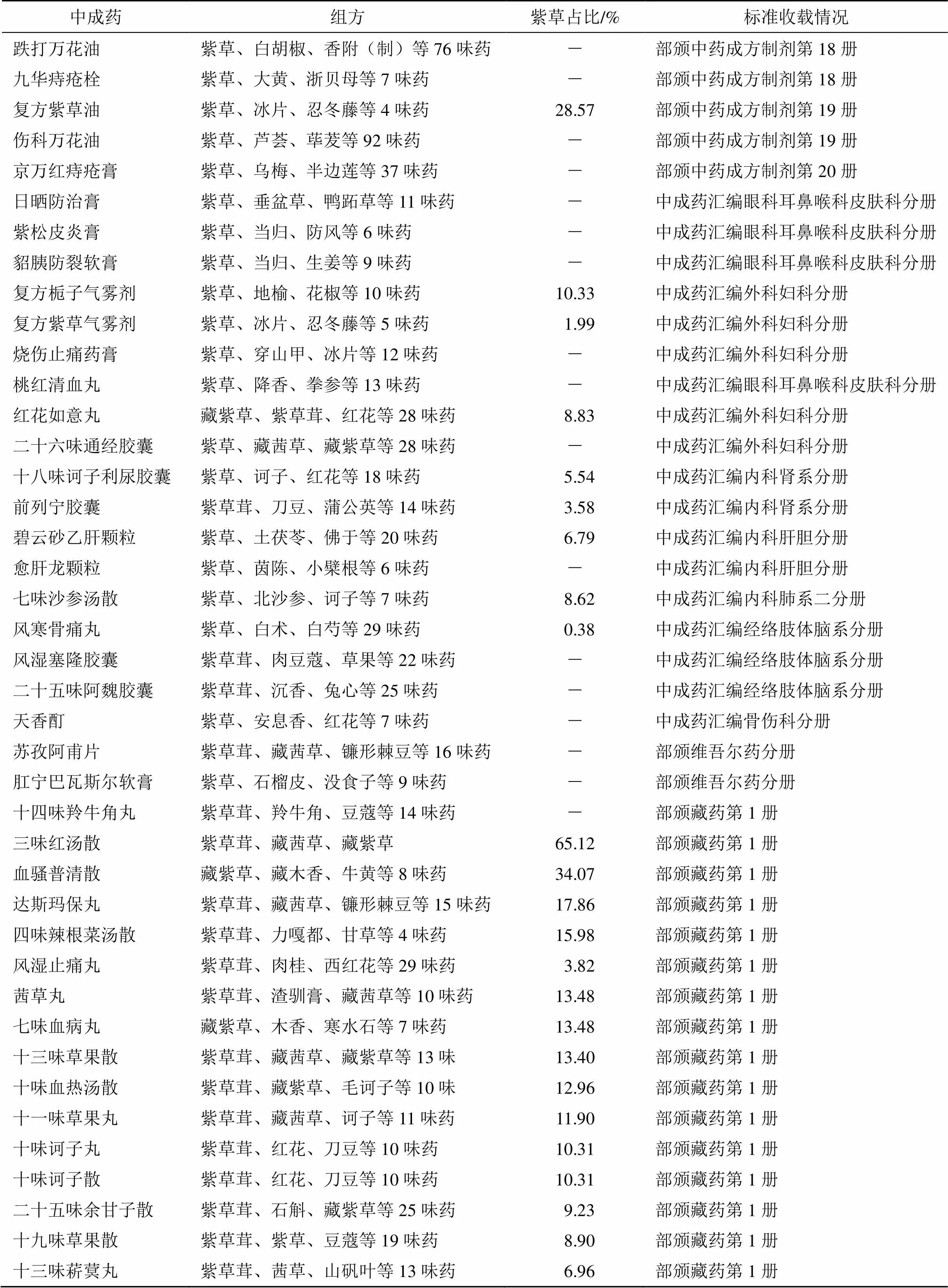
续表5
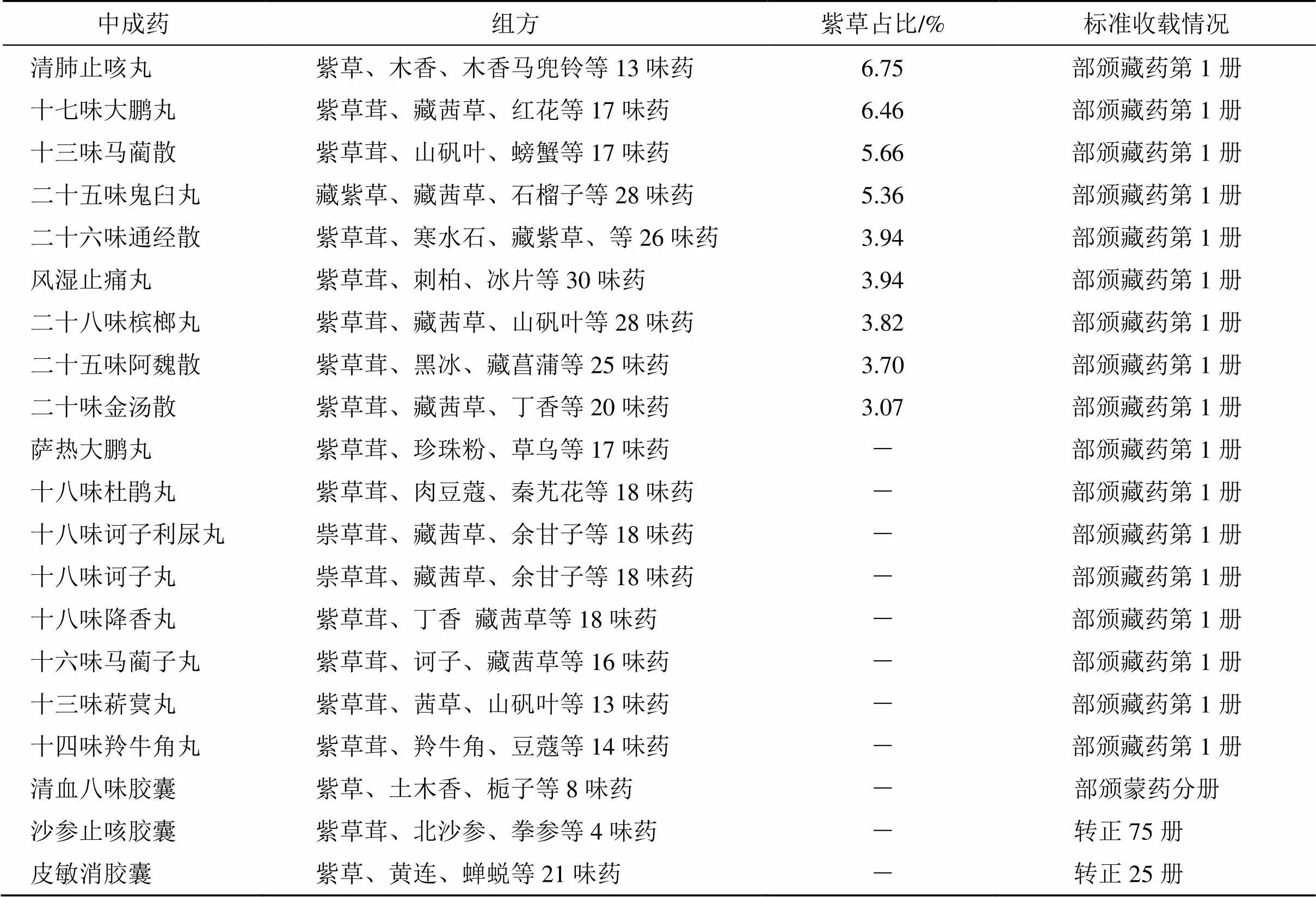
续表5
检索到含这4种中药的中成药较少(表6),其中含一点红的中成药共13种,处方多为清热解毒、消肿散瘀;含野马追的中成药共3种;含返魂草的中成药1种,为舒肝理气、清热解毒的处方;含滇紫草的中成药1种。值得注意的是野马追与滇紫草中尚无PAs成分报道,但是同属多种植物均含有PAs,有学者推测这些植物可能含有PAs[8],尚需要进一步的验证。
4 讨论与展望
PAs分布广泛,可通过传统草药、茶剂、谷物、功能性食品或奶制品、肉类等食物链的传递被人类摄食,从而导致肝毒性、肺毒性、遗传毒性、神经毒性和胚胎毒性等,甚至死亡。因此,含PAs的中草药及制剂一直是世界卫生组织等国际组织及国家严密监控的对象。如世界卫生组织于1988年推动了一项“吡咯里西啶生物碱环境卫生标准”方案[5],并强调了食物链中PAs污染对健康造成的危害。其他权威机构和监管机构也建议对每日PAs的摄入量进行严格的风险评估。德国卫生部规定[26],使用含PAs的中药产品时,外用剂量不得超过100 μg,每日内服剂量不超过1 μg,每年使用时间不得超过6周。2008年,英国食品、消费品和环境化学品毒性委员会指出[27],PAs暴露量超过0.007 μg/kg就可能增加患癌症的风险。
药典2020年版收录含PAs的中药材(不含饮片)共8种。通过检索常用的现行标准,发现含此8种中药材的中成药220种,但药典收录的种类并不多(仅40种),其余主要被收载于《卫生部药品标准》(129种)、《国家中成药标准汇编》(44种),少数被收录于《新药转正标准》。上述220味中成药功效多为清热解毒,包括含千里光、紫草、返魂草、一点红、佩兰等处方;还有以款冬花、野马追、滇紫草为主的止咳化痰处方。这些中成药涉及多种剂型(图3),177种(80.5%)为口服药物,包括丸剂、片剂、胶囊剂、颗粒剂、散剂、糖浆剂、煎膏剂、合剂、酒剂、冲剂等;43种(19.5%)为外用制剂,包括软膏剂、油剂、栓剂、橡胶膏剂、酊剂、气雾剂、洗剂、膏药剂等,含紫草的外用中成药有35种,含千里光、一点红的分别为5种和8种。此外,款冬花和紫草涉及处方最为广泛,且许多均为常用处方药,有些甚至为非处方药,患者可自行购买使用,如紫草软膏。且许多中成药服用对象为儿童或者婴儿,如小儿肺咳颗粒、小儿久嗽丸、小儿咳宁糖浆、小儿暑感宁糖浆、小儿肺热平胶囊、小儿羚羊散和小儿宝泰康颗粒,对于儿童用药安全提出了新的问题。
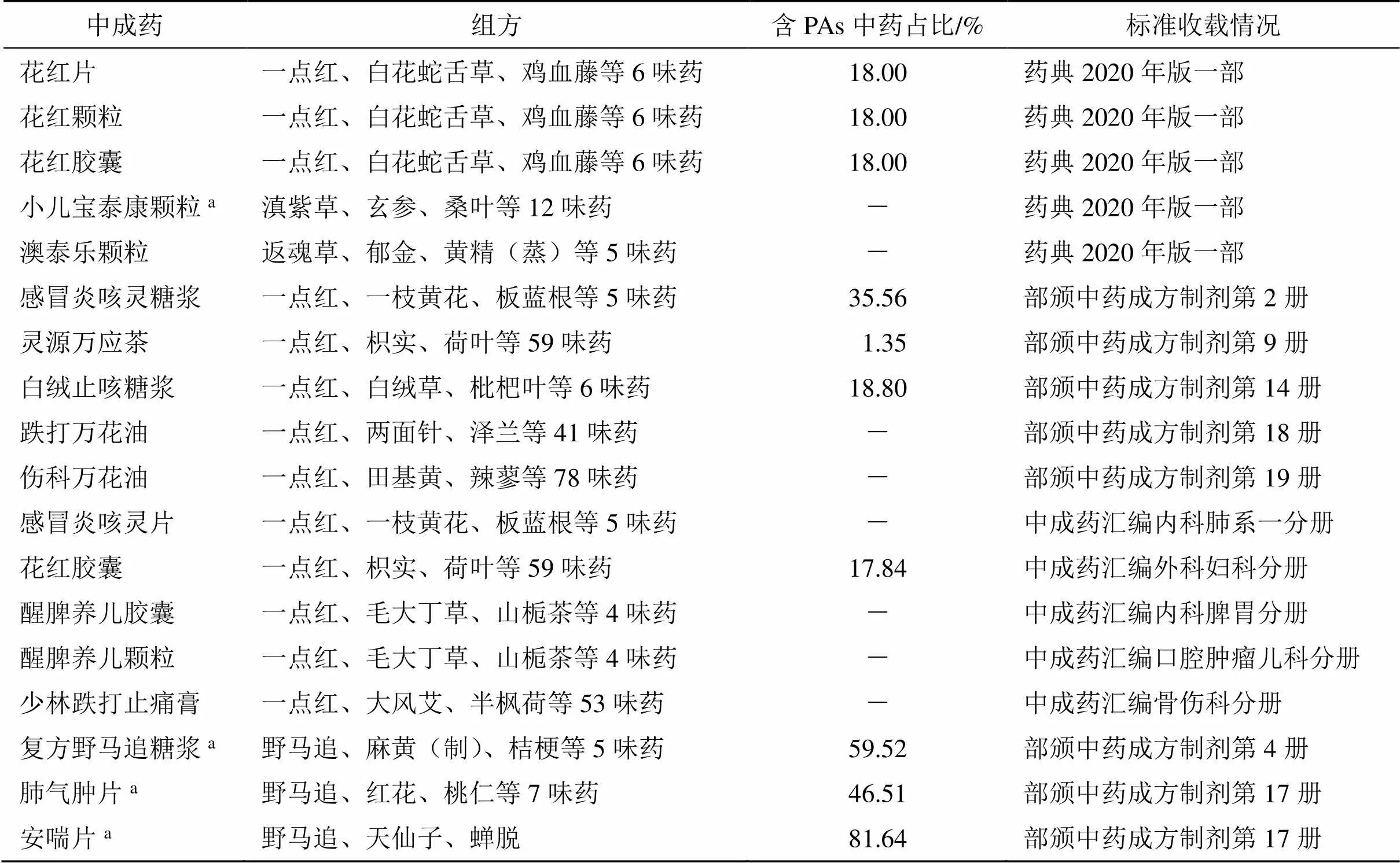
表6 其他中成药
a-滇紫草、野马追同属多种植物含有HPAs,推测其亦含HPAs
a-HPAs are identified in herbs from the same families

图3 含PAs中成药的剂型
药典规定了千里光药材中阿多尼弗林碱的限量。但是我国对于其他药材及中成药中PAs的限量均无明确规定,且关于这些中成药所含PAs含量的研究报道也极为少见。熊芬等[28]曾分析了千柏鼻炎片等14种在市场上流通的含千里光的制剂,结果在8种制剂中均检测到了阿多尼弗林碱,尤以千柏鼻炎片、千柏鼻炎胶囊中含量最高;且同一复方不同批次间含量差异较大,质量分数最高为156.1 μg/g,按该批制剂推荐用量每日摄入阿多尼弗林碱最高达1 030.26 μg,提示服用含千里光的制剂需注意其用药安全,对复方中千里光药材含量较高的制剂尤其应该注意阿多尼弗林碱的限量检查,以保障其临床用药安全。该研究也提示应进一步加强对此类中成药中PAs的检测分析,对于建立此类中成药的安全标准将具有更好的指导与借鉴意义。
不同中药所含PAs不同,可能导致中药及其制剂的毒性差异巨大,不可一概而论。因此,建议有关部门加强对含有PAs的中药与中成药的管控,发布含PAs中药与中成药的名录,并开展关于这些中药与中成药的化学成分检测、药理、毒理实验,且还应根据中药的七情配伍、炮制减毒、辨证论治等,综合评估这些中成药的安全性和有效性,并建立含PAs中药与中成药的安全标准,以保证用药安全,保障人类健康。
利益冲突 所有作者均声明不存在利益冲突
[1] Smith L W, Culvenor C C. Plant sources of hepatotoxic pyrrolizidine alkaloids [J]., 1981, 44(2): 129-152.
[2] Edgar J A, Roeder E, Molyneux R J. Honey from plants containing pyrrolizidine alkaloids: A potential threat to health [J]., 2002, 50(10): 2719-2730.
[3] Dickinson J O, Cooke M P, King R R,. Milk transfer of pyrrolizidine alkoloids in cattle [J]., 1976, 169(11): 1192-1196.
[4] Betz J M, Eppley R M, Taylor W C,. Determination of pyrrolizidine alkaloids in commercial comfrey products (sp.) [J]., 1994, 83(5): 649-653.
[5] International Program on Chemical Safety, International Program on Chemical Safety.[M]. Geneva: World Health Organization, 1988.
[6] 中华医学会消化病学分会肝胆疾病协作组. 吡咯生物碱相关肝窦阻塞综合征诊断和治疗专家共识意见(2017年, 南京) [J]. 中华消化杂志, 2017, 37(8): 513-522.
[7] Roeder E. Medicinal plants in China containing pyrrolizidine alkaloids [J]., 2000, 55(10): 711-726.
[8] 汤俊, 服部征雄. 《中国药典》含吡咯里西啶生物碱的中药品种与用药安全 [J]. 药学学报, 2011, 46(7): 762-772.
[9] Purchase R. Chemistry and toxicology of pyrrolizidine alkaloids [J]., 1987, 25(2): 204-205.
[10] Fang L X, Xiong A Z, Yang X,. Mass-spectrometry-directed analysis and purification of pyrrolizidine alkaloid/isomers in[J]., 2014, 37(15): 2032-2038.
[11] Fu P P, Xia Q S, Lin G,. Pyrrolizidine alkaloids: Genotoxicity, metabolism enzymes, metabolic activation, and mechanisms [J]., 2004, 36(1): 1-55.
[12] Ji L L, Zhang M, Sheng Y C,. Pyrrolizidine alkaloid clivorine induces apoptosis in human normal liver L-02 cells and reduces the expression of p53 protein [J]., 2005, 19(1): 41-46.
[13] Ji L L, Zhao X G, Chen L,. Pyrrolizidine alkaloid clivorine inhibits human normal liver L-02 cells growth and activates p38 mitogen-activated protein kinase in L-02 cells [J]., 2002, 40(12): 1685-1690.
[14] Liang Q N, Liu T Y, Ji L L,. Pyrrolizidine alkaloid clivorine-induced oxidative stress injury in human normal liver L-02 cells [J]., 2009, 3(6): 247-251.
[15] Chou M W, Wang Y P, Yan J,. Riddelliine N-oxide is a phytochemical and mammalian metabolite with genotoxic activity that is comparable to the parent pyrrolizidine alkaloid riddelliine [J]., 2003, 145(3): 239-247.
[16] Xia Q, Zhao Y, Lin G,. Pyrrolizidine alkaloid-protein adducts: Potential non-invasive biomarkers of pyrrolizidine alkaloid-induced liver toxicity and exposure [J]., 2016, 29(8): 1282-1292.
[17] Xiong A Z, Fang L X, Yang X,. An application of target profiling analyses in the hepatotoxicity assessment of herbal medicines: Comparative characteristic fingerprint and bile acid profiling ofL. andBuch.-Ham [J]., 2014, 406(29): 7715-7727.
[18] Zhang F, Wang C H, Wang W,. Quantitative analysis by HPLC-MS2of the pyrrolizidine alkaloid adonifoline in[J]., 2008, 19(1): 25-31.
[19] 熊爱珍, 杨莉, 杨雪晶, 等. UPLC-MS同时测定千里光和欧洲千里光中阿多尼弗林碱和千里光碱的含量 [J]. 中国中药杂志, 2011, 36(6): 702-705.
[20] 濮社班, 徐德然, 张勉, 等. 中药款冬中肝毒吡咯里西啶生物碱的LC/MSn检测 [J]. 中国天然药物, 2004, 2(5): 293-297.
[21] Liu K, Roeder E, Chen T H L,. Pyrrolizidine alkaloids fromfortune [J]., 1992, 31(7): 2573-2574.
[22] Röder E, Rengel-Mayer B. Pyrrolizidine alkaloids from[J]., 1993, 59(2): 192.
[23] Cheng D, Röder E. Pyrrolizidine alkaloids from[J]., 1986(6): 484-486.
[24] Asada Y, Furuya T, Shiro M,. Senecicannabine, a new pyrrolizidine alkaloid from[J]., 1982, 23(2): 189-192.
[25] 马鸿雁, 杨莉, 王长虹, 等. 单麻叶千里光中肝毒吡咯里西啶生物碱的分离与鉴定 [J]. 中国中药杂志, 2011, 36(2): 166-168.
[26] Schrenk D, Gao L, Lin G,. Pyrrolizidine alkaloids in food and phytomedicine: Occurrence, exposure, toxicity, mechanisms, and risk assessment-A review [J]., 2020, 136: 111107.
[27] Ma C H, Liu Y, Zhu L,. Determination and regulation of hepatotoxic pyrrolizidine alkaloids in food: A critical review of recent research [J]., 2018, 119: 50-60.
[28] 熊芬, 姜凯元, 熊爱珍, 等. 含千里光中药制剂中肝毒性成分阿多尼弗林碱的含量分析 [J]. 中国中药杂志, 2020, 45(1): 92-97.
Risk evaluation of Chinese patent medicine containing pyrrolizidine alkaloids
XIONG Fen1, GU Li-hua1, YANG Li1, 2, XIONG Ai-zhen1, 2, SONG Zong-hua3, WANG Zheng-tao1, 2
1. MOE Key Laboratory for Standardization of Chinese Medicines and SATCM Key Laboratory for New Resources and Quality Evaluation of Chinese Medicines, Institute of Chinese Materia Medica, Shanghai University of Traditional Chinese Medicine, Shanghai 201203, China 2. Shanghai R&D Center for Standardization of Traditional Chinese Medicines, Shanghai 201203, China 3. Chinese Pharmacopoeia Committee, Beijing 100061, China
Pyrrolizidine alkaloids (PAs) are a kind of alkaloids with bicyclic pyrrolidine rings. Most PAs are also called hepatotoxic PAs (HPAs) due to its highly hepatotoxicity. PAs are widely distributed in many medicinal plants from Compositae, Leguminosae, and BoraginaceaFamilies. Totally, eight crude drugs, such as Qianliguang (), Kuandonghua (), Peilan (), Zicao (), as well, and dozens of Chinese patent medicines (CPMs) prepared with these crude drugs have been officially recorded in the, 2020 edition. In addition, they are also contained in about 200 CPMs that are recorded in other monographs such as theand. However, there is no safety limitation standard of PAs in these crud drugs and CPMs, except for. Their potential threats to human health may be underestimated in clinic. For this reason, a systematical investigation was conducted to get the information about these PA-containing CPMs for a better understanding of the drugs’ safety in clinic for human health.
pyrrolizidine alkaloid;; Chinese materia medica; Chinese patent medicine; safety
R285
A
0253 - 2670(2021)17 - 5389 - 12
10.7501/j.issn.0253-2670.2021.17.031
2021-08-02
国家自然科学基金资助项目(81603384);上海市自然科学基金资助项目(20ZR1473300);上海市人才发展资金(2020099);上海中医药大学“杏林学者”计划(B1-GY21-409-04-06)
熊 芬(1994—),女,硕士,研究方向为中药分析。Tel: (021)51322506 E-mail: 1483352772@qq.com
王峥涛,沈阳药科大学1984级生药学硕士,现任上海中医药大学首席教授、中药研究所所长、中药标准化教育部重点实验室主任,1998年度国家杰出青年基金获得者。E-mail: ztwang@shutcm.edu.cn
熊爱珍,硕士生导师,主要从事中药安全性评价。E-mail: a.z.xiong@hotmail.com
[责任编辑 潘明佳]
