MBA交联羧甲基淀粉的制备及其絮凝性能研究
2021-09-03韦爱芬朱鸿雁韦莉敏解铁权
韦爱芬,朱鸿雁,刘 洋,韦莉敏,解铁权
(1.广西民族大学化学化工学院,广西 南宁 530008;2.林产化学与工程国家民委重点实验室,广西林产化学与工程重点实验室,广西林产化学与工程协同创新中心,广西 南宁 530008)
处理废水的方法很多,其中絮凝沉淀法是应用最广泛且最经济的方法[1]。絮凝剂是絮凝法水处理技术的核心[2-4],常用的絮凝剂有无机絮凝剂和人工合成有机高分子絮凝剂。无机絮凝剂存在用量大、稳定性差、絮体小、浮渣量大、后处理困难以及残留有毒副作用的金属离子等缺点[5]。人工合成有机高分子絮凝剂的价格昂贵,难降解,会残留单体而导致二次污染,限制了其在水处理行业的长期使用[6]。近年来发展起来的微生物絮凝剂因培养和提纯费用高、产量较低等原因,难以推广应用[7-8]。因此,开发价格低廉、安全无毒、环境友好的新型絮凝剂迫在眉睫。淀粉是天然有机高分子化合物,对淀粉进行醚化、酯化、交联、接枝等化学改性,在淀粉分子结构中引入特殊功能基团,可制得生物降解性好、无二次污染的改性淀粉絮凝剂。
目前改性淀粉絮凝剂主要以阳离子型为主[9],其中以阳离子型淀粉接枝丙烯酰胺等合成的高分子单体改性絮凝剂居多。淀粉接枝改性絮凝剂大多用淀粉接枝数倍于自身质量的单体而制得,此类絮凝剂兼有天然高分子和合成高分子的双重性能,有很好的絮凝效果,但游离有毒单体(如丙烯酰胺等)的释放以及污染的潜在可能不容忽视。因此,少用或不用合成高分子单体的改性淀粉絮凝剂,将成为淀粉絮凝剂开发应用的方向。羧甲基淀粉(Carboxymethyl starch,CMS)是淀粉在碱性条件下与氯乙酸或其钠盐发生醚化反应而制得的阴离子淀粉醚[10],是冷水可溶的聚电解质,具有大分子溶液增稠、保水、粘附性及成膜性,也具有羧基所固有的螯合、离子交换及多聚阴离子的絮凝作用[11]。但羧甲基淀粉糊液的耐酸、耐盐及耐剪切能力较低,限制了其在某些领域的应用。交联淀粉具有多维网状结构,具有黏度高、耐热、耐酸和耐酶解等优良特性,但不溶于冷水。对天然淀粉进行羧甲基化和交联的双重改性,可制得兼具羧甲基淀粉和交联淀粉优良特性的复合改性淀粉,可用作水处理絮凝剂。
本文以木薯淀粉为原料,用氯乙酸进行羧甲基化,用N,N′-亚甲基双丙烯酰胺(MBA)进行交联,采用“一步法”合成了交联羧甲基淀粉(Cross-linked carboxymethyl starch,CCMS)。通过FI-RT、SEM对产物结构进行了表征,研究了产物的耐酸碱和耐剪切等理化性质,并以高岭土悬浮液为模拟水样,测试了产物的絮凝性能,旨在为改性淀粉絮凝剂的研究开发与应用提供一定的基础参考。
1 实验部分
1.1 试剂与仪器
木薯淀粉、酒精、氢氧化钠、N,N′-亚甲基双丙烯酰胺(工业级);氯乙酸、乙酸、盐酸、乙酸、乙醇、羟基乙酸、铬变酸、浓硫酸、乙酸铵、乙二醇等(均为分析纯)。
DHG-9000型电热鼓风干燥箱,HH-2型恒温水浴锅,DSX-90型数显搅拌机,DV-3T流变仪,PHS-3C型pH计,723型可见分光光度计,Magna-IR550型傅里叶变换红外光谱仪,SUPRA-55-Sapphire场发射扫描电子显微镜等。
1.2 实验方法
1.2.1 “一步法” 制备交联羧甲基淀粉(CCMS)
称取250g木薯淀粉置于三口烧瓶中, 加酒精水溶液(酒精与水体积比为8∶1),配制成质量分数为25%的淀粉乳,在搅拌状态下加入质量分数50%(相对于淀粉质量)的氯乙酸,酸化20min,再加入质量分数为40%(相对于淀粉质量)的氢氧化钠,在冷凝回流状态下,将反应液加热至70℃,进行羧甲基化反应4h。取样,在剩余反应液中加入MBA,进行交联反应0.5h。取样,之后每隔0.5h取样1次,直至交联反应时间达2.5h,结束反应。每次取出的样品均用乙酸调节pH至6.5~7.5,用乙醇洗去未反应的试剂,烘干,得到交联羧甲基淀粉(CCMS)。调整MBA用量分别为0.5%、1.0%、2.5%、4.0%、5.0%、6.0%(相对于淀粉质量,下同),可制得性质不同的CCMS。其中,羧甲基化反应4h制得的是羧甲基淀粉(CMS)。
1.2.2 红外光谱表征
采用KBr压片法,用傅里叶变换红外光谱仪测定淀粉样品的红外光谱图,扫描波长范围500 cm-1~4000 cm-1。
1.2.3 扫描电镜表征
取适量干燥的淀粉样品,均匀涂抹在粘有双面导电胶的铜片上,经喷铂处理后在扫描电镜仪上进行观察和拍摄。
1.2.4 黏度的测定
称取10g淀粉样品(以干基计),加入乙醇水溶液(乙醇与水体积比为1∶9),配制成质量分数为2%的淀粉糊液,用DV-3T 流变仪,在60r·min-1的转速下,测定淀粉糊液在25℃时的黏度。
1.2.5 耐酸碱性能的测定
参照1.2.4的方法,用盐酸或氢氧化钠溶液分别调节淀粉糊液的pH为3、4、5、6、7、9、11、12,测定糊液黏度。淀粉糊液在酸性或碱性条件下具有较高的黏度,则说明其耐酸能力或耐碱能力较强。
1.2.6 耐剪切性能的测定
参照1.2.4的方法,分别在转速为60、80、100、120、140、160、180、200 r·min-1时 测 定 淀 粉 糊 液的黏度,分析黏度随转速变化的规律,并计算200r·min-1的黏度与60 r·min-1黏度的比值。比值越大,则说明耐剪切性能越好。
1.2.7 絮凝性能测试
将1g高岭土放入1L自来水中,在200 r·min-1转速下搅拌5min,得到质量浓度为1g·L-1的模拟水样。量取100mL模拟水样,加入淀粉絮凝剂CCMS,在200 r·min-1转速下搅拌5min,再静置絮凝一段时间,取上层清液,用分光光度计测定上清液的透光率。根据预先拟合得到的透光率-浓度曲线方程,计算上清液中高岭土的质量浓度,再计算高岭土的去除率。上清液的透光率越高,高岭土的去除率越大,说明淀粉的絮凝性能越好。
2 结果与讨论
2.1 结构表征
2.1.1 红外光谱分析
图1为CMS和CCMS的红外光谱图。CMS在1609 cm-1和1422 cm-1附近出现了羧酸盐C=O的特征吸收峰[1,12]。CCMS曲线中,3411 cm-1是-OH伸缩振动与N-H伸缩振动的叠加,特征吸收峰较CMS有所增强且向高频区位移。受MBA酰胺的C=O、C-N的伸缩振动以及N-H弯曲振动的影响,CCMS在1608 cm-1和1422 cm-1附近的特征吸收峰,较CMS略有增强和位移。以上分析表明CCMS分子链上含有酰胺基和羧基,说明已成功制备了交联羧甲基淀粉。

图1 CMS和CCMS的红外光谱图Fig.1 Infrared spectra of CMS and CCMS
2.1.2 扫描电子显微镜分析
放大3000倍拍摄的CMS、CCMS的SEM照片分别如图2(a)、(b)所示。可以看出,CMS颗粒表面有小凸起、凹陷和轻微裂纹,有小颗粒脱落的趋势;CCMS颗粒的表面粗糙,形貌结构杂乱,有聚集鳞片状、断裂和凹陷,小颗粒粘附于大颗粒,具有一定的网状结构,比表面积增大。CCMS这种独特的形貌结构,有利于提高淀粉对细小颗粒的吸附“架桥”和絮凝能力。

图2 CMS和CCMS的SEM照片Fig.2 SEM images of CMS and CCMS
2.2 CCMS的理化性质
2.2.1 CCMS黏度与MBA用量、交联反应时间的关系
按1.2.1的方法,改变MBA用量分别为0.5%、1.0%、2.5%、4.0%、5.0%、6.0%(相对于淀粉质量,下同),研究CCMS黏度与MBA用量、交联反应时间之间的关系,结果见图3。由图3可知,MBA用量为0.5%时,CCMS黏度随交联反应时间的延长而不断增大;MBA用量在1.0%~6.0%范围内时,随交联反应时间的延长,CCMS黏度先增大后减小。其中,交联反应时间为1.5h、MBA用量为5.0%的淀粉黏度最大,MBA用量为2.5%的淀粉黏度次之。交联反应时间超过1.5h后,因交联过度,淀粉黏度急剧降低。由此可见只有适度交联才能显著提高淀粉的黏度。这是因为交联键的引入使得淀粉分子形成了新的网状结构,分子链长度增加,糊化过程中的空间位阻增加,分子运动受限,因而黏度增大;当交联剂用量过大、反应时间过长时,大量交联键的引入,使得淀粉分子之间建立起了更加紧密的化学架桥,颗粒结构的强度过大,水分子在淀粉颗粒内部的渗透受阻,抑制了淀粉颗粒的膨胀糊化,黏度因此降低。

图3 CCMS黏度与MBA用量、交联反应时间的关系曲线Fig.3 The relation curve of CCMS viscosity, MBA dosage and crosslinking reaction time
2.2.2 MBA用量对CCMS糊液耐酸碱性能的影响
淀粉糊液的耐酸碱能力是淀粉理化性质的一项重要指标,直接影响淀粉应用效果的优劣。按1.2.1的方法,固定交联反应时间为1.5h,改变MBA用量分 别 为0.5%、1.0%、2.5%、4.0%、5.0%、6.0%,研 究MBA用量对CCMS糊液耐酸碱性能的影响,结果见图4。由图4可知,随着pH增大,CCMS黏度先增大后减小;当pH=6~7、MBA用量为0.5%~2.5%时,CCMS的黏度均达到较高值;pH=3~9、MBA用量为2.5%时,CCMS的整体黏度较高,且pH=7时黏度达到最高。当pH=11、MBA用量为4.0%~6.0%时,CCMS黏度均达到最高值。由此可见,适度的MBA交联,可使淀粉在酸碱性条件均保持较高的黏度,即淀粉糊液具有较好的耐酸碱性能。这是因为MBA分子中的2个活泼反应性官能团能在淀粉分子间起架桥作用,使得多个淀粉分子相互键合,交联成立体网状结构。交联键的存在使得CCMS具有较强的空间位阻,阻碍了外来离子对分子内糖苷键的进攻[13],从而提高了淀粉糊液的稳定性。本实验中,MBA用量为2.5%的CCMS,在较宽的pH范围内具有较高的黏度,且耐酸碱性能力较强,因而大大拓宽了CCMS的应用范围。

图4 MBA用量对CCMS耐酸碱性能的影响Fig.4 Effect of MBA dosage on acid and alkali resistance of CCMS
2.2.3 MBA用量对CCMS糊液耐剪切性能的影响
按1.2.1的方法,固定交联反应时间为1.5h,改变MBA用量分别为0.5%、1.0%、2.5%、4.0%、5.0%、6.0%,研究MBA用量对CCMS糊液耐剪切性能的影响,MBA用量、剪切速率与CCMS黏度之间的关系如图5所示。由图5可知,CCMS黏度随剪切速率的增大而减小,呈现“剪切稀化”特性。这是因为在淀粉凝胶体系中,分子间或分子内的作用力在较高的剪切速率下更容易被破坏[14]。计算图5中的各曲线在200 r·min-1的黏度与60 r·min-1黏度的比值百分数,考察耐剪切稳定性,结果如图6所示。由图6可知,随着MBA用量的增大,CCMS糊液的耐剪切稳定性先提高后降低,MBA用量为2.5%时,糊液的耐剪切性能最佳。可见,适度的MBA交联有效改善了淀粉糊液的耐剪切能力。这是因为交联改性在淀粉分子间引入了新的化学键,淀粉分子间以共价键形成了网状结构。分子间的缠结点增多,氢键作用得到增强,分子不易发生定向排列,淀粉糊液对机械搅拌产生的剪切力的敏感性降低,因而黏度较为稳定。

图5 CCMS黏度与MBA用量、剪切速率的关系曲线Fig.5 The relation curve of CCMS viscosity, MBA dosage and shear rate
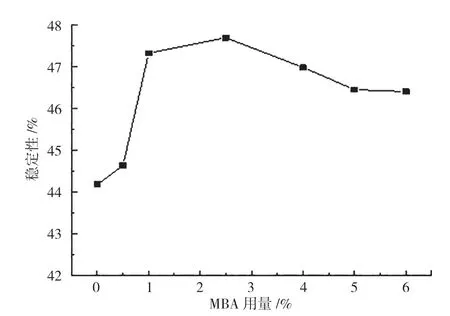
图6 MBA用量对CCMS耐剪切稳定性的影响Fig.6 Effect of MBA dosage on shear stability of CCMS
2.3 CCMS的絮凝性能
以质量浓度为1g·L-1的高岭土悬浮液为模拟水样,选取上述黏度适中、耐酸碱、耐剪切等综合性能最优的CCMS(MBA用量为2.5%、交联反应时间为1.5h)作为絮凝剂,研究CCMS用量、模拟水样pH、絮凝时间对絮凝效果的影响。
2.3.1 CCMS用量对絮凝效果的影响
以质量浓度为1g·L-1的高岭土悬浮液为模拟水样(测得pH=7.2),固定絮凝时间为30 min,改变CCMS用量,考察CCMS用量对絮凝效果的影响,CCMS在模拟水样中的质量浓度与透光率和去除率之间的关系如图 7 所示。由图7可知,较低的CCMS用量就能使模拟水样的透光率和高岭土的去除率得到迅速提高,达到较好的絮凝效果。在较宽的CCMS质量浓度范围(20~120 mg·L-1)内,水样的透光率和高岭土的去除率维持较高的水平。CCMS质量浓度大于120 mg·L-1后,透光率和去除率明显下降。这主要是因为CCMS属于阴离子型高分子长链化合物,分子内链段间电荷的排斥,有利于链扩展及絮凝能力的提高。当CCMS质量浓度较低时,吸附在高岭土颗粒表面上的淀粉高分子长链,会同时吸附另一个颗粒,通过“架桥”方式将多个颗粒絮聚,小颗粒聚集成网络絮体,从而提高了絮凝效果。羧甲基淀粉具有稳定性作用[10],CCMS因带有羧甲基基团,同样具有稳定性作用。当CCMS质量浓度过大时,吸附在颗粒表面的淀粉大分子对颗粒起稳定保护作用,颗粒之间的排斥作用增大,淀粉“桥连”絮凝的颗粒减少, 甚至有絮体重新分散,降低了絮凝效果,因此存在一个较佳的絮凝剂质量浓度范围。

图7 CCMS质量浓度与透光率、去除率的关系曲线Fig.7 The relation curve of mass concentration of CCMS with light transmittance and removal rate
2.3.2 pH对絮凝效果的影响
固定絮凝时间为30min,CCMS质量浓度分别为20mg·L-1和120mg·L-1,用HCl或NaOH调节质量浓度为1g·L-1的高岭土悬浮液模拟水样的pH,考察pH对絮凝效果的影响,pH、CCMS质量浓度与透光率及去除率之间的关系如图8所示。由图8可知,当模拟水样的pH=2时,透光率和高岭土去除率均为最大,絮凝效果最佳。随pH升高,透光率和去除率均逐渐降低,絮凝效果降低;在pH=5~7时,透光率和去除率曲线的变化较平缓,CCMS质量浓度为20 mg·L-1的絮凝效果,优于CCMS质量浓度为120 mg·L-1的效果。当模拟水样的pH=5、CCMS质量浓度为20 mg·L-1时,水样透光率为60.3%,高岭土去除率为63.4%。这主要是因为CCMS分子链上带有酰胺基和羧基,絮凝机理兼具“架桥”和“电中和”。当模拟水样为酸性时,CCMS中的羧基质子化较高,水样中的氢离子可部分中和高岭土颗粒表面的负电荷,CCMS捕捉吸附颗粒的能力增强,从而提高了絮凝效果。随着模拟水样的pH升高,伴随高岭土颗粒表面的负电荷增加,同时CCMS解离产生了负电荷,颗粒间的排斥力增大,絮凝剂的“架桥”能力受限,导致絮凝效果降低。

图8 pH、CCMS质量浓度与透光率、去除率的关系曲线Fig.8 The relation curve of pH, CCMS mass concentration and light transmittance and removal rate
2.3.3 絮凝时间对絮凝效果的影响
从2.3.2的实验结果看,低pH有利于提高絮凝效果,但为了避免强酸性溶液的二次处理,本实验对pH=5~7、CCMS质量浓度为20mg·L-1、质量浓度为1g·L-1的高岭土模拟水样进行实验,考察絮凝时间对絮凝效果的影响,结果见图9。由图9可知,在pH=5~7范围内,水样透光率和高岭土去除率随絮凝时间的延长而快速提高。当模拟水样的pH=5、絮凝时间为30min时,透光率为60.3%,去除率为63.4%,继续延长絮凝时间至120 min,透光率可达84.0%,去除率可达97.1%,可见CCMS的絮凝沉降速度较快,絮凝效果较好。这是因为CCMS分子链上半刚性的淀粉大分子骨架、羧甲基及酰胺基的协同作用,以及其独特的交联网状结构,增强了吸附“架桥”能力,使得细小颗粒聚集成大絮体,加速了沉降,增强了絮凝效果。
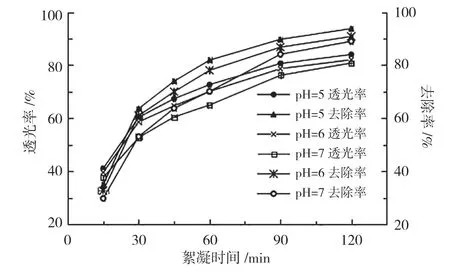
图9 絮凝时间与透光率、去除率的关系曲线Fig.9 The relation curve of flocculation time with light transmittance and removal rate
3 结论
1)FT-IR分析结果证明CCMS分子链上含有酰胺基和羧基,表明成功制备了MBA交联羧甲基淀粉。SEM分析结果表明,MBA交联羧甲基淀粉颗粒的表面结构粗糙、断裂、凹陷,聚集鳞片状,具有一定的网状结构,比表面积较大。
2)“一步法”合成的CCMS兼具羧甲基淀粉和交联淀粉的双重优点,产品黏度高,耐酸碱和耐剪切性能优良。淀粉分子链上酰胺基和羧甲基的协同作用,以及淀粉颗粒表面的粗糙、鳞片、断裂、凹陷的形貌结构,更有利于对细小颗粒的吸附“架桥”和絮凝。
3)以质量浓度为1g·L-1的高岭土悬浊液为模拟水样,测试了CCMS的絮凝性能。结果表明,将MBA用量为2.5%、交联反应时间为1.5h时制得的CCMS作为絮凝剂,在酸性和中性条件下可获得较好的絮凝效果。当模拟水样pH=5、CCMS质量浓度为20mg·L-1时,絮凝30min,水样的透光率为60.3%,高岭土去除率为63.4%;絮凝120 min,水样的透光率可达84.0%,高岭土去除率可达97.1%。
4)本文用少量的交联剂MBA制备交联羧甲基淀粉絮凝剂,不仅避免了合成高分子单体的大量引入,还获得了良好的絮凝效果。为进一步研究开发更加绿色环保的改性淀粉絮凝剂提供了实验数据参考。
