利拉鲁肽辅助治疗对糖尿病肾病患者血清炎症因子水平及肾功能的影响
2021-09-03马丽敏
马丽敏
(许昌市人民医院 药剂科,河南 许昌 461000)
糖尿病患者最常见的并发症为糖尿病肾病,随着生活习惯及环境变化,其发病率逐年上升。目前糖尿病肾病已成为糖尿病患者死亡的主要原因之一,其发病与患者糖代谢紊乱引发的非酶糖化、多元醇通路激活、肾脏血流动力学异常、合并高血压、血管活性物质代谢异常及遗传等因素有关。患者早期可出现尿中微量白蛋白的表现,疾病进展后可出现持续的蛋白尿、水肿、高血压、肾小球滤过率降低、肾功能不全等,给患者的日常生活造成严重影响,降低其生活质量。因此,临床治疗目标为控制患者血糖水平、降低胰岛素抵抗、延缓肾功能损伤[1]。利拉鲁肽作为一种长效胰岛素样类似物,主要通过刺激胰岛素的合成与分泌,抑制胰高血糖素,发挥降低血糖、保护肾功能的作用[2]。因此本研究旨在探讨利拉鲁肽辅助治疗对糖尿病肾病患者血清炎症因子水平及肾功能的影响,现将结果报告如下。
1 资料与方法
1.1 一般资料
选取许昌市人民医院2017年11月至2020年1月收治的100 例糖尿病肾病患者,按随机数字表法将其分为对照组(n=50)和观察组(n=50)。对照组男24 例,女26 例;年龄33~66 岁,平均(46.32±5.10)岁;病程5~12年,平均(8.12±2.07)年。观察组男23 例,女27 例;年龄34~65 岁,平均(46.27±5.08)岁;病程6~13年,平均(8.20±2.12)年。两组患者一般资料对比,差异无统计学意义(P>0.05),具有可比性。本研究经本院医学伦理委员会审核通过。
纳入标准:患者均符合中国2 型糖尿病防治指南(2017年版)[3]中糖尿病的诊断标准;经尿蛋白排泄率确诊为糖尿病肾病;患者及家属对本研究知情同意;无精神障碍。
排除标准:妊娠及哺乳期妇女;合并全身器官衰竭;对本次研究药物过敏;其他疾病导致的肾功损伤。
1.2 治疗方法
两组患者均予糖尿病患者常规治疗,如:控制饮食、适当运动及口服降压药。
对照组给予甘精胰岛素(国药准字S20173001,珠海联邦制药股份有限公司)治疗。甘精胰岛素于每晚睡觉前皮下注射,按照0.2 IU/(kg·d)的剂量。
观察组给予利拉鲁肽注射液(注册证号:S20160005,Novo Nordisk A/S)治疗。利拉鲁肽于上腹部皮下注射,初次使用剂量为0.6 mg,1 次/d,连续使用1 周,后增加至1.2 mg/ 次,1 次/d,最大使用剂量小于1.8 mg。
两组均治疗2 个月。
1.3 观察指标
①分别于治疗前后,采用酶联免疫吸附法检测两组血清炎症因子水平,包括白介素-6(IL-6)、白介素-8(IL-8)、肿瘤坏死因子(TNF-α);②比较两组治疗前后尿酸(UA)、尿素氮(BUN)和肾小球滤过率(GFR)、尿白蛋白肌酐比值(UACR)水平;③分别于治疗前后,抽取患者清晨空腹外周静脉血,检测两组糖化血红蛋白(HbA1c)、空腹血糖(FPG)及餐后2 h 血糖(2 h PG)水平。④记录两组治疗期间不良反应发生情况,如:腹泻、皮肤湿疹、头晕、恶心等,并计算不良反应发生率。不良反应发生率=(不良反应人数/ 总人数)×100%
1.4 统计学方法
应用SPSS 20.0 统计学软件分析数据,计量资料以±s表示,行t检验;计数资料以n(%)表示,行χ2检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 两组治疗前后肾功能比较
治疗后两组UA、BUN、GFR、UACR 水平均显著低于治疗前,且观察组显著低于对照组(P<0.05)。见表1。
表1 两组治疗前后肾功能比较(N=50,±s)

表1 两组治疗前后肾功能比较(N=50,±s)
组别UA/(μmol·L-1)tPBUN/(mmol·L-1)tP治疗前治疗后治疗前治疗后对照组380.25±66.90296.33±41.36760.777<0.0016.85±1.025.46±0.6812.601<0.001观察组375.11±75.36238.09±37.101242.151<0.0016.79±0.904.25±0.5323.026<0.001 t 0.3617.4120.3129.924 P 0.719<0.0010.756<0.001
2.2 两组治疗前后血清炎症因子水平比较
治疗后,两组IL-8、IL-6、TNF-α 水平均显著低于治疗前,且观察组显著低于对照组(P<0.05)。见表2。
表2 两组治疗前后血清炎症因子水平比较(N=50,±s)
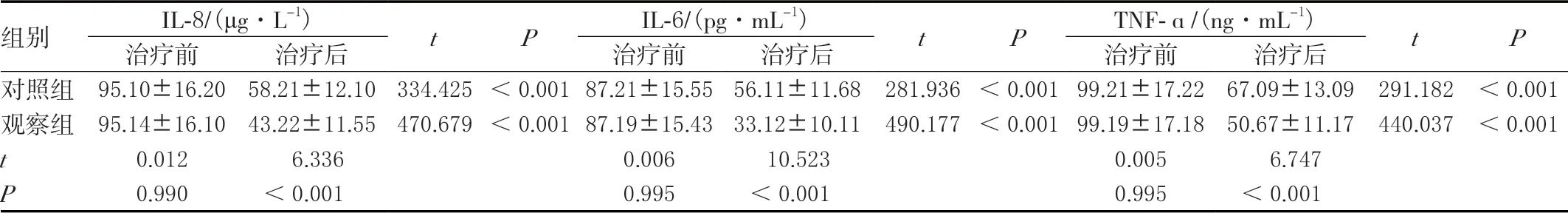
表2 两组治疗前后血清炎症因子水平比较(N=50,±s)
组别IL-8/(μg·L-1)tPIL-6/(pg·mL-1)tPTNF-α/(ng·mL-1)tP治疗前治疗后治疗前治疗后治疗前治疗后对照组 95.10±16.20 58.21±12.10 334.425<0.001 87.21±15.55 56.11±11.68 281.936<0.001 99.21±17.22 67.09±13.09 291.182<0.001观察组 95.14±16.10 43.22±11.55 470.679<0.001 87.19±15.43 33.12±10.11 490.177<0.001 99.19±17.18 50.67±11.17 440.037<0.001 t 0.0126.3360.00610.5230.0056.747 P 0.990<0.0010.995<0.0010.995<0.001
2.3 两组HbA1c 及血糖水平比较
治疗后,两组FPG、2 h PG 及HbA1c 水平均显著低于治疗前,且观察组显著低于对照组(P<0.05)。见表3。
表3 两组HbA1c 及血糖水平比较(N=50,±s)

表3 两组HbA1c 及血糖水平比较(N=50,±s)
组别HbA1c/%tPFPG/(mmol·L-1)tP2 h PG/(mmol·L-1)tP治疗前治疗后治疗前治疗后治疗前治疗后对照组7.84±2.436.59±2.3912.238<0.001 12.18±1.396.77±0.6749.044<0.001 16.79±1.658.34±1.5476.603<0.001观察组7.85±2.425.57±2.4020.669<0.001 12.21±1.305.38±0.6561.917<0.001 16.87±1.666.95±1.1089.929<0.001 t 0.0202.1290.11110.5290.2415.193 P 0.9830.0350.911<0.0010.809<0.001
2.4 两组治疗期间不良反应发生情况比较
两组不良反应发生率差异不显著(P>0.05)。经临床对症处理,患者出院前,不良反应症状均消失。见表4。
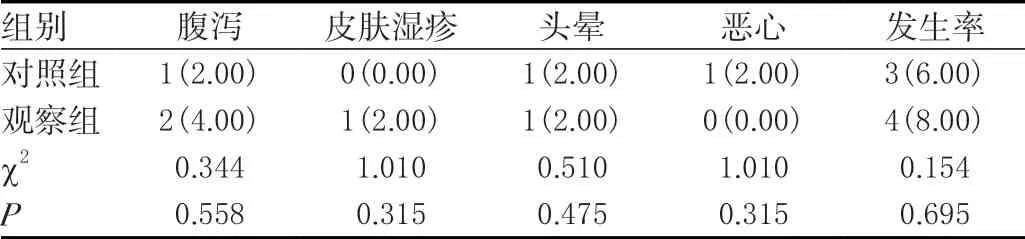
表4 两组治疗期间不良反应发生情况的比较[N=50,n(%)]
3 讨论
遗传、氧化、应激及代谢等是糖尿病肾病常见的发病机制,通过对糖尿病肾病的进一步研究发现[4],先天性免疫功能造成的慢性炎症是主要致病机制,糖尿病患者代谢功能较紊乱,会刺激机体炎症因子水平的分泌,相关研究报道,IL-8、IL-6、TNF-α 在糖尿病肾病的发病中发挥重要作用[5]。因此,降低糖尿病肾病患者炎症因子水平、改善其胰岛功能、有效控制血糖是临床治疗方向。利拉鲁肽作为胰高糖素样肽-1(GLP-1)类似物,可以增加机体环磷酸腺苷水平,与肾系膜细胞直接发生反应,发挥抗炎作用[6]。本次研究中,经治疗后观察组IL-8、IL-6、TNF-α 水平低于对照组。分析其中原因:利拉鲁肽可以抑制氧化酶的活性,延缓由TNF-α 水平升高造成的氧化应激反应,同时以GLP-1 受体为中介,刺激环磷酸腺苷,抑制肾小球系膜发生扩张,从而发挥抗炎作用;利拉鲁肽可通过抑制高糖或核转录因子,减弱IL-6 聚集而引发造成巨噬细胞对肾脏的损伤[7-8]。表明利拉鲁肽可以降低糖尿病肾病患者血清炎症因子水平,对患者预后起积极促进作用。
利拉鲁肽可以抑制胰高血糖素的分泌,发挥降低血糖作用。研究报道[9],肾脏、胰腺部位存在GLP-1,主要参与肾脏纳的排泄及血管紧张素的分泌;在糖尿病肾病患者的治疗中,利拉鲁肽能提高机体抗氧化能力,降低血清炎症因子对肾功能的损伤,保护血管内皮功能。本次研究中,治疗后观察组肾功能及血糖控制水平均优于对照组;表明利拉鲁肽通过降低糖尿病肾病患者炎症因子水平,延缓肾功能损伤。利拉鲁肽皮下注射后药效持续时间较久,具有55%的生物利用率,主要经体外进行排泄。本次研究中,两组不良反应发生率之间差异不显著,表明利拉鲁肽治疗糖尿病肾病安全性较好。
综上,利拉鲁肽可以降低糖尿病肾病患者血清炎症因子水平,改善肾功能,降低血糖,无明显不良反应,安全性较好。
