液相色谱-串联质谱法检测蜂蜜中酰胺醇类药物残留
2021-09-01张居舟
◎ 刘 毅,张居舟
(安徽省食品药品检验研究院,安徽 合肥 230051)
蜂蜜是由蜜蜂采集蜜源植物的花蜜或蜜露后,将其贮存于蜂巢内的巢脾中,并经充分酿造而成。成熟蜂蜜是一种具有浓郁花香味的天然甜物质,含有葡萄糖、氨基酸、矿物质、果糖、酶类和抗氧化物等,是对人体有益的天然食品[1]。随着生活水平的提高,人们对蜂蜜的需求量增长迅速,对其品质和质量的要求也越来越高,蜂蜜中兽药残留也逐渐得到人们关注。
酰胺醇类曾被称为氯霉素类抗生素,是抗生素的常用成分,对革兰氏阴性菌和革兰氏阳性菌有很强的杀灭作用,因其广谱的抗菌性被广泛应用于兽医临床,但该类药物经食物链进入人体后会对人体健康构成威胁[2]。酰胺醇类药物在蜜蜂养殖过程中曾被广泛使用,而农业农村部公告第250号已明确指出氯霉素及其盐、酯禁用于所有食品动物[3]。为保障消费者安全,控制酰胺醇类物质在蜂产品中的使用,有必要建立一种灵敏、高效的酰胺醇类物质残留检测技术。
目前,对蜂蜜等蜂产品中的多种酰胺醇类物质(包括琥珀氯霉素,棕榈氯霉素等)的检测方法并不多,本文建立了一种基于液相色谱-串联质谱法[4]检测蜂蜜中酰胺醇类药物残留的方法。试样经乙酸乙酯提取浓缩后用水溶解,Oasis HLB固相萃取柱净化,液相色谱-串联质谱仪测定,氯霉素用内标法定量,氟苯尼考、甲砜霉素、琥珀氯霉素、棕榈氯霉素用外标法定量[5]。
1 材料与方法
1.1 仪器与试剂
Waters TQ-S超高效液相色谱-串联四极杆质谱联用仪(美国Waters公司)。
氯霉素、甲砜霉素、氟苯尼考、氯霉素琥珀酸钠和氯霉素棕榈酸酯的标准物质,氯霉素氚代内标(氯霉素-D5),均购自德国Dr. Ehrenstorfer公司;甲醇、乙腈、乙酸乙酯(色谱纯,质谱纯),德国Merck公司;HLB固相萃取柱:Oasis HLB 6 mL/200 mg,美国Waters公司。其他所用试剂均为分析纯。
1.2 试验方法
1.2.1 溶液的配制
(1)标准储备溶液的配制。分别称取氯霉素、甲砜霉素、氟苯尼考、氯霉素琥珀酸钠和氯霉素棕榈酸酯标准物质5.0 mg,各自置于10 mL容量瓶中,用乙腈溶解并定容至刻度,配制成500 μg·mL-1的标准储备溶液。准确称取1.0 mg的氯霉素-D5标准物质,置于10 mL容量瓶中,用乙腈溶解定容至刻度配成100 μg·mL-1的内标标准储备溶液。
(2)混合标准溶液中间液的配制。分别准确移取适量的氯霉素、甲砜霉素、氟苯尼考、氯霉素琥珀酸钠和氯霉素棕榈酸酯标准储备溶液,用乙腈稀释成50 μg·mL-1的氯霉素、甲砜霉素和氟苯尼考、氯霉素琥珀酸钠和氯霉素棕榈酸酯混合标准溶液中间液。
(3)氯霉素氚代内标(氯霉素-D5)标准溶液中间液的配制。准确移取适量的氯霉素-D5标准储备溶液,用乙腈配成1 μg·mL-1内标中间溶液。
(4)混合标准工作溶液的配制。分别准确移取混合标准溶液中间液及内标中间溶液,用流动相稀释 成 浓 度 为0.1 ng·mL-1、0.5 ng·mL-1、1.0 ng·mL-1、2.0 ng·mL-1、5.0 ng·mL-1和10.0 ng·mL-1的标准工作溶液。
1.2.2 样品前处理
(1)提取。将蜂蜜置于不超过60 ℃的水浴中振荡,待样品全部融化后搅拌均匀,冷却至室温。称取5 g试样,精确到0.01 g,置于50 mL具塞离心管中,加入氯霉素氚代内标(氯霉素-D5)中间溶液和5 mL水,于涡旋混合器上涡旋混合1 min,使试样完全溶解。加入15 mL乙酸乙酯,在超声波振荡仪上超声振荡10 min,取出试样置于离心机中,以6 000 r·min-1离心5 min,准确吸取上层乙酸乙酯于15 mL离心管中,经氮气吹干,加入5 mL水溶解残渣,待净化。
(2)净化。HLB固相萃取柱分别用5 mL水和5 mL乙腈活化,将待净化液转移到固相萃取柱上,弃去流出液,待溶液完全流出后,依次用5 mL水和5 mL乙腈水溶液淋洗,弃去全部淋出液,抽至近干,用5 mL乙酸乙酯洗脱,收集洗脱液于10 mL离心管中,氮气吹干,用1 mL流动相定容,过0.22 μm有机相滤膜[6],供高效液相色谱-串联质谱仪测定。
1.2.3 液相色谱和质谱条件
(1)液相色谱条件。色谱柱:BEH C18柱,2.1×50 mm,粒径1.7 μm;流动相:A为含0.1%甲醇的水溶液,B为甲醇。流速:0.3 mL·min-1;柱温:35 ℃;进样量:2 μL。液相色谱梯度洗脱程序为:0~0.5 min,90%A;0.5~5.0 min,90%A~10%A;5.00~5.01 min,10%A~90%A;5.01~7.00 min,90%A。
(2)质谱条件。离子源:电喷雾离子源;检测方式:多反应监测;扫描方式:负离子扫描(ESI-);毛细管电压:3.00 kV(ESI-);脱溶剂气温度:440 ℃;脱溶剂气流速:800 L·h-1;锥孔电压:30 V;锥孔气流速:150 L·h-1。
2 结果与分析
2.1 优化质谱条件
在负离子扫描模式下确定目标化合物的母离子和定性、定量离子对并优化质谱的各参数质谱参数优化结果,见表1。
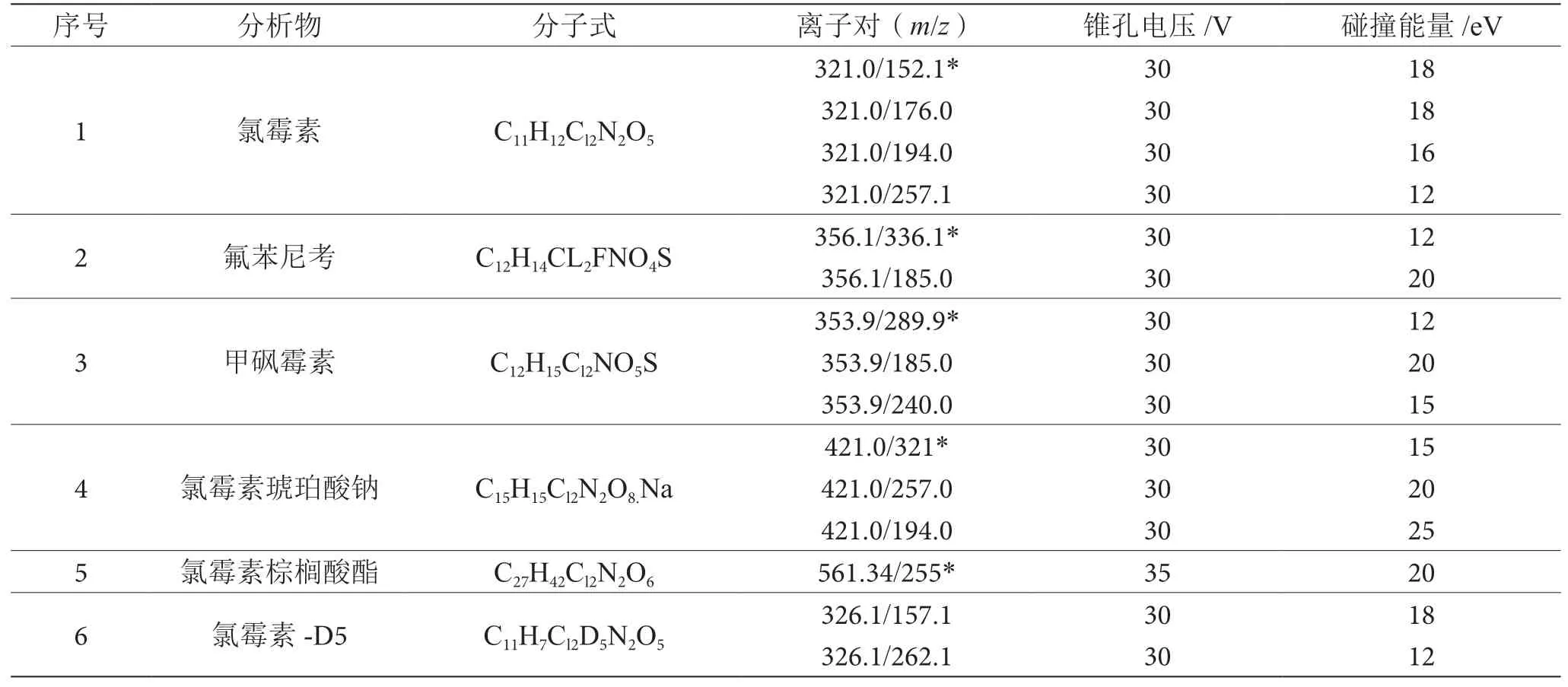
表1 6种化合物质谱参数表
2.2 线性范围与检出限
将5种酰胺醇类药物标准储备液分别配制成0.1 μg·L-1、0.5 μg·L-1、1.0 μg·L-1、2.0 μg·L-1、5.0 μg·L-1和10.0 μg·L-1的溶液进行检测,各类药物的检出限为0.1 μg·kg-1,定 量 限 为1.0 μg·kg-1,线 性 范 围 为0.1~10.0 μg·L-1,对应化合物的线性方程、相关系数见表2,以峰面积为纵坐标,标准溶液质量浓度作为横坐标,绘制标准曲线,各药物线性方程相关系数r>0.995。酰胺醇类物质总离子图见图1,各单一组分离子对图见图2。
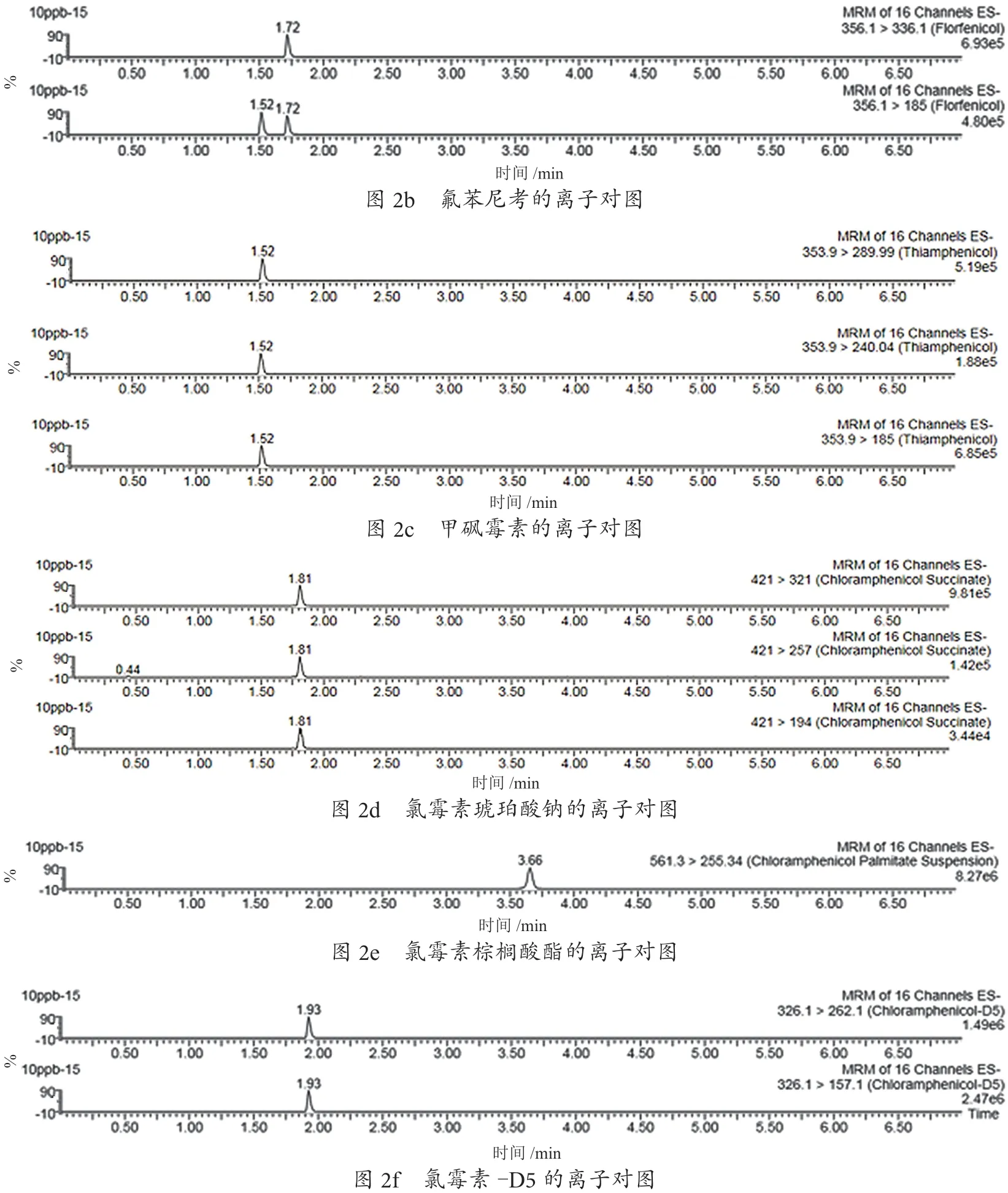
图2 各单一组分离子对图

表2 各类药物的工作曲线及相关系数表

图1 酰胺醇类物质总离子图

2.3 回收率与精密度
选用不含本文5种酰胺醇类药物的阴性蜂蜜样品进行3个浓度水平的加标回收试验[7],每个浓度的加标试验做6次平行。取各药物的加标量、相应的回收率平均值,结果见表3。

表3 阴性蜂蜜样品中酰胺醇类药物的平均回收率和相对标准偏差表(n=6)
2.4 方法实际应用
在合肥商超随机购买15批次蜂蜜样品,用本文方法进行检测,实验结果均为未检出,未发现酰胺醇类阳性样品[8]。
3 结论
本研究建立了高效液相色谱-串联质谱法测定蜂蜜中酰胺醇类药物残留量。5种酰胺醇类药物在0.1~10.0 μg·L-1的浓度范围内线性关系良好,相关系数r均大于0.995;方法检出限为0.1 μg·kg-1。加标水平在0.1~5.0 μg·kg-1范围内,蜂蜜基质中平均回收率在86.3%~101.0%,相对标准偏差RSD≤6.5%。该方法快速、准确、灵敏,可用于测定蜂蜜中酰胺醇类药物残留。
