丝穗金粟兰化学成分及其神经保护活性研究
2021-09-01陈芳有陈志超黄伟明卞玉婷双鹏程李宏焘罗永明
陈芳有,陈志超,黄伟明,卞玉婷,双鹏程,李宏焘,罗永明
江西中医药大学药学院,南昌 330004
金粟兰科(Chloranthaceae)金粟兰属(ChloranthusSwartz)植物有13种和5个变种,主要分布于长江以南各省[1]。金粟兰属植物是江西民间广泛使用的中草药,有着悠久的民间用药历史,野生药材资源丰富[2]。目前从金粟兰属植物中分离得到的化合物主要为倍半萜类、倍半萜二聚体类、二萜类等[3,4],现代药理研究表明金粟兰属植物具有良好的神经保护[5]、抗炎[6]、抗肿瘤[7]等活性。丝穗金粟兰Chloranthusfortunei(A.Gray)Solms-Laub又名四块瓦,为金粟兰属植物,具有祛风、除湿、活血、化瘀等功效[1]。
目前丝穗金粟兰的药效物质基础尚不够清楚,严重制约了该江西特色药用植物资源的开发和利用。为更好的阐明丝穗金粟兰化学物质基础和完善其生物活性研究内容,本实验采用多种色谱分离方法和波谱学方法对丝穗金粟兰95%乙醇提取物进行了化学成分研究,并采用H2O2损伤的PC12细胞模型评估单体化合物的神经细胞保护作用,期望为丝穗金粟兰的药物开发提供参考。
1 材料与方法
1.1 仪器与材料
Varian INOVA-500型核磁共振仪(美国瓦里安公司);JEOL ECZ-400S核磁共振仪(日本电子株式会社);Bruker AVANCE III HD 600 MHz型核磁共振仪(德国布鲁克公司);AB SCIEX Triple TOF5600+质谱仪(美国应用生物系统公司);高效液相色谱仪(Agilent 1100,美国安捷伦公司);旋转蒸发仪(Buchi R3,瑞士步琦公司);Shimadzu LC-6AD型制备液相仪(日本岛津公司);制备液相色谱柱ODS-A C18(20 mm × 250 mm,5 μm,北京绿百草科技有限公司);Sephadex LH-20凝胶(瑞士Amersham Pharmacia Biotech公司);柱色谱硅胶为青岛海洋化工厂产品;HPLC所用试剂(色谱纯乙腈、甲醇)为Merck公司产品;其他试剂为分析纯(西陇科学公司)。
丝穗金粟兰采于江西宜春(2016年11月),由邓可众副教授(江西中医药大学药学院)鉴定为丝穗金粟兰Chloranthusfortunei的全草,标本(20161118)存放在江西中医药大学中药化学教研室。
1.2 提取分离方法
切碎后的丝穗金粟兰(5.0 kg)用乙醇-水(V/V,95∶5)回流提取(50 L×2 h×3),减压浓缩后得丝穗金粟兰总浸膏。将粗提物分散于水中,先用石油醚萃取(2 L×3),得到石油醚部位12 g,然后用三氯甲烷(2 L×3)萃取,再分别采用乙酸乙酯(2 L×3)、正丁醇(2 L×3)萃取。石油醚部位(12 g)经硅胶柱色谱分离,石油醚-乙酸乙酯(V/V,50∶1→1∶1)梯度洗脱,TLC合并后得到流分A1~A7,其中A5部分(1.3 g)经硅胶柱色谱(石油醚-丙酮,9∶1)和制备液相得到化合物1(7 mg)和2(2 mg)。三氯甲烷萃取部分(40 g)经硅胶柱色谱分离,石油醚-丙酮(V/V,1∶0→1∶1)梯度洗脱,经过TLC检测合并之后共得到10个组分(B1~B10)。其中B2(0.9 g)组分经硅胶柱色谱(石油醚-丙酮,15∶1)得化合物3(5 mg);B6组分(5.1 g)经硅胶柱色谱(石油醚-丙酮,5∶1)分离,再经凝胶柱色谱和制备液相分离分别得4(2 mg)、5(13 mg)、6(3 mg)、7(3 mg)。乙酸乙酯萃取物(20 g)经硅胶柱色谱(氯仿-甲醇,V/V,1∶0→2∶1)得到6个组分(C1~C6)。C4(3.2 g)经硅胶柱色谱(氯仿-甲醇,9∶1)、凝胶柱色谱(甲醇)得8(17 mg)和9(20 mg)。C5(2 g)经硅胶柱色谱(氯仿-甲醇,4∶1)得10(8 mg)和14(7 mg)。正丁醇部分(20 g)经硅胶柱色谱分离(氯仿-甲醇,V/V,40∶1→1∶1)得D1~D8。D3部分(1.1 g)经柱色谱(甲醇)、制备液相得到化合物11(6 mg)、12(8 mg)和13(10 mg)。
1.3 神经保护活性研究
神经保护活性实验采用H2O2损伤的PC12细胞模型,CCK8法检测PC12细胞活力。将PC12细胞(1×104个/mL)接种到96孔板,每孔加入细胞混悬液100 μL,每组设3个复孔。给药组加入10 μL化合物(10 μM),阳性药组加入10 μL儿茶素(Catechin,50 μM) ,其他组加入等量的培养基。同时每孔加入双氧水(H2O2,500 μM),24 h后再加入CCK8(5 μL)培养2 h,测定OD值(450 nm处),然后计算细胞存活率[5,8,9]。
2 实验结果
2.1 结构鉴定
化合物1淡黄色油状物;ESI-MS:m/z231 [M+H]+,分子式为C15H18O2。1H NMR(600 MHz,CDCl3)δ:7.08(1H,s,H-12),5.80(1H,dd,J= 18.0,10.8 Hz,H-1),4.99(1H,m,H-3α),4.95(1H,d,J= 17.4 Hz,H-2α),4.94(1H,d,J= 10.8 Hz,H-2β),4.74(1H,br s,H-3β),3.00(1H,s,H-5),2.91(1H,d,J= 17.4 Hz,H-9β),2.76(1H,d,J= 17.4 Hz,H-9α),2.17(3H,d,J= 1.8 Hz,H-13),1.82(3H,dd,J= 1.2,0.6 Hz,H-15),1.17(3H,s,H-14);13C NMR(150 MHz,CDCl3)δ:145.6(C-1),115.7(C-2),113.1(C-3),141.2(C-4),64.2(C-5),194.9(C-6),119.3(C-7),165.6(C-8),33.7(C-9),42.9(C-10),120.2(C-11),139.6(C-12),9.1(C-13),24.9(C-14),25.0(C-15)。经与文献[10]对比鉴定该化合物为curzerenone(结构见图1)。
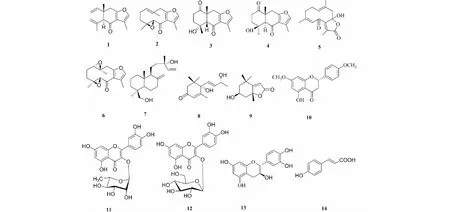
图1 从丝穗金粟兰中分离得到的化合物Fig.1 Compounds isolated from C.fortunei
化合物2白色粉末;ESI-MS:m/z247 [M+H]+,分子式为C15H18O3。1H NMR(600 MHz,CDCl3)δ:7.08(1H,s,H-12),5.48(1H,dd,J= 12.0,4.2 Hz,H-1),3.81(1H,s,H-5),3.75(1H,d,J= 16.2 Hz,H-9β),3.68(1H,d,J= 16.2 Hz,H-9α),2.52(1H,m,H-2α),2.30(1H,m,H-3α),2.23(1H,m,H-2β),2.12(3H,d,J= 1.2 Hz,H-13),1.60(3H,s,H-15),1.34(3H,s,H-14),1.28(1H,m,H-3β);13C NMR(150 MHz,CDCl3)δ:131.4(C-1),24.8(C-2),38.1(C-3),64.1(C-4),66.7(C-5),192.4(C-6),123.4(C-7),157.2(C-8),42.0(C-9),122.4(C-10),131.2(C-11),138.2(C-12),10.4(C-13),15.3(C-14),15.9(C-15)。经与文献[11]对比鉴定该化合物为蓬莪术环氧酮。
化合物3白色无定形粉末;ESI-MS:m/z285 [M+Na]+,分子式为C15H18O4。1H NMR(600 MHz,CDCl3)δ:7.11(1H,s,H-12),3.06(1H,d,J= 18.0 Hz,H-9α),2.93(1H,d,J= 18.0 Hz,H-9β),2.89(1H,s,H-5),2.72(1H,m,H-2β),2.44(1H,m,H-2α),2.19(3H,d,J= 1.2 Hz,H-13),2.02(1H,m,H-3β),1.90(1H,m,H-3α),1.72(3H,s,H-15),1.26(3H,s,H-14);13C NMR(150 MHz,CDCl3)δ:211.1(C-1),34.8(C-2),39.0(C-3),70.4(C-4),62.2(C-5),195.5(C-6),119.1(C-7),165.9(C-8),35.7(C-9),51.2(C-10),119.4(C-11),140.3(C-12),9.1(C-13),20.4(C-14),23.9(C-15)。经与文献[12]对比鉴定该化合物为curcodione。
化合物4无色棱柱状结晶(甲醇);ESI-MS:m/z285 [M+Na]+,分子式为C15H18O4。1H NMR(600 MHz,CDCl3)δ:7.11(1H,s,H-12),3.15(1H,d,J= 18.0 Hz,H-9α),3.11(1H,m,H-2α),2.80(1H,s,H-5),2.78(1H,d,J= 18.0 Hz,H-9β),2.22(1H,m,H-2β),2.18(3H,d,J= 1.2 Hz,H-13),2.16(1H,m,H-3α),1.76(1H,m,H-3β),1.53(3H,s,H-14),1.41(3H,s,H-15);13C NMR(150 MHz,CDCl3)δ:213.0(C-1),33.7(C-2),39.6(C-3),69.8(C-4),60.8(C-5),196.3(C-6),120.4(C-7),165.1(C-8),34.9(C-9),52.7(C-10),118.8(C-11),140.2(C-12),8.9(C-13),30.4(C-14),20.2(C-15)。经与文献[13]对比鉴定该化合物为chlorantene C。
化合物5无色颗粒状结晶(甲醇);ESI-MS:m/z285 [M+Na]+,分子式为C15H18O4。1H NMR(600 MHz,DMSO-d6)δ:6.30(1H,s,H-5),4.87(1H,m,H-1),2.71(1H,d,J= 12.6 Hz,H-9α),2.68(1H,m,H-3α),2.39(1H,d,J= 12.6 Hz,H-9β),2.16(1H,m,H-2α),2.03(1H,m,H-2β),2.01(1H,m,H-3β),1.92(3H,s,H-13),1.85(3H,s,H-14),1.59(3H,s,H-15);13C NMR(150 MHz,DMSO-d6)δ:128.2(C-1),26.0(C-2),29.9(C-3),148.3(C-4),129.5(C-5),191.2(C-6),155.2(C-7),109.8(C-8),48.7(C-9),135.9(C-10),135.9(C-11),170.6(C-12),10.4(C-13),24.9(C-14),18.3(C-15)。经与文献[14]对比鉴定该化合物为(1E,4Z)-8-hydroxy-6-oxogermacra-1(10),4,7(11)-trieno-12,8-lactone。
化合物6淡黄色油状物;ESI-MS:m/z263 [M+H]+,分子式为C15H18O4。1H NMR(600 MHz,CDCl3)δ:7.10(1H,br s,H-12),3.78(1H,s,H-5),3.69(1H,d,J= 16.8 Hz,H-9α),2.93(1H,dd,J= 10.8,2.4 Hz,H-1),2.82(1H,d,J= 16.8 Hz,H-9β),2.41(1H,m,H-3α),2.22(1H,m,H-2α),2.18(3H,d,J= 1.8 Hz,H-13),1.53(1H,m,H-2β),1.49(1H,m,H-3β),1.33(3H,s,H-14),1.16(3H,s,H-15);13C NMR(150 MHz,CDCl3)δ:69.1(C-1),23.8(C-2),36.1(C-3),63.7(C-4),63.3(C-5),189.8(C-6),122.6(C-7),156.1(C-8),39.6(C-9),57.9(C-10),123.4(C-11),138.4(C-12),10.5(C-13),16.8(C-14),15.3(C-15)。经与文献[15]对比鉴定该化合物为zederone epoxide。
化合物7淡黄色油状物;ESI-MS:m/z307 [M+H]+,分子式为C20H34O2。1H NMR(600 MHz,CDCl3)δ:5.89(1H,dd,J= 17.4,10.8 Hz,H-14),5.18(1H,dd,J= 17.4,1.2 Hz,H-15a),5.04(1H,dd,J= 10.8,1.2 Hz,H-15b),4.78(1H,J= 1.2 Hz,H-17a),4.47(1H,d,J= 1.2 Hz,H-17b),3.73(1H,d,J= 10.8 Hz,H-19a),3.36(d,J= 10.8 Hz,H-19b),2.36(1H,m,H-7β),1.91(1H,m,H-7α),1.80(1H,m,H-6β),1.78(1H,m,H-1β),1.77(1H,m,H-12b),1.69(1H,m,H-3β),1.53(1H,m,H-9),1.52(1H,m,H-11a),1.48(2H,m,H-2),1.34(1H,m,H-11b),1.29(1H,m,H-6α),1.25(1H,m,H-12a),1.25(3H,s,H-16),1.24(1H,m,H-5),1.05(1H,m,H-1α),1.03(1H,m,H-3α),0.95(3H,s,H-18),0.63(3H,s,H-20);13C NMR(150 MHz,CDCl3)δ:39.1(C-1),19.1(C-2),35.5(C-3),39.0(C-4),56.4(C-5),24.5(C-6),38.7(C-7),148.3(C-8),57.4(C-9),39.8(C-10),17.9(C-11),41.4(C-12),73.8(C-13),145.2(C-14),111.8(C-15),27.2(C-16),106.8(C-17),28.1(C-18),65.1(C-19),15.4(C-20)。经与文献[16]对比鉴定该化合物为13-epitorulosol。
化合物8淡黄色油状物;ESI-MS:m/z225 [M+H]+,分子式为C13H20O3。1H NMR(500 MHz,CDCl3)δ:5.89(1H,s,H-4),5.85(1H,dd,J= 16.0,5.0 Hz,H-8),5.76(1H,d,J= 16.0 Hz,H-7),4.40(1H,m,H-9),2.43(1H,d,J= 17.0 Hz,H-2α),2.22(1H,d,J= 17.0 Hz,H-2β),1.89(3H,s,H-13),1.28(3H,d,J= 6.0 Hz,H-10),1.06(3H,s,H-12),0.99(3H,s,H-11);13C NMR(125 MHz,CDCl3)δ:41.3(C-1),49.8(C-2),198.6(C-3),124.9(C-4),163.6(C-5),79.2(C-6),129.1(C-7),135.8(C-8),68.1(C-9),23.8(C-10),23.0(C-11),24.2(C-12),19.1(C-13)。经与文献[17]对比鉴定该化合物为vomifoliol。
化合物9淡黄色油状物;ESI-MS:m/z197 [M+H]+,分子式为C11H16O3。1H NMR(500 MHz,CD3OD)δ:5.75(1H,s,H-3),4.21(1H,m,H-6),2.42(1H,dd,J= 14.0,4.0 Hz,H-7),1.98(1H,dd,J= 14.5,3.5 Hz,H-5),1.76(3H,s,7a-CH3),1.73(1H,dd,J= 14.0,4.0 Hz,H-7),1.53(1H,dd,J= 14.5,3.5 Hz,H-5),1.47(3H,s,4-CH3),1.28(3H,s,4-CH3);13C NMR(150 MHz,CD3OD)δ:185.7(C-2),113.3(C-3),174.4(C-3a),37.2(C-4),48.0(C-5),67.2(C-6),46.4(C-7),89.0(C-7a),27.4(C-4-CH3),27.0(C-4-CH3),31.1(C-7a-CH3)。经与文献[18]对比鉴定该化合物为(-)-loliolide。
化合物10无色油状物;ESI-MS:m/z323 [M+Na]+,分子式为C17H16O5。1H NMR(600 MHz,CDCl3)δ:12.03(1H,s,5-OH),7.38(2H,d,J= 9.0 Hz,H-3′,5′),6.95(2H,d,J= 9.0 Hz,H-2′,6′),6.07(1H,d,J= 2.4 Hz,H-8),6.04(1H,d,J= 2.4 Hz,H-6),5.36(1H,dd,J= 13.2,3.0 Hz,H-2),3.81,3.83(各3H,s,7,4′-OCH3),3.10(1H,dd,J= 16.8,12.6 Hz,H-3b),2.78(1H,dd,J= 16.8,3.0 Hz,H-3a);13C NMR(150 MHz,CDCl3)δ:79.2(C-2),43.4(C-3),196.2(C-4),164.3(C-5),95.2(C-6),168.1(C-7),94.4(C-8),163.1(C-9),103.3(C-10),130.5(C-1′),127.9(C-2′),114.4(C-3′),160.2(C-4′),114.4(C-5′),127.9(C-6′),55.5,55.8(7,4′-OCH3)。经与文献[19]对比鉴定该化合物为7,4′-dimethylnaringenin。
化合物11黄色粉末;ESI-MS:m/z449 [M+H]+,分子式为C21H20O11。1H NMR(500 MHz,CD3OD)δ:7.29(1H,s,H-2′),7.27(1H,d,J= 8.5 Hz,H-6′),6.87(1H,d,J= 8.5 Hz,H-5′),6.30(1H,s,H-8),6.14(1H,s,H-6),5.31(1H,s,H-1′′),0.91(3H,d,J= 6.0 Hz,H-6′′);13C NMR(150 MHz,CD3OD)δ:158.4(C-2),136.2(C-3),179.6(C-4),159.2(C-5),99.8(C-6),165.8(C-7),94.7(C-8),163.1(C-9),105.8(C-10),122.9(C-1′),116.3(C-2′),146.3(C-3′),149.7(C-4′),116.9(C-5′),122.9(C-6′),103.5(C-1′′),72.0(C-2′′),72.1(C-3′′),73.2(C-4′′),71.9(C-5′′),17.6(C-6′′)。经与文献[20]对比鉴定该化合物为quercetin-3-O-α-L-rhamnopyranoside。
化合物12黄色粉末;ESI-MS:m/z465 [M+H]+,分子式为C21H20O12。1H NMR(400 MHz,CD3OD)δ:7.71(1H,s,H-2′),7.58(1H,d,J= 8.0 Hz,H-6′),6.86(1H,d,J= 8.4 Hz,H-5′),6.39(1H,s,H-8),6.20(1H,s,H-6),5.24(1H,d,J= 7.6 Hz,H-1′′),3.70,3.57(各1H,m,H-6′′),3.48(1H,m,H-3′′),3.42(1H,m,H-4′′),3.31(1H,m,H-2′′),3.22(1H,m,H-5′′);13C NMR(150 MHz,CD3OD)δ:158.4(C-2),135.6(C-3),179.5(C-4),162.9(C-5),99.9(C-6),166.1(C-7),94.7(C-8),159.0(C-9),105.6(C-10),123.1(C-1′),116.0(C-2′),145.9(C-3′),149.8(C-4′),117.5(C-5′),123.2(C-6′),104.3(C-1′′),75.7(C-2′′),78.1(C-3′′),71.2(C-4′′),78.4(C-5′′),62.5(C-6′′)。经与文献[21]对比鉴定该化合物为quercetin-3-O-β-D-glucopyranoside。
化合物13白色粉末;ESI-MS:m/z313 [M+Na]+,分子式为C15H14O6。1H NMR(500 MHz,DMSO-d6)δ:6.74(1H,s,H-2′),6.70(1H,d,J= 7.5 Hz,H-6′),6.61(1H,d,J= 7.5 Hz,H-5′),5.91(1H,s,H-8),5.71(1H,s,H-6),4.50(1H,d,J= 7.0 Hz,H-2),3.84(1H,m,H-3),2.65(1H,dd,J= 16.0,4.5 Hz,H-4a),2.35(1H,dd,J= 16.0,8.0 Hz,H-4b);13C NMR(125 MHz,DMSO-d6)δ:81.1(C-2),66.5(C-3),27.9(C-4),156.3(C-5),95.3(C-6),156.6(C-7),94.0(C-8),155.5(C-9),99.2(C-10),130.8(C-1′),114.7(C-2′),145.0(C-3′),145.0(C-4′),115.3(C-5′),118.6(C-6′)。经与文献[22,23]对比鉴定该化合物为儿茶素。
化合物14淡黄色粉末;ESI-MS:m/z163.2 [M-H]—,分子式为C9H8O3。1H NMR(400 MHz,DMSO-d6)δ:7.50(2H,d,J= 8.0 Hz,H-2,6),7.49(1H,d,J= 16.0 Hz,H-7),6.77(2H,d,J= 8.0 Hz,H-3,5),6.27(1H,d,J= 16.0 Hz,H-8);13C NMR(125 MHz,DMSO-d6)δ:125.3(C-1),130.1(C-2),115.8(C-3),159.6(C-4),115.8(C-5),130.1(C-6),144.2(C-7),115.4(C-8),168.0(C-9)。经与文献[24]对比鉴定该化合物为香豆酸。
2.2 神经保护活性筛选结果
在10 μM浓度下,化合物1~7和10使H2O2损伤的PC12细胞的细胞存活率从43.41%±1.59%分别提高到62.61%±5.23%、64.87%±8.42%、56.06%±6.65%、65.87%±5.34%、60.54%±3.32%、68.11%±4.76%、45.27%±2.12和54.96%±1.51%。结果(见图2)显示倍半萜类化合物(1~6)表现出较好的活性。
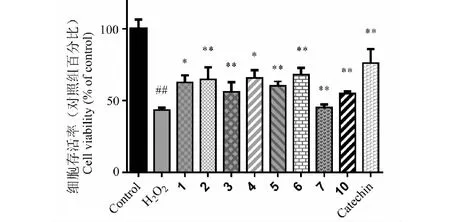
图2 化合物1~7和10的神经保护活性结果Fig.2 Neuroprotective effect of compounds 1-7 and 10
3 结果与讨论
本文从丝穗金粟兰全草95%乙醇部位中分离并鉴定了14个化合物,包括7个倍半萜类(1~6、8)、1个二萜(7)、1个单萜(9)、4个黄酮类(10~13)和1个酚酸(14)。同时考察了部分化合物对H2O2损伤的PC12细胞生长的影响,倍半萜类化合物(1~6)表现出中等的神经细胞保护作用。结合前期对同属植物的活性成分研究推测倍半萜类成分可能为丝穗金粟兰神经保护活性成分。目前从金粟兰属植物中分离得到的化合物主要为倍半萜类、倍半萜二聚体类、二萜类等[3],特别是乌药烷型倍半萜及其二聚体是该属植物的特征性成分,但目前从丝穗金粟兰里面发现的该类成分还较少。
阿尔兹海默病(Alzheimer’s disease,AD)是导致全球老年人死亡的神经类重大疾病之一,临床上多见AD患者脑功能逐渐减退同时伴有血瘀,因而采用活血化瘀中药治疗每每见效,从活血化瘀中药中发掘抗AD创新药物前景广阔[25]。金粟兰属药材作为江西省多种中药制剂的原料药应用,具有祛风除湿、活血散瘀等功效,从该属植物中分离得到的倍半萜类化合物表现出良好的神经保护活性[5,8]。后续我们将进一步深入探讨金粟兰属中倍半萜类化合物的脑神经保护作用,将以目前分离得到的倍半萜及其二聚体为分子模板,采用分子印迹的方法进行定向分离,以期获得结构新颖的化合物。然后在分子对接和构效关系分析的指导下进行化合物对PC12细胞的保护作用筛选,通过检测ROS的含量以及p-AMPK、Sirt 1、p-Sirt 1和Sirt 3等蛋白的表达量,从缓解氧化应激损伤等方面探讨金粟兰属植物治疗AD的作用机制,阐明该属植物神经保护活性物质基础。
