顶空气相色谱法测定一次性使用输液器中粘合剂的迁移量
2021-08-23薄晓文刘爱娟沈永孟凯刘叶
薄晓文,刘爱娟,沈永,孟凯,刘叶
(山东省医疗器械和药品检验研究院,国家药品监督管理局生物材料器械安全性评价重点实验室,山东省医疗器械生物学评价重点实验室,济南 250101)
一次性使用输液器在临床上主要用于静脉输液,因其简单方便、无交叉性传染等优点而被广泛使用,消耗量巨大[1–2]。一次性使用输液器与人体的血液直接接触,其在临床使用过程中溶出的物质会直接进入人体血液循环系统,存在潜在的安全风险,因而被列为三类医疗器械,其安全性日益受到人们的重视。但由于工艺等原因的限制,目前一次性使用输液器生产过程多使用有机溶剂作为组件粘合剂[3],包括丙烯酸甲酯、四氢呋喃和环己酮等。其中,丙烯酸甲酯有辛辣气味,具有呼吸道刺激性、免疫毒性和神经毒性等性质[4]。四氢呋喃有乙醚气味,是一种中枢神经抑制剂,低浓度时会引起头痛及鼻咽刺激,高浓度时有麻醉作用,浓度高于25 000 μg/g时会致死[5]。环己酮较为常用,有强烈刺鼻气味,并且对肝脏及心血管功能有一定影响[6]。已有文献表明[2,7],一次性使用输液器在模拟临床输注药物时会释放环己酮进入药液,因此,准确测定一次性使用输液器在输液过程中粘合剂的迁移量对输液器的质量控制和人们的用械安全具有重要意义。
目前,关于输液器中的环己酮残留的研究报道较多[2,6–9],但有关输液器中的丙烯酸甲酯和四氢呋喃的迁移研究未见有文献报道。此外,文献中多采用水、乙醇水溶液或乙醇[3,8–9]作为浸提介质进行输液器中环己酮迁移量的研究。但是,由于环己酮微溶于水,可与醇等有机溶剂混溶,因而无论用水还是乙醇作为浸提介质,均会过低或过高地估计输液器中环己酮的溶出量,不能真实反映输液器的临床使用风险。许凯等人采用临床输注药物作为浸提介质[2,6–7],考察了输液器临床使用过程中环己酮的溶出量,采用液体进样的方式,浸提液需要用正己烷、乙酸乙酯等溶剂萃取处理后方可进样分析,操作繁琐。
顶空气相色谱法具有操作简单、基质干扰小、准确可靠等优点[8],笔者选取了乳酸左氧氟沙星氯化钠注射液、甘露醇注射液、注射用奥美拉唑钠和脂肪乳注射液4种典型的临床常用药物,通过模拟临床使用的方式制备浸提液,建立了顶空气相色谱法同时测定流经输液器的药液中的粘合剂丙烯酸甲酯、四氢呋喃和环己酮,为输液器的临床安全性评价提供了方法和依据。
1 实验部分
1.1 主要仪器与试剂
气相色谱仪:7890B型,安捷伦科技(中国)有限公司。
丙烯酸甲酯对照品:编号为96–33–3,纯度为100%,德国默克公司。
四氢呋喃对照品:编号为109–99–9,纯度为99.9%,德国默克公司。
环 己 酮 对 照 品:编 号 为108–94–1,纯 度 为99.9%,德国默克公司。
N,N-二甲基甲酰胺(DMF):编号为127–19–5,色谱纯,德国默克公司。
氯化钠注射液:100 mL含氯化钠0.9 g,批号为1907302721,济宁市辰欣药业股份有限公司。
乳酸左氧氟沙星氯化钠注射液:100 mL含乳酸左氧氟沙星0.3 g(按C18H20FN3O4计)与氯化钠0.9 g,批号为116190623,浙江医药股份有限公司新昌制药厂。
甘露醇注射液(20%):250 mL含50 g甘露醇,批号为SA19090508,山东华鲁制药有限公司。
注射用奥美拉唑钠:40 mg (以C17H19N3O3S计),批号为1906174,湖南五洲通药业有限责任公司。
脂肪乳注射液(C14~24):250 mL含50 g(大豆油)与3 g(卵磷脂),批号为B19040702CW–1,黑龙江科伦制药有限公司。
1.2 仪器工作条件
顶空条件:80 ℃平衡30 min;色谱柱:DB–624型毛细管柱[30 m×0.25 mm,1.40 μm,安捷伦科技(中国)有限公司];进样口温度:250 ℃;分流比:10∶1;流量:1.0 mL/min;柱温:初温为40 ℃,保持5 min,然后以10 ℃/min升温至100 ℃,再以20℃/min升温至240 ℃并保持2 min;FID检测器温度:250 ℃。
1.3 实验步骤
1.3.1 标准溶液的配制
混合标准溶液:分别精密称取丙烯酸甲酯对照品21.6 mg、四氢呋喃对照品19.2 mg、环己酮对照品22.3 mg,分别置于预先加有适量DMF的10 mL容量瓶中,加DMF稀释至标线,摇匀,即得各物质标准储备液。分别精密量取丙烯酸甲酯标准储备液2 mL、四氢呋喃标准储备液2 mL及环己酮标准储备液3 mL,置于10 mL容量瓶中,加DMF稀释至标线,摇匀,即得混合标准溶液。
混合标准储备液:精密称取丙烯酸甲酯对照品55.8 mg、四氢呋喃对照品48.4 mg、环己酮对照品86.0 mg,置于预先加有适量DMF的25 mL容量瓶中,加DMF稀释至标线,摇匀,即得混合标准储备液。
1.3.2 样品供试液的制备
选取4种有代表性的临床常用输注药物,包括乳酸左氧氟沙星氯化钠注射液、甘露醇注射液、注射用奥美拉唑钠及脂肪乳注射液,分别按照其使用说明书中最严格的用法用量,通过模拟静脉滴注的方式制备样品浸提液,具体方法如下:
(1)乳酸左氧氟沙星氯化钠注射液:滴注体积为100 mL,滴注时间为60 min;
(2)甘露醇注射液:滴注体积为250 mL,滴注时间为6 h;
(3)注射用奥美拉唑钠氯化钠注射液:称取注射用奥美拉唑钠60 mg,用氯化钠注射液溶解并定容至100 mL,即得,滴注体积为100 mL,滴注时间为60 min;
(4)脂肪乳注射液:滴注体积为250 mL,滴注时间为250 min。
分别取氯化钠注射液、乳酸左氧氟沙星氯化钠注射液、甘露醇注射液、注射用奥美拉唑钠氯化钠注射液及脂肪乳注射液作为空白对照液。
2 结果与讨论
2.1 药物选择
一次性使用输液器在临床使用时输注的药物种类繁多,不可能对所有种类药物输注过程中的粘合剂迁移量进行考察。因此选取了4种有一定代表性的临床常用药物,乳酸左氧氟沙星氯化钠注射液为酸性药物,甘露醇注射液为中性药物,注射用奥美拉唑钠氯化钠注射液为碱性药物,脂肪乳注射液为脂溶性药物。
2.2 顶空条件的选择
中国药典(2020年版)通则0861 《残留溶剂测定法》[10]中给出的顶空条件如下:以水为溶剂时顶空瓶平衡温度为70~85 ℃,顶空瓶平衡时间为30~60 min。刘颖玲等[8]的研究结果表明,平衡时间为30 min时,环己酮便可达到气液平衡;若温度过高,水蒸气会影响检测器和色谱柱,温度过低检测灵敏度则会降低,平衡温度为80 ℃时,两者可兼顾。所用输注药物均为水溶液,所分析目标物质中环己酮沸点最高,因此综合考虑选择顶空平衡温度为80 ℃,平衡时间为30 min。
2.3 程序升温条件的选择
分离是定量的基础,为使目标物丙烯酸甲酯、四氢呋喃及环己酮得到良好的分离,对程序升温条件进行了优化。
首先,设置了简单的升温程序,即初温40 ℃保持5 min,然后以20 ℃/min的速率升至240 ℃并保持3 min,初步考察目标物的保留时间及分离情况。结果表明,丙烯酸甲酯的保留时间为7.151 min,四氢呋喃的保留时间为7.350 min,环己酮的保留时间为11.659 min,丙烯酸甲酯和四氢呋喃未能完全分离。在此基础上优化升温程序,将丙烯酸甲酯和四氢呋喃保留时间附近的升温速率减慢,即将程序升温条件更改为初温40 ℃保持5 min,然后以10 ℃/min的速率升至100℃,再以20 ℃/min的速率升至240 ℃并保持2 min,在此条件下目标物可完全分离。
2.4 方法学考察
顶空进样法可避免复杂的样品前处理过程,具有操作简单、杂质干扰少等优点,但其也存在基质效应问题。已有文献报道[11–13],样品基质的不同可显著影响目标物的检出量与回收率,干扰测定的准确度。本研究共涉及4种样品基质,分别为乳酸左氧氟沙星氯化钠注射液、甘露醇注射液、注射用奥美拉唑钠氯化钠注射液和脂肪乳注射液。试验发现,注射用奥美拉唑钠氯化钠注射液对丙烯酸甲酯的测定有干扰,其回收率仅为50%。脂肪乳注射液对丙烯酸甲酯、四氢呋喃及环己酮的测定均有干扰,其回收率分别为55%、73%及57%左右。
顶空气体中各组分的含量,既与其本身的挥发性有关,又与其在样品基质中的溶解度有关[13]。3种待测粘结剂中环己酮沸点最高(155 ℃),丙烯酸甲酯次之(80 ℃),四氢呋喃最低(66 ℃)。水溶性方面,四氢呋喃可与水混溶,丙烯酸甲酯和环己酮均微溶于水。脂肪乳注射液为脂溶性药物,与氯化钠注射液相比,对上述3种粘结剂的溶解效果更好,尤其是对水溶性较差的丙烯酸甲酯和环己酮,故导致其回收率偏低,检出限偏高。因此,为消除基质效应,提高测定的准确度,对于测定时存在基质干扰的目标物,应均在相应的样品基质上建立标准曲线,并进行相应的方法学考察。
2.4.1 专属性考察
用氯化钠注射液配制一定质量浓度的混合标准溶液进样分析,色谱图如图1所示。由图1可知,目标物四氢呋喃、丙烯酸甲酯及环己酮色谱峰的分离度良好。对样品浸提液进样分析,可知在各目标物出峰位置无其它干扰峰存在,表明方法的专属性良好。

图1 混合标准溶液色谱图
2.4.2 线性关系与检出限、定量限
分别精密量取1.3.1混合标准溶液1、5、10、20、30、40、50 μL至预先加有5 mL氯化钠注射液的20 mL顶空瓶中,密封,混匀,即得以氯化钠注射液为基质的系列混合标准溶液;分别精密量取1.3.1丙烯酸甲酯标准储备液0.4、1、2、4、6、8 μL至预先加有5 mL注射用奥美拉唑钠氯化钠注射液样品基质的20 mL顶空瓶中,密封,混匀,即得以注射用奥美拉唑钠氯化钠注射液为基质的丙烯酸甲酯系列标准溶液;分别精密量取1.3.1混合标准储备液0.4、1、2、4、6、8 μL至预先加有5 mL脂肪乳注射液样品基质的20 mL顶空瓶中,密封,混匀,即得以脂肪乳注射液为基质的系列混合标准溶液。
将上述各系列标准溶液进样分析,以色谱峰面积(A)为纵坐标,质量浓度(C)为横坐标进行线性回归。配制一定浓度的标准溶液并进样分析,以信噪比(S/N)约为3时的浓度为检出限,以S/N约为10且具有良好精密度和回收率时的浓度为定量限。计算得各目标物在不同样品基质中的线性范围、线性方程、相关系数、检出限、定量限,结果列于表1。
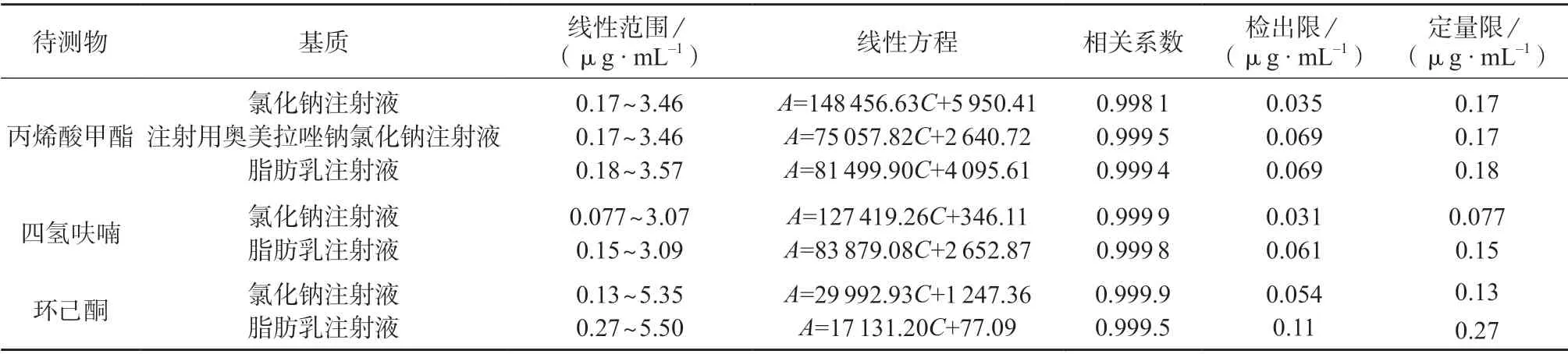
表1 线性范围、线性方程、相关系数、检出限、定量限
2.4.3 精密度试验
配制低、中、高三种浓度水平的标准溶液,在1.2工作条件下分别连续测定6次,计算色谱峰面积相对标准偏差(RSD),不同基质下各待测物的精密度试验结果列于表2~表4。由表2~表4可知,该方法进样重复性为0.36%~7.25%,符合相关标准要求[14]。

表2 丙烯酸甲酯精密度试验结果

表3 四氢呋喃精密度试验结果

表4 环己酮精密度试验结果
2.4.5 加标回收试验
精密量取样品基质各5 mL于20 mL顶空瓶中,分别加入不同体积混合标准储备液,密封,混匀,进样分析,每个浓度水平平行测定3次,结果列于表5~表7。由表5~表7可知,加标回收率为72.52%~119.67%,测定结果的相对标准偏差为0.10%~5.46%,符合相关标准[14]。

表5 丙烯酸甲酯加标回收试验结果(n=6)

表6 四氢呋喃加标回收试验结果(n=6)

表7 环己酮加标回收试验结果(n=6)
2.5 样品测定
精密量取样品浸提液5 mL,置于20 mL顶空瓶中,密封,进样分析。结果显示,所有样品浸提液中均为未检出丙烯酸甲酯、四氢呋喃及环己酮,输液器在输注脂肪乳注射液时,丙烯酸甲酯、四氢呋喃及环己酮的检出限较高,分别为17.28、15.35、26.72 μg/套。
3 结论
ICH Q3C[15]给出的四氢呋喃每日允许暴露量(PDE)为7.2 mg/d,美国环境保护署预计[2]的环己酮安全剂量为25 mg/d,通过大鼠静脉NOAEL值计算得环己酮安全剂量为50 mg/d。丙烯酸甲酯的允许限量未见有文献报道,我国职业卫生标准GBZ 2.1–2019[16]规定的丙烯酸甲酯的时间加权平均容许浓度(PC–TWA)为20 mg/m3,是环己酮PC–TWA(50 mg/m3)的0.4倍。参考环己酮的安全剂量25 mg/d,计算出丙烯酸甲酯静脉接触途径的安全剂量为10 mg/d。本研究样品中丙烯酸甲酯、四氢呋喃及环己酮均未检出,且其安全限值分别为其检出限的579、469、936倍,粘合剂的迁移量均远低于其安全限值。
采用顶空气相色谱法对一次性使用输液器药物输注过程中粘合剂丙烯酸甲酯、四氢呋喃及环己酮的迁移量进行了研究,该方法简单、快速、准确、专属性强,可同时测定一次性输液器中粘结剂丙烯酸甲酯、四氢呋喃和环己酮的迁移量,为一次性使用输液器的质量控制和安全性评价提供了参考。
