铁尾矿制备聚合硫酸铁实验及造纸污水处理效果初步评价
2021-08-12纪丁愈李云祯
纪丁愈,李云祯,邹 渝
(1.四川水利职业技术学院,四川崇州611231;2.四川省生态环境科学研究院)
在开采煤矿、金属矿以及冶金时会产生大量的尾矿废弃物,对于尾矿的处理前期都是采用集中堆积处理,但是随着尾矿量的增多,尾矿堆积形成的尾矿坝也越来越高,使得高尾矿坝稳定性能变差,给周围建筑物以及施工人员带来严重的安全隐患,且金属尾矿以及浮选厂排出的尾矿对于土地和空气的污染也较为严重[1-3]。同时,作为重要战略物资的自然资源属于不可再生能源,我国较低的矿产资源综合利用率以及回收利用率,使得矿产资源的浪费极大。因此,如何科学有效地处理大量尾矿成为一个棘手的问题[4]。一般情况下,对于尾矿资源的利用,都是将其作为建筑材料的掺料制备尾矿类混凝土、水泥土等材料,避免了过渡开采砂石材料导致的水土流失等问题[5];其次,由于尾矿中富含微量元素,通过磁化处理制备出磁化尾矿,可以有效地提高土地内部的磁性,更加利于植物和农作物的生长;其次,尾矿也可以作为充填料,有效地降低生产成本和提升矿产资源的回采率[6-8]。
同时,水资源作为生命的源泉,可以有效限制人类的发展和生存[9],故对污染水进行净化处理和二次饮用是解决缺水地区水资源匮乏的有效手段。而污染水中的污染物常常以溶解状态、胶体粒子、微小颗粒或液体等形式存在,一般可以采用絮凝法对污水进行处理,从而达到污染水净化、可饮用的标准,故可以利用尾矿来制备聚合铁盐、并对其进行复合改性后得到可净化污染水的絮凝剂[10]。因此,本文将废弃的铁尾矿进行酸浸还原实验,将铁资源从尾矿中提取出来,并以此为原料制备絮凝剂PFPS;通过絮凝实验来验证不同pH、不同絮凝剂用量以及不同沉降时间作用下,絮凝剂PFPS对污染水的处理效果。
1 实验材料和方法
1.1 实验材料及仪器
采用的铁尾矿取自四川某地区的尾矿坝,选取2、1、0.5、0.25、0.075 mm的5种不同孔径的筛子对铁尾矿进行筛分实验。本文选用粒径大于0.5 mm的尾矿砂总含量超过50%的中粗砂。
对铁尾矿的化学成分进行分析,得到该铁尾矿(选取100 g为研究对象)的化学成分见表1。由表1可知,该铁尾矿砂中SiO2的含量最多,故该尾矿砂可以定义为高硅鞍山型铁尾矿。
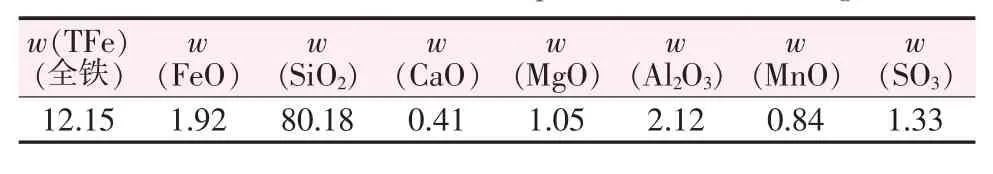
表1 铁尾矿的主要化学成分Table 1 Main chemical composition of iron tailings %
主要仪器:EDX1800B型XRF衍射仪;D840IWZ型电子搅拌仪;FA1004型电子分析天平和恒温箱。
1.2 实验方法
1.2.1 酸浸还原实验
一般影响酸浸实验中全铁浸出率的因素主要有温度、搅拌时间、搅拌速度[11-12]。本文将设定20、40、60、80、100、120、140、160℃共8个温度条件,搅拌时间设置为0.5、1、1.5、2、2.5、3 h共6个条件,搅拌 速 度 设 置 为50、100、150、200、250、300、350和400 r/min。通过上述不同条件计算得出全铁浸出率,得到不同因素对全铁浸出率的影响机制。
一般影响还原实验中硫酸亚铁还原率的外部因素主要有时间、温度和铁粉的掺入量。本文将温度分别设定为20、40、60、80、100、120℃共6种,还原时间分别设置为0.5、1、1.5、2、2.5、3 h共6种,铁粉的过量设系数置为0.20%、0.50%、0.80%、1.10%、1.40%和1.70%。
1.2.2 聚合硫酸铁合成实验
考察不同磷酸钠溶液用量、温度、时间和双氧水的用量对聚合硫酸铁合成实验的影响[13-14],本文采用0.15 mol/L的磷酸钠溶液,用量设定为0.7、0.9、1.1、1.3、1.5、1.7 mL共6种,温度设置为20、25、30、35、40、45℃共6种,时间设置为0.1、0.2、0.3、0.4、0.5、0.6 h共6种,浓度为0.4 mol/L的双氧水溶液,用量设置为0.5、1、1.5、2、2.5、3 mL共6种。
1.2.3 聚合硫酸铁对污水处理中外部因素的影响
本文主要采用四川成都锦丰纸业股份有限公司地池中的造纸污水作为研究对象,并通过过滤措施将污水中悬浮物和泥土进行处理。为了更好地描述聚合硫酸铁对污水处理实验中外部因素对处理效果的影响,考察不同pH、聚合硫酸铁用量、沉降时间对处理效果的影响实验[15-16]。本文将pH设定为4、5、6、7、8、9共6种,聚合硫酸铁的质量浓度设为0.5、1、1.5、2.0、2.5、3.0 g/ml共6种,沉降时间设置为0.1、0.2、0.3、0.4、0.5、0.6 h共6种。
2 结果与讨论
2.1 酸浸还原实验及其影响因素分析
2.1.1 不同条件下的全铁浸出率结果分析
根据上述计算得出的全铁浸出率,绘制不同条件作用下全铁浸出率的变化规律曲线如图1所示。
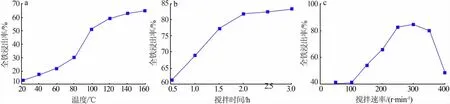
图1 不同条件作用下全铁浸出率的影响变化规律曲线Fig.1 Change rule curves of the influence of total iron leaching rate under different conditions
由图1a可知,随着温度不断升高,尾矿中全铁浸出率呈现类似线性的增大趋势,但是100℃之后,尾矿中全铁浸出率的曲线变化率随着温度的升高开始降低。100℃时全铁浸出率已经达到160℃时全铁浸出率的80%以上,且在温度为80℃和100℃期间,尾矿中全铁浸出率增长最大约为21.07%。原因可能为80~100℃时,铁尾矿活化性能达到最佳,因此,在综合经济与实验条件因素的基础上,选择100℃作为尾矿全铁浸出实验的最佳温度。由图1b可见,随着搅拌时间的延长,尾矿中全铁浸出率呈现出先增大后逐渐趋于稳定的变化趋势,且在搅拌时间达到2.5 h时相对2 h的尾矿中全铁浸出率只增长了约0.67%。刚开始浸出率增大是由于随着搅拌时间的延长铁尾矿中富含三氧化二铁的固体颗粒与酸性溶液反应时,会有效提升尾矿颗粒与酸性溶液的接触,加快反应速率;但在搅拌2 h以后,全铁浸出率曲线的变化率逐渐保持平稳,故选择2 h为尾矿全铁浸出实验的最佳搅拌时间。
从图1c中可以看出,随着搅拌速度的增大,尾矿中全铁浸出率呈现出先增大后减小的变化趋势;当搅拌速度为300 r/min时,尾矿全铁浸出率达到了最大值。这是由于此时尾矿在溶液中分布处于均匀状态,使反应更加充分;当搅拌速度大于300 r/min时尾矿全铁浸出率出现下降趋势,这是由于搅拌速度过快,使悬浮在溶液中的尾矿颗粒与反应物被甩到瓶壁上结成固体,与酸性溶液的反应程度降低。但是搅拌速度为大于350 r/min时,全铁浸出率急剧下降,这可能是由于搅拌速率太快导致尾矿颗粒与反应物被甩到器壁上结成固体的总量增多,使参与浸出还原反应的铁尾矿减少,最终全铁浸出率下降。故选择搅拌速度为300 r/min作为尾矿全铁浸出实验最佳搅拌速度。
2.1.2 不同条件下的硫酸亚铁还原率结果分析
根据设定条件,绘制出不同条件下的全铁浓度和Fe3+还原率变化规律曲线如图2所示。由图2a可见,随还原温度的升高,全铁浓度呈现增大趋势;Fe3+还原率曲线在60℃之前速率增加较大,在60℃以后缓慢增加基本接近水平。这是由于温度升高,使游离的Fe3+氧化性能有所增强,Fe3+与铁粉发生的化学反应更加充分。故60℃作为Fe3+还原实验的最佳实验还原温度。由图2b可知,随着还原实验时间的延长,Fe3+还原率的变化规律呈现先快后慢的增长变化。还原时间为1.5 h时Fe3+的还原率已达到3 h时Fe3+还原率的90%以上。而全铁浓度在1.5 h以后增加也较为缓慢,且接近平衡。这是由于还原时间延长,游离的Fe3+与铁粉反应的时间延长,反应更加充分,但随着时间的持续延长,游离Fe3+含量会逐渐降低,2 h时全铁浓度仅增长了3.09%,Fe3+的还原率也只增长了5.91%。因此,将1.5 h作为Fe3+还原实验的最佳实验时间。从图2c可以看出,随着铁粉的掺入量的增加,Fe3+还原率却呈现出先增大后趋于水平增长的变化规律,而全铁浓度也呈现出先增大后趋于稳定增长的变化规律,增长转折点在铁粉过量系数为1.10%附近,且Fe3+还原率要远远大于全铁还原率。这是由于溶液中游离的Fe3+具有很强的氧化性,在加入铁粉之后,溶液中游离的Fe3+与铁粉优先发生还原反应,当铁粉掺量持续增加时才与溶液中酸性离子发生化学反应,使全铁浓度稳定增长,综上可知,铁粉的过量系数选为1.10%。
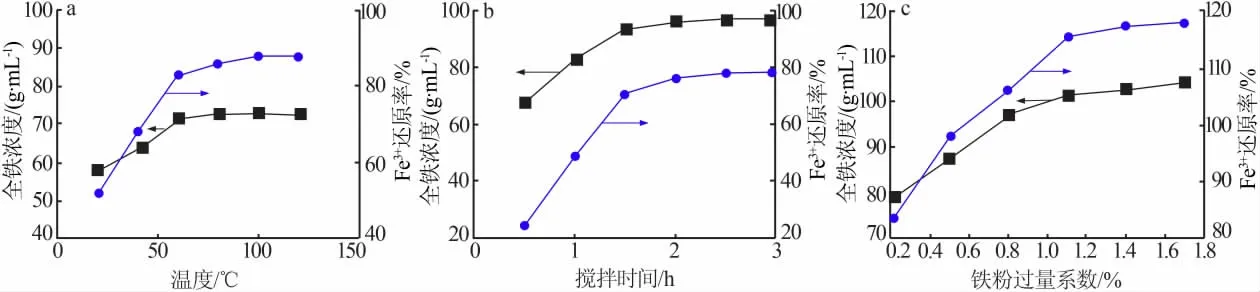
图2 不同条件下的还原率变化规律曲线Fig.2 Change rule curves of reduction rate under different conditions
2.2 聚合硫酸铁合成实验结果分析
为了得到磷酸钠对聚合硫酸铁产生的影响,对不同条件下聚合硫酸铁的合成进行实验,并绘制出不同条件作用下盐基度的影响变化规律曲线如图3所示。
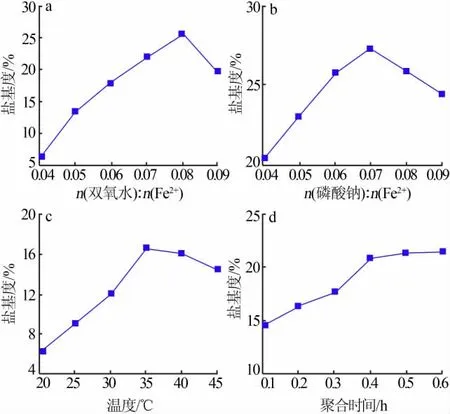
图3 盐基度的影响变化规律曲线Fig.3 Chang rule curves of the influence of basicity
由图3a可知,随着双氧水用量的增加,盐基度呈现先增后减的变化规律,且在n(双氧水)∶n(Fe2+)为0.08时,盐基度取最大值为25.54%。这是由于双氧水的用量增大时,溶液中的亚铁离子会不断地被氧化生成全铁离子,当n(双氧水)∶n(Fe2+)为0.08时,溶液的颜色几乎不再发生变化,此时可认为溶液中的亚铁离子已全部被氧化。故在综合经济与实验条件因素的基础上,选择n(双氧水)∶n(Fe2+)为0.08。
由图3b可知,随着n(磷酸钠)∶n(Fe2+)的增大,盐基度呈现出先增大后减小的变化规律,且在n(磷酸钠)∶n(Fe2+)为0.07时,盐基度取最大值为27.27%,这是由于当硫酸添加量较少时,此时铁离子会与溶液充分发生氧化反应生成硫酸亚铁,进而抑制了聚合硫酸铁的合成,故选择n(磷酸钠)∶n(Fe2+)为0.07。
由图3c和3d可见,随着聚合温度和时间的增大,盐基度均呈现先增大后趋于稳定的变化规律。在聚合温度为35℃时,盐基度取最大值为16.68%;聚合时间为0.4 h时,盐基度取最佳值为20.85%。分析原因,是由于温度过低导致聚合硫酸铁所需的聚合热量不够,得到的聚合硫酸铁絮凝剂的絮凝效果较差,但是温度过高后,聚合温度提供给聚合硫酸铁热量过多,使聚合硫酸铁絮凝剂的稳定性较差。只有在合适的外界温度和聚合温度时,才能得到稳定性好、絮凝效果好的聚合硫酸铁。由实验数据分析可得,由于聚合时间过短,聚合反应进行的不够彻底,得到聚合硫酸铁含量较少;但是随着聚合时间的持续增大,聚合反应进行相对彻底,聚合反应物剩余更少,最终聚合硫酸铁的增长率也相应减小。在综合经济与实验条件因素的基础上,选择聚合温度为35℃、聚合时间为0.4 h。
2.3 聚合硫酸铁对污水处理实验结果分析
分析不同pH、聚合硫酸铁用量和沉降时间对污水处理效果,并绘制出不同pH、聚合硫酸铁用量和沉降时间作用下污水的余浊、透光率的变化规律如图4所示。
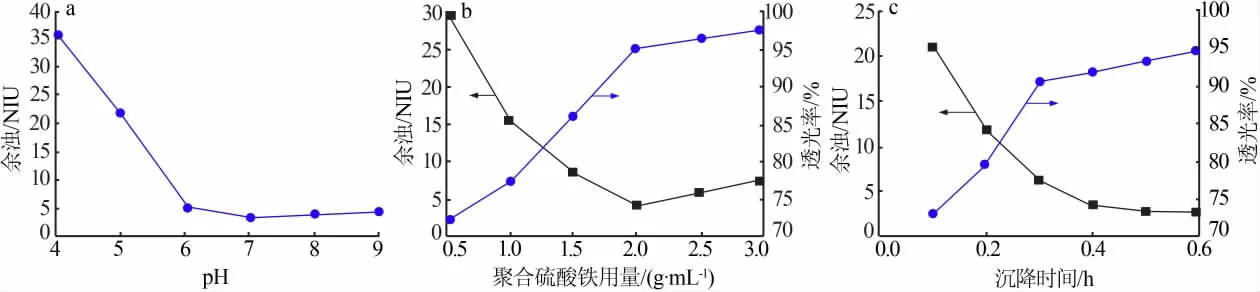
图4 不同条件作用下污水处理效果曲线Fig.4 Sewage treatment effect curve under different conditions
由图4a可知,随着pH的不断增大,溶液由酸性变为中性再变为碱性,而污水的余浊却呈现出先减小后缓慢增大的变化规律。在pH为7(中性环境中)时污水的余浊值最小为3.06 NIU,即在pH为7~9时聚合硫酸铁对于污水的处理效果最好。这是由于在碱性和偏碱性环境下聚合硫酸铁通过水解产生带有正电荷的物质,具有强烈的电中和桥联聚合作用,会使得聚合硫酸铁对于污水的处理效果最好。
由图4b可知,随着聚合硫酸铁用量的增大,污水的余浊呈现出先减小后缓慢增大的变化规律,但是污水的透光率却呈现出先增大后趋于稳定的变化规律。在聚合硫酸铁的质量浓度为2.0 g/mL时,透光率的增长率和余浊的降低率开始出现平稳变化趋势,这是由于聚合硫酸铁的电中和能量较强,使得水中的杂质都吸附在絮凝剂上,但是随着聚合硫酸铁用量的增大,絮凝剂电荷会出现逆变现象,导致聚合硫酸铁的电中和效果减弱,进而导致污水的余浊上升、透光率下降。
由4c可以看出,随沉降时间的延长,污水的余浊呈现先减小后趋于稳定的变化规律,但是污水的透光率却呈现出先增大后趋于稳定的变化规律,在沉降时间为0.3 h时,透光率的增长率和余浊的降低率开始出现平稳变化趋势,这是由于聚合硫酸铁的絮凝体具有良好的沉降性能,沉降时间越长处理后的水质透光率越大。在综合经济与实验条件因素的基础上,pH为7~9聚合硫酸铁的质量浓度为2.0 g/mL、沉降时间为0.3 h时聚合硫酸铁对于污水的处理效果最好。
3 结论
1)综合经济因素与实验条件因素的基础上,选择温度为100℃作为尾矿全铁浸出实验的最佳温度,此温度条件下,铁尾矿活化性达到最佳状态;选择搅拌时间为2 h作为全铁浸出实验的最佳时间,此搅拌时间达到了浸出率增长的峰值;选择搅拌速度为300 r/min作为全铁浸出实验的最佳搅拌速度,此搅拌速度可以使尾矿和溶液反应更充分。2)考虑到外部因素对硫酸亚铁还原率的影响,还原试验中硫酸亚铁还原率的最佳还原温度为60℃,最佳还原时间为1.5 h,选择还原铁粉的过量系数为1.10%时,Fe3+还原率增长速度最快,此后呈现缓慢增长的变化规律。3)聚合硫酸铁合成试验中选择35℃为最佳聚合温度,此温度下,盐基度达到最大;考虑综合经济因素,选择0.4 h为最佳聚合时间;在n(双氧水)∶n(Fe2+)为0.08∶1、n(磷酸钠)∶n(Fe2+)为0.07∶1时,盐基度取得最大值,之后呈减小变化的规律。4)聚合硫酸铁对污水处理试验中,随着pH的不断增大,污水的余浊却呈现出先减小后缓慢增大的变化规律,在pH为7(中性环境中)时污水的余浊值最小;聚合硫酸铁的质量浓度为2.0 g/mL、沉降时间为0.3h时,透光率的增长率和余浊的降低率出现平稳变化趋势;在上述条件下,对于污水的处理效果最好。
