右丙亚胺联合参麦治疗靶向药物心脏毒性的临床研究
2021-08-10李莺
李莺
(江西省萍乡市人民医院全科·老年病科,江西 萍乡 337000)
心脏毒性是指肿瘤靶向药物治疗中出现的不良反应,会影响患者的心脏功能。临床常见靶向药物的心血管毒性包括心力衰竭、高血压、心律失常、血栓形成等,但目前,关于心血管毒性的发生机制尚未明确[1]。尽管靶向治疗使更多肿瘤患者获益,但其引发的心血管毒性也引起了临床的广泛关注。目前,右丙亚胺或右丙亚胺联合用药治疗心脏毒性的临床相关报道主要集中于肿瘤化疗心脏毒性方面,临床效果显著[2]。但关于右丙亚胺或右丙亚胺联合用药治疗靶向药物所致心脏毒性报道较少。基于此,本研究旨在探讨右丙亚胺联合参麦治疗靶向药物心脏毒性的临床效果,现报道如下。
1 资料与方法
1.1 临床资料 选取2017年11月至2019年12月本院收治的靶向药物心脏毒性患者62例,按随机数字表法分为两组,各31例,患者疾病分期均为Ⅱ~Ⅲ期。对照组男23例,女8例;年龄22~72 岁,平均(50.47±6.15)岁;乳腺癌14 例,血液系统肿瘤 17 例。观察组男 24 例,女7 例;年龄21~73 岁,平均(50.53±6.11)岁;乳腺癌13 例,血液系统肿瘤18 例。两组患者临床资料比较差异无统计学意义,具有可比性。本研究已通过医院伦理委员会审核批准。
1.2 纳入与排除标准 纳入标准:①均无右丙亚胺、参麦药物过敏史;②既往无心脏病、心律失常等疾病史;③患者及家属均自愿签署知情同意书。排除标准:①伴有肝、肾功能异常者;②合并重要器官性质病变者;③妊娠期或哺乳期女性;④精神疾病者。
1.3 方法 两组患者均予以蒽环类药物进行化疗,乳腺癌患者采用环磷酰胺(瀚晖制药有限公司,生产批号:20161104,规格:0.5 g)500 mg/m2加30 mL 0.9%氯化钠溶液静脉滴注,氟尿嘧啶(海南卓泰制药有限公司,生产批号:20160407,规格:10 mL∶0.25 g)500 mg/m2缓慢静脉滴注,阿霉素(北京协和药厂,生产批号:20160703,规格:10 mg)60 mg/m2静脉注射,血液系统疾病患者采用静脉输液管内注射柔红霉素(深圳万乐药业有限公司,生产批号:20160201,规格:20 mg)2 mg/kg。21 d为1个疗程。
1.3.1 对照组 采用传统丹参注射液(国药集团宜宾制药有限责任公司,国药准字Z51020167,规格:10 mL/支)治疗,化疗前采用丹参注射液静脉滴注治疗,10 mL 予以5%葡萄糖注射液100 mL稀释后使用。治疗3个月。
1.3.2 观察组 采用右丙亚胺(江苏奥赛康药业有限公司,国药准字H20061157,规格:250 mg)联合参麦(四川川大华西药业股份有限公司,国药准字Z20053303,规格:15 mL/支)治疗,右丙亚胺快速静滴60 mg/m2,参麦静脉滴注,每次30 mL,每天1次。于化疗前30 min使用,治疗3个月。
1.4 观察指标 比较两组治疗前、治疗3 个月后心功能(LVEF)水平,使用心脏多普勒彩色超声仪进行检测。比较两组治疗前、治疗3个月后心脏生物学标志物(CTnT)水平,采用南京诺尔曼生物技术有限公司CTnT测定试剂盒(免疫增强比浊法),并严格按照试剂盒说明书进行检测。比较两组治疗3个月心电图异常变化情况,包括窦缓/窦速、房性期前收缩、传导阻滞、ST-T段改变。
1.5 统计学方法 采用SPSS 22.0软件进行数据处理,计量资料以“”表示,组间用独立样本t检验,组内用配对样本t检验,以[n(%)]表示计数资料,采用χ2检验,以P<0.05 为差异具有统计学意义。
2 结果
2.1 两组LVEF 水平比较 治疗前,两组LVEF 水平比较差异无统计学意义;治疗后,两组LVEF均降低,但观察组高于对照组(P<0.05),见表1。
表1 两组LVEF水平比较(,%)
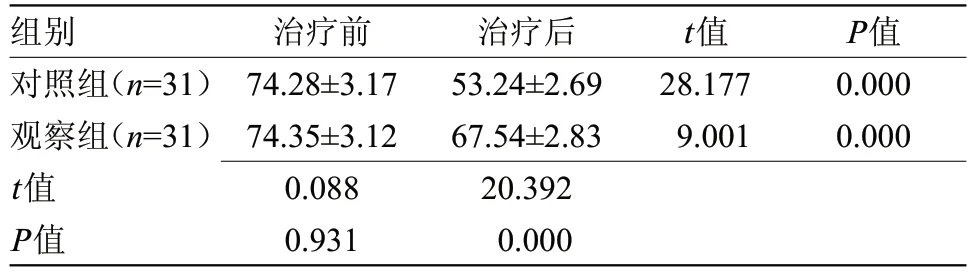
表1 两组LVEF水平比较(,%)
组别对照组(n=31)观察组(n=31)t值P值治疗前74.28±3.17 74.35±3.12 0.088 0.931治疗后53.24±2.69 67.54±2.83 20.392 0.000 t值28.177 9.001 P值0.000 0.000
2.2 两组CTnT 水平比较 治疗前,两组CTnT 比较差异无统计学意义;治疗后,两组CTnT均升高,但观察组低于对照组(P<0.05),见表2。
表2 两组CTnT水平比较(,ng/mL)

表2 两组CTnT水平比较(,ng/mL)
组别对照组(n=31)观察组(n=31)t值P值治疗前0.28±0.11 0.27±0.09 0.392 0.697治疗后1.21±0.14 0.85±0.31 5.893 0.000 t值29.083 10.004 P值0.000 0.000
2.3 两组心电图异常发生情况比较 观察组心电图异常发生率低于对照组(P<0.05),见表3。

表3 两组心电图异常发生情况比较[n(%)]
3 讨论
靶向治疗大部分与靶位点相关联。有研究认为,对于靶向药物导致的心脏毒性患者,预防比治疗更重要[3]。心电图变化可直接反映心脏毒性,心室射血分数是从容积角度反映心室射血功能,是一个容积比率指标;CTnT是主要调节心肌肌肉收缩的蛋白质,是出现心肌梗死症状的指示物。本研究结果显示,治疗后,两组LVEF均降低,CTnT均升高,但观察组变化幅度小于对照组,观察组心电图异常发生率低于对照组(P<0.05),表明右丙亚胺联合参麦治疗靶向药物心脏毒性效果优于传统丹参注射液治疗,能减缓心功能受损,减少心电图异常变化。抗肿瘤药物常见的心脏不良反应包括心电图改变、心肌缺血/梗死、左室射血分数下降、慢性心力衰竭(HF)、QT间期延长、心肌炎和心律失常等[4]。右丙亚胺为EDTA 的环状衍生物,易穿透细胞膜,在细胞内转变为开环螯合剂,其为蒽环类抗生素产生心脏毒性的原因[5-7]。参麦与化疗药物联合使用,具有协同作用,可减少化疗药物引起的不良反应,使肾上腺皮质系统兴奋,增加清除休克时各种病理性物质,改善心、肝、脑等重要脏器的供血和微循环、抗凝,进而提升癌症患者身体状况,并提高NK、LAK 活性及TH/TS 值等细胞免疫功能指标,保护骨髓造血功能[8-9]。参麦主要成分为红参、麦冬,其中红参复脉固脱、益气摄血;麦冬润肺清心、泻热生津;共奏益气固脱,养阴生津之效。且现代药理学研究显示,红参具有一定的抗氧化、抗肿瘤、抗衰老等作用,麦冬具有抗疲劳、清除自由基、提高细胞免疫功能、降血糖、抗心律失常、抗肿瘤的作用[10-11]。右丙亚胺和参麦注射液对使用蒽环类药物所致的心脏毒性有保护作用,能减轻不良反应对心脏的损伤。肿瘤患者靶向治疗前应积极重视心脏评估,掌握其评估方法,在治疗期间进行心脏功能评估,包括动态监测心率和血压,定期检查心脏功能、电解质、甲状腺功能和血脂,一旦出现慢性心衰症状,应先停止抗肿瘤药物治疗,并采用常规的慢性心衰治疗措施加以处理。
综上所述,右丙亚胺联合参麦治疗靶向药物心脏毒性效果优于传统丹参注射液治疗,能减缓患者心功能受损,减少心电图异常变化,值得临床推广使用。
