带蒂结肠移植治疗有胃或食管手术史的食管癌患者的临床分析
2021-07-29张葆勋杨兴国
余 振 于 磊 于 涛 张葆勋 杨兴国 杜 鑫
北京同仁医院胸外科,北京 100730
食管癌为中国地区性常见恶性肿瘤之一,其治疗原则是以手术切除病变食管、胃代食管为主的综合性治疗,其5 年生存率为30%~40%[1]。对有胃手术史再发胃贲门或下段食管癌者,再次切除病变食管,以残胃或空肠替代食管获得成功的文献报道甚多[2-3]。如果食管癌患者因胃十二指肠溃疡、食管破裂、食管狭窄等相关疾病曾行胃或食管手术史,再次外科治疗无法使用传统的胃代食管手术,只能选择放射治疗或安放食管内支架,可暂时缓解进食困难,却达不到根治目的。本研究回顾性分析在北京同仁医院(以下简称“我院”)接受带蒂结肠移植手术的病例,评估对既往有食管或胃手术史的食管癌患者,采用病变食管切除、结肠代食管手术治疗的可行性及长期预后结局。
1 资料与方法
1.1 一般资料
回顾性分析1992 年3 月—2018 年3 月就诊我院胸外科曾接受食管、胃手术史再罹患食管癌并接受根治性手术的患者112 例。纳入标准:①诊断符合食管癌规范化诊治指南[1],病理证实为食管癌;②既往有胃或食管的手术史;③按国际抗癌联盟食管癌分期标准[4]为T1N0M0~T3N1M0的患者。排除标准:①合并其他脏器肿瘤;②心肺储备功能差,无法耐受手术;③术前结肠造影示结肠变异无法使用结肠移植者;④远处转移,无手术指征;⑤存在明显手术禁忌证。112 例食管癌患者中既往接受7种不同的食管或胃手术,术后至诊断为食管癌的时间为0.5~22 年,中位时间5.5 年,其中男82 例,女30 例,年龄40~74 岁,中位年龄56.5 岁。既往手术、现患食管癌部位及TNM 分期见表1,癌瘤长度为2~6 cm。鳞癌106 例,鳞腺癌4 例,腺癌2 例。本研究经我院医学伦理委员会批准。
1.2 治疗方法
1.2.1 外科治疗及手术方式 既往手术史及食管重建术见表1。本研究患者通过术前结肠钡气双重造影(图1)、肠系膜上动脉、肠系膜下动脉血管造影(图2)及术中多普勒血流检测(见图3A)评估结肠供血血管的走行范围、血管搏动强度及边缘血管的情况[3]。带血管蒂的结肠段(图3B、3C)经食管床或胸骨后径路提起至颈部与下咽或颈段食管吻合(图3D)。5 例患者行间置带蒂短结肠段替代食管手术,此术式保留了食管下段及贲门;从腹部游离带血管蒂的横结肠长约8~15 cm,经膈孔向上提至后纵隔,分别与切除病变后的食管上、下断端进行端端吻合。有关结肠段血供、蠕动方向及上提通道见表1~2。5 例患者接受经左胸入路病变食管切除+顺行胃管或倒置胃管替代食管术式:将输出空肠袢与切断胃空肠吻合口的输入空肠袢端侧吻合,将残胃连同胃网膜左动脉、胃短动脉全部提至弓上进行食管胃吻合。倒置胃管者,使用切割缝合器将胃大弯制作成管状胃,将食管与胃在弓上吻合。

图1 术前结肠钡气双重造影了解结肠形态
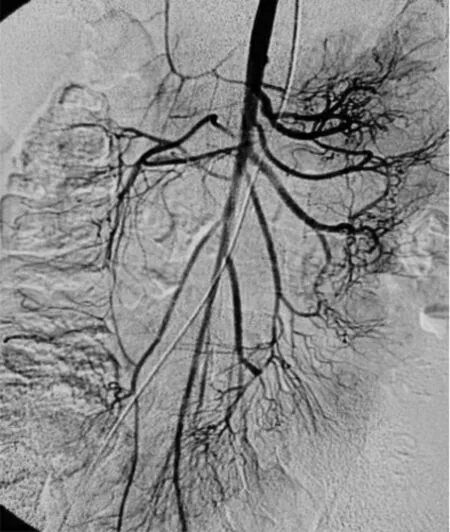
图2 术前肠系膜血管造影显示移植结肠段血管走行及分布

图3 经胸骨后通道带蒂结肠段上提至颈部与颈段食管进行吻合

表1 112 例患者既往手术史、现患食管癌病变部位和分期、食管重建术式(例)
1.2.2 观察指标及随访 近期疗效(围术期并发症;术后生活质量Spitzer 评分[5-6],包括日常活动情况、健康状况、家庭及朋友的帮助情况、对未来生活的展望,每项按实际状况0~2 打分,该指数上下限为0~10 分)和远期疗效(通过生存曲线观察3 年及5 年生存率,累积生存率的计算是将各个时点的生存概率进行乘积计算而来,考虑删失数据的影响)。患者术后1 年内每3个月复查胸部CT、颈部和腹部超声检查,每6个月复查上消化道造影检查,随后3 年每6个月进行一次常规随访,5 年后每年进行年度随访。
1.3 统计学方法
采用R(version 3.4.3)软件进行统计学分析。计数资料采用百分率表示。采用Kaplan-Meier 生存分析,评估3 年及5 年生存率,采用Log-rank 检验比较不同TNM 分期食管癌患者生存曲线。以P <0.05 为差异有统计学意义。

表2 结肠段血供、蠕动向及上提通道
2 结果
2.1 近期结局
术后30 d 内并发症17 例(15.2%),结肠-食管颈部吻合口瘘5 例,Ⅰ型呼吸衰竭3 例,阻塞性肺不张3 例,不完全性肠梗阻2 例,房颤2 例,室上性心动过速1 例,声音嘶哑1 例,均经相关对症处理后获得治愈。2 例患者为倒置胃管+食管癌切除、结肠代食管手术,因腹腔粘连较重,肠游离松解时间较长,分别于术后第3 天、第5 天死于肺栓塞及多脏器功能衰竭(占全组病例1.8%)。17 例接受逆蠕动长段结肠移植术患者中,12 例诉偶有口臭或咽喉不适感,症状持续半年逐渐消失。术后Spitzer 生活质量评分为空肠造口者<5 分;食管改道者6~7 分;食管癌切除者7~9 分。
2.2 远期结局
本研究中位随访时间为52个月,中位生存期为39个月,全部患者术后3 年生存率为51.35%,5 年生存率为23.53%。54 例Ⅰ期与ⅡA 期患者3 年生存率为61.89%,5 年生存率为43.32%。58 例ⅡB 期与Ⅲ期患者3 年生存率为42.43%,5 年生存率为10.29%。Kaplan-Meier 生存曲线(图4),Ⅰ+ⅡA 期与ⅡB+Ⅲ期患者生存率比较,差异有统计学意义(P=0.003)。
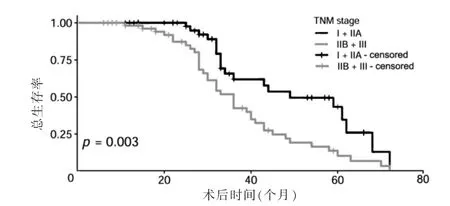
图4 Ⅰ+ⅡA 期与ⅡB+Ⅲ期食管癌患者行结肠代食管手术的生存曲线比较
3 讨论
食管癌恶性程度较高,手术是最有效的治疗方式[7-8]。既往有食管或胃手术史再患食管癌者,若无明显手术禁忌证,仍可选择再次手术[7-9]。当前人造食管尚未成功应用于临床,目前主张采用自体组织重建食管[10]。有研究采用皮瓣、空肠及显微血管吻合游离肠段代食管术,均有一定的技术难度和弊端,亦有学者考虑采用结肠代食管术[3,5,11-15]。该术的并发症率和死亡率比胃代食管高[16-17],但通过近半个世纪对结肠代食管术的基础和临床应用研究,已使该术并发症发生率和死亡率分别由40%、11%下降到15.0%、1.9%[14,18],本研究术后3 年及5 年总生存率分别为51.35%及23.53%,与之前文献报道结果相似[14,16,18],Ⅰ+ⅡA 期患者生存率高于ⅡB+Ⅲ期患者(P=0.003),提示TNM 分期是食管肿瘤切除结肠代食管手术长期预后的主要危险因素。
带蒂结肠移植过程中最重要的步骤是保持结肠移植物足够的血供[19]。肠系膜血管具有高度可变异的血管解剖结构,据文献报道,右结肠动脉、中结肠动脉和左结肠动脉具有不同的分支模式,在89%的标本中,左结肠动脉在离脾曲不到3 cm 的地方出现分支,而在25%的标本中,左结肠动脉发出横向分支,在下降部分与边缘动脉相连[20]。我们在实际工作中发现,边缘动脉始终是恒定且发育良好的。左结肠动脉可呈T型或V型分支,也可呈多分支,左结肠动脉右支与中结肠动脉左支汇合,形成边缘动脉[3]。肠系膜下动脉、髂内动脉之间通过直肠动脉的连接为左结肠提供了额外的血液供应[20-21]。由于结肠分支的这些解剖变异,结扎任何主要分支前必须对肠系膜进行临时钳夹并判断移植结肠段血运,这种方法可以保证边缘动脉在移植结肠段的连续性[3,21]。
与右半结肠相比,左半结肠的优势在于其血供更加集中,解剖变异较少,管径更接近食管管径[22]。此外,左半结肠壁比右半结肠壁厚,不像右半结肠壁那么薄弱,也不容易扩张[21]。有报道显示,左半结肠移植手术后表现出更少的酸和胆汁反流,降低吸入性肺炎的风险[23]。左半结肠的主要缺点是在一些老年人群中,结肠病变如憩室病的存在,使其不能作为适合的移植肠段[21]。对于大多数结肠移植食管重建的病例,后纵隔路径似乎是大多数外科医生的首选,后纵隔通路为颈部提供了更短、最直接的路径,移植物血管损伤和近端导管静脉充血的风险较小,但在二期重建手术中,后纵隔的粘连几乎总是存在,此时胸骨后路径是最好的选择。胸骨后路径术后可进行局部放疗,抑制癌细胞微残留,有效延长生存期[24-25]。
