传统工业大锅与小锅炒制羊肉臊子挥发性风味物质差异分析
2021-07-28王永瑞罗瑞明
柏 霜,王永瑞,罗瑞明
(宁夏大学农学院,宁夏 银川 750021)
羊肉臊子是中国西北地区著名传统炒制肉制品,其主要原料来自于滩羊肉。炒制肉制品是中式烹饪的特色加工方式,与油炸、煎等其他油炸方法相比,这种烹煮方式可以使肉具有独特的烹饪品质,并能更好地保留如VB1、VB6以及锌、镁和铁等微量元素[1]。长期以来,小锅炒制羊肉臊子备受青睐,而大锅炒制的羊肉臊子却难以炒出小锅羊肉臊子的风味。工业大规模生产的炒制肉制品很大一部分在炒制过程中没有与锅底充分接触,最终的肉制品并不是被炒制熟,而是被高温蒸汽加热熟(炒制过程温度最高为100 ℃,类似于炖煮),导致大锅炒制肉制品风味物质含量少,风味淡薄[2]。小锅炒制物料大部分是贴锅层炒制,能够充分受热,美拉德反应、脂质氧化热降解等反应充分,促进挥发性风味物质生成。然而,到目前为止,有关炒制肉制品的研究多为某一种调味品对炒制肉制品的影响,如香茅对小炒肉风味的影响[3],对大锅与小锅炒制肉制品本身风味及品质差异鲜见报道。此外,复杂的传热传质动力学和准确的炒制操作技巧也限制了炒制肉制品在工业生产中的应用。因此,研究大锅与小锅炒制羊肉臊子挥发性风味物质差异及其品质变化的内在机制很有必要。
电子鼻和气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)也经常被用来研究食品风味,以校正感官评价的主观判断[2]。GC-MS已经成为鉴定肉类食品挥发性化合物的主要方法之一。顶空固相微萃取因其快速、简单、环保等优点被广泛应用于食品中挥发性物质的萃取。
羊肉臊子作为一种传统特色肉制品,对其风味、品质研究报道较少。本实验通过顶空固相微萃取与GC-MS联用技术对以滩羊肉为原料炒制羊肉臊子过程中的挥发性化合物进行分析,研究工业大锅与小锅不同炒制阶段挥发性风味化合物差异性。以期为羊肉臊子的风味检测、工业化生产品质控制、智能风味炒制机研制提供技术支撑。
1 材料与方法
1.1 材料与试剂
滩羊肉来自宁夏盐池县大夏牧场食品有限公司。为减少不用月龄滩羊肉风味物质不同及未阉割公羊膻味较重对本实验的影响,选择滩羊为6 月龄阉割公羊,经屠宰、放血、去内脏、清洗,然后贮存在-80 ℃超低温冰箱。精选滩羊后腿肉,分割整理,切除腿骨、软骨、淋巴、筋腱,去净肉皮表面污物,剔除表面脂肪,切成1 cm×1 cm×1 cm大小肉丁备用。脂肪采用成块羊尾脂肪,切成1 cm×1 cm×1 cm大小备用,每个样品瘦肉与脂肪质量比为7∶3。
2-甲基-3-庚酮、正构烷烃(C6~C30)(均为色谱级) 上海西宝生物科技有限公司;花椒、料酒、生抽等调味料 佛山市海天(高明)调味食品有限公司。
1.2 仪器与设备
PEN3.5电子鼻 德国Airsense公司;DW-8L930超低温冰箱(-86 ℃) 无锡冠亚恒温制冷技术有限公司;H-SY2L-NI 6-C恒温水浴锅 北京长源实验设备厂;BSD1600-30A/MN1808麦饭石电热锅 深圳市邦仕达科技有限公司;2010 Plus GC-MS联用仪 日本岛津公司;固相微萃取头 美国Supelco公司;TESTO735-2型数字温度计 德国德图公司;ZFGRQ400智能自翻式燃气炸炒锅 河北世轩科技有限公司。
1.3 方法
1.3.1 羊肉臊子炒制工艺
本实验炒制工艺来自宁夏涝河桥肉食品有限公司(图1)。将130 kg(肥瘦比3∶7)羊肉丁腌制15 min,油温80 ℃(7.5 kg胡麻油)时倒入工业大锅中(电压380 V,功率4.4 kW),选定炒制程序(翻炒频率24 次/min)炒制35 min,炒制25 min时温度达到95 ℃(宁夏平均海拔1 000 m,水的沸点在95 ℃左右)。小锅为平底锅(小火档位800 W),将7 kg羊肉丁腌制15 min,煸炒去水8 min(最高温度95 ℃)后倒入3 kg脂肪丁煸炒出油6 min(最高温度150 ℃)小锅内继续炒制200 s(最高温度126 ℃)。
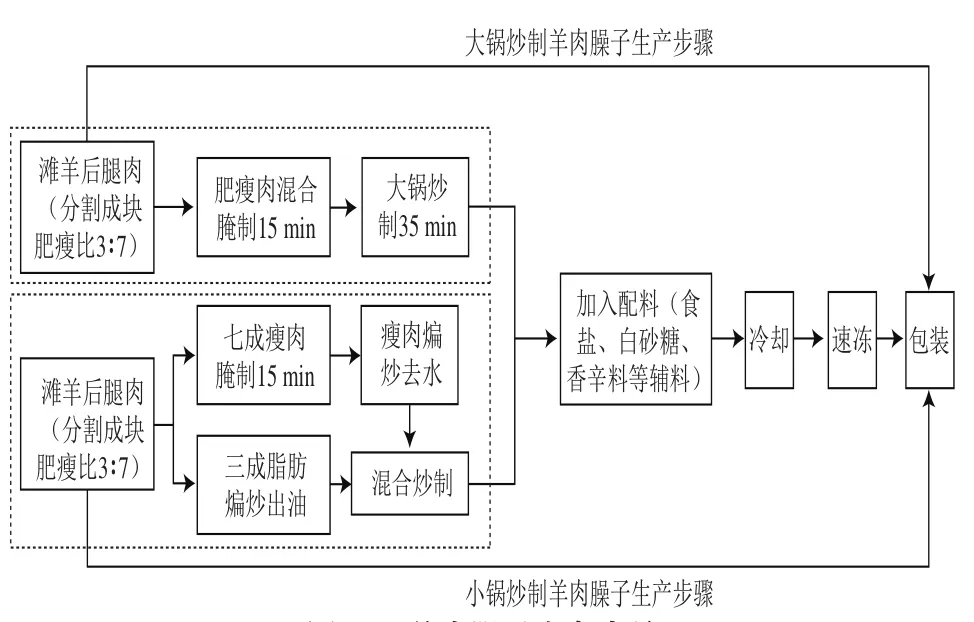
图1 羊肉臊子生产步骤Fig.1 Flow chart depicting the production process for industrial stir-fired diced mutton
1.3.2 电子鼻分析
电子鼻由10 个金属氧化物半导体传感器组成,具有一定特异性,包括W1C(对芳香族化合物敏感)、W5S(对氮氧化物敏感)、W3C(对氨类和芳香型化合物敏感)、W6S(对氢气敏感)、W5C(对烯烃和芳香型化合物敏感)、W1S(对烃类物质敏感)、W1W(对硫化氢敏感)、W2S(对醇类和部分芳香型化合物敏感)、W2W(对芳香化合物和有机硫化物敏感)、W3S(对烷烃敏感)[4]。
实验前,取5 g样品放入20 mL密闭瓶中,于25 ℃水浴中平衡20 min后用电子鼻进行测定。电子鼻设置参数:样品测定间隔时间1 s;冲洗时间100 s;零点调整时间10 s;样品准备时间5 s;样品测试时间100 s。测量完毕,用清洁空气冲洗容器,直到传感器信号返回基线。
1.3.3 挥发性化合物分析
采用顶空固相微萃取与GC-MS结合的方法从样品中萃取、分离和检测挥发性化合物。3 g肉末样本和3 mL饱和氯化钠溶液添加到20 mL顶空瓶中,涡旋振荡30 s,60 ℃水浴平衡20 min,萃取头吸附30 min(50/35 μm DVB/CAR/PDMS)[5]。
GC条件:DB-WAX毛细管柱(30 m×0.25 mm,0.25 μm);升温程序:起始温度40 ℃,保持3 min,然后以5 ℃/min升到200 ℃,再以10 ℃/min升到230 ℃,保持3 min。载气为He,恒定流速2 mL/min,进样口温度250 ℃,压力112.0 kPa,不分流。
MS条件:电子电离源;电子能量70 eV;传输线温度280 ℃;离子源温度230 ℃;接口温度250 ℃;溶剂延迟2.5 min;质量扫描范围m/z50~350。
用半定量方法计算挥发性化合物的含量,以质量浓度0.489 6μg/μL的2-甲基-3-庚酮为内标物,通过峰面积与质量浓度的关系计算得到未知化合物的质量浓度[2],按下式计算:

式中:Ax、Ai分别为目标化合物的峰面积和内标化合物的峰面积;Cx、Ci分别为目标化合物和内标化合物质量浓度/(μg/μL)。
1.4 数据处理
所有结果均为3 次重复的平均值。采用Origin 2020b软件绘制电子鼻雷达图,采用SPSS 24.0软件进行电子鼻主成分分析(principal component analysis,PCA),采用MetaboAnalyst 4.0对GC-MS数据进行相关性分析、PCA。
2 结果与分析
2.1 电子鼻响应
2.1.1 电子鼻雷达指纹图谱
如图2所示,工业大锅与小锅炒制羊肉臊子在每个加工步骤的电子鼻雷达图气味轮廓曲线差异明显。炒制处理降低了0 min、原料肉样品W1C的信号响应值,说明炒制处理可以降低甲苯等芳香烃类化合物,这与牛肉炒制结果相同[2]。工业大锅与小锅炒制羊肉臊子W5S、W1S、W1W、W2S、W2W的响应值均高于0 min、原料肉样品的响应值,说明羊肉臊子炒制过程中产生了大量挥发性化合物,是羊肉臊子香气的主要物质。电子鼻W5S传感器对氮氧化合物敏感,从图2可以看出,W5S在不同炒制阶段的响应值高于0 min、原料肉的响应值,证明了炒制热加工可以促进羊肉中氮氧化合物的释放,而含氮杂环化合物一般有烤肉香气特征,也主要来源于美拉德反应[6]。W2S传感器对醇类化合物敏感,响应值高于0 min、原料肉不同的处理阶段,证明工业大锅与小锅炒制羊肉臊子过程可以促进羊肉中醇的释放,特别是小锅SFF 6 min醇类化合物含量达到最大值(表1),脂肪有助于肉类风味的形成[7]。工业大锅与小锅炒制羊肉臊子W1C、W3C、W5C、W3S、W6S对样品信号强度较低,样品间信号强度无显著差异。其中由于脂类氧化产生的氢过氧化物没有任何气味是导致W6S气味轮廓曲线无差异的原因,说明不同炒制热加工对羊肉臊子部分芳香族化合物、氨类、烯烃类、烷烃类化合物的影响不大。影响肉风味的化合物主要是由热降解和Maillard反应生成[8]。含硫化合物是肉香味中非常重要的一类嗅感物质,有研究发现加热牛肉挥发性成分中去掉硫化物,肉香味几乎完全消失[2,9]。W1W和W2W传感器均对硫化物敏感,而小锅SFF阶段电子鼻W1W和W2W响应值明显高于MSF、SFRW阶段和工业大锅炒制各时间,说明滩羊脂肪在高温炒制阶段含硫化物含量显著增加,如二甲基砜、3-甲硫基丙醛随着热加工阶段的进行浓度逐渐增大,在SFF阶段浓度达到最大值。含硫化合物的形成途径非常复杂,除硫胺素的降解、脂肪中少量蛋白分子高温分解等途径外,呋喃类衍生物形成含硫化合物也是一条重要的途径[9]。

图2 羊肉臊子炒制加工不同阶段电子鼻雷达图Fig.2 E-nose response radar of stir-fried diced mutton samples from different processing stages
2.1.2 电子鼻PCA
如图3所示,贡献率越高,PC对原始多指标信息的反映越好[10]。前2 个PC的累计方差贡献率大于90%,说明前2 个PC覆盖了样品绝大多数气味信息[11],PC1代表总方差的78.52%,PC2代表总方差的16.00%。样品的差异主要体现在PC1上。工业大锅炒制羊肉臊子不同时间点(0~35 min)的样本可以很容易地分为8 组,小锅不同加工阶段(Raw、SFRW、SFF和MSF)可以很容易地分为4 组。当样品重叠或接近时(工业大锅0 min与小锅原料肉),说明它们的挥发性化合物相似。除0 min、原料肉外,工业大锅5~35 min、小锅不同加工阶段的分布区域不同。双标图中W1C、W3C、W5C与炒制0 min、原料肉样本相关,W2S、W3S、W1S、W6S、W5S、W2W、W1W与大锅炒制5~35 min、小锅不同加工阶段(SFRW、SFF和MSF)样本相关。分析表明,不同炒制热加工阶段对羊肉臊子中的氮氧化物、芳香族化合物和烷烃、醇类硫成分有显著影响,对烷烃、氢化物和氨类化合物影响不大。因此,电子鼻是鉴别工业大锅与小锅炒制羊肉臊子不同加工时间点香气属性的有效工具,但不同加工过程中不同时间点具体的化合物很难鉴别。
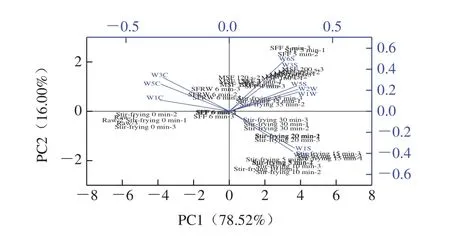
图3 炒制羊肉臊子不同加工过程的电子鼻PC双标图Fig.3 PCA biplot of E-nose data for stir-fried diced mutton samples from different processing stages
2.2 工业大锅与小锅炒制羊肉臊子不同加工阶段聚类相关性热图分析
如图4所示,聚类相关性热图分析能够明显地将工业大锅与小锅炒制羊肉臊子不同加工阶段区分开来,说明工业大锅与小锅炒制羊肉臊子不同加工阶段的挥发性化合物之间差异明显。聚类相关性热图中4 个红色区域代表不同炒制阶段的样品之间的相似性。原料肉与炒制0 min在同一区域,炒制5 min、煸炒去水6 min、炒制10 min、煸炒去水7 min、炒制15 min、煸炒去水8 min在同一区域,炒制20~30 min、混合炒制120~200 s在同一区域,炒制35 min、煸炒脂肪4~6 min在同一区域。这一结果也与电子鼻的结果相对应(图2和图3)。

图4 工业大锅与小锅炒制羊肉臊子加工阶段聚类相关性热图分析Fig.4 Cluster correlation heat map analysis of industrial large and small wok stir-fried diced mutton at different processing stages
2.3 基于GC-MS技术对工业大锅与小锅炒制羊肉臊子风味的差异性分析
肉风味与表面颜色的变化是由于美拉德反应和脂质的热降解,以及2 种反应的相互作用而产生的[12]。为更好了解羊肉臊子的风味,利用固相微萃取-GC-MS对工业大锅与小锅炒制羊肉臊子不同加工阶段挥发性化合物进行分析。如表1所示,大锅炒制羊肉臊子共检测出104 种化合物、小锅共检测出171 种化合物,其中大锅与小锅的挥发性化合物主要有醛类(20∶24(分别为20 种和24 种,下同))、醇类(24∶35)、酮类(16∶31)、酸类(9∶13)、酯类(8∶11)、吡嗪类(2∶5)、吡啶类(0∶5)、呋喃类(1∶4)、醚类(2∶3)、碳氢化合物(13∶22)、芳香族化合物(8∶12)、其他(1∶6)。工业大锅与小锅炒制羊肉臊子醛类、醇类、酮类、酯类和碳氢化合物的相对含量均较高。此外,吡嗪类和呋喃类化合物随着炒制时间的延长而增加。

表1 工业大锅与小锅炒制羊肉臊子挥发性风味物质种类及含量Table 1Types and relative contents of volatile flavor compounds identified in industrial large and small wok stir-fried diced mutton at different processing stages
2.4 工业大锅与小锅炒制羊肉臊子主要挥发性风味物质PCA
如图5所示,除大锅炒制20 min和25 min的样品分离不明显外,不同炒制时间点工业大锅与小锅炒制羊肉臊子不同加工阶段挥发性化合物的分离效果较好。

图5 工业大锅与小锅炒制羊肉臊子加工阶段挥发性风味物质PCAFig.5 PCA of volatile flavor compounds in industrial large and small wok stir-fried diced mutton at different processing stages
醛类化合物由于较低的感知阈值,即使是在少量的情况下,也常常呈现出特殊香气[13]。GC-MS检测出大锅与小锅羊肉臊子样品中醛类化合物数量为20∶24,十三醛、十四醛、辛醛、壬醛、己醛、庚醛、十二醛、癸醛、苯甲醛、3-噻吩甲醛、2-十一醛、(E)-2-辛醛、(E)-2-壬醛、(E)-2-己醛、(Z)-2-庚醛、(Z)-2-癸醛、(Z)-3,7-二甲基-2,6-辛二醛、(E,E)-2,4-壬二烯醛、(E,E)-2,4-十二烯醛和(E,E)-2,4-癸二烯醛这20 种醛类化合物是大锅与小锅羊肉臊子中共有的醛类,苯乙醛、2-羟基苯甲醛、(E)-4-癸醛和(E)-2-癸醛是小锅羊肉臊特有的醛类物质。随着温度的升高,醛类化合物的含量在煸炒脂肪6 min、炒制20 min时达到最大值,这可能是小锅煸炒脂肪6 min阶段脂肪出油温度与脂质热降解速率都达到最大值,大锅炒制20 min时脂质热降解速率增大。醛类化合物主要由脂质氧化产生己醛、壬醛、辛醛、庚醛、戊醛、2-己醛和苯甲醛[14],说明羊肉臊子中的醛类主要由脂质氧化产生。这些化合物也在鸡肉[15]、牛肉[16]和黑猪肉[17]的中发现。己醛在所有醛类化合物中含量最高,这可能也是羊肉臊子高风味品质的主要原因。己醛是肉脂质氧化过程中产生的主要醛类[18],其含量升高可能是由于不饱和脂肪酸在高温下发生脂质氧化所致(样品中脂肪含量为30%)。苯甲醛(樱桃味)来源于苯丙氨酸的Strecker降解,为羊肉臊子风味提供了特有的香气。研究表明,苯甲醛在加工过程中产生了杏仁和焦糖的特殊风味[13,19]。3-噻吩甲醛在炒制后期被检测到,其结构表明其来源于游离的Cys,而不是含有Cys的肽[8]。高温热加工过程可以快速促进多不饱和脂肪酸的氧化,从而产生更多的自由基攻击其他不易氧化脂肪酸,例如油酸可以促进庚醛、辛醛、壬醛和其他醛类物质的形成[20]。
醇类化合物具有较高气味阈值的,一般认为对肉类产品风味贡献较小[10]。GC-MS检测出大锅与小锅羊肉臊子样品中醇类化合物数量为24∶35,1-十七烷醇、芳樟醇、2-(十二烷基)乙醇、2,4-二甲基环己醇、苯甲醇、4-壬醇、4-乙基环己醇、2-呋喃甲醇、2-乙基-1-己醇、2,3-二甲基-2,3-丁二醇、[R-(R*,R*)]-2,3-丁二醇、2,3-丁二醇、2-甲氧基-1-丙醇、1-戊醇、1-辛烯-3-醇、2-丁基-1-辛醇、1-辛醇、1-壬烯-3-醇、己醇、十六醇、1-庚醇、1-十二烷醇、(E)-2-辛烯-1-醇和1-丁醇24 种醇类化合物是大锅与小锅羊肉臊子所共有,苯乙醇、正十三烷-1-醇、2-苯氧基乙醇、2-(2-丁氧基乙氧基)-乙酸酯乙醇、2-甲基-2-十一碳硫醇、(E)-2-十三烯-1-醇、2-壬醇、乙酸-2-呋喃乙醇、(2Z)-3-戊基-2,4-戊二烯-1-醇、5-甲基-2-(1-甲基乙基)-1-己醇和1,3-丙二醇10 种醇类化合物是小锅羊肉臊所特有。如表1所示,羊肉臊子的醇类化合物含量受热加工温度与时间的影响。所有样品中均检测到脂质氧化分解产生的1-辛烯-3-醇和1-戊醇。考虑到醇类化合物的阈值较高,短直链醇类物质可能对产品风味没有贡献。但1-正醇、1-己醇、1-十二醇、4-壬醇等长直链醇类物质阈值相对较低,对产品的香气有促进作用[21]。此外,1-辛烯-3-醇、(E)-2-辛烯-1-醇、1-壬烯-3-醇等支链醇具有较低的阈值,可能对羊肉臊子的香气有显著影响。脂肪族醇可能通过不饱和醇促进肉品风味,而不饱和醇的阈值低于饱和醇[21]。例如,在不同的温度和时间组合下,煮制和烤制的羊肉中检测到大量具有产生蘑菇气味的1-辛烯-3-醇[22-23]。然而,具有较高气味阈值的醇类物质一般不被认为是肉类产品的重要风味贡献者[10]。
酮类化合物被认为对肉类和肉制品的香气有很大的影响,因为酮类物质会散发出一种特殊的气味,并且在食物中大量出现[15]。GC-MS检测出大锅与小锅羊肉臊子样品中酮类类化合物数量为16∶31,反式-3-壬烯-2-酮、壬-3,5-二烯-2-酮、羟基丁酮、6-甲基-5-庚烷-2-酮、(Z)-6,10-二甲基-5,9-十一碳二烯-2-酮、6,10-二甲基-5,9-十一碳二烯-2-酮、3-乙基-2-十五酮、2-十一酮、2-吡咯烷酮、2-戊基环戊酮、2-庚酮、2-癸酮、2,3-辛二酮、2-甲基-3-辛酮和2(5H)-呋喃酮15 种酮类物质是大锅与小锅羊肉臊子所共有,5-乙基二氢-2(3H)呋喃酮是大锅炒制羊肉臊子特有的酮类物质,5-(2-丁基乙基)-吡咯烷-2-酮、3-丁基环戊酮、2-(1-甲基-2-氧丙基)-环己酮、3-壬烯-2-酮、3-乙基-2-十三酮、2-十三酮、2-哌啶酮、2-壬酮、四氢-6-丙基-2H-吡喃-2-酮、四氢-6-戊基-2H-吡喃-2-酮、四氢-6-甲基-2H-吡喃-2-酮、四氢-2H-吡喃-2-酮、5-丁二氢-2(3H)-呋喃酮、1-辛烯-3-酮、1-庚烷-3-酮和1,4-环己-2-烯二酮16 种酮类物质是小锅羊肉臊子所特有。2,3-辛二酮可以被认为是区分不同炒制阶段的重要化合物之一,因为其含量差异很大,在某些阶段可以检测到,而在其他阶段则没有。虽然羟基丁酮(甜的,黄油味)在烤牛肉中不是主要的气味影响因素[24],但它在羊肉臊子中浓度很高,可能对整体气味感知有微妙的影响。
酯类化合物通常具有典型的香甜味和果香味,主要由酸类和醇类物质在肉制品中酯化产生[25]。GC-MS检测出大锅与小锅羊肉臊子样品中酯类化合物数量为8∶11,2-氧代壬酸甲酯、正己酸乙烯酯、L-泛酰内酯、肉豆蔻酸异丙酯、二乙基甲磺酸甲酯、γ-十二内酯和δ-壬内酯是大锅与小锅羊肉臊子中共有的酯类物质,碳酸十一烷基乙烯酯是大锅炒制羊肉臊子特有的酯类物质,丁内酯、3-甲基-2-氧代戊酸甲酯、戊二酸二甲酯和丁二酸二甲酯是小锅羊肉臊特有的酯类物质。肉豆蔻酸异丙酯在所有酯类中含量最高,大锅炒制0~20 min内随温度升高显著升高,在25~35 min内随温度下降显著下降。特别的,内酯类物质可能来自于羟基酸分子的内酯化[26]。
高分子质量的酸类化合物酸性较弱,对肉类风味的贡献不明显,而低分子质量的酸类由于具有较强的酸性,对肉类风味贡献较大[27]。中链酸(C6~C11)挥发性更强,对肉的香气影响更大[16],在本研究中,检测到正丁酸、己酸、壬酸、辛酸、(E,E)-2,4-壬二烯醛、戊酸等中链酸。GC-MS检测出大锅与小锅羊肉臊子样品中酸类化合物数量为9∶13,醋酸、二乙基乙酸、丁酸、己酸、壬酸、辛酸、戊酸、十四酸和2-乙基己酯苯甲酸9 种酸类物质是大锅与小锅羊肉臊子所共有,2-甲基丙酸、庚酸、3-甲基丁酸和(R)-(-)-4-甲基己酸4 种酸类物质是小锅羊肉臊所特有。
在肉类加热过程中,脂类的美拉德反应和热降解也产生了呋喃、吡啶和吡嗪类等大量的杂环化合物[28]如2-呋喃甲醇、2(5H)-呋喃酮、2-戊基呋喃、甲基吡嗪、2,3-二甲基吡嗪等均在工业大锅与小锅炒制羊肉臊子中检测到。5 种吡啶类化合物只在小锅炒制羊肉臊子中检测到,这是因为工业大锅炒制羊肉臊子最高温度只有95 ℃,而小锅炒制最高温度可达到150 ℃,其中氨与脂肪氧化产物2,4-癸二烯反应生成的2-戊基吡啶是构成羊肉香味的重要挥发性化合物[29]。亚油酸氧化产生的2-戊基呋喃可归因于脂肪和肉质香气,其形成通常与热加工过程有关[15]。工业大锅与小锅炒制羊肉臊子碳氢化合物数量为13∶22,在挥发性化合物中占很高的比例,但由于其气味阈值相对较高[30],对样品整体风味贡献不大。D-柠檬烯是由调味品和香料产生的[31]。2-甲基-2-十一硫醇和二烯丙基二硫化物主要来源于半胱氨酸、胱氨酸等含硫氨基酸和硫胺素化合物(VB1)的热降解,从而产生熟肉的香气[32]。醇类、醛类、酮类、酸类、酯类等挥发性化合物共同构成了羊肉臊子独特的风味。
3 结 论
采用固相微萃取-GC-MS与电子鼻测定工业大锅与小锅炒制羊肉臊子风味成分。GC-MS共检测出工业大锅炒制羊肉臊子104 种挥发性化合物,小锅炒制羊肉臊子171 种挥发性化合物,其中大锅与小锅的挥发性化合物主要有醛类(20∶24)、醇类(24∶35)、酮类(16∶31)、酸类(9∶13)、酯类(8∶11)、吡嗪类(2∶5)、吡啶类(0∶5)、呋喃类(1∶4)、醚类(2∶3)、碳氢化合物(13∶22)、芳香族化合物(8∶12)、其他(1∶6)。结果显示电子鼻对工业大锅与小锅炒制羊肉臊子不同加工阶段的香气具有明显的响应,W1S、W1W、W2S、W2W、W3S传感器与所有样本有较强的相关性,虽有部分重叠,但电子鼻能够很好地区分不同加工时间点的工业大锅与小锅炒制羊肉臊子。工业大锅与小锅炒制羊肉臊子不同加工阶段的聚类相关性热图与挥发性化合物PCA表明在不同的炒制阶段有很好地区分,证明固相微萃取-GC-MS和电子鼻技术评价工业大锅与小锅炒制羊肉臊子风味可行。
