单纯后路及后-前联合入路手术治疗非治愈性结核性胸腰椎后凸畸形的临床疗效研究*
2021-07-21麦尔旦江麦合木提杨文鹏买尔旦买买提武峻申戴志兵江仁兵盛伟斌
麦尔旦江·麦合木提 杨文鹏 买尔旦·买买提 武峻申 戴志兵 江仁兵 盛伟斌
(1.新疆医科大学附属肿瘤医院骨与软组织科,乌鲁木齐 830011;2.新疆医科大学第一附属医院脊柱外科,乌鲁木齐 830054)
脊柱结核常累及胸腰椎,是引起脊柱后凸的常见病因。畸形的发展包括Ⅰ期(活动期)和Ⅱ期(静止期)。90%以上的Ⅰ期患者,结核侵蚀并破坏前柱结构而引起椎体塌陷[1]。Rajasekaran[2]报道当结核累及胸椎或胸腰段并破坏造成单一节段椎体的塌陷时,会导致35°~40°的脊柱后凸畸形,而累及腰椎并破坏造成单一节段椎体的塌陷时,会导致20°的脊柱后凸畸形。抗结核药物对控制结核感染方面非常有效。多数Ⅰ期脊柱结核患者经抗结核治疗后局部形成僵硬性骨性融合,遂进入Ⅱ期,这是脊柱结核治愈的标志。但也有部分患者因椎体破坏严重、前柱骨缺损大并有较多死骨、死腔的形成,虽经长期正规抗结核治疗但迁延不愈,表现为反复发作,成为Ⅰ期的非治愈性脊柱结核。随结核的反复发作及累及破坏节段的增加,后凸畸形进一步加重,甚至顶椎附近椎体或邻近几个节段椎体出现倾倒现象[3-5]。对于轻度后凸畸形采取单纯后路手术就能达到满意的治疗效果,而病变累及多节段的严重后凸畸形采取单纯后路手术时,对充分病灶清除、支撑植骨,重建脊柱稳定性方面仍存争议[4]。本研究通过回顾性分析2010年3月至2019年9月期间我院收治的43例不同程度的非治愈性结核性胸腰椎后凸畸形病例,分析其临床疗效及总结其治疗方法,报告如下。
1 资料与方法
1.1 一般资料
自2010年3月至2019年9月期间收治了1164例脊柱结核患者。纳入标准:①病灶累及胸、腰椎(T2~L4)的非治愈性脊柱结核;②接受手术治疗并临床资料完整者。排除标准:①非结核性脊柱畸形;②合并肿瘤、无法耐受手术者;③配合度及依从性差者。根据纳入与排除标准,共43例患者纳入本研究。
根据Cobb角、结核累及节段数、破坏椎体数及完全丢失椎体数,将2010 年3 月至2019 年9 月收治的43 例非治愈性结核性胸腰椎后凸畸形患者进行分组。轻度组(Cobb 角≤80°和符合下列任意一项):①累及节段数≤3 个;②破坏椎体数≤6 个;③完全丢失椎体数≤3个。重度组(Cobb角>80°和符合下列任意一项):①累及节段数>3个;②椎体破坏数>6个;③完全丢失椎体数>3个。
轻度组16例患者,其中男7例,女9例;采用后路经椎间孔入路病灶清除、椎体间融合内固定治疗患者6 例,采用一期经后路病灶清除、Smith-Petersen(SP)截骨加压融合术治疗患者10 例。年龄2~53岁,平均(18.5±14.5)岁。结核病程0.5~16 年,平均(4.5±4.2)年。抗结核史2~12个月,平均(8.1±3.4)个月。9例(56.3%)患者术前表现不同程度的结核中毒症状,如低热、盗汗等。3 例(18.8%)患者形成窦道。美国脊柱损伤协会(American Spinal Injury Association,ASIA)脊髓损伤分级D 级14 例,E 级2 例。VAS评分2~5 分,平均(3.3±1.1)分;ODI 评分5.4%~34.0%,平均18.3%±8.1%。采用Surgimap 软件测量Cobb 角为35°~78°,平均61.1°±14.0°。术前脊柱矢状面偏移(sagittal vertical axis,SVA)为13.3~68.7 mm,平均(29.1±12.9)mm。病变累及1~3个节段,平均(1.7±0.7)个节段;破坏椎体数为2~5 个,平均(2.9±0.9)个;完全丢失椎体数为0.5~3个,平均(1.5±0.8)个。红细胞沉降率(erythrocyte sedimentation rate,ESR)增高13(81.3%)例,C 反应蛋白(C-reactive protein,CRP)增高11(68.8%)例。
重度组27例患者,其中男10例,女17例,均采用后柱截骨、悬臂梁技术+牵引矫正联合前路植骨融合治疗。年龄2~38 岁,平均(17.3±9.9)岁。结核病程1~32 年,平均(11.5±7.3)年。抗结核史6~18 个月,平均(11.7±3.2)个月。16例(59.3%)患者术前表现不同程度的结核中毒症状。3 例(11.1%)患者形成窦道。ASIA 分级B 级2 例,C 级4 例,D 级20 例,E 级1例。VAS 评分0~8 分,平均(3.0±1.9)分;ODI 评分5.4%~49.6%,平均20.2%±11.3%。采用Surgimap 软件测量Cobb 角为81°~144°,平均105.2°±17.7°。术前矢状面SVA 为-97~79 mm,平均(40.5±20.4)mm。病变累及3~6个节段,平均(3.6±1.0)个节段;破坏椎体数为2~10 个,平均(5.4±2.0)个;完全丢失椎体数为1.5~8个,平均(4.0±2.1)个。ESR增高22(81.5%)例,CRP增高15(55.6%)例。所有患者术后随访12~48个月,平均(30.8±6.7)个月。
本研究获得医院伦理委员会批准(20180223-157),患者均签署知情同意书。
1.2 手术方法
所有患者均采用气管插管全身麻醉。术中全程行感觉诱发电位(somatosensory evoked potential,SEP)和运动诱发电位(motor evoked potential,MEP)监测。
后路手术:麻醉生效后,患者取俯卧位在C 型臂X线机辅助下取后侧以顶椎为中心向上、下延伸3~4个椎体沿棘突取纵行切口。充分暴露术区,用骨膜剥离器剥离椎旁肌并显露棘突、双侧椎板至小关节突外侧缘,横突根部,病变部位上、下至少2~4个椎体对称植入椎弓根螺钉。病变位于胸腰段(T10~L2)患者,病灶清除前先于一侧放置连接棒临时固定,避免节段间移位导致脊髓损伤。于另一侧切除上、下关节突,可切除部分椎板充分显露手术视野,用神经剥离子小心显露神经根及硬膜囊外侧缘,然后小心沿椎旁分离。病变累及胸椎者,如有暴露困难时可切除肋骨近端,必要时可切断、结扎节段神经、血管束。显露结束后彻底清除坏死椎间盘、肉芽组织、死骨、死腔及脓肿,同法行对侧病灶清除(图1)。除病变位于胸腰段患者外其余患者,在病变椎椎间隙水平面用超声骨刀或枪状咬骨钳切除双侧小关节突关节、椎板、棘突及韧带。病灶清除前一侧放置连接棒临时固定,显露清楚后彻底清除坏死椎间盘、肉芽组织、死骨、死腔及脓液,用超声骨刀或骨锉修平上、下椎体骨面行关节突部分截除SP截骨术。将临时固定棒改放置于对侧,同样的方法进行对侧,最终通过连接钉、棒进行矫形固定(图2)。
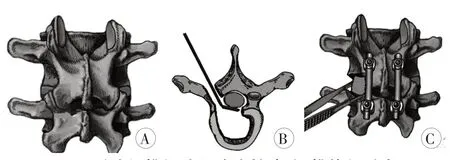
图1 后路经椎间孔入路病灶清除、椎体间融合内固定手术示意图
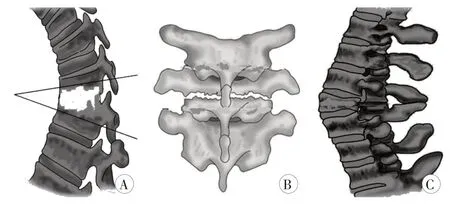
图2 经后路病灶清除、SP截骨加压融合手术示意图
后-前联合手术:麻醉生效后患者常规暴露术区,植入椎弓根螺钉后一侧用已预弯的短棒临时固定,于对侧截骨节段后方切除棘上、棘间韧带,应用超声骨刀或椎板咬骨钳切除双侧部分小关节突关节、棘突及椎板(图3A)。调换临时固定棒后同法行截骨松解。后凸顶部两侧经横突间及椎间孔吸出前方脓液,清除部分坏死椎间盘组织及死骨。交替安装两对长棒,解除临时固定棒,通过悬臂梁技术+纵向牵引(分别在双侧腋下和踝关节处牵引)矫正畸形(图3B)。确认SEP 及MEP 监测无异常后,依次更换预弯好的连接棒并加以固定(图3C)。矫正畸形后根据结核破坏部位程度、范围及手术耐受情况选择同期或二期经胸腔或腹膜外入路彻底清除剩余的病变组织,选取合适大小的植骨块植入椎体骨缺损处(图3D),使其达到充分支撑植骨的目的。
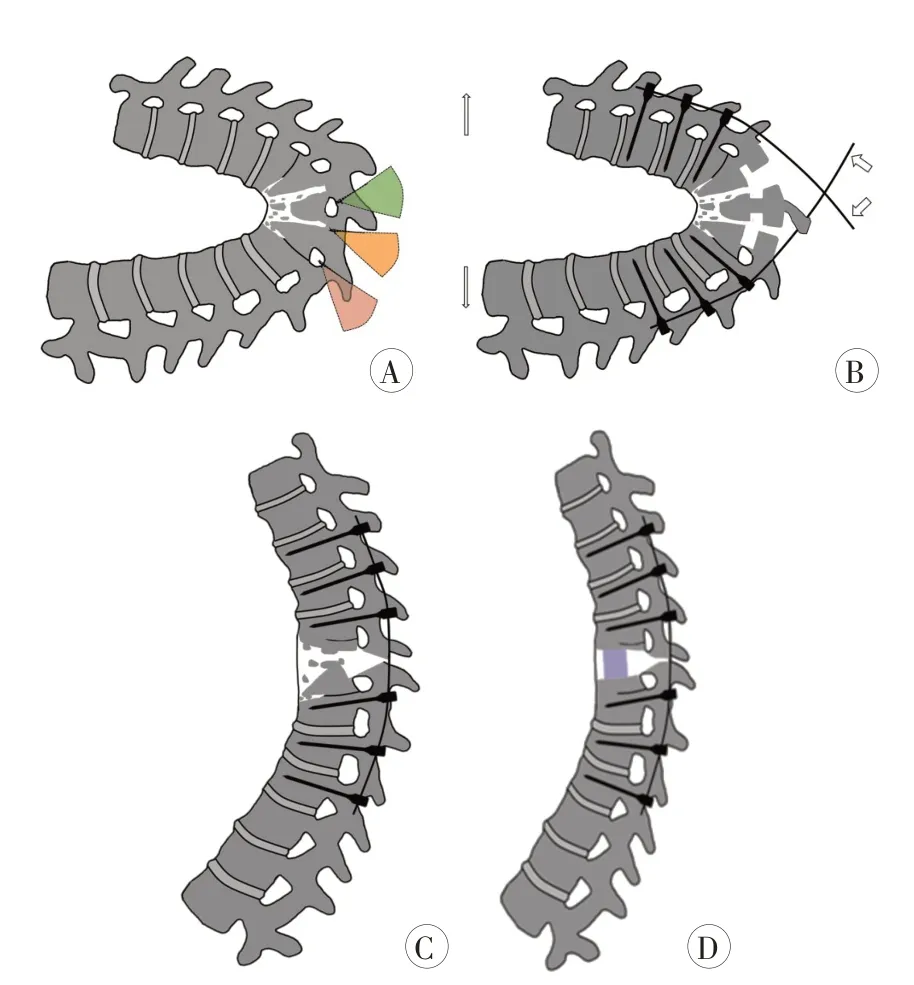
图3 后柱截骨、悬臂梁技术+牵引矫正联合前路植骨融合治疗重度非治愈性结核性胸腰椎后凸畸形示意图
所有患者矫形完成后行唤醒试验检查双下肢运动情况。C 型臂X 线机透视确定病变截骨区及内固定无异常后,放置引流管1根,生理盐水冲洗术野,后方椎板间行自体+同种异体骨粒植骨,病灶区放置链霉素2~4 g,逐层缝合关闭切口。术中收取脓液行结核分枝杆菌培养及药敏实验,术中切除的组织送病理检查。术后卧床1~3 d,预防性应用抗生素2~3 d,严密观察患者神志、感觉、运动、引流、饮食及功能锻炼情况并继续服用四联抗结核药物,辅以保肝、保肾药物。术后3 个月可停用吡嗪酰胺,6 个月停用乙胺丁醇,继续服用异烟肼、利福平至术后12~18 个月。术后每个月复查1 次肝、肾功能,若出现药物反应或肝、肾功损害,及时调整化疗药物。
1.3 观察指标
根据临床症状、手术时间、术中出血量、手术并发症、复发率、植骨融合程度、后凸畸形Cobb 角矫正率、脊柱矢状面偏移(sagittal vertical axis,SVA)及手术前后身高差,评价该手术疗效。症状和功能评价指标包括VAS、美国脊柱损伤协会(American Spinal Injury Association,ASIA)脊髓损伤分级、ODI、Kirkaldy-Willis 功能评分。实验室检查指标包括ESR、CRP。采用植骨融合Eck 等级标准评价植骨融合程度。
1.4 统计学方法
应用SPSS 22.0软件进行统计分析。计量资料以均数±标准差表示,组间比较采用t检验。以P<0.05为差异有统计学意义。
2 结果
43 例患者均顺利完成手术治疗,切口均一期愈合。所有患者都达到结核治愈,随访期间均未出现结核复发、假关节形成、内固定松动及断裂。末次随访时植骨患者均达到Ⅰ级融合,融合率为100%。
轻度组:手术时间140~420 min,平均(238.8±68.4)min,术中出血量100~1800 ml,平均(653.1±444.4)ml,术后后凸Cobb 角为8°~32°,平均21.2°±7.0°,矫正率为41%~85%,平均63.5%±14.8%;末次随访为12°~35°,平均24.9°±7.3°,Cobb 角丢失1°~9°,平均3.7°±2.0°。术后矢状面SVA 11~45 mm,平均(24.2±11.6)mm(表1)。手术前后身高差为5~43 mm,平均(26.2±12.1)mm。术后(出院前)VAS改善率为75%,与术前比较,术后和末次随访VAS评分降低(t=7.89、11.49,P<0.05)。术后(出院前)ODI 改善率为66.7%,与术前比较,术后和末次随访ODI 评分降低(t=7.32、8.67,P<0.05,表2)。术前神经功能ASIA分级D 级的14 例患者末次随访时均恢复到E 级,所有患者均为E 级。根据Kirkaldy-Willis 功能评分标准,优13例,良1例,中2例,总优良率为87.5%。
重度组:手术时间210~530 min,平均(343.0±71.5)min,术中出血量300~2600 ml,平均(1168.5±606.7)ml,术后后凸Cobb 角为5°~47°,平均28.2°±10.3°,矫正率为53%~94%,平均72.9%±9.8%;末次随访9°~57°,平均32.4°±10.9°,Cobb 角丢失1°~8°,平均4.3°±1.8°。术后矢状面SVA-34~45 mm,平均(26.6±12.6)mm(表1)。手术前后身高差为31.5~172.7 mm,平均(64.0±43.2)mm。术后(出院前)VAS改善率为47.5%,与术前比较,术后和末次随访VAS评分降低(t=6.3、7.4,P<0.05)。术后(出院前)ODI改善率为68.1%,与术前比较,术后和末次随访ODI 评分降低(t=8.4、9.1,P<0.05,表2)。末次随访时除1例术前ASIA 分级B 级患者仅改善至D 级外,其余患者均改善至E级(表3)。根据Kirkaldy-Willis 功能评分标准,优24例,良2例,中1例,总优良率为88.9%。
表1 两组手术前后及末次随访后凸Cobb角和矢状面SVA()

表1 两组手术前后及末次随访后凸Cobb角和矢状面SVA()
注:与术前比较,△P<0.05
表2 两组手术前后及末次随访VAS评分和ODI评分()
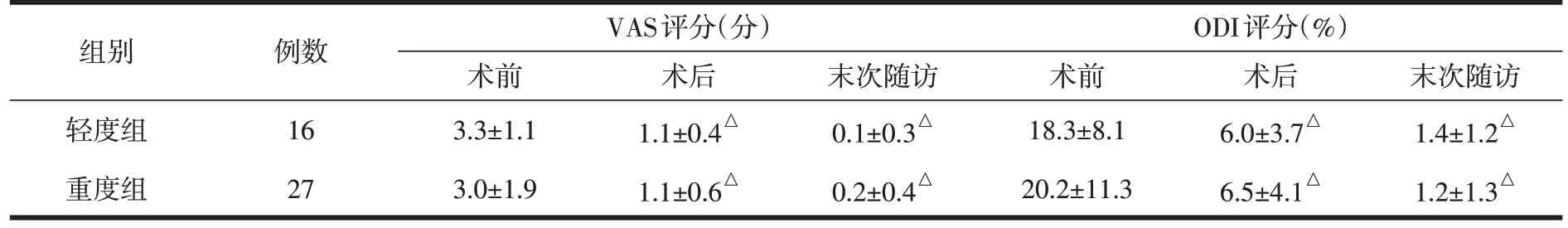
表2 两组手术前后及末次随访VAS评分和ODI评分()
注:与术前比较,△P<0.05
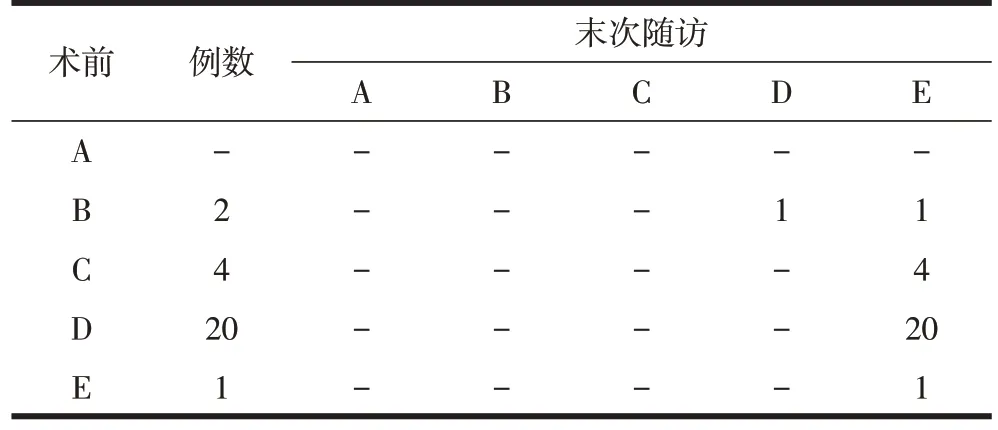
表3 重度组27例患者术前和末次随访ASIA分级(n)
并发症情况:1例重度非治愈性结核性胸腰椎后凸畸形术后第2天出现进行性下肢肌力下降,结合影像学资料考虑为脊髓缺血,并急诊行神经探查椎管减压术。术后当天输注悬浮红细胞2个单位、给予激素及下肢康复治疗,出院时右下肢肌力达到3 级,左下肢2 级,术后6 个月复查时能正常行走,双下肢肌力恢复正常。5例患者术后出现脑脊液漏(轻度2例,重度3 例),8 例患者出现胸腔积液(轻度4 例,重度4例),经腰椎穿刺置管、胸水穿刺引流、抗炎及营养支持治疗后均治愈。典型病例见图4、5。
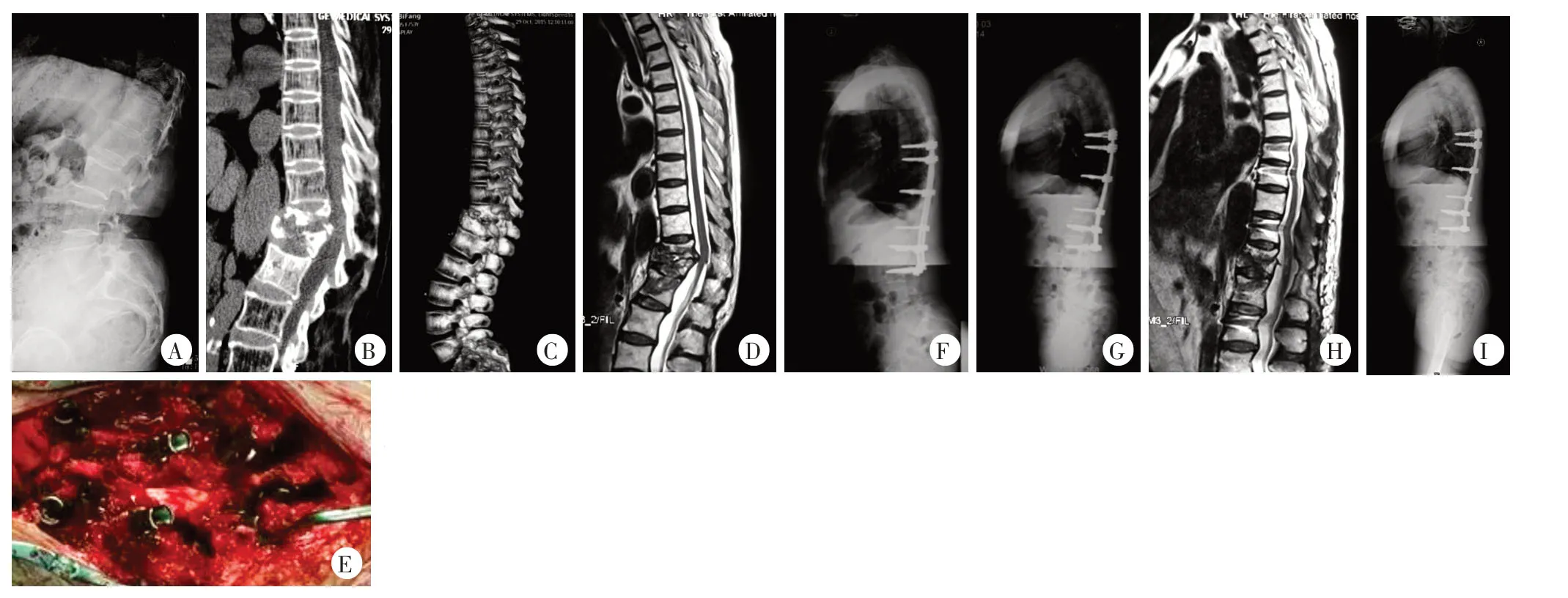
图4 患者,女,53岁,轻度非治愈性结核性胸腰椎后凸畸形,ESR 42 mm/h,CRP 21.2 mg/L
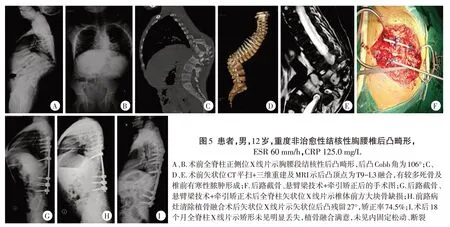
图5 患者,男,12岁,重度非治愈性结核性胸腰椎后凸畸形,ESR 60 mm/h,CRP 125.0 mg/L
3 讨论
3.1 非治愈性脊柱结核的临床表现及手术入路选择
非治愈性脊柱结核的表现与活动期(Ⅰ期)脊柱结核相似。但是大多数活动期脊柱结核经正规抗结核治疗后局部形成僵硬性骨性融合,表现为治愈性脊柱结核。而非治愈性脊柱结核虽经长期正规抗结核治疗后仍有反复出现不同程度的低热、盗汗、腰背酸痛、双下肢无力及背部窦道形成等临床表现,局部未能形成骨性融合、椎旁或椎前有寒性脓肿并周围组织软化、腰大肌脓肿等影像学表现,以及ESR、CRP增高的实验室检查特点。所以其治疗首先通过外科手术彻底清除病变区域的死骨、死腔及干酪样病变组织,联合围手术期及术后正规抗结核治疗是其治愈的关键,伴有后凸畸形者,需考虑矫正畸形、重建脊柱稳定性及减少脊髓神经压迫。现有大量的文献报道通过后方入路治疗陈旧性结核性后凸畸形[1,3,6-8],均取得了较好的治疗效果。后路手术有较好的后凸畸形矫正能力,但病灶清除方面仍存在较大争议[9]。Lee等[10]提出单纯后路手术仅适用于椎体破坏局限的早期脊柱结核的治疗。Chang等[11]认为结核累及多个节段且脊柱后凸较大时后路矫形联合前路病灶清除植骨融合术的临床疗效更为理想。因此,结合本研究患者结核累及节段数、椎体破坏数及Cobb角等病例特点,轻度组选择单纯后路手术,重度组选择后-前联合手术。
3.2 轻度非治愈性结核性胸腰椎后凸的治疗效果
在前期治疗局限于胸腰段(T10~L2)部分病变的脊柱结核时发现后路经椎间孔入路病灶清除、椎体间融合内固定手术不仅手术创伤小,操作方便,并发症少,而且可以同时达到彻底病灶清除及中重度后凸畸形矫正的目的[12]。而对于治疗除了胸腰段以外其余节段脊柱结核时发现采用经后路病灶清除、SP截骨加压融合术,可使病灶清除更彻底,脊髓减压更充分,并且在直视下完成后凸畸形的矫正,从而减少脊髓损伤等严重并发症,而且对病灶水平的后方结构行横行截骨后可直接进行加压,节段间可完成闭合,不需要行前方骨缺损处植骨融合或支撑植骨,同样达到骨愈合的目的,还可获得良好的畸形矫正和脊柱稳定性[8]。因此病变位于胸腰段(T10~L2)患者采用后路经椎间孔入路病灶清除、椎体间融合内固定术,而对位于其余节段的患者采用后路病灶清除、SP 截骨加压融合术。手术时间、术中出血量、术后后凸Cobb 角、后凸矫正率、Cobb 角丢失、术后VAS改善率、术后ODI 改善率、神经功能恢复情况与相关文献报道差异不大[1,3,10,13-15],术后未出现结核复发、假关节形成、内固定松动及断裂。可见此手术方法对于轻度非治愈性结核性胸腰椎后凸的治疗同样可达到满意的畸形矫正及彻底病灶清除的目的,是较理想的手术治疗方式。
3.3 重度非治愈性结核性胸腰椎后凸的治疗效果
在治疗重度非治愈性结核性胸腰椎后凸畸形时发现,其有以下特点:①脊柱柔韧性好,牵引可达到满意的效果;②病变累及并破坏多节段(>3 个节段);③顶椎附近椎体或邻近几个节段椎体出现倾倒现象;④椎旁或椎前有寒性脓肿并周围组织软化;⑤Cobb角>80°。因此,采用单纯后路后凸节段切除截骨(vertebral column resection,VCR)技术时,为了达到彻底病灶清除并充分支撑植骨的目的,需要扩大切除后方正常结构或采取六级截骨,进而增加手术时间及术中出血量,并通过加压后柱完成矫形时,难以避免脊髓皱褶、脊髓缺血等严重神经并发症。Zeng等[15]及Lü 等[16]通过悬臂梁技术矫正重度陈旧性后凸畸形,均取得了满意的矫形效果,并有效避免了脊髓皱褶而导致脊髓损伤。结合本研究患者脊柱柔韧性好、牵引效果可、病变累及破坏节段多而很难通过后路达到彻底病灶清除及充分大块支撑植骨特点,选择通过后柱截骨、悬臂梁技术+牵引矫形联合前路植骨融合手术。该手术方法的优点包括:①可达到彻底病灶清除及充分大块支撑植骨目的并保留后纵韧带的完整性;②减少后方正常结构的切除及后路手术节段动脉破裂出血不易控制而导致的手术时间延长等难题;③减少矫正重度后凸畸形时因支撑物移位、断裂而导致脊髓损伤及延迟愈合的风险。本研究手术时间、术中出血量及并发症发生率明显低于文献报道。术后后凸Cobb角、后凸矫正率、Cobb角丢失、术后VAS 改善率、术后ODI 改善率、神经功能恢复情况与相关文献报道差异不大[5,7,15-17]。术后未出现结核复发、假关节形成、内固定松动及断裂。可见此手术方法对于重度非治愈性结核性胸腰椎后凸的治疗可达到满意的畸形矫正、彻底病灶清除及充分大块支撑植骨的目的,而且手术时间、术中出血量及严重并发症发生率较低,是安全可靠的手术治疗方式。但亦发现其存在一些缺点:①手术创伤大,不适合体弱、心肺功能异常及营养不良者;②术中需改变体位,增加医源性损伤及感染的概率。
综上,彻底清除病变区域的死骨、死腔及干酪样病变组织联合围手术期及术后正规抗结核治疗对于非治愈性结核性胸腰椎后凸的治疗极为重要。其次通过术前仔细评估,在严格掌握适应证的前提下,充分做好围手术期管理,术中的细致操作,保持术中血压的稳定、持续神经电生理监测及术中和术后行唤醒试验检查双下肢运动情况,均有助于提高手术的安全性。
