药学干预改进国家重点监控药品使用的实践及效果分析
2021-07-19张美玲ZHANGMeiling赵云ZHAOYun
□ 张美玲 ZHANG Mei-ling 赵云 ZHAO Yun
为进一步落实深化医药卫生体制改革重点工作,有效控制医药费用不合理增长,提高医疗机构合理用药水平,加强医药购销、应用领域的廉政风险防控,2017年10月浙江省卫生计生委下发了《关于做好医疗机构重点监控药品管理工作的通知》(浙卫办医政〔2017〕8号),要求各医疗机构建立本单位的重点监控药品管理目录,对本单位使用的辅助性、营养性、临床易滥用的药品进行统计和排序,经药事委员会组织相关专家进行合理用药评价分析后,遴选出本单位重点监控药品目录,并落实重点监控药品的监测、预警、点评通报制度;建立重点监控药品奖惩考核机制;加强重点监控药品管理工作督导检查。2019年7月国家卫生健康委员会下发了《关于印发第一批国家重点监控合理用药药品目录(化药及生物制品)的通知》(国卫办医函〔2019〕558号)[1],要求各省级卫生健康行政部门会同中医药主管部门在《目录》基础上,形成省级重点监控合理用药药品目录并公布,各医疗机构在国家级、省级目录基础上形成本机构重点监控合理用药药品目录,加强目录内药品的全程管理,进一步规范医生处方行为,对纳入目录中的药品制定用药指南或技术规范,明确规定临床应用的条件和原则;开展处方审核和处方点评,加强处方点评结果的公示、反馈及利用;对用药不合理问题突出的品种,采取排名通报、限期整改、清除出本机构药品供应目录等措施,保证合理用药[2]。
随着国家一系列辅助用药、重点监控药品相关文件的出台,对价格高、用量大、非治疗辅助性等药品实施重点监管成为各医疗机构合理用药监管的重点,2017年11月,我院药事管理与药物治疗学委员会根据文件要求界定了重点监控药物的范畴和目录,共有5大类34个品种纳入重点监控药品目录,分别为质子泵抑制剂、中药注射剂、非治疗性辅助药品、营养制剂、抗菌药物,并针对这些药品构建了一系列监管措施[3]。2019年国家卫健委下发的国家重点监控合理用药药品目录(化药及生物制品)共20个品种,其中15个品种是我院原有监管的药品,5个品种未在我院药品使用目录中。现采用回顾性分析方法,通过统计分析15个国家重点监控药品的使用情况,分析评价我院事前、事中、事后全程药学干预措施的成效,以期为国家重点监控药品在临床的合理使用提供参考。
资料与方法
1.资料来源。统计分析2016年10月—2017年9月和2019年1月—2019年12月我院15个国家重点监控药品的使用量、使用金额和点评数据,其中2016年10月至2017年9月是省级重点监控药品目录确立之前,2019年1月至2019年12月是国家重点监控药品目录颁布之后。15个国家重点监控药物品种分别为:单唾液酸四己糖神经节苷脂注射液、脑苷肌肽注射液、奥拉西坦注射液、磷酸肌酸钠注射液、小牛血清去蛋白注射液、前列地尔注射液、曲克芦丁脑蛋白水解物注射液、注射用复合辅酶、转化糖电解质注射液、胸腺五肽注射液、依达拉奉注射液、注射用骨肽粉、脑蛋白水解物片、长春西汀注射液、马来酸桂哌齐特注射液。
2.方法。通过医院电子病历系统和病历夹管理系统,点评分析2016年10月—2017年9月和2019年1月—2019年12月的15个国家重点监控药品病例共1500份,病例抽取方法为在上述时间段内从每个药品使用病例中随机抽取50例,点评依据中华医学会及中华医学会各专业学组制定的疾病诊疗指南、专家共识和药品说明书等。通过点评发现问题并对重点监控药品制定监管措施,措施如下:
2.1 制定监控目录。近几年随着重点监控相应文件的出台,医院根据文件要求综合病种结构和用药情况建立本院的《重点监控药品目录》,该目录经过药事管理与药物治疗学委员会讨论投票通过,目录内药品除国家重点监控药品目录和省级重点监控药品目录外,还包含在本院用量偏大、不合理用药突出的其它非治疗性用药。纳入目录的药品在医院药品字典库中药品通用名前面加“★”标注,提醒临床医护人员该药品为重点监控药品,请严控用药指征和疗程;并在新药引进遴选原则中,增加对重点监控药品的控制,严格执行“一品两规”,从源头上做好监管。
2.2 实施动态预警。监察室每月对重点监控药品的用药量及金额进行排序,对排名前10位医生和所在科室进行公示。药学部对重点监控药品排名前3位的品种进行用量限制,第一个月不超过上月用量的80%;第二个月仍排名前3位,用量控制在上月用量的60%;若连续三个月均排名前3位,则采取停用1个月处理。重点监控药品若连续3个月排名前10位且用药不适宜率超过10%,先予以用量控制在上个月用量的50%并提交院药事管理与药物治疗学委员会讨论是否暂停使用,暂停期限一般为3~6个月。对已暂停使用的重点监控药品,若临床确需使用,可由相应科室提出申请并经院药事管理与药物治疗学委员会讨论通过后方可恢复使用。
2.3 利用审方软件实时监控。我院专科临床药师分析每个科室的重点监控药品使用情况,利用进病房查房和临床科室业务学习等机会宣讲各病区该类药品使用中存在的问题,并提出合理使用的建设性意见和建议,审方药师利用合理用药软件进行事前设置,如特定的专科用药只能特定科室、特定的专科临床医生才可以开具,药品的疗程、溶媒、给药方式等进行事前维护,在医生开医嘱时起到干预作用,如遇特殊情况医生可选择修改并实施双签名,审方药师也可借助软件与医生实时沟通, 借助信息化手段介入患者用药全过程,及时与医生、护士等临床治疗团队成员沟通用药环节存在的问题或建议。
2.4 制定点评标准。临床药师依据中华医学会及中华医学会各专业学组制定的疾病诊疗指南、专家共识和药品说明书制定《重点监控药品合理性评价标准》,充分考虑药品成本与疗效等因素,严格按照药品说明书规定的适应证、用法用量和疗程用药,保证临床用药安全、有效、经济[4-6]。并根据点评中发现的问题分类整理形成药学建议挂内网供临床医护人员参考,如《关于桂哌齐特、左卡尼汀、丹红注射液合理用药建议》《质子泵抑制剂临床使用规范》《中药注射剂临床使用管理规范》《非治疗性辅助用药临床使用规范》等等,促进临床规范使用相应药品。
2.5 制定超说明书用药使用规定。医院制定《超说明书使用管理制度》,原则上不得随意扩大药品说明书规定的适应证、用法用量及疗程等,不允许出现超说明书用药,若有充分循证依据(指南) 支持某一药品可超说明书用药,需由临床医生填写《超说明书备案申请表》《超说明书用药风险及应急预案表》,经科主任签字并附相关支持资料;临床药师对提供的超说明书资料进行技术审核,形成《超说明书医学循证技术评估》;递交至医院药事管理与药物治疗学委员会讨论;医院药事管理与药物治疗学委员会审核通过的药品再递交至医院医学伦理委员会审批,医务部对审批通过的药物超说明书使用情况进行备案并公布;公布的超说明书情况临床可直接按批准方案使用,但经管医生需与患者或其家属签订知情同意书。这一规定大大杜绝了重点监控类药品在临床的超适应症使用情况。
2.6 制定合理用药考核方案。临床药师每季度开展重点监控药品相关病历的全点评工作,点评结果内网公示一周无异议后药讯刊登、科主任例会反馈、医生大会反馈,典型不合理病例则递交专家质询会议,点评结果纳入医务部季度绩效考核,并作为年终优秀科室和优秀个人的评选依据。
2.7 开展专家质询。临床药师点评中发现的典型不合理病例提交给医务部,医务部每季度从院合理用药评价小组暨处方点评专家组成员中随机抽取15名专家,组成该季度专家质询组并召开质询会,由专家质询组听取被质询科室或人员的说明与解释,质询专家对被质询科室或人员的说明与解释进行综合评估,认定用药是否合理。如认定其不合理,同时提出整改和处理意见。现场2/3专家认定用药医嘱不合理,则判定为不合理,反之即认为合理。在不合理医嘱判定中,半数以上专家认定为一般不合理的,则判定为“一般不合理”,每份病例扣罚200元从绩效考核中扣除,半数以上专家认定为严重不合理的,则判定为“严重不合理”,每份病例扣罚500元从绩效考核中扣除;门急诊处方考核到个人、住院病例考核到医疗组。
2.8 做好用药监测和不良反应上报工作。药学部组织药品不良反应知识培训及用药宣教,要求临床医护人员对重点监控药物做好监测并如实上报存在的不良反应情况,通过编辑《药品不良反应信息简报》及发布药物警戒信息等警醒临床规范合理用药,保障患者用药安全[7-8]。
结果
1.重点监控药品监管前后的使用情况。重点监控药品监管前(2016年10月—2017年9月)年销售金额为3391.40万元,监管后(2019年1月—2019年12月)年销售金额为1577.34万元,通过监管,重点监控药品占药品比例从5.78%下降至3.25%,降幅达43.77%,出院患者人均药品费用从11351.14元下降至7179.34元,降幅为36.75%。具体详见表1。
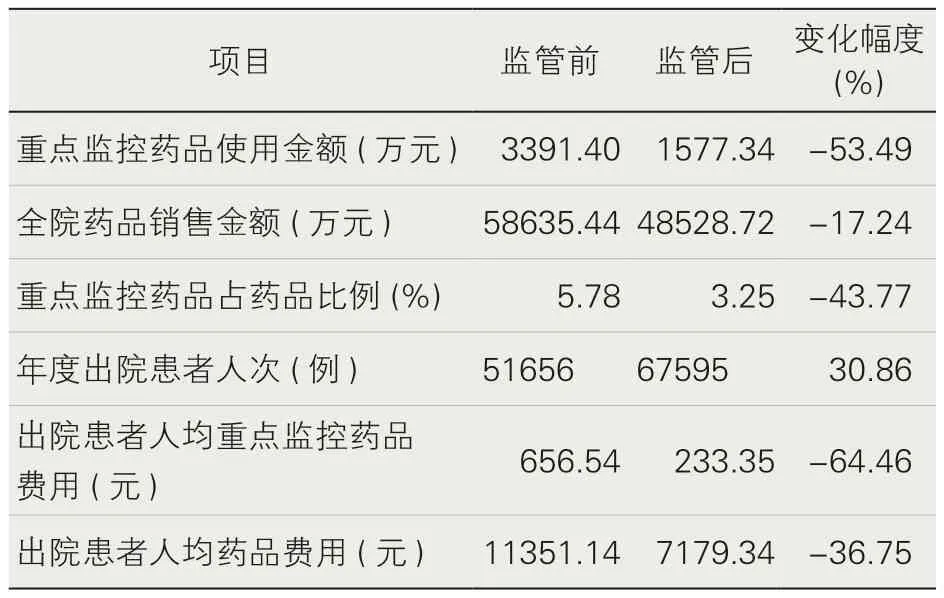
表1 监管前后医院药品使用及相关情况
2. 15种国家重点监控药品监管前后使用情况。重点监控药品监管前单药销售金额最高的为前列地尔注射液,2016年10月―2017年9月销售金额为990.99万元,监管后(2019年1月―2019年12月)销售金额为512.93万元,降幅为48.24%;降幅最大的药品为胸腺五肽注射液,降幅为90.65%,年销售金额从35.17万元降至3.29万元,降幅最低的为磷酸肌酸钠注射液,降幅为18.37%,年销售金额从92.25万元降至75.30万元。具体详见表2。
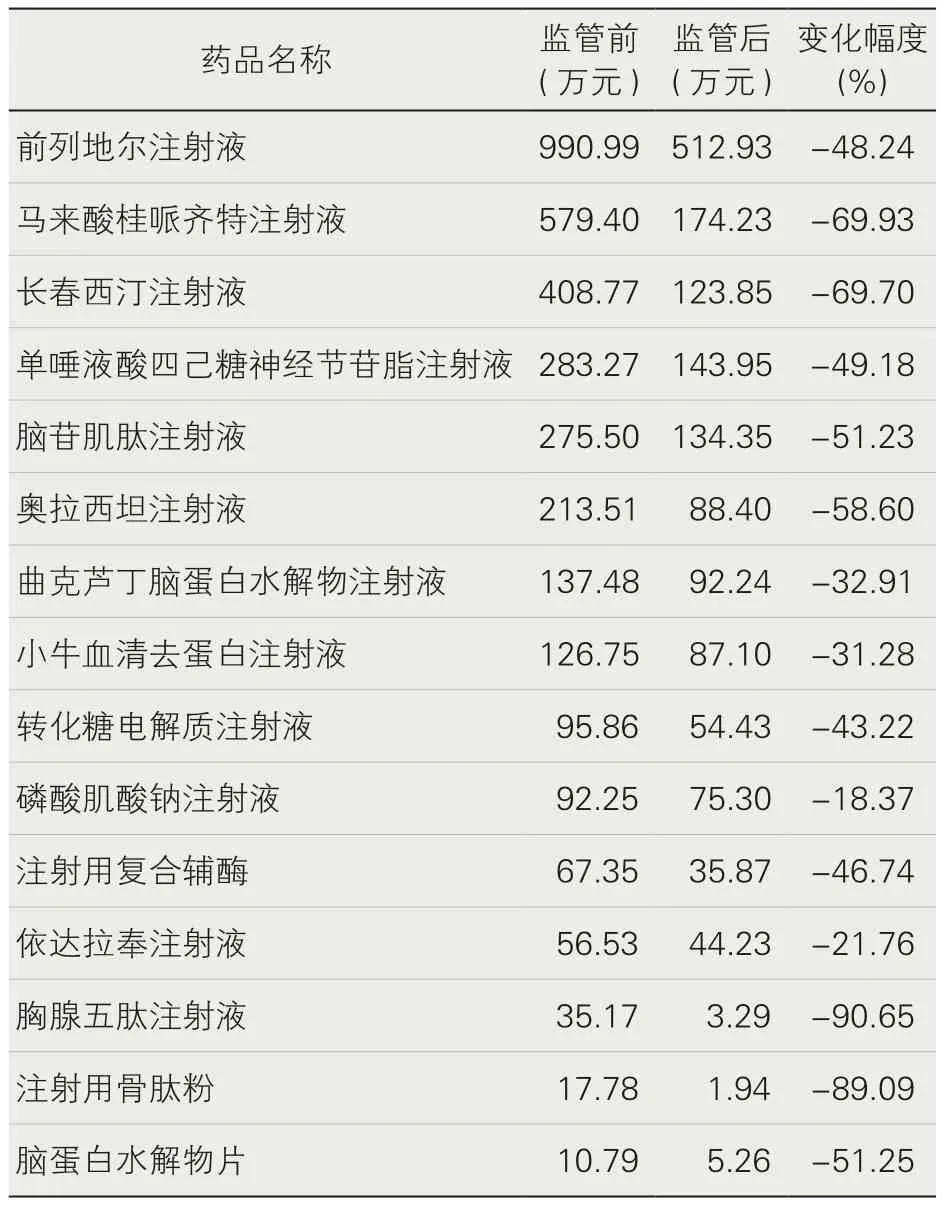
表2 监管前后15种国家重点监控药品费用及变化
3.药品使用的合理性评价。临床药师依据中华医学会及中华医学会各专业学组制定的疾病诊疗指南、专家共识和药品说明书制定每个重点监控药物的点评标准,并随机抽取每个药品使用病例50例,根据点评标准对药物使用合理性进行评价,包括适应症、用法用量、溶媒选择、疗程、药物配伍、用药禁忌、不良反应等,并对典型不合理病例进行个案分析。监管前的病例点评结果显示合理率最高的为注射用骨肽粉,合理率为80%,合理率最低的为马来酸桂哌齐特注射液,合理率为12%;监管后重点监控药品合理率均达92%以上,增幅最大的为马来酸桂哌齐特注射液,合理率从12%提升为92%,其中依达拉奉注射液和小牛血清去蛋白注射液监控后合理率为100%。具体详见表3。从每个药物不合理情况分析中可见,适应症不合理的前3个药分别是转化糖电解质注射液、胸腺五肽注射液、脑蛋白水解物片,不合理例数占比均为100%;用法用量不合理的前3个药分别是小牛血清去蛋白注射液、单唾液酸四己糖神经节苷脂注射液、前列地尔注射液,不合理例数占比分别为88.46%、55.56%、28.57%;溶媒不合理的前3个药分别是马来酸桂哌齐特注射液、注射用复合辅酶和长春西汀注射液,不合理例数占比分别为90.91%、83.33%、66.67%;疗程不合理的前3个药分别是曲克芦丁脑蛋白水解物注射液、脑苷肌肽注射液、依达拉奉注射液,不合理例数占比分别为92.86%、75.00%和57.14%具体详见表4。
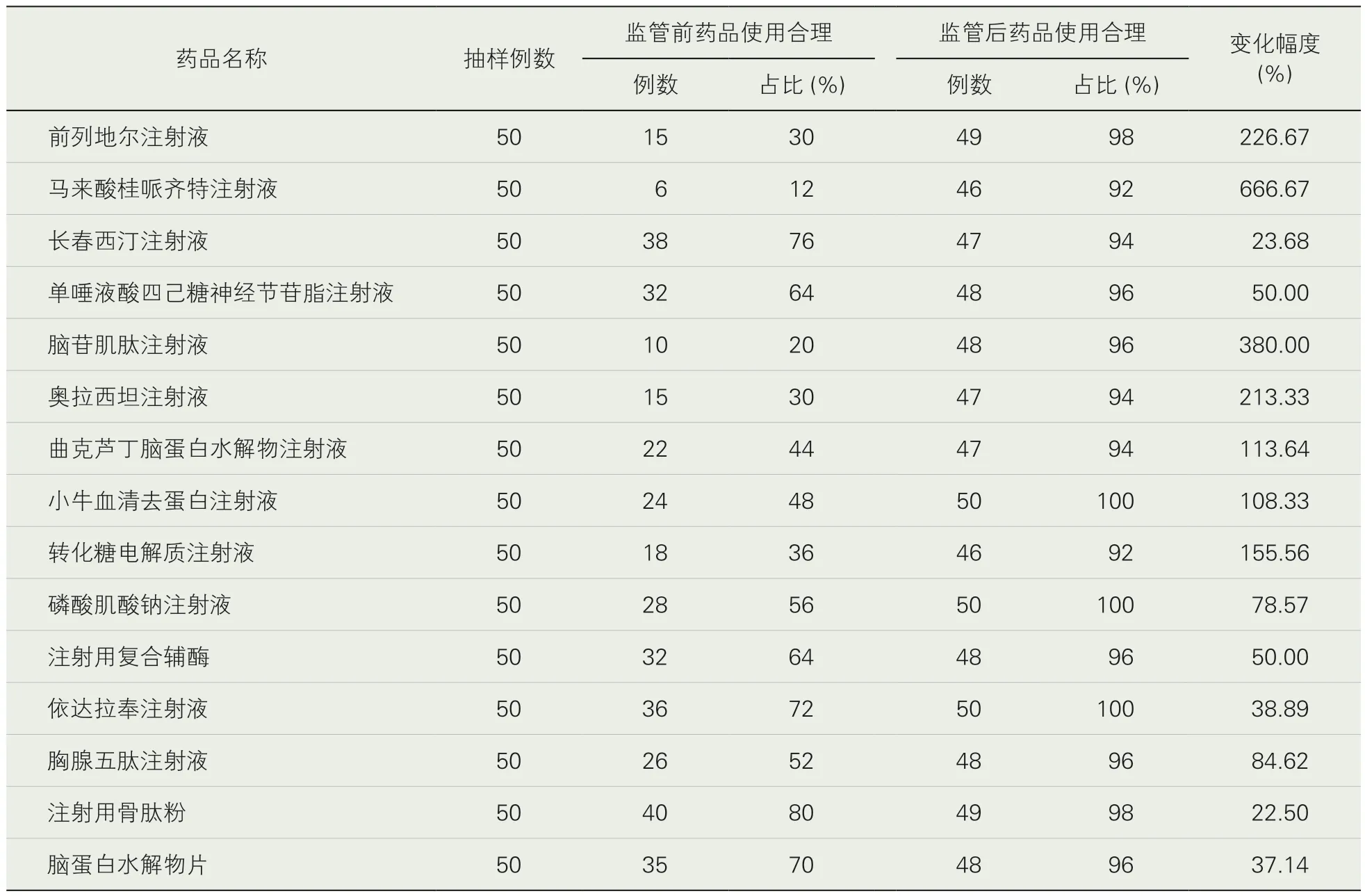
表3 监管前后15种国家重点监控药品使用合理分布
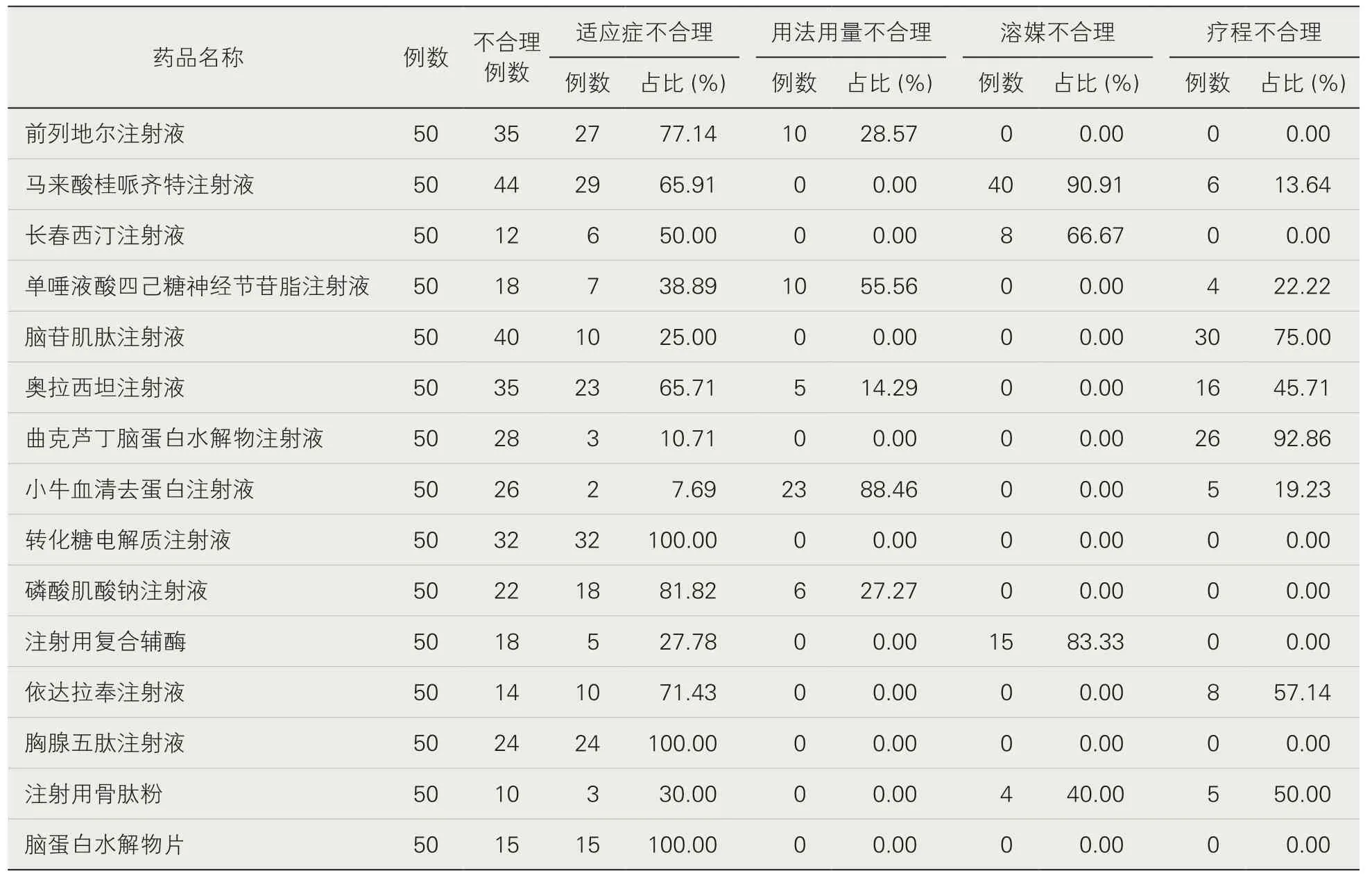
表4 监管前后15种国家重点监控药品使用不合理分布
4.不良反应发生情况。在本次点评中,均未在病程录中发现明确记载的不良反应;药师通过查看医院经营决策系统不良反应上报模块发现有1例患者在静脉注射前列地尔注射液时出现血管炎情况,后经局部用药缓解,但该不良反应未在病程记录中体现。
讨论
随着医保支付方式分类改革不断推进,构建以DRG收费模式为主,其他收费模式为辅的立体化收付组合形式将逐渐推向各级医疗机构,DRG收费模式将有效控制医药费用不合理增长,倒逼医疗机构大力提高合理用药水平,尤其是临床中使用量大的非治疗性药品的有效监管是医院药事管理的重中之重。
通过建立国家级、省级及院级的重点监控药品目录,应用信息化手段对重点监控药品的采购、使用等情况实施动态监测、超常规预警和公示公告,利用合理用药软件实时在线审方和实时监控,通过临床药师定期宣讲和点评,对临床科室和医生应用重点监控药品中存在的不合理情况进行及时反馈,点评结果纳入季度绩效考核,严重不合理情况进行专家质询等一系列监管措施,医务、药学、临床科室各司其职并强化协作管理,形成工作合力,切实加强重点监控药品事前、事中、事后各个环节的全过程管理与监控,进一步完善重点监控药品临床应用管理制度、工作机制和责任追究制度,确保临床重点监控药品安全、合理、经济的使用。
