局域表面等离子体共振酶联免疫法的显色方法及检测应用
2021-07-14翁国军李剑君赵军武
申 珣, 翁国军*,2, 李剑君, 朱 键, 赵军武*
(1.西安交通大学生命科学与技术学院,生物医学信息工程教育部重点实验室,陕西西安 710049;2.重庆大学生物流变科学与技术教育部重点实验室,重庆 400044)
近年来,随着纳米技术的兴起和发展,金属纳米颗粒由于其独特的性能和优点(高稳定性、易于合成、易于表面修饰等)在传感平台的应用显著增加[1,2]。金属纳米颗粒的局域表面等离子体共振使其拥有尖锐的光谱吸收、散射峰、增强电磁场,以及可见光范围内的可调光谱和高吸光系数,逐渐成为一种新的优良显色底物[3]。随着金属纳米结构制备技术的提升,可以通过控制其形状、大小、组成、周围介质环境来响应生物识别事件并产生颜色变换,构造等离子体生物传感器用于快速、灵敏、便携化的检测[4 - 9]。在此基础上,本文总结了将局域表面等离子体共振与传统的酶联免疫吸附分析法(ELISA)相结合的新的比色策略:局域表面等离子体共振ELISA的显色原理和方法,并介绍其在疾病诊断[10]、食品和环境检测[11]等领域的比色检测进展,最后对当前存在的问题和未来的发展方向进行了分析。
1 局域表面等离子体共振ELISA的原理
1.1 局域表面等离子体共振
局域表面等离子体共振(Localized Surface Plasmon Resonance,LSPR)效应是金属纳米粒子所具有的一种独特的光学性质。金属中导电的自由电子是由价电子构成的,这些价电子不受带正电的原子核的束缚,会在原子核之间振荡形成一个平衡的体系,这种正负离子完全分离的体系和原子被电离得到的等离子体很相似,所以被称为金属中的等离子体。当外界的光或者电磁场对等离子体自由电子产生干扰时,自由电子就会产生一个相对的位移,同时由于反向的库仑力作用,会在正电荷的周围做往复振荡,这种现象就被叫做等离子体振荡,当这种振荡频率与外界入射光频率相同时,就会产生局域表面等离子共振[12 - 15]。
值得注意的是,由于上述局域表面等离子体共振的作用,大部分入射光的能量被限制在金属纳米颗粒的周围,从而产生了强大的局部电磁场[16]。增强的局部电磁场提高了金属纳米颗粒的光学性能,使其表现出高的LSPR的吸光系数,比常规的有机染料的吸光系数高出几个数量级[17]。金属纳米颗粒的局域表面等离子体共振一般处于可见光至近红外光波段,其胶体溶液能够显示出醒目的颜色,可用于可视化检测。金属纳米颗粒的局域表面等离子体共振特性带来的高吸光系数,以及醒目的胶体溶液颜色使其成为构建高灵敏度、可视化检测比色传感器的优秀显色底物。
1.2 局域表面等离子体共振ELISA
1971年,瑞典学者Engvail、Perlmann和荷兰学者Van Weerman、Schuursfen分别报道了将免疫技术发展为检测液体中微量物质的固相免疫测定方法,即酶联免疫吸附分析法(Enzyme-Linked Immunosorbent Assays,ELISA)。在传统的ELISA中,信号是由酶催化底物产生的有色或者发光物质组成的,这种比色或化学发光信号与通过免疫反应附着在免疫复合物上的酶的数量成正比,通过酶标仪对目标分子进行定量测量[18,19],具有特异性强、灵敏度高、快速检测、廉价、操作简单的优点,目前已经被广泛的用于环境污染[20]、食品[11,21]、医学[22]等领域中。在比色ELISA中,可以通过肉眼直接观察这种信号来检测一定浓度的目标分子,适合在无法使用复杂仪器的情况下使用,但是当目标分析物的浓度较低时,肉眼来分辨浅色溶液的区别会导致较大的误差。由于金属纳米颗粒特殊的光学性质,Stevens等首先提出将基于金属纳米颗粒的LSPR现象和传统的ELISA相结合,称为局域表面等离子体共振ELISA法[23,24],用葡萄糖氧化酶[13,25]、过氧化氢酶[2,4,26]、碱性磷酸酶[12,14,27 - 30]等标记的抗体来实现信号的转化和放大,以金属纳米颗粒作为酶联中的显色底物,改变金属纳米颗粒的距离、形状、尺寸、种类使得溶液颜色改变。局域表面等离子体共振ELISA与传统的ELISA不同之处在于,前者不是基于同种颜色色度深浅的区分,而是基于溶液不同颜色的明显变化,可通过“裸眼”观察对目标分析物浓度进行定性定量检测[30]。
在局域表面等离子共振ELISA理论提出的初期,溶液的颜色变化主要是由目标分析物的存在导致金属纳米颗粒的聚集而产生的[23,24,31],这种颜色变化只能定性的检测溶液中是否存在一定量的待测目标物,但不能对于待检测物质进行(半)定量分析,因此在应用上还存在一定的缺陷。2016年,Li等[14]提出了利用种子介导的金纳米棒(Au NRs)的生长过程来实现多色的ELISA法,利用不同浓度的目标分析物引起的多种颜色的变化对待检测物实现半定量检测,补充了前者的不足。接着,在2018年Lin等[26]提出的通过对银包覆的金纳米双锥体的定量蚀刻来引起溶液颜色彩虹般的变化,进一步增加了颜色变化的数量,提高了检测的精度,目前有着较大的应用前景。
2 局域表面等离子体共振ELISA显色方法
到目前为止,各种形貌、组成的金属纳米颗粒已经被用于构建基于局域表面等离子体共振ELISA法的比色传感器,包括金纳米球(Au NBs)、金纳米棒(Au NRs)、金纳米双锥体(Au NBPs)[29]、金纳米花(Au NFs)[32]、银纳米三角板(Ag TNPs)[20,33]、核/壳Au@Ag纳米球[27]、核/壳Au@Ag纳米棒[26,34]等,结合了这些纳米颗粒的等离子免疫传感器已经可以用于检测各种靶标。局域表面等离子体ELISA法的显色方法主要可以分为两类,如图1所示,分别是基于分散/聚集的距离变化、基于蚀刻/生长的形貌变化的显色方法。有研究证明,采用不同的金属纳米颗粒和显色方法,构建的比色传感器的灵敏度也有所不同[29]。如何根据目标分析物选择合适的纳米金属材料以及显色策略,是构建基于局域表面等离子体共振ELISA法的比色传感器的重点。

图1 局域表面等离子体共振ELISA法的显色方法Fig.1 Colorimetric methods of localized surface plasmon resonance ELISA
2.1 基于分散/聚集的距离变化的显色方法
目标诱导的金属纳米颗粒的分散/聚集是典型的LSPR显色方法之一[23,24,35]。当金属纳米颗粒间的距离在其粒径长度的2.5倍时,表面等离子体产生的共振耦合使其LSPR光谱红移[36],溶液颜色发生显著的变化,通过观察颜色对目标进行定性测量。Stevens等[24]根据这一原理设计出一种免疫传感器,用肉眼检测血清中的前列腺特异性抗原(Prostate Specific Antigen,PSA)和HIV衣壳抗原p24的存在。在基于聚集/分散的距离变化的显色方法中,H2O2诱导的金纳米颗粒(Au NPs)聚集状态的改变将影响纳米颗粒的光学性质,而实验中H2O2的浓度很大程度上决定了纳米颗粒聚集的程度,当H2O2处于高浓度时,纳米颗粒以非聚集的胶体悬浮液的形式生长,溶液呈现出红色,当H2O2处于低浓度时,纳米颗粒聚集成簇使得溶液呈现出蓝色,因此在检测中控制H2O2的浓度至关重要。Yang等[13]通过H2O2抑制苯二硼酸(Benzene-1,4-Diboronic Acid,BDBA)的硼酸和柠檬酸的α-羟基羧酸盐之间的相互作用,能够使聚集的Au NPs分散开并伴随溶液颜色的改变。将H2O2/BDBA/Au NPs探针与免疫分析法相结合,溶液中目标检测物的浓度和H2O2的浓度成正比,H2O2的浓度决定Au NPs的聚集程度和溶液的颜色,成功的测量了人体免疫球蛋白IgG和人前列腺特异性抗原PSA,肉眼可检测到的最低浓度分别为0.1 ng/mL和4 ng/mL。
2.2 基于刻蚀/生长的形貌变化的显色方法
上述基于金属纳米颗粒的分散/聚集的常规LSPR显色方法具有设计简单、灵敏度高的优点,能够实现对目标分子的超灵敏检测。但是在反应的过程中,除了由于目标诱导产生的Au NPs的聚集外,外部环境造成的温度、pH、盐和带电分子的改变同样会引起Au NPs的聚集,这种无响应的自聚集将会导致假阳性/阴性结果[4,37]。其次,由于产生颜色变化的种类单一,这种方法只能用于目标分子的定性检测,存在一定的局限性。近年来,多色变化的等离子体传感器的出现解决了这一问题,通过目标分析物诱导的金属纳米颗粒形貌的蚀刻/生长来引起其LSPR峰的移动,由于移动的LSPR峰占据了大部分的可见光谱,溶液颜色产生多色变化[12 - 15,17],更适用于裸眼定量检测分析物的浓度。
2.2.1 单组分金属纳米颗粒的刻蚀与生长金属纳米颗粒的形貌变化可以通过溶液中的氧化/还原的过程产生,目标分子诱导溶液中的氧化/还原反应,反应中氧化剂/还原剂的量与目标分子的浓度存在对应关系,当溶液中的Au3+/Ag+被氧化剂/还原剂逐渐蚀刻/生长在纳米颗粒的表面时,会造成纳米颗粒尺寸/形状的改变并伴随LSPR共振峰的移动。
氧化剂能够蚀刻金属纳米颗粒并造成形状、尺寸的改变[28,33,38 - 41]。例如氧化剂蚀刻的Au NRs的纵横比改变,能够引起纵向LSPR峰的显著蓝移和肉眼可见的多色变化。2016年,Ma等[38]设计了一种基于Au NRs 蚀刻的免疫传感器,能够对蛋白质和核酸进行裸眼半定量检测。在他们的研究中首次提出了将Au NRs 作为显色底物,通过选择性缩短Au NRs的长度产生一系列的颜色变化,这些变化几乎覆盖了从400 nm 到760 nm的整个可见光范围,使得通过肉眼能够轻松辨别。接着,在另一项研究中,Ma等[2]用同样的方法裸眼半定量检测癌胚抗原CEA和PSA,在溶液中添加具有Au NRs的酸性溶液,Au NRs被TMB2+氧化生成Au+。在CTAB存在的情况下,该过程选择性的发生在棒的末端,使得棒的长度缩短而直径几乎保持不变。除了Au NRs,具有高纵横比和锋利边缘的Ag TNPs由于更强的等离子体共振,常被用于构建超高敏感度的免疫传感器。Yuan等[39]就利用H2O2氧化蚀刻Ag TNPs产生的颜色变化作为信号,通过构建间接竞争性pELISA的方法定性定量检测氟喹诺酮类抗生素,检测限为0.24 ng/mL,显示出高灵敏度和良好准确性。Liang等[33]用类似的方法检测癌症标志物的浓度,其中Ag TNPs被H2O2氧化成小尺寸的球形纳米颗粒,产生蓝紫色颜色的改变。
通过控制反应过程中还原剂的浓度,可以轻松生长或合成不同尺寸和形状的纳米颗粒。Liu等[25]设计了一种5 nm直径的Au NPs生长的方法,利用葡萄糖氧化酶催化生成的H2O2改变Au NPs直径。在此基础上,Zhao等[42]利用金纳米团簇(Au NCs)的催化特性,将Au NCs和Au NPs两者同时用于构建等离子体免疫传感器,通过Au NCs的催化作用控制溶液中H2O2的浓度从而影响Au NPs的生长过程。以上两种方法都利用Au NPs尺寸改变引起的颜色变化作为显色信号,而Au NBPs比Au NPs具有更尖锐的边缘,更高的局域场增强和灵敏度,是一种良好的显色底物。例如Wang等[40]通过抗坏血酸(AA)介导Au NBPs生长显色的方法证明了这一策略。在他们的实验中,以抗体作为识别人表皮生长因子受体-2(Human Epidermal Growth Factor Receptor 2,HER2 ECD)的探针,水解产生的AA还原溶液中的Au+调节金锥体的生长,Au NBPs 的不同生长阶段与不同浓度的AA对应,视觉检测限在0.5 ng/mL,该检测限远低于血清中HER2 ECD的截止值,可用于乳腺癌的早期诊断。
2.2.2 核/壳结构金属纳米颗粒的刻蚀与生长纳米金属颗粒的LSPR的共振峰的位置对于特定材料具有高度的特异性,例如直径13 nm的金纳米球的LSPR在520 nm处有吸收峰,然而尺寸相同的Ag NPs的LSPR吸收峰在470 nm处[43,44]。将Au NPs作为生长衬底来生长其他具有良好的读出性能的材料,产生核/壳型纳米结构,可进一步提高检测范围和灵敏度[1,4,5,26,27,29]。目前,常见的生长衬底有Au NBs[27]、Au NRs[34,35]、Au NFs[32]、Au NBPs[26,29]等。
近年来的研究表明,具有尖锐边缘的材料例如Au NBPs,通常具有更好的灵敏度,在其表面包覆银层得到的Au NBP@Ag纳米棒,具有类似于Au NRs的特性,通过控制Ag NRs的长度可以轻易地在可见光到近红外区域的宽光谱范围内调整其等离子体波长,为新型基于贵金属纳米颗粒设计的比色传感器的构建提供了新思路[16,46]。例如Lin等[26]利用羟基自由基介导Au NBPs@Ag NRs的定量蚀刻的方法成功检测了鳞状上皮细胞癌抗原。在反应的过程中,与蚀刻Au NRs的单向移动相比,Au NBPs@Ag NRs表现出多向的LSPR峰的移动,纵向LSPR峰先蓝移,再红移,最后再蓝移,颜色变化的种类较之Au NRs的蚀刻的单向移动更多,灵敏度更高。Xu等[29]利用4-氨基苯酚还原银沉积在Au NBPs表面的过程设计了一种超灵敏比色法检测H5N1病毒,在生长过程中Au NBPs表面银壳厚度的变化改变了金的折射率,引起LSPR峰的蓝移和颜色改变。接着,在Au NBPs@Ag NRs构建的比色传感器的基础上,Wei等[47]设计了一种双模式免疫传感器,以介孔SiO2纳米球作为载体固定二抗和DNA引物,通过杂交链反应捕获碱性磷酸酶,其催化产生的抗坏血酸具有双重功能,一方面可以充当电子供体来捕获CdS/ZnO空心纳米棒阵列中的空穴,导致光电流的增加。另一方面,抗坏血酸的还原性使银在Au NBPs表面沉积,银壳的形成和增厚导致了生动的色彩变化和光谱的蓝移,不同的机制和相对独立的信号转导使该方法构建的传感器具有更加准确可靠的性能。
3 局域表面等离子体共振ELISA检测应用
3.1 在疾病诊断中的应用
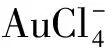
3.1.2 在病原体检测中的应用(1)病毒颗粒的检测:对于病毒颗粒的检测,Zhou等[27]提出了一种ALP诱导金属化的比色检测的方法检测H9N2禽流感病毒。将酶促反应和金属纳米颗粒的独特光学性质结合起来,可以极大的增强光信号,能够检测到低至17.5 pg/mL的H9N2病毒,为病毒颗粒的检测提供了高效、简便的方法。类似的,Zhan等[48]利用ALP介导的Au NPs聚集的比色方法来检测呼吸道合胞病毒(Respiratory Syncytial Virus,RSV),ALP催化ATP去磷酸化生成腺苷和磷酸盐,而腺苷使得溶液中的Au NPs分散,颜色由蓝色变为红色。金属离子的引入使得去磷酸化的反应加速,进一步加速了反应时间,血清中RSV的检测限低至0.021 pg/mL。(2)其他病原体的检测:Marilene等[49]利用局域表面等离子共振ELISA的方法成功检测了利什曼原虫,这种检测方法不需要复杂的仪器,检测利什曼原虫的灵敏度为94.7%,特异性为100%,在受感染地区可作为检测利什曼原虫感染的辅助工具。而Nie等[50]开发了一种用于梅毒螺旋体检测的等离子体ELISA的方法,溶液中存在的梅毒螺旋体导致免疫复合物的形成,乙酰胆碱酯酶催化乙酰硫胆碱水解产生硫胆碱,硫胆碱使得Au NPs团聚,利用LSPR吸收光谱的移动和溶液颜色的显著改变定量测量梅毒螺旋体,检测限为0.98 pg/mL,是传统的ELISA法灵敏度的1 000倍。
3.2 在食品和环境的检测应用
3.2.1 有毒有机物的检测有毒有机物的实时、快速监测对于食品安全和环境保护都有着重要的意义。利用酶催化生成的H2O2影响金属纳米颗粒的生长过程、存在状态是局域表面等离子共振ELISA的常见方法之一。例如Peng等[51]设计出了一种基于H2O2介导Au NPs生长的比色传感器,成功检测了甲基睾酮(Methyltestosterone,MT)的浓度。MT是一种在牛的生产周期被非法使用的生长促进剂,随着食物链进入人体后能潜在威胁人体健康,破坏生态环境。通过这种方法可以快速、灵敏的检测低至0.03 ng/mL的MT,具有重要的实用价值。Zhan等[52]利用H2O2还原Au3+在金种子表面生长的原理,设计了一种免疫传感器检测玉米中的伏马菌素B1(Fumonisin B1,FB1)的浓度,FB1浓度的增加引起Au NPs的生长,溶液产生无色到紫色的颜色变化,肉眼观察的检测限为1.25 ng/mL,具有较高的准确性和灵敏度。类似的,Liang等[35]利用H2O2、辣根过氧化物酶(Horseradish Peroxidase,HRP)和酪胺诱导的Au NPs聚集/分散的方法检测农产品中的赭曲霉毒素A(Ochratoxin A,OTA)的含量,以Au NPs聚集/分散的状态改变引起的颜色变化作为检测过程中的输出信号。在HRP催化H2O2的诱导下,酪胺的酚聚合可以引发Au NPs的聚集,而被OTA标记过的过氧化氢酶(Catalase,CAT)则作为消耗H2O2的竞争抗原,这种方法可以用肉眼检测到150 pg/mL的OTA。而在另一项研究中,Pei等[32]利用脲酶诱导银金属化的方法同样对农产品中OTA的含量进行了检测。OTA标记的脲酶作为竞争抗原能够水解尿素为氨,在氨分子存在的情况下,葡萄糖中甲酰基还原Ag+在Au NSs的表面生成银壳,肉眼检测OTA的检测极限在40 pg/mL,具有更高的灵敏度。这种方法对其他常见的霉菌毒素也具有出色的选择性,在定性和定量测量真菌毒素和其他污染物方面有着较大的应用价值。
3.2.2 细菌的检测对于水和食品中细菌的快速、准确检测是目前食品安全和环境检测中迫切需要解决的问题。Chen等[53]设计了一种基于CAT介导的Au NPs生长的方法检测食品中的单核增生李斯特菌的数量。该方法采用夹心形式,通过携带聚丙烯酸刷的SiO2纳米粒子作为“CAT的容器”,极大的增加了酶的负载和对于信号的放大作用,从而能够在超低浓度下检测李斯特菌的数量。使用这种方法检测磷酸盐缓冲液中李斯特菌的检出限在8×101CFU/g,具有良好的特异性和敏感性,能够超灵敏检测细菌病原体。Gao等[45]设计了一种基于脲酶诱导银金属化的免疫传感器测量肠炎沙门氏菌,捕获的脲酶能够催化脲水解为二氧化碳和氨,在葡萄糖存在的情况下,生成的氨可以还原Ag+并形成银壳沉积在Au NRs的表面。随着银壳厚度的增加和长宽比的减小,LSPR峰出现明显的蓝移和溶液颜色的多色变化,通过肉眼观察的检出限在1.21×101CFU/mL。
3.2.3 有毒阳离子的检测随着工业的快速发展,越来越多不可降解的重金属离子通过各种途径排放在土壤和水体中,使得生态系统和食物链处于高污染的状态,对于这些重金属阳离子的检测对人体健康和环境保护有着重要的意义。Yao等[20]提出了通过H2O2对Ag TNPs蚀刻的方法来检测水中Cr(Ⅲ)含量,利用竞争性ELISA来构建一个信号产生的机制,其中Ag TNPs被H2O2蚀刻的程度与溶液中Cr(Ⅲ)含量的浓度密切相关,随着蚀刻的程度不同,溶液产生的相应的颜色变化,肉眼可检测样品中6.25 ng/mL的Cr(Ⅲ)。
4 总结与展望
本文主要介绍了局域表面等离子体ELISA方法的原理以及构建的比色传感器在可视化“裸眼”检测中的应用。由于这种传感策略将传统的ELISA的方法和金属纳米颗粒相结合,既提高了检测的灵敏度和检测范围,在疾病诊断、食品安全监测和环境质量控制等方面都有着较大的应用空间。但是这种基于金属纳米颗粒构建的比色传感策略仍然存在一些问题需要解决。首先,这种传感机制是基于金属纳米颗粒的距离、尺寸、形貌、构成的变化来实现的,因此研究制备出具有光学和化学稳定性的纳米材料至关重要,目前制备金属纳米颗粒的方法不能满足合成大规模使用的高度均匀的纳米材料,而且大多数合成方案都需要较长的孵育时间和繁琐的洗涤步骤,限制了这些传感器的实际应用。其次,贵金属纳米材料胶体的色彩变化灵敏度还需进一步提高,大部分检测目标物在低浓度时引起的色彩变化还不足以通过肉眼直接分辨。因此制备出稳定的具有高度均匀性的金属纳米颗粒,以及对其光学性质的理论研究仍然是未来这一领域需要持续探索的方向。
总之,和传统的ELISA检测方法相比,基于局域等离子共振ELISA构建的比色传感器具有更高的灵敏度和更易于“裸眼”观察的多色变化。这些明显的优势为其在医疗、卫生、食品、环境检测中的应用奠定了良好的基础。
