基于真实情境的项目式复习
2021-07-08薛琴
薛琴
摘 要:本文以多维度探析磷酸铁锂结构为例,开展“物质结构与性质”专题复习。展示基于真实情境的项目式学习在中学化学教学中的应用,培养化学学科核心素养。
关键词:项目式学习; 真实情境; 磷酸铁锂; 教学案例
中图分类号:G633.8 文献标识码:A 文章编号:1006-3315(2021)5-020-002
《普通高中化学课程标准(2017年版)》指出要重视开展“素养为本”的教学。真实、具体的情境是学生化学学科核心素养形成和发展的重要平台。化学学科核心素养一方面需要在真实问题情境下才能表现出来,另一方面也只有在分析和解决具体的真实情境问题时才能得到培养和发展。
项目式学习是一种以学生为中心,落实学生核心素养的重要教学方式。建构主义学习理论是项目式学习重要的理论基础。学习者的学习是以他们自己的经验为背景,基于已有的知识鉴别新知识,最后重新建构个人化知识。传统的学习从学科概念出发,通过例题和练习巩固概念,知识往往是碎片化和割裂的;基于真实情境的项目式学习强调从宏观的视角辨析化学反应,从微观的尺度进行探析,基于证据进行推理形成认知模型,在问题解决中形成严谨求实的科学态度。
一、设计思想
“物质结构与性质”(选修三)考点内容零碎,没有如原子结构的发现化学史推理的逻辑线索。教师可以根据教学内容自己开发教学情境开展项目式复习,打破教材知识模块界限,构建零碎知识之间的内在联系,实现教学内容的有效整合。以磷酸铁锂电池为真实情境背景的试题在高考中多次出现。考查的内容涉及化学工业流程、电化学知识、物质结构与性质等,是项目式复习的好素材[1]。
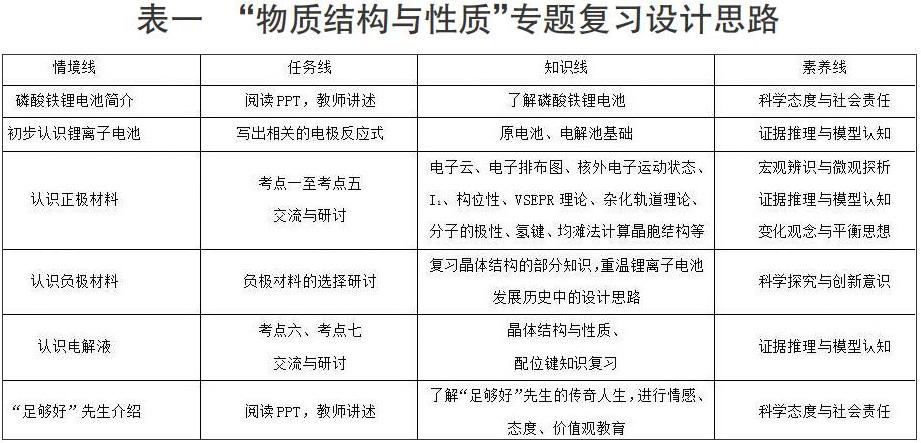
本文以多维度探析磷酸铁锂电池结构开展“物质结构与性质”专题复习为例,以磷酸铁锂电池真实情境为载体,以任务为驱动、学生为主体,进行项目式复习。让学生从多维度认识和探究磷酸铁锂电池,为学生后续复习提供可迁移的方法形成以点带面的联想式复习。教学中注重情境线、任务线(学生活动线)、知识线、核心素养线的有机整合,凸显了基于真实情境的项目式化学教学特色。
二、教学过程
(一)课堂导入以及真实情境创设
2019年诺贝尔化学奖公布,瑞典斯德哥尔摩皇家科学院将这项荣誉授予了三名科学家,以表彰他们在锂电池发展上做出的杰出贡献。其中,97岁的约翰·古迪纳夫(John B. Goodenough)更是刷新了获奖年龄最大的纪录。古迪纳夫是钴酸锂、锰酸锂和磷酸铁锂正极材料的发明人,锂离子电池的奠基人之一。
(二)初步认识锂离子电池(学生讨论并完成学案)
【情境】锂离子电池内部主要由正极、负极、电解质及隔膜组成。目前正极材料主要是钴酸锂(LiCoO2)、锰酸锂(LiMn2O4)、镍酸锂(LiNiO2)。磷酸铁锂动力电池是用磷酸铁锂(LiFePO4)材料做电池正极的锂离子电池,是锂离子家族的新成员。这种电池具有能量密度高、安全性能好、原材料来源广泛等优点。目前被广泛应用于新能源汽车上。
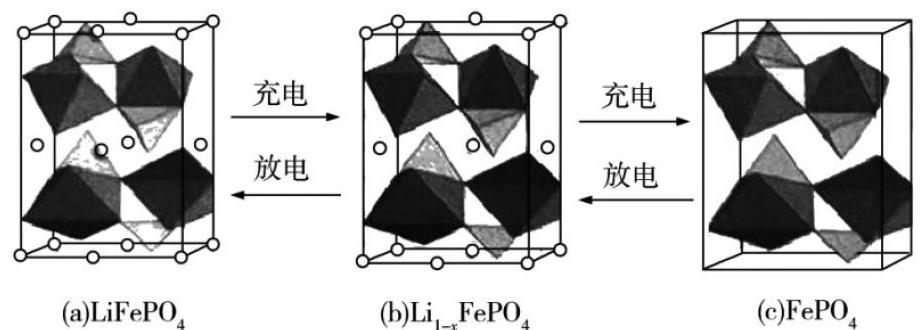
【任务】以钛酸锂和磷酸亚铁锂做电极组成电池,充电时发生的反应为Li4Ti5O12 + LiFePO4 = Li4+xTi5O12 + Li1-xFePO4(0 【设计意图】 通过初步认识锂离子电池引入情境,回顾电化学基础知识,进行思维热身。提醒学生不要将知识割裂,要注重高三复习的整体性。 (三)认识正极材料(学生讨论并完成学案) 【考点1】核外电子排布 (1)基态Li+的核外电子云轮廓图的形状怎样?画出基态Li原子的电子排布图。 (2)基态Fe2+与Fe3+离子中未成对的电子数之比是多少?Fe3+比Fe2+稳定的原因是什么? (3)在周期表中,与Li的化学性质最相似的邻族元素是什么?该元素基态原子核外M层电子的自旋状态怎样? 【考点2】第一电离能 给出Li及其周期表中相邻元素的第一电离能数据,回答: (1)I1(Li)>I1(Na),原因是什么? (2)I1(Be)>I1(B)>I1(Li),原因是什么? 【考点3】立体构型、等电子体 (1)在正极材料磷酸铁锂中,磷酸根离子的空间构型是怎样的?与磷酸根互为等电子体的分子有哪些?其中P的价层电子对数是多少?杂化轨道类型? (2)价层电子对的立体构型和分子的立体构型是一回事吗?两者有什么区别和联系? 【考点4】键的极性、分子极性、氢键 PH3是_____键(填“极性”或“非极性”)形成的_____分子(填“极性”或“非极性”),其在水中的溶解性比NH3小,原因是什么? 【设计意图】 以认识正极材料为情境线索将零碎知识点整合。其基本思路是以电子→原子→原子组合为主线,以任务驱动学生交流与研讨,根据考点层层推进。复习原子结构相关理论、价层电子对互斥理论、杂化轨道理论、等电子体理论、氢键理论。能够计算中心原子上的孤电子对数,并根据孤电子对数和σ键电子对数确定中心原子上的价层电子对数,推导VSEPR模型的空间构型和杂化轨道类型。能够根据VSEPR理论确定分子的空间构型,理清键的极性和分子极性的关系。 【考点5】有关晶胞的计算(学生讨论并完成学案) 【任务】(2020年新课标Ⅰ卷)LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO4的单元数有____个。电池充电时,LiFeO4脱出部分Li+,形成Li1-xFePO4,结构示意图如(b)所示,则x=_______,n(Fe2+)∶n(Fe3+)=_______。 【设计意图】 整合空间想象力、化学信息、推理、分析图像和计算的能力。特别复习“均摊法”的应用。 (四)认识负极材料(阅读材料后开展讨论) 【情境】锂电池在充电过程中,Li+还原时形成树枝状金属锂。其在生长过程中会不断消耗电解液并导致金属锂的不可逆沉积,造成低库伦效率;同时,锂枝晶的形成甚至还会刺穿隔膜导致锂离子电池内部短接,造成电池热失控继而引发燃烧爆炸。如何利用锂元素的优势又克服锂枝晶的弊端呢?关键在于寻找能够承载Li+嵌入和脱嵌的正负极材料。 【任务】 投影石墨的层状结构的球棍模型。给出数据:石墨中层与层的间距335pm、每层中两个碳原子之间的键长142pm、Li+半径60pm。回答: (1)在石墨层状晶体结构中,层与层之间如何结合?每层中的相邻碳原子之间如何结合? (2)从结构的角度解释石墨具有良好导电性的原因。晶体中碳原子的杂化类型?石墨是否适合做负极材料? 学生经过讨论发现:石墨中碳原子都是SP2杂化,杂化的碳原子与未参与杂化的P轨道上的电子形成大π键,从而使石墨具有优良的导电能力。另外基于石墨晶体层与层间距和Li+半径大小的数据,十分适合Li+反复嵌入和脱出,可以考虑使用石墨作为负极材料[2]。 【设计意图】 从宏观辨识到微观探析,复习晶体结构的部分知识。通过理论联系实际应用,培养学生的科学探究与创新意识,树立结构决定性质的思想。重温锂离子电池发展历史中的设计思路,提升化学学科核心素养。 (五)认识电解液(学生讨论并完成学案) 【考点6】晶体结构与性质 LiPF6在是锂离子电池电解液的重要组成部分,一般采用PF5、LiF为原料制备。上述原料的熔点PF5和LiF熔点高低比较,比较依据是什么? 【考点7】配位键及其形成条件 LiPF6在有机溶剂中具有适中的解离常数,且能与正负极材料匹配,是目前使用最广泛的锂盐。[PF6]-中P原子与F-形成配位键,不考虑空间构型,用示意图表示[PF6]-的结构。[PF6]-中提供孤电子对的原子是什么?判断依据? 【设计意图】 证据推理与模型认知,复习晶体结构与性质、配位键知识。 (六)了解“足够好”先生的传奇人生 【设计意图】 情感态度价值观的教育不是空喊口号,而是潜移默化、润物细无声的。约翰·古迪纳夫(John B. Goodenough),“足够好”先生30岁才入行,58岁时提出了钴酸锂,75岁时提出了磷酸铁锂,94岁时研制出全固态电池,97岁获得诺贝尔化学奖,至今仍然在全固态电池的研究工作一线。有人说他的研究已经足够好了,但是他却不这么认为。生命不息,奋斗不止。看完这位老爷子的故事,我只有一个想法:我们年轻人,还有什么理由不努力! 三、教学反思 1.复习课若局限于对已学知识的简单重复和再现,用碎片化的知識去思考和解决问题,就容易忽略知识体系的完整性,会导致思考不够深刻。项目式复习,打破了原有知识的孤立性和零散性,有如一条线索,将一颗颗知识的珍珠串起。通过围绕一个主题讲述故事,开展研究,不仅促使学生对所学知识融会贯通,拓展了复习的深度和广度,而且激发了学生的学习兴趣,进一步提高了他们的思维能力。 2.本节课从磷酸铁锂电池出发,以化学学科核心素养的培养为宗旨,围绕相关内容的研究和讨论,整合了物质结构与性质多个高考热门考点,从多个维度进行教学,不仅落实了基础知识,还把主动权交给学生,让他们在真实情境的项目式学习中自主完成知识的构建。项目式学习注重核心知识的再建构,创建真实的驱动性问题,用高阶学习包裹低阶学习,将素养转化为持续的学习实践。 参考文献: [1]单旭峰,宋修明.真实情境的高考化学命题理论与实践[J]中学化学教学参考,2019(5):1-5 [2]江合佩.走向真实情境的项目化学习[M]济南:山东科学技术出版社,2020.7:267-269
