参芪降糖颗粒联合利拉鲁肽用于二甲双胍治疗失效的2型糖尿病患者的应用价值
2021-06-30蒙绪标刘婷婷符兰芳熊青林珠
蒙绪标 刘婷婷 符兰芳 熊青 林珠
海南省海口市人民医院内分泌科(海口570208)
近年来,糖尿病在我国的发病率日益增加,且发病年龄日益年轻化,目前有超过1 亿[1]的患者正在承受糖尿病及其引发的并发症,其中95%以上的糖尿病为2 型糖尿病。二甲双胍[2]是目前应用最广泛的降糖药,但是临床发现随着病情进展单独使用二甲双胍有时无法有效调节糖尿病患者的血糖水平,因此急需寻找其他降糖药治疗二甲双胍治疗失效的2 型糖尿病患者,而在选用联合治疗药物时应尽量选用不同作用机制存在协同作用的药物,以对抗复杂的病理生理机制。利拉鲁肽是一种用于治疗2 型糖尿病的胰高血糖素样肽-1长效类似物[3],可以长效保护胰岛β细胞,改善血糖水平。近年来,中药制剂逐渐成为糖尿病临床治疗的热点,薛光辉等[4]发现参芪降糖颗粒具有益气养阴,滋脾补肾的功效,可用于治疗2 型糖尿病。此外,LI 等[5]发现参芪降糖颗粒可改善胰岛素抵抗指数,有效降低2 型糖尿病血糖水平。因此,本研究拟考察参芪降糖颗粒联合利拉鲁肽在二甲双胍治疗失效的2 型糖尿病中的应用前景。
1 资料与方法
1.1 一般资料研究对象为2017年4月至2019年10月于本院就诊并接受治疗的150 例2 型糖尿病患者,采用随机数字表法分为A、B、C 三组,每组各50 例,年龄35 ~60 岁。三组患者在年龄和性别、病程、BMI 等临床资料见表1,差异无统计学意义(P>0.05)。本研究由医院伦理委员会批准进行,患者及家属签订知情同意书。
表1 三组患者的临床资料Tab.1 Clinical treatment of three groups of patients±s

表1 三组患者的临床资料Tab.1 Clinical treatment of three groups of patients±s
组别例数年龄(岁)性别(男/女)病程(年)BMI(kg/m2)A组B组C组F/χ2值P值50 50 50 49.21±8.27 47.86±8.73 49.13±5.44 0.494 0.611 23/27 28/22 24/26 1.120 0.571 5.12±1.39 4.87±1.25 4.92±1.57 0.440 0.645 28.93±5.71 28.11±4.47 27.52±4.56 1.025 0.361
1.2 入排标准纳入标准:(1)患者已确诊患有2型糖尿病,临床症状符合中国2 型糖尿病防治指南(2017年版)对2 型糖尿病的诊断标准[6];(2)患者仅服用过二甲双胍,且服药剂量达到药物最大耐受剂量(2 g/d),服药时间1 个月以上,糖化血红蛋白水平控制不佳在>7%;(3)患者认知和社交无障碍。排除标准:(1)备孕或妊娠期患者;(2)患有其他类型糖尿病的患者;(3)胰腺和甲状腺功能障碍,患者近期服用过其他影响糖代谢的药品;(4)因其他疾病导致肝肾和胰腺功能受损。
1.3 方法给予患者基础治疗,主要包括饮食、运动等。保持患者原二甲双胍(规格:0.5 g/片,国药准字H20023370,中美上海施贵宝制药)的使用方案,口服给予2 g/d。在此基础上对A 组给予利拉鲁肽注射液(规格:18 mg/3 mL,国药准字J20160037,丹麦诺和诺德公司)第1 周皮下注射剂量为0.6 mg/d,自第2 周起增至1.2 mg/d,每天1 次,治疗3 个月。B 组给予参芪降糖颗粒(规格:3 g/袋,国药准字Z10950075,鲁南厚普制药),每天3 次,每次1 g,治疗3 个月。C 组在基础治疗和二甲双胍治疗基础上,给予利拉鲁肽联合参芪降糖颗粒,利拉鲁肽和参芪降糖颗粒的治疗方案同A、B 组。
1.4 观察指标
1.4.1 血糖指标分别采集三组患者治疗前后的指尖血糖样本,并通过血糖仪(华益)测定空腹血糖(FPG)和餐后2 h 血糖(2h-PG)。分别采集三组患者治疗前后的静脉血5 mL,4 ℃离心10 min(3 000 r/min),取上层血清通过高效液相色谱法检测三组组治疗前后的糖化血红蛋白(HbA1c)水平。
1.4.2 疗效空腹血糖≤6.1 mmol/L,餐后2 h 血糖≤7.8 mmol/L 记作显著有效;空腹血糖≤7.8 mmol/L,餐后2 h 血糖≤11.1 mmol/L 记作有效;空腹血糖和餐后2 h 血糖均无改善则为无效[7]。治疗有效率=显著有效率+有效率。
1.4.3 内脂素分别采集三组患者治疗前后的静脉血5 mL,4 ℃离心10 min(3 000 r/min),取上层血清采用人内脂素检测试剂盒(北京方程生物科技有限公司)通过酶联免疫吸附法测定内脂素水平。
1.4.4 胰岛功能采用胰岛素β细胞功能指数(HOMA-β)和胰岛素β细胞抵抗指数(HOMA-IR)评价胰岛功能。HOMA-β=20×空腹胰岛素(FINs)/(FPG-3.5),HOMA-IR=FPG×FINs/22.5。其中,采用放射免疫法测定FINs。
1.4.5 中医证候积分比较观察并对比三组患者治疗前后的中医证候积分,观察患者是否有以下症状:口干舌燥,心悸烦躁,盗汗失眠,四肢乏力等。轻度症状记作1 分,中度症状记作2 分,重度症状记作3 分,无以上症状则记作0 分。
1.4.6 安全性评价记录并对比三组治疗过程中后的不良反应发生发生情况。
1.5 统计学方法本研究采用软件SPSS 21.0 进行数据分析,计量资料以()表示,多组间比较采用单因素方差分析,两两比较采用LSD-t检验,治疗前后比较采用配对资料t检验。计数资料以例(%)表示,组间比较采用χ2检验。P<0.05 认为差异有统计学意义。
2 结果
2.1 血糖指标治疗前三组的血糖指标差异无统计学意义(P>0.05),治疗后三组的血糖指标均明显降低,且C组的FPG、2h-PG 和HbA1c水平均明显低于A 组和B 组(P<0.05),治疗后A 组和B 组仅FPG 差异有统计学意义(P<0.05)。B 组和C 组治疗前后的血糖指标差异有统计学意义(P<0.05),A 组治疗前后的FPG 和HbA1c 差异有统计学意义(P<0.05)。见表2。
表2 三组治疗前后血糖指标Tab.2 Three groups of blood glucose indicators before and after treatment±s
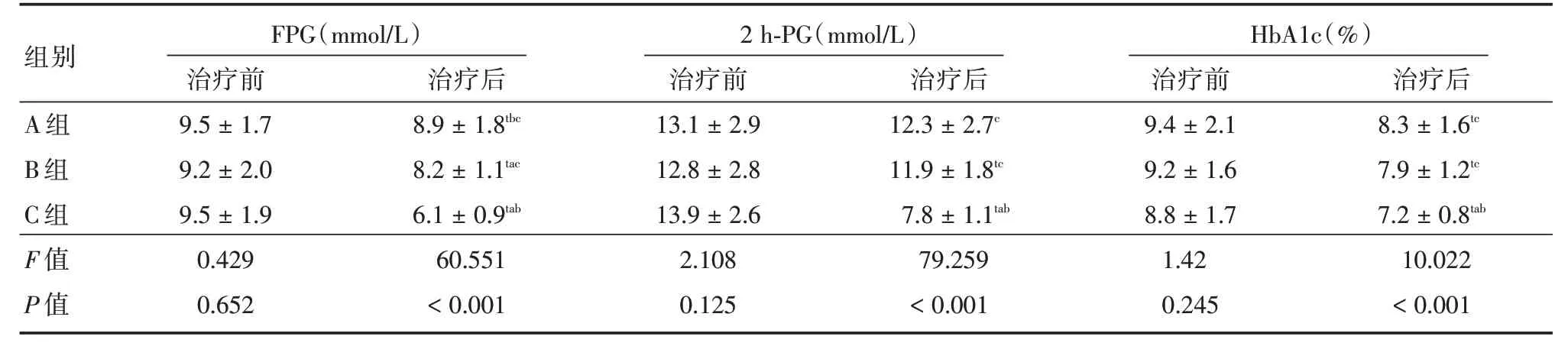
表2 三组治疗前后血糖指标Tab.2 Three groups of blood glucose indicators before and after treatment±s
注:与本组治疗前相比,tP <0.05;与A 组治疗后相比,aP <0.05;与B 组治疗后相比,bP <0.05;与C 组治疗后相比,cP <0.05
mmol/L)2 h-PG(mmol/L)HbA1c(%)治疗后治疗前治疗后治疗前治疗后组别A 组B 组C 组F 值P 值FPG(治疗前9.5±1.7 9.2±2.0 9.5±1.9 0.429 0.652 8.9±1.8tbc 8.2±1.1tac 6.1±0.9tab 60.551<0.001 13.1±2.9 12.8±2.8 13.9±2.6 2.108 0.125 12.3±2.7c 11.9±1.8tc 7.8±1.1tab 79.259<0.001 9.4±2.1 9.2±1.6 8.8±1.7 1.42 0.245 8.3±1.6tc 7.9±1.2tc 7.2±0.8tab 10.022<0.001
2.2 疗效治疗后A 组的总有效率为78%,B 组的总有效率为82%,C 组的总有效率为96%,C 组总有效率显著高于A 组和B 组(P<0.05),治疗后A 组和B 组的疗效对比差异无统计学意义(P>0.05)。见表3。
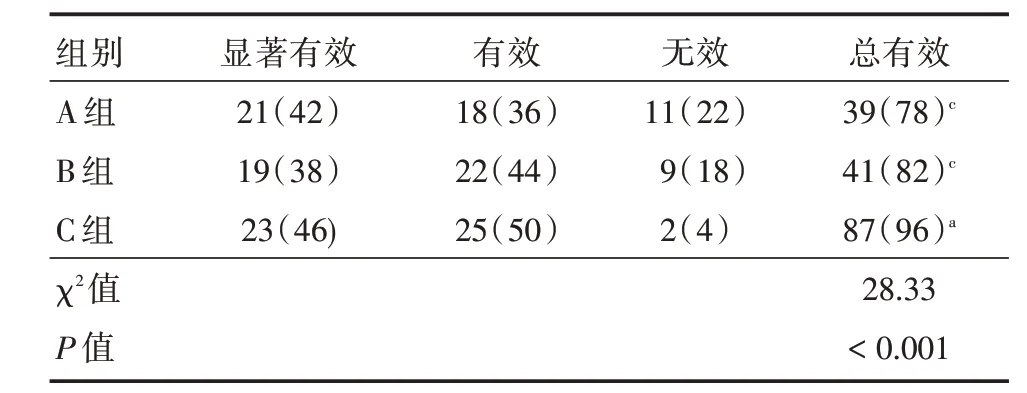
表3 三组治疗后临床疗效Tab.3 The clinical efficacy of the three groups after treatment例(%)
2.3 内脂素治疗前三组的内脂素水平差异无统计学意义(P>0.05),治疗后三组的内脂素水平均明显降低,且C 组的内脂素水平均明显低于A 组和B组(P<0.05),治疗后仅A组和C组差异有统计学意义(P<0.05)。三组治疗前后的内脂素水平差异有统计学意义(P<0.05)。见表4。
表4 三组治疗前后内脂素水平Tab.4 Visfatin levels before and after treatment in the three groups±s

表4 三组治疗前后内脂素水平Tab.4 Visfatin levels before and after treatment in the three groups±s
注:与本组治疗前相比,tP <0.05;与A 组治疗后相比,aP <0.05;与B组治疗后相比,bP <0.05;与C组治疗后相比,cP <0.05
组别A 组B 组C 组F 值P 值内脂素(μg/L)治疗前28.4±8.6 27.8±8.7 28.1±9.3 0.057 0.944治疗后21.3±5.2tc 20.1±4.9t 18.1±5.8ta 4.629 0.011
2.4 胰岛功能治疗前三组的胰岛功能无明显差异(P>0.05),治疗后三组的HOMA-β和HOMA-IR均明显改善,且C 组的HOMA-β明显高于A 组和B组(P<0.05),治疗后A 组和B 组的胰岛功能差异无统计学意义(P>0.05)。三组治疗前后的胰岛功能均差异有统计学意义(P<0.05)。见表5。
表5 三组治疗前后胰岛功能Tab.5 Pancreatic islet function before and after treatment in the three groups±s
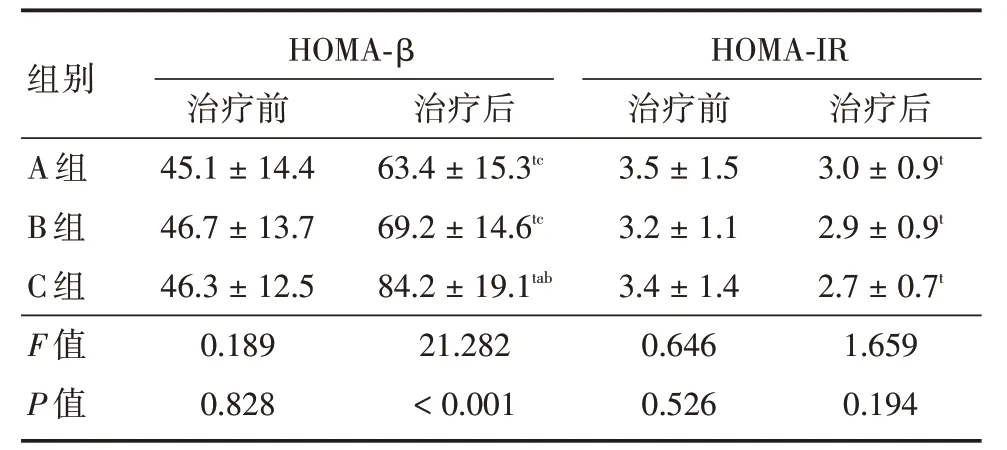
表5 三组治疗前后胰岛功能Tab.5 Pancreatic islet function before and after treatment in the three groups±s
注:与本组治疗前相比,tP <0.05;与A 组治疗后相比,aP <0.05;与B组治疗后相比,bP <0.05;与C组治疗后相比,cP <0.05
组别A 组B 组C 组F 值P 值HOMA-β治疗前45.1±14.4 46.7±13.7 46.3±12.5 0.189 0.828治疗后63.4±15.3tc 69.2±14.6tc 84.2±19.1tab 21.282<0.001 HOMA-IR治疗前3.5±1.5 3.2±1.1 3.4±1.4 0.646 0.526治疗后3.0±0.9t 2.9±0.9t 2.7±0.7t 1.659 0.194
2.5 中医证候积分治疗前三组的中医证候积分无明显差异(P>0.05),治疗后三组的中医证候积分均明显降低,且C 组的中医证候积分明显低于A 组和B 组(P<0.05)。治疗后A 组和C 组、B 组和C 组差异有统计学意义(P<0.05)。三组治疗前后的胰岛功能差异有统计学意义(P<0.05)。见表6。
表6 三组治疗前后中医证候积分Tab.6 Three groups of TCM syndrome scores before and after treatment±s
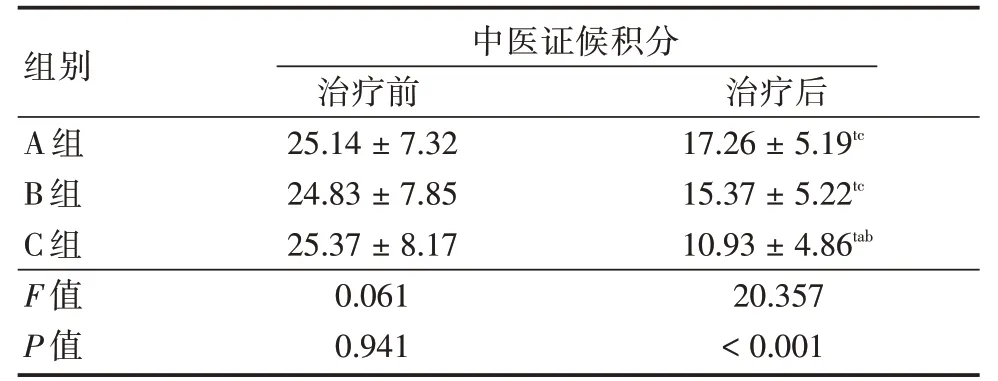
表6 三组治疗前后中医证候积分Tab.6 Three groups of TCM syndrome scores before and after treatment±s
注:与本组治疗前相比,tP <0.05;与A 组治疗后相比,aP <0.05;与B 组治疗后相比,bP <0.05;与C 组治疗后相比,cP <0.05
组别A 组B 组C 组F 值P 值中医证候积分治疗前25.14±7.32 24.83±7.85 25.37±8.17 0.061 0.941治疗后17.26±5.19tc 15.37±5.22tc 10.93±4.86tab 20.357<0.001
2.6 安全性评价治疗后A 组的总不良反应发生率为10%,B 组的总不良反应发生率为6%,C 组的总不良反应发生率为12%,三组在治疗过程中均未出现严重不良反应。C 组总不良反应发生率高于A 组和B 组,但是差异无统计学意义(P>0.05)。见表7。
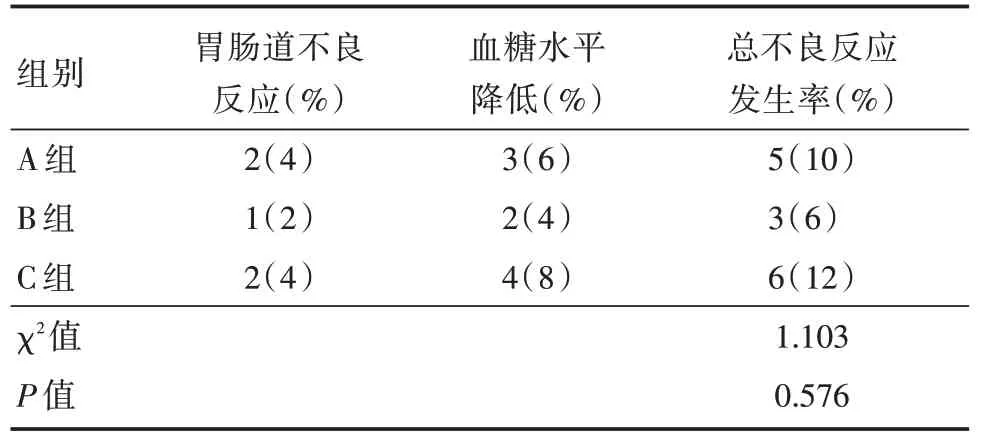
表7 三组不良反应发生率Tab.7 The incidence of adverse reactions in the three groups例(%)
3 讨论
糖尿病一种体内糖代谢异常的临床综合征,目前临床治疗中尚无有效的根治方法[8]。二甲双胍是目前应用最广泛的降糖药[9],其治疗机制是抑制肝糖原从而改善胰岛素抵抗,但是部分2 型糖尿病患者服用二甲双胍后控糖效果不佳。因此,临床治疗中需要联合其他不同机制的降糖药物[10],协同治疗日益复杂的发病机制。根据中国2 型糖尿病防治指南(2017年版)的指导,二甲双胍作为经过长期临床治疗检验的有效的降糖药,是2 型糖尿病患者的首选,患者无不良反应的前提下,二甲双胍应保留在治疗方案中。2 型糖尿病的主要发病机制有胰岛功能障碍和胰岛素抵抗,因此,本研究保持使用可改善胰岛素抵抗的二甲双胍[11],还采用可改善胰岛功能障碍的利拉鲁肽联合治疗二甲双胍治疗失效的2 型糖尿病患者。近年来,中医药逐渐成为糖尿病治疗的热点,中国古代就对糖尿病有明确的记载,古代医药典籍中将糖尿病称为“消渴症”。中医认为消渴症的病因是不良生活习惯导致脾胃失调,阴虚燥热、气血亏损,机体糖代谢异常,人体无法正常吸收能量(精气),人体血糖水平异常增高从而影响其他组织功能。因此,中医主张使用益气养阴,滋脾补肾的中药配方治疗消渴症。参芪降糖颗粒是一种主要成分为人参和黄芪的中药复合制剂,近年来常用于治疗消渴症,其功效主要为改善气血,补脾益肾[12]。
由血糖指标结果可看出,治疗后C 组的FPG、2h-PG 和HbA1c 水平均明显低于A 组和B 组(P<0.05),治疗后A 组和B 组仅FPG 差异有统计学意义(P<0.05)。这说明参芪降糖颗粒和利拉鲁肽均可以有效改善二甲双胍治疗失效的2 型糖尿病患者的血糖。此外,实验结果表明,治疗后A组的总有效率为78%,B 组的总有效率为82%,C 组的总有效率为96%,C 组总有效率显著高于A 组和B 组(P<0.05)。说明联合用药能够更加有效控制血糖水平。当人体血浆葡萄糖水平升高时,胰高血糖素样肽-1(GLP-1)可刺激胰岛β细胞分泌胰岛素降低血糖水平[13],利拉鲁肽属于人工合成GLP-1 长效类似物—,使其可以代替与GLP-1受体结合,有效修复胰岛β细胞[14],改善胰岛功能并延长其体内循环时间,实现长期有效稳定患者血糖水平[15]。参芪降糖颗粒中的人参皂苷可刺激胰岛β细胞分泌胰岛素[16],从而降低体内血糖水平。此外,参芪降糖颗粒还可以提高物质运输胰岛素的能力[17],从而提高胰岛素的利用效率,实现更好降糖效果。
近年来有研究发现,内脂素作为新型的脂肪细胞因子,广泛存在于机体脂肪组织中,能够促进脂肪细胞分化,影响糖脂代谢,参与机体炎症反应和胰岛素抵抗,可调节烟酰胺磷酸核糖转移酶活性,促进生成烟酰胺腺嘌呤二核苷酸,从而刺激胰岛β细胞分泌胰岛素,从而降低体内血糖水平发挥类胰岛素效应[18]。此外,有研究发现[19],2 型糖尿病患者的内脂素水平高于正常人,对其机制进一步研究对于糖尿病患者的诊断、治疗以及预后评估具有重要意义。治疗后三组的内脂素水平均明显降低,且C 组的内脂素水平均明显低于A 组和B组(P<0.05),治疗后仅A 组和C 组差异有统计学意义(P<0.05)。三组治疗前后的内脂素水平差异有统计学意义(P<0.05)。实验结果表明利拉鲁肽和参芪降糖颗粒均可以有效降低患者的内脂素水平,分析认为利拉鲁肽可以抑制多种炎性反应的起始因子——核因子-κB 的激活[20],从而降低机体内脂素水平。此外,联合用药改善患者内脂素水平的效果更佳,原因可能是参芪降糖颗粒中的人参皂苷通过调控AsTP3 及p-AKT/FoxO1 通路可调节肝脏葡萄糖代谢[21],抑制高胆固醇血症,减少内脏脂肪堆积,从而降低内脂素水平。
HOMA-IR 和HOMA-β常用于评估机体胰岛素抵抗水平,HOMA-IR降低和HOMA-β提高说明机体对胰岛素的敏感性增强,即胰岛功能发生改善。实验结果表明,治疗后三组的HOMA-β和HOMA-IR均明显改善,且C 组的HOMA-β明显高于A 组和B组(P<0.05)。这是因为利拉鲁肽可以有效改善胰岛功能,保护和修复胰岛β细胞分泌胰岛素,从而降低血糖水平。参芪降糖颗粒改善胰岛功能的原因可能是,参芪降糖颗粒中的黄芪可以修复胰岛β细胞,激发胰岛β细胞活性,从而改善胰岛功能[22]。此外,参芪降糖颗粒中的人参皂苷可抑制Na+-K+-ATP 通道活性[23],降低胰岛β细胞耗氧量,从而起到保护胰岛β细胞作用。因此,联合用药通过不同机制协同作用,改善胰岛功能增强。
从中医角度来看,治疗后C 组的中医证候积分明显低于A 组和B 组(P<0.05)。这是因为参芪降糖颗粒作为一种中药复方制剂,其中人参可以补气益脾,覆盆子可以养肾益肝,麦冬和地黄可以滋阴生津,五味子可以益气生精等,诸药配伍能够滋脾补肾、益气养阴、肺肾同调对治疗消渴症有明显效果。实验结果表明,中西医的联合应用可产生协同作用,从而发挥更好降糖疗效。
由安全性评价实验结果可看出,三组在治疗过程中均未出现严重不良反应。C 组总不良反应发生率高于A 组和B 组,但是差异无统计学意义(P>0.05)。这提示联合治疗并未增加药物不良反应,安全性较好。
本研究发现,利拉鲁肽和参芪降糖颗粒均可以改善二甲双胍治疗失效的2 型糖尿病患者的血糖、内脂素水平、胰岛功能和中医证候积分,但联合用药组有更好的降糖和调节胰岛能力。此外,糖尿病是一种慢性疾病,口服给药的参芪降糖颗粒的患者依顺性更好,适合长期使用。综上所述,利拉鲁肽联合参芪降糖颗粒在二甲双胍治疗失效的2 型糖尿病方面具有更广阔的临床应用前景。但因本研究的研究对象数量有限,为单中心的临床研究,之后仍需大样本量的多中心研究加以佐证。
