蒙药材白石脂中二氧化硅和三氧化二铁含量的测定方法
2021-06-24白文明渠弼王来兵那生桑
白文明 渠弼 王来兵 那生桑
白石脂为硅酸盐类矿物多水高岭石族多水高岭石的一种白色块状物,具有愈伤、接骨、干脓、止血、除脑疾等功效,是蒙药制剂常用药材之一[1]。现行《中华人民共和国药典(一部)》收载的成方制剂复方珍珠散的处方包含该药材的炮制品煅白石脂,但白石脂本身并不是《中华人民共和国药典(一部)》收载的药材品种[2]。现在有关白石脂质量标准的研究仍停留在性状描述、理化鉴别及检查等阶段[1],既无完善的药材质量标准,也缺乏科学、系统的研究案例。尤其对白石脂化学成分的定量分析尚未见任何研究报道,属于空白阶段。白石脂作为原矿物药,受到采集矿区的自然环境及形成过程等复杂因素的影响,不同批次药材的化学成分可能存在差异[3],而且药材及饮片在市场流通过程中存在以次充好、以假乱真等现象[4-5],所以建立白石脂相应化学成分的定量分析方法是制订白石脂质量标准体系的前提条件。本研究基于抗坏血酸与含硅成分、邻菲罗啉与含铁成分的显色作用[6-7],尝试建立基于紫外—可视分光光度法测量白石脂中二氧化硅(SiO2)和三氧化二铁(Fe2O3)含量的定量分析方法,并进行系统的方法学考察。
1 材料
1.1 药材
6批次白石脂药材分别购自河北安国中药材市场、安徽毫州中药材市场、河南禹州中药材市场,经内蒙古医科大学生药教研室渠弼教授鉴定为硅酸盐类矿物药白石脂。
1.2 主要仪器和试剂
TU-1901型双光束紫外—可见分光光度计(北京普析通用仪器有限责任公司);二氧化硅对照品(99.9%,aladdin industrial corporation);三氧化二铁对照品(99.9%,aladdin industrial corporation);95%乙醇、盐酸、硝酸、茜素磺酸钠、钼酸铵、抗坏血酸、无水碳酸钠、碳酸钾、硼砂等均为市售分析纯。
2 二氧化硅含量测定的方法学考察
2.1 供试品溶液的制备及含量测定方法
取105℃干燥至恒重的本品细粉约0.5 g,精密称定,置铂金坩埚中,加3 g碳酸钾—硼砂混合熔剂,搅拌均匀。盖上坩埚盖,从低温开始升高温度,再950~1000℃熔融10分钟。取出,冷却至室温后,将坩埚和盖一并放入加热至微沸的盛有100 mL,2 mol/L硝酸溶液的300 mL烧杯中,继续保持微沸状态,直至熔融物完全溶解,用水洗净坩埚及盖,然后将溶液冷却至室温,移入250 mL容量瓶中,加水稀释至刻度,摇匀。
精密量取上述溶液10.00 mL,置100 mL容量瓶中,用水稀释至刻度,摇匀后精密量取10.00 mL,置100 mL容量瓶中,加水至约40 mL,依次加入5 mL 1 mol/L盐酸溶液、8 mL 95%乙醇溶液、6 mL 5%钼酸铵溶液。放置30分钟,加入20 mL 6 mol/L盐酸溶液、5mL 1%抗坏血酸溶液,用水稀释至刻度,摇匀。放置1小时后,以水为空白。按照紫外—可见分光光度法(通则0401)[8],在660 nm波长处测定吸光度,从标准曲线上读出供试品溶液中含二氧化硅的含量(mg/mL),按下列公式计算,即得白石脂样品中二氧化硅的含量。
注:wSiO2:二氧化硅质量分数(%);m2:100 mL测定溶液中二氧化硅的含量,单位为毫克(mg);250:全部试样溶液与所分取试样溶液的体积比;m1:试样的重量,单位为克(g)。
2.2 线性关系试验
取经1000~1100 ℃灼烧至恒重的二氧化硅对照品0.20 g,精密称定,置铂金坩埚内,加2 g无水碳酸钠,搅拌均匀,在1000~1100 ℃高温下熔融15分钟。冷却,用水将熔块浸出于盛有热水的300 mL烧杯中,待全部溶解后冷却至室温,移入1000 mL容量瓶中,用水稀释至刻度,摇匀,精密吸取10 mL上述溶液于100 mL容量瓶中,用水稀释至刻度,摇匀,即得(每1 mL中含二氧化硅0.02 mg)。
精密量取对照品溶液0.00 mL、4.00 mL、6.00 mL、8.00 mL、10.00 mL、12.00 mL、17.00 mL、20.00 mL,分别置100 mL容量瓶中,各加水至约40 mL,依次加入5 mL 1 mol/L盐酸溶液、8 mL 95%乙醇溶液、6 mL 5%钼酸铵溶液。放置30分钟,加入20 mL 6 mol/L盐酸溶液、5 mL 1%抗坏血酸溶液,用水稀释至刻度,摇匀。放置1小时后,以水为空白。按照紫外—可见分光光度法(通则0401)[8],在660 nm波长处测定吸光度。以吸光度为横坐标,浓度为纵坐标,绘制标准曲线。
标准工作曲线的线性回归系数r=0.9998,回归方程为Y=6.721X-0.02471,表明SiO2浓度在0~4.2 μg/mL范围内,呈良好的线性关系。结果见表1、图1。
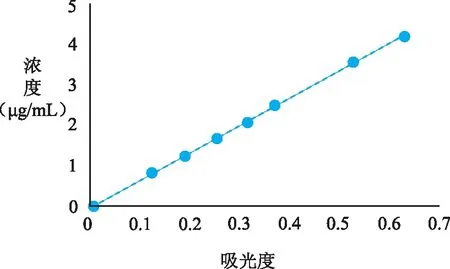
图1 SiO2的标准工作曲线

表1 各SiO2标准溶液的浓度及吸光度数据
2.3 精密度试验
按供试品溶液制备方法制得供试品溶液1份,连续测定吸光度6次,结果表明,仪器的测量精密度良好。结果见表2。

表2 SiO2含量的精密度试验数据
2.4 稳定性试验
按供试品溶液制备方法制得供试品溶液1份,分别于制得溶液的0小时、1小时、2小时、4小时、6小时、8小时后进行一次吸光度测定。结果表明,供试品溶液在480分钟内稳定。结果见表3。
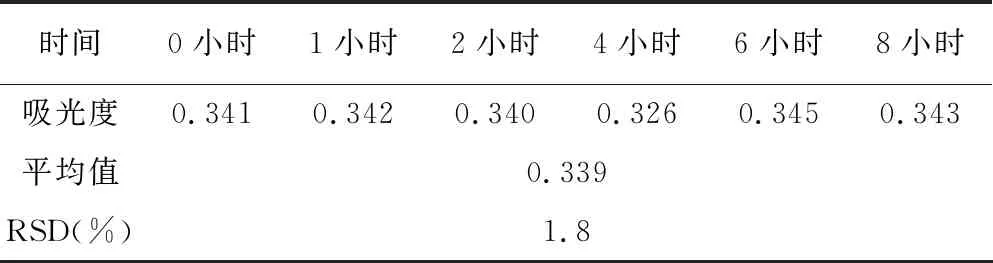
表3 SiO2含量的稳定性试验数据
2.5 重现性试验
按供试品溶液制备方法平行制备6份供试品溶液,分别测定其含量。结果表明,方法的重现性良好。结果见表4。
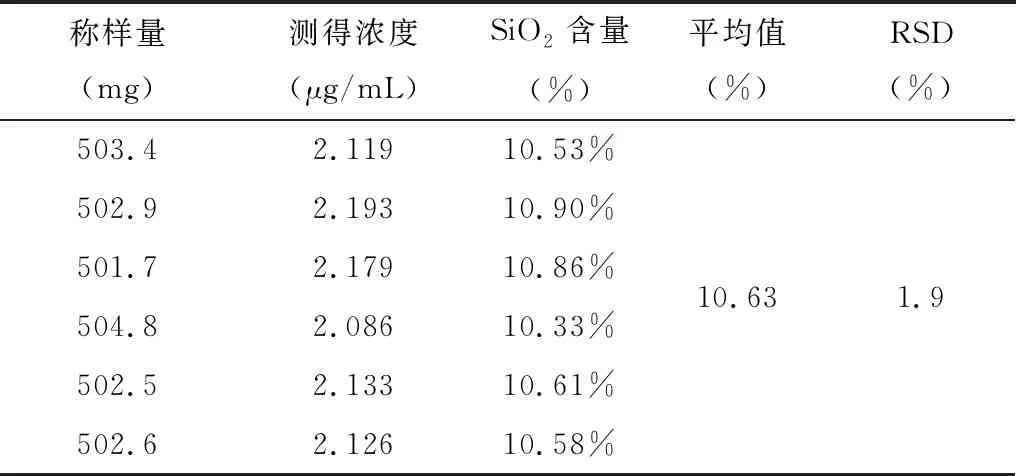
表4 SiO2含量的重复性试验数据
2.6 加样回收率试验
供试品称样量减半,按二氧化硅对照品加入量与所取供试品中二氧化硅含量之比1.5∶1、1∶1、0.5∶1加入二氧化硅对照品后,按供试品溶液制备方法制得供试品溶液6份(各比例2份),分别测定其含量。结果表明,方法的准确度良好。结果见表5。
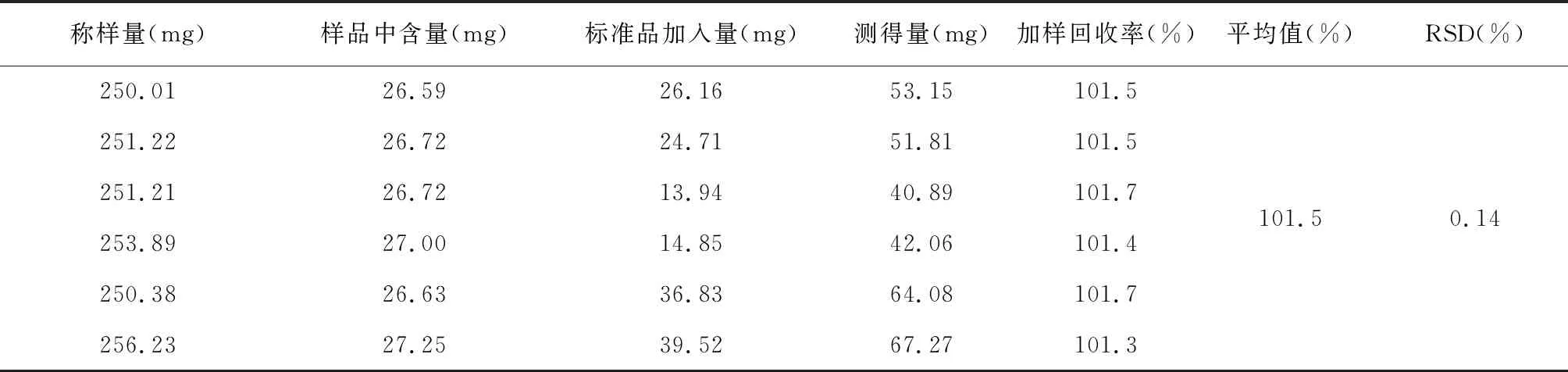
表5 SiO2含量的加样回收率试验数据
3 三氧化二铁含量测定的方法学考察
3.1 供试品溶液的制备及含量测定方法
取105℃干燥至恒重的本品细粉约0.5 g,精密称定,置铂金坩埚中,加3 g碳酸钾—硼砂混合熔剂(1∶1),搅拌均匀。盖上坩埚盖,从低温开始升高温度,再950~1000℃熔融10分钟。取出,冷却至室温后,将坩埚和盖一并放入已加热至微沸的盛有100 mL 2 mol/L硝酸溶液的300 mL烧杯中,继续保持微沸状态,直至熔融物完全溶解,用水洗净坩埚及盖,然后将溶液冷却至室温,移入250 mL容量瓶中,加水稀释至刻度,摇匀。
精密量取上述溶液5.00 mL,置100 mL容量瓶中,按照对照品溶液制备项下的方法,自“加水至约50 mL”起,依法在510 nm处测定吸光度,从标准曲线上读出供试品溶液中Fe2O3的含量(mg)。
注:wFe2O3:三氧化二铁的质量分数(%);mFe2O3:100 mL测定溶液中三氧化二铁的含量,单位为毫克(mg);50:全部试样溶液与所分取试样溶液的体积比;m试样:试样的重量,单位为克(g)。
3.2 线性关系试验
取经950℃灼烧至恒重的三氧化二铁对照品0.10 g,精密称定,置于300 mL烧杯中,加30 mL 6 mol/L盐酸溶液,低温加热至全部溶解,冷却后移入1000 mL容量瓶中,用水稀释至刻度,摇匀,即得(每1 mL中含二氧化硅0.1 mg)。
精密量取对照品溶液0.00 mL、1.00 mL、2.00 mL、3.00 mL、4.00 mL、5.00 mL,分别置于100 mL容量瓶中,加水至约50 mL,加入5 mL 1%抗坏血酸溶液,放置5分钟,再加入5 mL 0.2%邻菲罗啉溶液、2 mL 10%乙酸铵溶液,在不低于20℃下放置30分钟,加水稀释至刻度,摇匀。以水为空白,按照紫外—可见分光光度法(通则0401)[5],在510 nm波长处测定吸光度。以吸光度为横坐标,浓度为纵坐标,绘制标准曲线。
标准工作曲线的线性回归系数r=0.9996,回归方程为Y=0.8679X-0.002406,表明三氧化二铁浓度在0~0.5290 mg/mL范围内,呈良好的线性关系。见表6、图2。

表6 各Fe2O3标准溶液的浓度及吸光度数据
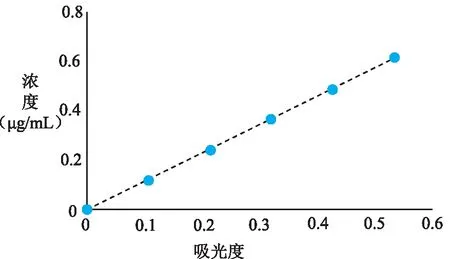
图2 Fe2O3的标准工作曲线
3.3 精密度试验
按供试品溶液制备方法制得供试品溶液1份,连续测定吸光度6次,结果表明,仪器的测量精密度良好。结果见表7。

表7 Fe2O3含量的精密度试验数据
3.4 稳定性试验
按供试品溶液制备方法制得供试品溶液1份,分别于制得溶液的0小时、1小时、2小时、4小时、6小时、8小时后进行一次吸光度测定,结果表明,供试品溶液在480分钟内稳定。结果见表8。
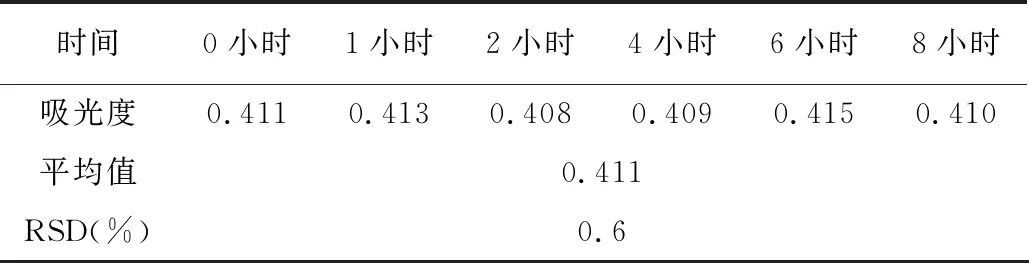
表8 Fe2O3含量的稳定性试验数据
3.5 重现性试验
按供试品溶液制备方法平行制备6份供试品溶液,分别测定其含量,结果表明,方法重现性良好。结果见表9。
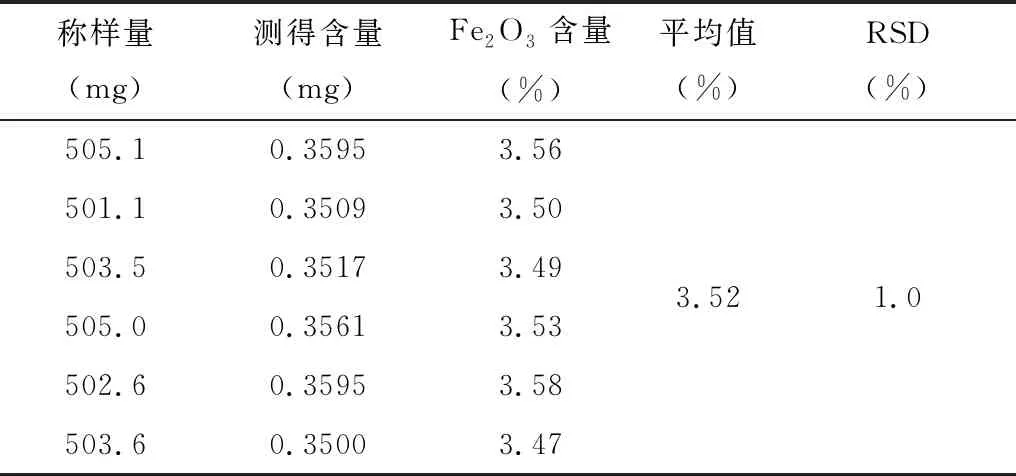
表9 Fe2O3含量的重复性试验数据
3.6 加样回收率试验
供试品称样量减半,按三氧化二铁对照品加入量与所取供试品中三氧化二铁含量之比1.5∶1、1∶1、0.5∶1加入三氧化二铁对照品后,依法制备供试品溶液6份(各比例2份),分别测定其含量,计算加样回收率。结果表明,方法的准确度良好。结果见表10。
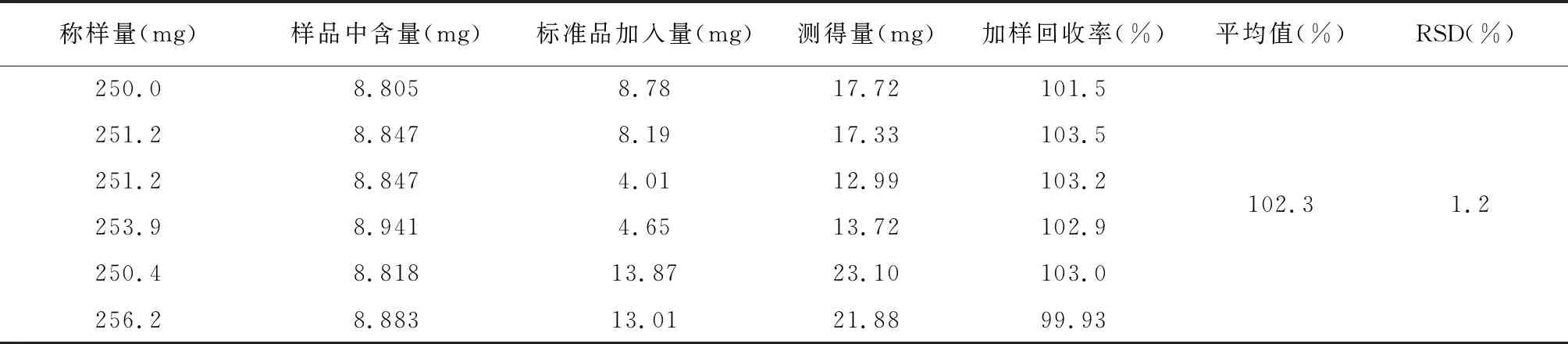
表10 Fe2O3含量的加样回收率试验数据
依法对6批次白石脂药材中二氧化硅和三氧化二铁含量进行了测定,结果见表11。

表11 各批次样品SiO2、Fe2O3含量的测定数据
4 结果与讨论
本试验通过系统的方法学研究,建立了原矿物药白石脂中二氧化硅(SiO2)和三氧化二铁(Fe2O3)含量测定的方法,为白石脂质量标准研究提供了重要的理论依据。所建立的紫外—可见分光光度法测得的含量数据表明,不同批次、不同产地原药材的二氧化硅和三氧化二铁含量具有较明显的差异,可能与原矿物的形成过程和自然环境的差异有关。
