原发性肝癌患者应用索拉菲尼血药浓度与不良反应关系分析
2021-06-20赵翠芬彭程程
赵翠芬,彭程程
(河南省商丘市民权县人民医院肿瘤内科,河南 商丘 476800)
原发性肝癌(primary liver cancer,PLC)简称肝癌,肝癌患者行肝移植手术后肿瘤复发与转移是目前尚未能解决的问题,也是影响肝移植临床疗效的主要原因[1]。由于该疾病早期症状不显著,确诊时已经属于晚期,故而无法接受根治手术治疗,错过最佳治疗时机。采用手术和化疗的方法可以改善患者的临床症状,但是其预后效果较差[2]。随着研发的不断进行,多激酶抑制剂索拉非尼作为晚期肝癌的治疗药物已经得到很好的应用和推广。国外有研究指出[3],高血压、手足综合征是索拉菲尼特征性的不良反应,其他消化系统、血液系统的不良反应发生率较低。但国内针对此类患者其疗效和安全性尚不明确。基于此,该研究应用索拉菲尼进行治疗原发性肝癌患者,分析索拉菲尼血药浓度与不良反应之间的联系,现报道如下。
1 资料与方法
1.1 一般资料
选取该院接受治疗的原发性肝癌患者60例为研究对象,采用计算机随机分组的方式,将研究对象按照1∶1的比例分为对照组(n=30)及试验组(n=30)。对照组男患者16例,女患者14例;年龄36~78岁,平均年龄为(56.24±8.16)岁;肿瘤节转移TNM(tumor node metastasis,TNM)分期:Ⅱ期8例,Ⅲ期15例,Ⅳ期7例。试验组男患者17例,女患者13例;年龄35~77岁,平均年龄为(55.31±8.36)岁;TNM分期:Ⅱ期6例,Ⅲ期16例,Ⅳ期8例。患者及家属知情同意,并签署知情同意书。该研究经医学伦理委员会批准。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 纳入标准与排除标准
纳入标准:入组患者经病理组织相关检查,均明确诊断为原发性肝癌患者;美国东部肿瘤协作组ECOG(eastem cooperative oncology group,ECOG)评分≤2分患者;知情同意。排除标准:合并高血压、糖尿病患者;合并血液循环系统、泌尿系统、消化系统疾病以及其他可对并发症诊断产生干扰疾病患者。
1.3 方法
所有患者入组后,均完善相关临床检查,在诊断明确后均进行肝动脉灌注化疗栓塞术化疗治疗,采用Seldinger技术进行股动脉穿刺,将导管鞘以及导管(5F)置入肝动脉,利用高压注射器将造影剂注射在肠系膜上动脉或腹腔动脉干内,明确肿瘤位置、数量后,采用化疗栓塞药物表柔比星30 g与栓塞剂超液化碘20 mL的混合液对肿瘤靶血管进行栓塞,可根据肿瘤实际情况及碘油的扩散情况对药品使用剂量进行调整。两组患者均口服索拉非尼(进口药品注册证号H20130137;规格:0.2 g),对两组患者血药浓度进行检测和控制,调整药物使用剂量,将试验组患者血药浓度控制在>4.78 μg/mL,将试验组患者的血药浓度控制在≤4.78 μg/mL。若治疗期间出现不良反应,可给予药物辅助治疗;若是出现疾病进展或者恶化,可停止使用,选择其他疗法。
1.4 观察指标
由两名经验丰富的医师对患者药物不良反应进行诊断和统计,若患者在治疗期间出现血压升高(收缩压>140 mmHg,舒张压>90 mmHg)可诊断为索拉菲尼相关高血压;若患者出现手足部位皮肤损伤、腹泻、血细胞(白细胞、血小板、血红蛋白、淋巴细胞等)减少等,则可分别诊断为手足综合征(图1)、消化系统相关并发症及血液系统相关并发症。并采用CTC3.0评价标准为患者不良反应发生程度进行评价。
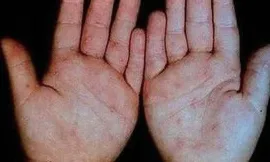
图1 手足综合征特征
1.5 统计方法
采用SPSS 26.0统计学软件予以数据处理,计数资料以频数(n)和百分比(%)表示,两组不良反应发生率比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 不良反应发生情况
60例研究对象不良反应发生率为43.33%(26/60),高血压发生占比最高,为13.33%(8/60),血液系统相关并发症发生占比最低,为3.33%(2/60);CTC3.0分级,1~4级分别发生10例、10例、4例、2例,见表1。
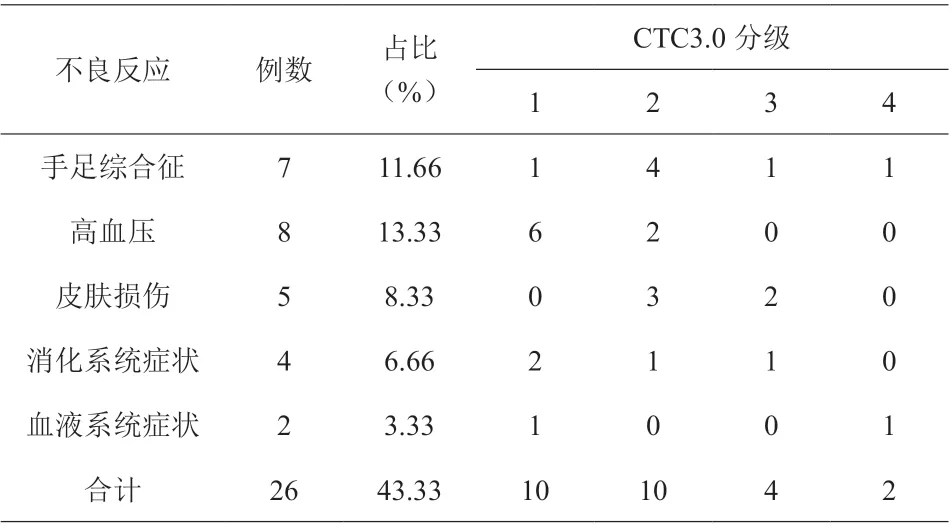
表1 患者不良反应发生情况统计[n(%)]
2.2 两组患者不良反应发生情况比较
试验组患者不良反应发生率显著低于对照组(23.33%<63.33%),差异有统计学意义(P<0.05),见表2。
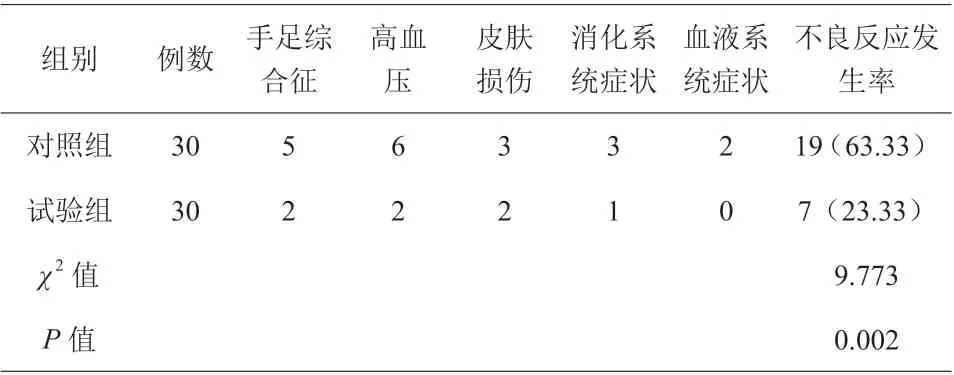
表2 两组患者不良反应发生情况比较[n(%)]
3 讨论
原发性肝癌好发于中年人群中,受食物霉菌、病毒感染、生活习惯(长期吸烟、饮酒)的影响,原发性肝癌发病率高且较为迅速,严重威胁着人们的生命安全与健康。但原发性肝癌的治疗存在局限性,一经发现已经是晚期。随着研发的不断进行,多激酶抑制剂索拉非尼作为晚期肝癌的治疗药物已经得到很好的应用和推广。尽管如此,对于使用不同血药浓度的索拉菲尼时会出现一定的不良反应。手足部皮肤反应、高血压是索拉菲尼最具特征性的不良反应。有研究指出,索拉菲尼不良反应的发生与其血药浓度之间具有密切的关系,较高的血药浓度可增加高血压、手足皮肤损伤发生的概率。索拉非尼抗癌机制及其不良反应具体如下。
3.1 索拉非尼抗癌机制
索拉非尼具有广泛的抗癌作用,较多地应用于没有进行手术的原发性肝癌患者中。该药对血管内皮生长因子受体VEGFR(vascular endothelial growth factor receptor,VEGFR)、血小板衍生因子受体PDGFR(platelt derived factor receptor,PDGFR)途径[6]的酪氨酸激酶受体产生抑制作用,对新生肿瘤血管产生抑制作用,对肿瘤细胞的血液供应产生干预作用[7-9]。该药同时具有拮抗肿瘤细胞及抗血管生成的作用,可产生较为理想的抗癌作用,有效延长原发性肝癌患者的生存时间。
3.2 不同血药浓度的索拉菲尼对高血压影响
有报道称[10],应用索拉非尼对原发性肝癌患者进行治疗,发生高血压的概率在25%。本研究高血压的发生率为13.33%,稍低于报道中的25%;并且试验组患者高血压发生例数低于对照组(2例<6例),说明高血压的发生与索拉菲尼的血药浓度具有一定的联系。索拉菲尼主要通过引起血管收缩,进而导致血压升高。此外,索拉菲尼具有一定的抗血管作用,可减少小动脉血管的数量,也是导致患者血压升高的重要原因。Liu Z等[11]、邵宝儿等[12]研究发现,索拉菲尼血药浓度与患者高血压发生概率之间具有正比关系。该研究结果与之相符。
采用索拉非尼对原发性肝癌患者进行治疗,对患者肾素-血管紧张素-醛固酮系统有一定的激活作用,因此,可选择血管紧张素受体转化酶抑制剂(angiotensin-converting enzyme inhibitor,ACEI)类降压药物对患者血压情况进行干预,若药物减压无效或患者出现高血压危象等,则应考虑停止使用索拉非尼进行治疗[10-13]。
3.3 不同血药浓度的索拉菲尼对手足综合征影响
手足部位皮肤反应是索拉菲尼另一种具有特征性的不良反应,常在服药2~3周左右出现相关症状。患者常表现为掌面、关节处、易受到摩擦部位等手足位置出现红斑、刺痛、感觉障碍等症状。有研究指出[13-15]手足综合征的发生率可达20%以上,高于本研究试验结果11.66%。手足综合征的发生,与患者血药浓度之间具有正比关系,邵文雨等[16]报道中出现手足综合征患者索拉菲尼血药浓度显著高于未出现手足综合征患者;并且血药浓度>4.78 μg/mL者,发生手足综合征的概率显著增加。本研究结果与之一致。
有学者认为[17-21]若患者出现手足部位皮肤表现,则说明患者对索拉菲尼的反应性较好,因此可以根据患者是否出现手足部位皮肤表现及出现程度的差异,对索拉菲尼治疗效果进行预测。针对出现的轻度的手足综合征,多数患者未经干预,若患者症状较为严重,则需要采取干预措施以提高患者生存质量,如采用炉甘石洗剂等缓解瘙痒症状;采用保护措施,降低手足部位出现摩擦、挤压等。
3.4 应用索拉菲尼的其他不良反应
胃肠道相关不良反应主要以恶心、呕吐、腹泻、便秘为主,该研究共4例(对照组3例,试验组1例)患者出现胃肠道相关不良反应,占比6.66%。其发生机制尚未明确,可能与索拉菲尼对胃肠道的直接刺激作用有关[22]。血液系统的不良反应较为少见,该研究共2例(均为对照组患者)患者有血液系统不良反应表现,占比3.33%,给予特殊干预后,均好转,并未对治疗产生影响。
综上所述,索拉非尼具有理想的肝癌治疗效果,但其不良反应与血药浓度之间具有正比关系,对其高剂量的应用产生了严重的限制。临床在保证治疗效果的前提下,应视具体情况调整索拉菲尼的使用剂量,以达到降低不良反应发生概率和提高患者生存质量的目的。此外,虽然索拉非尼为具有多靶点的靶向药物,但抗癌机制较为单一,单独应用疗效较为局限,临床可考虑联合其他抗癌药物共同应用,以获得理想的治疗效果。该次研究样本例数较少,对应用索拉菲尼血药浓度与不良反应关系的研究并不是特别全面,在以后的研究中,增加样本数量,完善研究。
