无糖型强力枇杷露的安全性评价研究*
2021-06-20陈昕昕邵田莉黄秋平张晓洁蔡溢谌红献
陈昕昕,邵田莉,黄秋平,张晓洁,蔡溢,谌红献**
(1.中南大学湘雅二医院精神卫生研究所,湖南 长沙 410011;2.深圳市康宁医院精神科,广东 深圳 518000)
20世纪90年代,我们曾发现何首乌具有肝毒性作用、马兜铃酸成分具有肾毒性作用、麻黄具有神经毒性作用等,可见,对中药药物开展安全性评价十分重要。但由于中药成分复杂,具有用药起效慢、周期长、体内作用部位广等特点,导致安全性评价研究开展的难度较大。
强力枇杷露是《卫生部药品标准中药成方制剂》中记载的中药成分药物制剂[1],由多种中药成分及辅料构成,因含有罂粟壳成分而具有较好的止咳效果。罂粟壳是《中国药典》中记载的麻醉制剂、有毒制剂,也是麻醉药物中唯一的中药饮片[2]。罂粟壳中的阿片类药物成分进入脑血屏障后作用于延髓,能够抑制咳嗽中枢及咳嗽反射,起到止咳效果[3]。此外,强力枇杷露中添加的防腐剂辅料苯甲酸钠,如长期过量服用会损伤神经系统[4],并产生细胞毒性[5],提高致癌风险[6]。因此,对强力枇杷露进行安全性评价具有重要意义。
半数致死量(Median Lethal Dose,LD50)是指在固定时间内(24~48 h)内予以实验物质后,能够引起实验动物死亡率达到50%的实验物质的剂量,作为传统急性经口毒性实验的常用指标,用于衡量不同药物的毒性大小和优劣。测量药物LD50方法有很多,常用的有序贯法(即上下法,Up-and-Down Procedure)和霍恩氏法,还有寇氏法、累积法、回归法(logistic)等。序贯法包括两个实验过程,即限度试验和主实验[7],使用程序或者特殊公式来计算LD50,是国际上进行急性毒性试验的替代方法[8],也是我国政府部门检测化学药物急性毒性的推荐方法[9]。
目前,国内对强力枇杷露的研究主要集中在成分和质量方面,尚未发现有针对其安全性开展的研究。强力枇杷露中的吗啡成分,具有一定的依赖性和毒性。吗啡的毒理作用表现在体内代谢会增加肝脏内的自由基,破坏肝脏组织,使体内的一氧化氮增加[10]。既往研究中,如对老鼠注射3个月吗啡,会引起雄性老鼠的生殖细胞结构变化及数量减少[11]。吗啡依赖的小鼠对毒性反应更加敏感,腹腔注射甲基苯丙胺的LD50约为正常小鼠的一半[12]。此外,强力枇杷露中的辅料苯甲酸钠属于一种防腐剂,同样具有细胞毒性[13]。综合以上情况,研究无糖型强力枇杷露的安全性是有必要的,本文使用序贯法来测量该药物的LD50,并观察其毒性作用。
1 实验材料与方法
1.1 实验动物
成年健康未孕雌性Sprague Dawley(SD)大鼠[14]、初始体重200±20 g(由湖南斯莱克景达实验动物有限公司提供)。SD大鼠进入实验室后,置于12 h明暗节律的动物房内一周适应,期间予以自由饮食。
1.2 实验试剂及器材
由无糖型强力枇杷露的厂家提供的10倍浓缩的无糖型强力枇杷露(所有成分和辅料都等比例浓缩10倍)以及未添加罂粟壳成分的无糖型强力枇杷露的10倍浓缩的溶媒试剂;大鼠灌胃针;5 mL注射器;消毒酒精;电子秤。
1.3 给药方式及分组
SD大鼠的给药方式为灌胃。通过上下法来进行试验,虽然对于测试未知药物LD50的推荐起始剂量为175 mg·kg-1[14],但根据既往吗啡半数致死量的研究,我们将无糖型强力枇杷露测试的初始剂量按照其中所含吗啡的量来计算。吗啡LD50的范围在151~257 mg·kg-1[15],按照250 mg·kg-1来计算,无糖型强力枇杷露中吗啡的检测浓度为0.096 mg·mL-1[16],算出SD大鼠无糖型强力枇杷露的LD50初始测试剂量为2 600 mL·kg-1(250 mg·kg-1/0.096 mg·mL-1≈2 600 mL·kg-1),每只SD大鼠体重按0.2 kg来计算,每日灌胃的剂量为2 600 mL,这在实验操作过程中是不可能完成的,我们将用10倍浓缩无糖型强力枇杷露、10倍浓缩的溶媒试剂来减少灌胃量。使用10倍浓缩液后,每只SD大鼠的每日灌胃量为52 mL(液体是蒸馏水时,大鼠最大灌胃体积为80 mL·kg-1[17]),灌胃频率为5 mg·1.5 h-1。
将SD大鼠随机分为实验组和对照组,实验组予以含有罂粟壳的10倍浓缩无糖型强力枇杷露,对照组则予以对应剂量的10倍浓缩的溶媒试剂。
1.4 实验方法
在此实验中我们采取序贯法来测试无糖型强力枇杷露的LD50,这个方法包括两个实验,限度实验和主实验。
1.4.1 限度实验步骤
在限度实验中,采用初始剂量无糖型强力枇杷为2 600 mg·kg-1对SD大鼠进行灌胃,若第一只SD大鼠灌胃后(两周内)死亡,则直接进入主实验,LD50<2 600 mg·kg-1;若第一只大鼠存活,将该剂量继续给予另外两只大鼠,若两只都存活则存活的SD大鼠总数达到3只,LD50≥2 600 mg·kg-1;如果至少有一只大鼠死亡,该剂量继续给予另外两只大鼠,直到存活或死亡的大鼠总数达到3只。根据限度实验的结果可估计LD50是否高于此剂量。
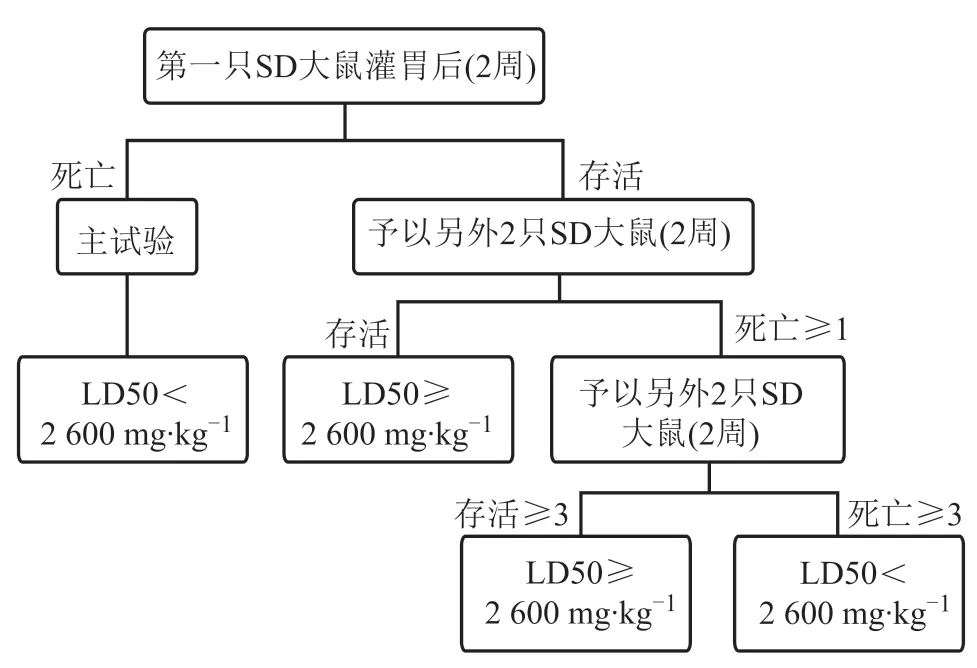
图1 限度实验的实验流程
1.4.2 主实验步骤
根据限度实验的结果,无糖型强力枇杷露的LD50低于2 600 mg·kg-1(相当于给予每只大鼠10倍浓缩无糖型强力枇杷露52 mL),因此主实验中采用该剂量作为第一只SD大鼠的灌胃剂量。在第一只之后的SD大鼠我们将遵循急性药理毒性试验指南一般原则。在急性药物毒性试验指南中,所选剂量可从以下序列中选择:1.75 mg·kg-1、5.5 mg·kg-1、17.5 mg·kg-1、55 mg·kg-1、175 mg·kg-1、550 mg·kg-1、1 750 mg·kg-1、5 000 mg·kg-1……[14]。在决定是否对下一只动物灌胃之前,每只SD大鼠都应认真观察48小时,后一只动物剂量的上升或下降由前一只动物的死亡或存活决定;从第1只动物改变算起到停止试验标准之一,停止实验,计算LD50。无糖型强力枇杷露大概的LD50根据公式lgLD50=Σ(nX)/Σn计算,其中n是每个剂量的动物总数,X是每个剂量的对数剂量,取反对数就可以获得大概的无糖型强力枇杷露的LD50。
当满足下列停止实验标准之一时,停止实验:
(a)连续3只动物存活;
(b)任意连续的6只SD大鼠中有5只连续发生存活/死亡转换;
(c)第一只SD大鼠发生存活/死亡转换之后,至少有4只SD大鼠进入试验,并且其LD50估算值的范围超出临界值(2.5倍)。(首次转换的第4只SD大鼠之后,对每次给药进行计算)。
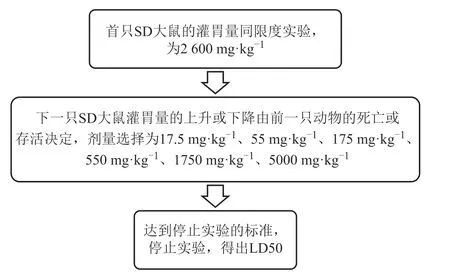
图2 主实验的实验流程
1.4.3 其他观察指标
每天灌胃后连续观察动物的反应,至少14天,每隔一天观察一次,以便能观察到毒性反应出现的时间及其恢复时间、动物死亡时间等。观察的指标包括一般指标(如动物外观如何、活动情况、对刺激的反应、分泌物、排泄物等)、动物的死亡情况(死亡的时间、濒死前的反应等)等。记录所有的死亡情况、出现的症状,以及症状起始的时间、严重程度、持续时间等。
所有的试验动物均要进行大体解剖,包括在试验过程中因为濒死而被处死的动物、在实验过程中死亡的动物及试验结束时仍然存活的动物。解剖后发现组织器官出现体积、颜色、质地等方面的改变时,均应予以记录并对其进行病理学检查。
2 结果
2.1 限度实验结果
在限度实验中,第一只SD大鼠在第四次灌胃后死亡,即20 mL后死亡,按照指南的实验步骤,我们应该进入主实验,但是为了降低操作对SD大鼠造成意外死亡的可能,我们又进行了两对灌胃操作。三对结果如表1所示:

表1 限度实验灌胃后SD大鼠的状态
由限度实验结果,可以推测无糖型强力枇杷露的LD50低于2 600 mg·kg-1。
2.2 主实验结果
主实验结果如表2所示,首只SD大鼠灌胃量为52 mL(2 600 mg·kg-1),灌胃后大鼠死亡;前一只大鼠死亡,故第2只大鼠的灌胃量选择低一级的剂量35 mL(1 750 mg·kg-1),灌胃后死亡;故第3只大鼠灌胃剂量为11 mL,灌胃后存活;第4只大鼠灌胃剂量为35 mL,灌胃后死亡;第5只大鼠灌胃剂量为11 mL(550 mg·kg-1),灌胃后存活;第6只大鼠灌胃剂量为35 mL,灌胃后死亡;第7只大鼠灌胃剂量为11 mL,灌胃后存活。此时,从第3只大鼠起到第7只大鼠连续5次发生存活/死亡转换,满足了停止实验标准的第二条,实验停止,不再对序列中1.75 mg·kg-1、5.5 mg·kg-1、17.5 mg·kg-1、55 mg·kg-1等剂量进行实验。根据公式计算得出lgLD50等于3.05,无糖型强力枇杷露在雌性SD大鼠的LD50大概值为1 122 mg·kg-1。

表2 主实验各剂量级灌胃后实验组SD大鼠的状态
2.3 其他观察指标
在限度实验和主实验的实验过程中,每只予以剂量为175 mg·kg-1及300 mg·kg-1的10倍无糖型强力枇杷露时,实验组SD大鼠在第3次灌胃后,即15 mL浓缩药物出现腹部隆起,可触及肠型;行为方面实验组较对照组挣扎减少,反射减少,尿量及排便减少,按及膀胱处有尿液排出,口唇的分泌物减少,并在实验操作当天死亡;而对照组在灌胃相同次数及剂量时,腹部未见明显隆起,肠型触及不明显,活动及反射均较实验组好,但也弱于灌胃前的状态,粪便排出由干燥到稀松。这些实验组SD大鼠均在第四次灌胃后1小时左右死亡,死亡之前呼吸变得深而慢,活动能力明显下降。每只予以剂量为55 mg·kg-1的10倍浓缩枇杷露时,虽然SD大鼠的活动减少,腹部稍有膨隆,但其反射存在,有明显的应激反应。经过14天的观察,实验组存活的SD大鼠在第三天逐渐恢复饮食,大小便恢复至正常颜色及状态;相应的对照组活动可,在观察的第二天,大小便恢复至正常颜色及状态。
每只实验组的SD大鼠死后及经过14天观察期的SD大鼠,都予以了大体解剖,解剖后发现在实验操作当天死亡的实验组SD大鼠的肺叶明显减小;胃肠道组织蓄积较多的药品浓缩液,膀胱充盈。存活下来的实验组SD大鼠及对照组SD大鼠在麻醉后解剖,肺叶未见明显萎缩,胃肠道中未见明显液体残留,膀胱未见明显充盈。
3 讨论
3.1 无糖型强力枇杷露LD50评价
药物的急性毒理作用一般通过测定动物的LD50及最大给药量来衡量[18],在本研究中我们通过LD50 来评价无糖型强力枇杷露的安全性。在本实验中,根据上下法测得的无糖型强力枇杷露的LD50的估计值为1 122 mg·kg-1。根据GHS急性经口毒性分级原则,无糖型强力枇杷露的毒性属于低毒水平[19]。无糖型强力枇杷露临床推荐剂量为每日45 mL,一个成年人(按体重为60 kg来计算)每天无糖型强力枇杷露的剂量为0.75 mg·kg-1,参考徐叔云《药理实验方法学》转化,按体表面积计算等效剂量的比值来计算,人与SD大鼠的转换系数为6.3,SD大鼠的临床每日推荐剂量为4.725 mg·kg-1,远远低于其LD50。既往对于枇杷露类的研究多侧重于成分、质量及临床应用[20],本研究首次通过上下法测定无糖型强力枇杷露的LD50,结果显示该药物的毒性作用较低。
3.2 生理状况及解剖结果评价
在给SD大鼠灌胃过程中,观察到SD大鼠在灌胃15 mL的10倍浓缩液后,相当于成人剂量7 143 mL(15 mL×10 / 0.2 kg×60 kg / 6.3=7 143 mL),SD大鼠的活动明显减少,呼吸开始变得急促,腹部可触及肠型,刺激肛门时,SD大鼠的大小便较对照组明显减少,表示药物抑制了消化系统及泌尿系统的功能。在灌胃20 mL的浓缩液后,相当于成人剂量9 524 mL(20 mL×10 / 0.2 kg×60 kg / 6.3=9 524 mL),SD大鼠死亡,解剖后发现SD大鼠的肺部明显萎缩,胃肠道内充满药物,膀胱也是充盈状态。以上实验结果都显示无糖型强力枇杷露在大剂量使用时具有镇静、抑制呼吸、抑制胃肠蠕动及排空、引起尿潴留的作用。
3.3 阿片类物质的影响
无糖型强力枇杷露中含有罂粟壳,其中的吗啡及可待因等成分都属于阿片类物质。阿片类物质能通过血脑屏障,抑制中枢神经系统的功能,产生镇静作用[21];阿片类物质还能抑制消化系统的腺体分泌,导致胃排空延迟,幽门及回盲括约肌运转延迟[22];在过量使用时,还会导致呼吸抑制的严重不良事件[23];对于泌尿系统的影响是会引起尿潴留,主要是由于阿片类物质影响抗利尿激素的释放,并导致尿道平滑肌痉挛[24]。由于对照组SD大鼠未出现上述毒性反应,提示无糖型强力枇杷露中含有的罂粟壳可能是导致呼吸、消化和泌尿系统毒性的主要因素。
3.4 辅料的影响
苯甲酸钠是无糖型强力枇杷露的辅料之一,是一种常见的防腐剂。苯甲酸钠会干扰微生物细胞膜的通透性,影响细胞膜对氨基酸的吸收;苯甲酸分子进入细胞内后,会抑制微生物细胞内的呼吸酶系统,使微生物ATP的产生减少或停止,从而起到防腐的作用[25]。在主实验和限度实验中,对照组SD大鼠经过不含罂粟壳的10倍浓缩溶媒试剂灌胃后,在14天的观察期内均存活,且未见明显的毒性作用,该结果提示无糖型强力枇杷露中的辅料苯甲酸钠可能不是其产生毒性反应的主要因素,即便如此苯甲酸钠的毒性也不可忽视。
综上所述,无糖型强力枇杷露的毒性分级属于低毒水平,其中的罂粟壳及苯甲酸钠等成分在既往研究中都明确表示过量会产生毒理反应,因此在临床使用时要严格根据使用说明书及医嘱服药。
4 结论
无糖型强力枇杷露的LD50约为1 122 mg·kg-1,毒性分级属于低毒等级,根据无糖型强力枇杷露的推荐临床服用剂量是安全的,并不会引起上述的毒理反应。但使用过大剂量时对SD大鼠胃肠蠕动、呼吸、泌尿及行为反射都有抑制作用,严重时会导致SD大鼠的死亡。
