不同粒径腐殖酸颗粒对土壤有效态镉的影响
2019-04-18林义成傅庆林丁能飞李凝玉
邹 传,郭 彬,林义成,傅庆林,*,刘 琛,丁能飞,李凝玉,李 华
(1.浙江农林大学 环境与资源学院,浙江 杭州 311300; 2.浙江省农业科学院 环境资源与土壤肥料研究所,浙江 杭州310021)
腐殖酸是自然界中广泛存在的大分子聚合物,可通过吸附、交换和络合等作用,对重金属的生物地球化学行为产生重要影响[1]。研究表明,腐殖酸可促使重金属从易被植物吸收利用的交换态向难被植物吸收利用的有机结合态和残渣态转化[1-2],其作为重金属钝化剂可进行大田应用[3-5];然而,也有研究发现施用腐殖酸对土壤重金属起到了活化作用[6]。一些学者对腐殖酸的主要组分进行分离,发现分子量相对较低的富里酸能够促使可给态镉的增加,而芳构化程度高且高分子量的胡敏酸则对可给态镉有一定的抑制和钝化作用[7]。由此可见,腐殖酸兼具钝化和活化土壤重金属的作用,但目前关于腐殖酸不同组分对土壤重金属有效性的调控作用机制在本研究检索范围内还不多见。
已有研究表明,施用有机物料可显著增加土壤可溶性有机物(dissolved organic matter, DOM)含量,提高土壤重金属的活性和迁移能力[8],从而活化土壤重金属[9]。腐殖酸大分子表面结构存在易变性,其对土壤重金属有效性的影响不仅与化学组成有关,同时也与其粒径大小和溶解度有关。因此,通过调节腐殖酸粒径,改变腐殖酸的DOM组分溶解情况,有可能会影响土壤中重金属形态转化和生物活性的去向。
研磨是改变腐殖酸物料粒径以提高其溶解率的有效方法[10-11]。为此,本研究开展了不同研磨条件下腐殖酸颗粒的水溶性特征分析,进而研究其对土壤镉有效性的影响,以期为合理利用腐殖酸调控土壤镉的生物有效性提供理论依据和技术支撑。
1 材料与方法
1.1 试验样品
供试土壤采自杭州市某矿区镉重度污染农田,为潜育水稻土。土壤Cd含量10.20 mg·kg-1,土壤有机质含量2.15%,土壤pH值5.85,碱解氮含量113.31 mg·kg-1,有效磷含量18.26 mg·kg-1,速效钾含量112.45 mg·kg-1。
试验所用腐殖酸样品购自山东创新腐殖酸科技股份有限公司,为风化煤矿源腐殖酸,其物化性质如下:N、C、H、S元素含量分别为0.748%、46.307%、3.445%、0.098%,pH值4.13,溶解率14.17%,羧基、酚羟基、总酸性基含量分别为3.063、0.317、3.379 mmol·g-1。
1.2 不同研磨条件下的腐殖酸样品制备
利用DM-04L变频行星式球磨机(南京大冉科技有限公司)研磨腐殖酸,制备不同粒径的腐殖酸颗粒。综合设置时间、转速、物料体积(球罐体积为100 mL)、研磨转子(大-中-小)数量等4因素,根据腐殖酸溶解率、溶解液DOM获得5种腐殖酸样品:未经研磨的腐殖酸样品标为CK,4种经过研磨处理的腐殖酸样品依粒径从大到小依次标为G1~G4。如表1所示,随着腐殖酸样品粒径减小,腐殖酸样品的溶解率增大,腐殖酸溶液的D254依次增大,说明腐殖酸溶液中DOM含量增高[12-13]。
1.3 腐殖酸溶液与滤渣制备
取CK及G1~G4等5种腐殖酸样品各2 g,加入蒸馏水50 mL,振荡24 h,5 000 r·min-1离心5 min后,固液分离,分别得到腐殖酸溶液和滤渣样品。
1.4 原腐殖酸对Cd的吸附试验
选取CK样品(未溶解)及其滤渣2种样品,开展Cd等温吸附试验。设置Cd浓度梯度:500、750、1 000、1 200、1 400 mg·L-1,将2种样品按固液质量体积比1∶20加不同浓度的Cd溶液,恒温(25 ℃)振荡(220 r·min-1)24 h,5 000 r·min-1离心5 min,过滤后测定上清液中Cd浓度,绘制腐殖酸样品及滤渣的Cd2+等温吸附曲线[14]。
1.5 土壤培养试验
取供试土壤80 g,分别加入按1.3节方法制备获得的5种腐殖酸溶液50 mL或滤渣2 g,充分混匀,培养30 d后,破坏性采样,测定土壤pH、有机质含量及有效态Cd含量。
1.6 测定方法
腐殖酸元素分析:用德国Elementar vario isotope cube同位素有机元素分析仪测定。腐殖酸pH值:按1∶10的固液质量体积比制备浸提液,以pH计(雷磁PHS-3E)测定。腐殖酸溶解率:按2∶50的固液质量体积比制备浸提液,测定。腐殖酸溶液D254:用紫外可见分光光度计(上海仪电INESA-L6),在254 nm下测定腐殖酸溶液的吸光值。腐殖酸基团含量:羧基含量以Ca。(CH3COO)2滴定法测定,总酸性基含量以NaOH滴定法测定,酚羟基含量为总酸性基与羧基含量之差[15],用溶解液基团含量表示溶解部分的腐殖酸所带走的基团含量,以原腐殖酸的基团含量结合研磨后的腐殖酸溶解率间接计算得出。腐殖酸样品红外光谱分析:用傅里叶红外光谱仪(德国布鲁克VERTEX70)测定,固体采用KBr压片法,液体则直接测定。扫面电镜分析:用台式扫描电镜(HITACHI日立TM3000)扫描腐殖酸样品,进行分析。溶液Cd2+含量:采用Cd2+选择性电极法(齐威PXS-Cd)测定[8]。土壤pH值:按1∶2.5的土水质量体积比制备浸提液,用pH计(雷磁PHS-3E)测定[16]。土壤有机质含量:采用低温外热重铬酸钾氧化法测定[16]。土壤有效态镉含量:采用二乙烯三胺五乙酸(DTPA)浸提,用电感耦合等离子体发射光谱仪(德国耶拿ICP-MS)测定表1研磨处理参数及其样品性质
Table1Parameters of grinding and properties of according samples

样品Sample物料体积Materialvolume/mLt/min转速Speed/(r·min-1)转子数量(大-中-小)Rotor quantity(Large-Middle-Small)溶解率Dissolutionrate/%溶液D254值D254 value of solutionCK————14.170.5240G130904501-4-514.330.5909G2301502501-4-514.330.6686G310902501-4-514.500.6960G430902502-7-815.170.7528
表中D254值为腐殖酸溶液稀释20倍后测得值。
D254value in the above table was measured after 20 times dilution of the solution.
2 结果与分析
2.1 腐殖酸可溶组分对土壤Cd吸附的影响
为明确腐殖酸中的可溶组分对土壤Cd吸附的影响,开展了腐殖酸样品(CK)与其去除可溶组分后的腐殖酸滤渣对Cd离子吸附能力的比较研究。结果表明(图1),2种材料对Cd的吸附量均随初始Cd浓度的加大而增加。在Cd浓度较低时,等温吸附线的斜率较大,即曲线较陡部分,此时为Cd快速吸附阶段,可能与有机官能团和Cd产生螯合作用有关,即腐殖酸本身所带有的大量官能团,如羟基(—OH)、羧基(—COOH)与Cd络合[1];在Cd浓度较高时,吸附曲线趋于平缓,吸附量增加较慢,逐渐达到平衡,这一阶段为腐殖酸的慢速吸附,可能是Cd的物理吸附所致,即Cd离子吸附于腐殖酸颗粒表面,这与朱丽珺等[14]的研究结果相一致。
随着Cd浓度增加,腐殖酸滤渣对Cd的吸附量的增幅高于腐殖酸样品,且在Cd浓度高于200 mg·L-1时,两者差异达到显著水平。采用朗缪尔(Langmuir)方程[17-18]拟合了Cd的等温吸附曲线(表2),决定系数R2达极显著水平(P<0.01)。拟合结果表明,腐殖酸滤渣最大吸附量为18.77 mg·g-1,大于腐殖酸样品的18.17 mg·g-1。吸附常数在一定程度上反映了腐殖酸吸附Cd的能级,其值越大,说明反应在常温下能自发进行的程度愈强,生成物愈稳定,对Cd的吸附能力越强。腐殖酸滤渣的吸附常数值(0.289 9)大于腐殖酸样品(0.151 9),说明腐殖酸滤渣对Cd的吸附能力高于腐殖酸样品。造成上述结果的原因在于,腐殖酸中的可溶组分对Cd存在解吸作用,从而使腐殖酸对土壤Cd的钝化作用有所减弱。前人研究也表明,土壤中腐殖酸可溶组分的增加会导致土壤吸附重金属的能力降低[19],引起土壤中Cd活性增加[20]。因此,通过研磨控制腐殖酸粒径,可促进其可溶组分在水中的溶解,通过收集腐殖酸滤渣可达到强化腐殖酸钝化效果的目的。

图1 腐殖酸样品及其滤渣对Cd2+的吸附曲线Fig.1 Cd adsorption curves of humic acid and its residue fractions
表2吸附模型拟合结果
Table2Fitting result of adsorption model

样品Sample拟合方程Equation modelR2腐殖酸Humic acidqe=18.1700×0.1519Ce1+0.1519Ce0.9292滤渣Residue fractionsqe=18.7738×0.2899Ce1+0.2899Ce0.8662
qe、Ce分别为平衡吸附量和平衡浓度。
qe,Cerepresented equilibrium adsorption capacity and equilibrium concentration, respectively.
2.2 腐殖酸不同组分对土壤pH及有机质、有效态Cd含量的影响
为方便后文描述,将加入CK腐殖酸样品对应溶液和滤渣的处理分别简记为CK溶液和CK滤渣,其他样品处理的表述与之相似,分别对应于G1~G4溶液和G1~G4滤渣。如图2所示,将各腐殖酸样品的溶液及滤渣加入土壤中,培养30 d后,土壤pH值发生不同程度的变化:G3、G4溶液处理的土壤pH值较CK溶液处理的土壤显著(P<0.05)下降,G1~G4滤渣处理的土壤pH值较CK滤渣处理均显著(P<0.05)下降。这可能是由于腐殖酸含有大量的羧基、酚羟基,致其本身呈酸性[1,21]。因此,向土壤中加入腐殖酸的可溶或不溶组分均会降低土壤pH。而且,本试验中,G3、G4滤渣处理的土壤pH显著(P<0.05)低于G1、G2处理,G1、G2滤渣处理的土壤pH显著(P<0.05)低于CK滤渣,G3、G4溶液处理的土壤pH显著(P<0.05)低于CK溶液处理,而G1、G2溶液处理的土壤pH与CK溶液处理相比却无显著差异。这些结果暗示,腐殖酸样品(溶液及滤渣)对土壤pH的酸化作用可能与腐殖酸样品的粒径有关,样品粒径越小,其对土壤的酸化作用越强。
本试验所用的腐殖酸样品富含有机物质,C含量达46%。如图2所示,G3滤渣处理的土壤有机质含量显著(P<0.05)高于CK滤渣处理,但与其他处理并无显著差异,加入腐殖酸溶液的各处理间土壤有机质含量并无显著差异。这可能是因为腐殖酸样品溶解所产生的有机质含量较低,对土壤的有机质影响较小。本研究结果与靳志丽等[22]、吴炳孙等[23]的研究结果一致。
如图2所示,G1~G4滤渣处理的土壤有效态Cd含量显著(P<0.05)低于CK滤渣处理,G2~G4 溶液处理的土壤有效态Cd含量显著(P<0.05)高于CK溶液和G1溶液处理。谷勋刚等[24]研究表明,有机肥中的水溶性物质被去除后,促进了土壤中Cu和Cd的沉淀;Zeng等[25]的研究表明,土壤DOM含量增加会显著提高提高重金属的生物有效性;何雨帆等[26]研究也表明,腐殖酸中的胡敏酸和富里酸分别具有钝化和活化土壤Cd的作用,从而分别降低和增加了小白菜对Cd的吸收。本研究显示,随着G1~G4样品腐殖酸溶液中DOM的增加,G1~G4溶液对镉的活化作用显著增强,相应滤渣的钝化作用亦显著增强。
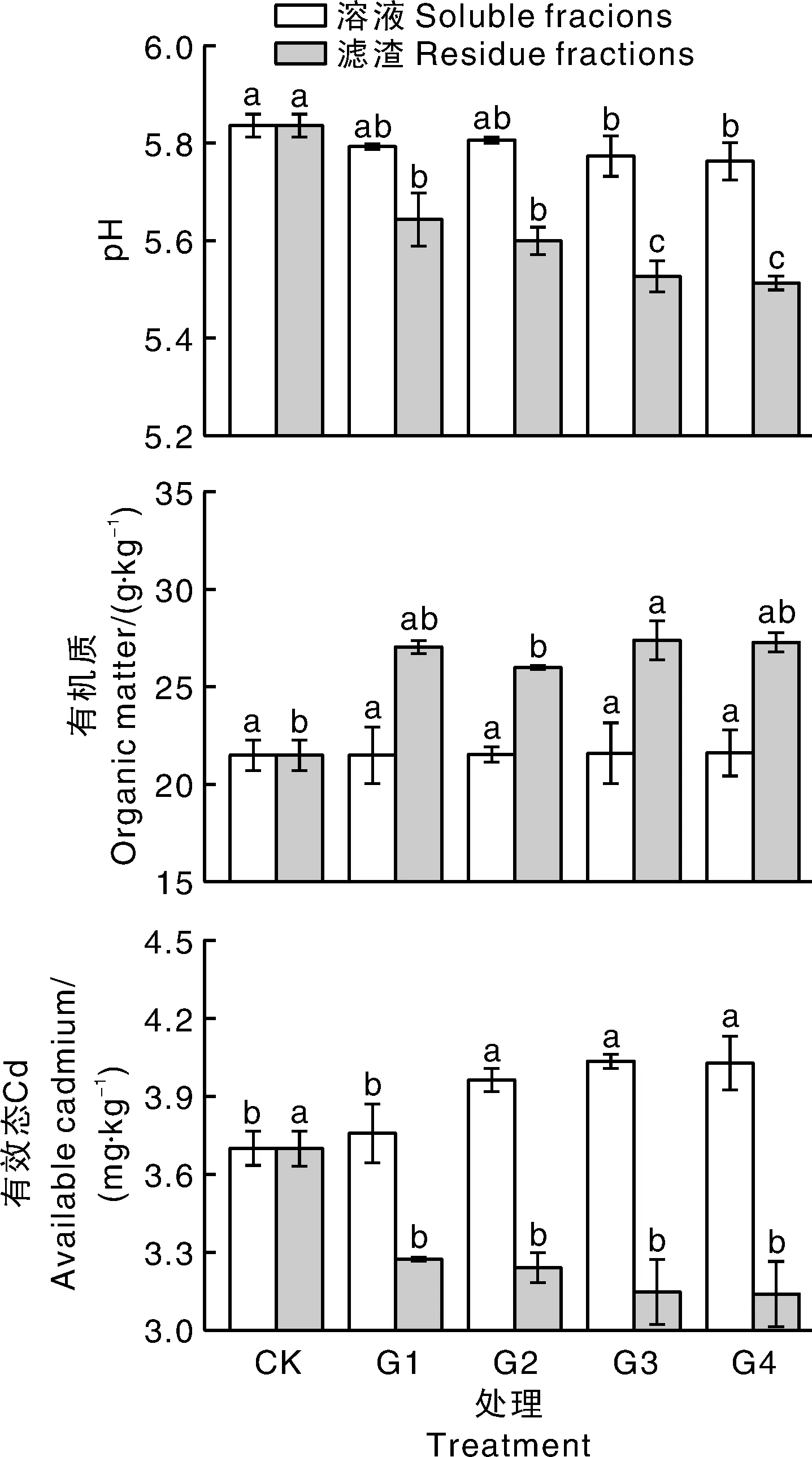
同一系列柱上无相同字母的表示差异显著(P<0.05)。Bars in the same serial marked without the same letters indicated significant difference at P<0.05.图2 不同处理对土壤pH及有机质、有效态Cd含量的影响Fig.2 Effect of different treatments on soil pH and contents of organic matter and available Cd
2.3 腐殖酸材料成分分析
2.3.1 电镜扫描
为探究腐殖酸对Cd吸附的作用机理,进行了腐殖酸电镜扫描分析(图3)。结果显示,腐殖酸颗粒表面无规则、凹凸不平有棱角,整体型无定型,且大孔隙较少,只存在因表面凹凸所形成的小孔隙。随着研磨后可溶物的溶解程度增加,剩余的腐殖酸颗粒表面突起部分更小、更圆滑,数量显著增加。
腐殖酸本身已有较高的比表面积,高达2 000 m2·g-1,远大于黏土矿物和金属氧化物的比表面积[27]。电镜扫描结果表明,研磨处理后的腐殖酸比表面积进一步增加,强化了腐殖酸颗粒对Cd的吸附效果。
2.3.2 腐殖酸残渣和可溶组分的基团分析
腐殖酸分子结构复杂,含有众多官能团,富含羧基、酚基等活性基团[1]。为此,本研究对腐殖酸样品在研磨、溶解处理后的羧基、酚羟基含量进行测定,用以探究腐殖酸可溶与不溶组分对Cd作用的机理。红外光谱分析表明,1 705、1 604、1 384、1 269 cm-1等波数代表了羧基基团(图4,横线为基线)[28-29]。随着研磨后可溶组分的溶解程度增加,腐殖酸滤渣羧基含量逐渐增加(图4,表3),酚羟基含量逐渐降低(表3)。G4(研磨后溶解度最高的腐殖酸样品)的上述4个波峰面积均高于CK(溶解度最低的腐殖酸样品,未经研磨),表明滤渣中羧基基团占比有所提高。前人对生物吸附剂Cd吸附能力的研究发现,分子量较大、芳构化程度高的组分富含羧基,在吸附、钝化Cd中起到了积极作用[30]。此外,腐殖酸羧基可提供电子与Cd2+发生配位作用生成Cd络合物[1,14]。因此,腐殖酸残渣单位羧基含量的提高可强化腐殖酸吸附Cd的能力。

图3 腐殖酸颗粒电镜扫描图像Fig.3 Scanning electron microscope images of humic acid particles
红外光谱中,3 500~3 200 cm-1代表了酚羟基基团。分析表明,G4样品的腐殖酸溶液中,该区域的峰面积(酚羟基含量)大于CK。说明研磨处理后,随着腐殖酸样品粒径减小,腐殖酸溶液中酚羟基含量逐渐增加,羧基含量逐渐降低(表3;图5,横线为基线,B图为A图局部放大)。
综上,结合测定结果,研磨后的腐殖酸可溶与不溶组分对Cd的作用都得到了加强。腐殖酸不溶组分的分子量较大、芳构化程度高,从而形成了不溶性的络合物,固定了土壤中的镉;而腐殖酸可溶部分作为可溶性有机物,形成溶解性Cd,促进土壤镉的活化[7]。
2.4 相关性分析
相关分析表明,土壤有效态Cd与溶液羧基和酚羟基含量成正相关(表4),且与酚羟基的相关系数大于羧基,表明溶液中酚羟基对Cd的螯合能力大于羧基。与之相反,土壤有效态Cd与滤渣中的羧基和酚羟基含量成负相关,且与羧基的相关程度高于酚羟基,表明滤渣中的羧基对Cd的螯合能力大于酚羟基。

图4 CK与G4滤渣的腐殖酸红外光谱图Fig.4 Infrared spectrogram of humic acid from residue parts of CK and G4

图5 CK与G4溶液的腐殖酸红外光谱图Fig.5 Infrared spectrogram of humic acid from soluble parts of CK and G4
表3不同样品的腐殖酸基团单位含量
Table3Unit content of humic acid group in different samples mmol·g-1

样品Sample滤渣 Residue fractions羧基Carboxyl酚羟基Phenolic hydroxyl溶液 Soluble fractions羧基Carboxyl酚羟基Phenolic hydroxylG13.1090.2962.7880.443G23.1620.2892.4710.484G33.1990.2442.2500.747G43.3250.1321.4971.351
表4土壤有效态Cd与羧基、酚羟基含量的相关关系
Table4Correlation coefficients between soil available Cd and carboxyl, phenolic hydroxyl

组分Fraction羧基Carboxyl酚羟基Phenolic hydroxyl溶液Soluble fractions0.442∗0.695∗滤渣Residue fractions-0.977∗∗-0.739∗
*和**分别表示相关性达到显著(P<0.05)和极显著(P<0.01)水平。
* and ** represented significant correlation atP<0.05 andP<0.01, respectively.
3 结论
本研究表明,Langmuir吸附模型可较好地拟合腐殖酸对Cd的吸附。将腐殖酸样品研磨后,去除腐殖酸的可溶组分,剩余的残渣施入土壤进一步提高了土壤的有机质含量,降低了土壤的pH和有效态Cd含量。研磨减小了腐殖酸的粒径,提高了腐殖酸的溶解率,研磨后腐殖酸残渣对Cd的吸附能力及饱和吸附量均高于原腐殖酸样品。这可能与研磨后的腐殖酸残渣比表面积增大、羧基基团含量提高有关。研磨后的腐殖酸溶液对土壤Cd具有活化作用,可能与其酚羟基基团含量增加有关。
