直接催化分解氧化亚氮的金属氧化物催化剂研究进展
2021-06-17刘久欣王新承李翠清宋永吉
刘久欣,王新承,李翠清,王 虹,宋永吉
(1. 北京工业大学 环境与生命学部,北京 100124;2. 北京石油化工学院 化学工程学院燃料清洁化及高效催化减排技术北京市重点实验室,北京 102617)
氧化亚氮(N2O),无色、有甜味,具有轻微的麻醉效果,吸入会使人发笑,故又称笑气。长期以来未发现对人体产生危害,广泛应用于医学、汽车、航天等领域[1-2]。但近年来研究发现,N2O严重消耗臭氧层物质,引起温室效应等一系列环境问题,因此在1997年签订的《京都议定书》中被列为六大温室气体之一,其全球变暖潜能值(GWP)是CO2的310倍[3-4]。N2O主要来自于自然界和人类生产活动的排放,其中人为排放的N2O主要来自硝酸及己二酸生产、汽车发动机尾气排放以及化石燃料和生物质的燃烧等[5-6]。据估算,人类每年向大气排放的N2O为(5~7)×106t,约占总排放量的30%~40%[7]。在2014年的联合国政府间气候变化专门委员会(IPCC)发布的第五次评估报告中指出,大气中的N2O质量浓度比工业化前水平超过20%,已达到3.24×10-7mg/m3,并且每年仍以0.3%左右的速率增加,因此N2O的减排已刻不容缓。
N2O减排的主要方法有高温热分解法、(非)选择性催化还原法和直接催化分解法等。其中直接催化分解法是在催化剂的作用下将N2O直接分解为N2和O2,操作简便,无二次污染,是目前应用最广的N2O减排方法[8-9]。用于N2O直接催化分解的催化剂主要包括负载型贵金属催化剂、分子筛催化剂、半导体光催化剂以及金属氧化物催化剂[10-11]。其中金属氧化物催化剂不仅成本低、热稳定性好,而且具有优异的氧化还原性能和较高的N2O催化分解活性,是目前最具有发展前景的一类催化剂,因此国内外学者对金属氧化物催化剂直接催化分解N2O进行了大量研究,并取得了很大的进展。
本文介绍和总结了各类金属氧化物催化剂(单组分金属氧化物、尖晶石型氧化物、类水滑石氧化物、(类)钙钛矿型氧化物、负载型金属氧化物等)的结构特点及其催化分解N2O的性能,为后续直接催化分解N2O的金属氧化物催化剂的研究提供思路。
1 单组分金属氧化物催化剂
单组分金属氧化物主要包括过渡金属氧化物(Fe2O3、NiO、Co3O4、CuO等)、稀土金属氧化物(La2O3、CeO2等)和碱土金属氧化物(CaO、BaO、MgO等),通常由金属硝酸盐热分解和沉淀法制备,制备方法十分简便[12]。研究者们很早便开始了对单组分金属氧化物催化剂的研究,表 1总结了近几年部分单组分金属氧化物催化剂对N2O的催化性能。

表 1 部分单组分金属氧化物对N2O的催化性能
OHNISHI等[13]测试了沉淀法制备的各单组分金属氧化物在有氧条件下的N2O分解活性,其催化活性的大小顺序为:NiO > Co3O4> CuO > MnO2≈ MgO > Fe3O4> Al2O3≈ CeO2≈ Cr2O3;同时研究发现,NiO的催化活性受制备条件的影响较小,而Co3O4与之相反。MA等[14]测试了以介孔SiO2为硬模板制备的一系列具有介孔结构的单组分金属氧化物催化剂在无氧条件下的N2O分解活性,并与商业单组分金属氧化物进行比较,其中介孔Co3O4、介孔CuO、介孔MnO2、介孔Mn2O3、介孔Mn3O4和介孔NiO的N2O分解活性高于它们的商业对应物,同时发现,介孔Co3O4的孔径和壁厚会影响其催化活性。CHROMCAKOVA等[15]采用不同沉淀剂(NH3·H2O,NaOH,Na2CO3)和反应条件(OH--Co摩尔比、老化时间)制备了一系列Co3O4催化剂前驱体,研究发现不同沉淀剂和初始OH--Co摩尔比制备的前驱体显示出不同的相组成,但在500 ℃空气条件下焙烧后的产物均为尖晶石型Co3O4,其中以Na2CO3为沉淀剂制备的Co3O4的催化活性最高,由此可见制备方法的不同会影响前驱体结构进而影响催化分解N2O的活性。因此,对于单组分金属氧化物催化剂来说,在不同制备方法和反应条件下,NiO和Co3O4较其他单组分金属氧化物催化剂具有更高的N2O催化分解活性,是N2O分解过程中最活跃的单组分金属氧化物催化剂,其中Co3O4的催化活性受制备条件的影响较大。
单组分金属氧化物的结构组成比较简单,因此适用于N2O催化分解反应机理的研究。KARLSEN等[17-18]探究了不同比表面积的CaO对催化分解N2O性能的影响,研究发现CaO的高不饱和位点极为活跃,但易受O2的毒害,而中等和低不饱和位点则是N2O分解活性持续稳定的原因,因此可以推断氧化物的结构会影响其催化分解N2O的性能。此外,随着DFT理论的应用,对N2O催化反应机理的研究更加深入。PISKORZ等[19]采用DFT分子模拟方法研究了N2O在钴尖晶石(100)表面分解的主要机理,结果发现,N2O活化和表面O原子复合是反应的关键步骤。而对于氧转移路线,反应基本上受到N—O键断裂的高活化能的限制,氧中间体的表面扩散是通过阳离子和阴离子位点之间的连续跳跃而发生的。同时观察到水和氧中毒主要与共吸附物种的位阻效应有关。WU等[20]研究了CaO对N2O分解及其分解产物的选择性的影响,结果表明,CaO可以催化N2O的分解,并且N2的选择性比NO高,CaO催化N2O分解的N2/NO产物体积浓度比在947 ℃时达到最小值12.1。他们还利用DFT计算研究了CaO(100)表面N2O分解的N2和NO路线,发现由于能量势垒相对较低,且缺乏自发的NO生成路径,N2O分解生成N2的可能性大于NO生成路径。
综上可见,单组分金属氧化物虽然制备方法简单,但由于结构单一、比表面积较低,其催化分解N2O活性较差,而且对水蒸气和O2的抗性也较差,不适用于工业应用,主要用于催化机理研究。
2 复合金属氧化物催化剂
相较于单组分金属氧化物,复合金属氧化物对N2O的催化分解有相互促进作用,甚至部分复合金属氧化物的催化性能可以与贵金属催化剂相媲美,是目前金属氧化物催化剂的主要发展方向。复合金属氧化物催化剂主要包括尖晶石型氧化物(AB2O4)、类水滑石型氧化物、(类)钙钛矿型氧化物(ABO3或A2BO4)、六铝酸盐型氧化物以及负载型金属氧化物[21]。
2.1 尖晶石型氧化物
尖晶石型氧化物的化学式为AB2O4,其中A离子通常是占据四面体位置的二价阳离子,可与4个O2-相邻,形成以A2+为中心的正四面体结构;B离子是在八面体位置中的三价阳离子,可与6个O2-相邻,形成以B3+为中心的正八面体结构;n(A)∶n(B)=1∶2[22]。表 2总结了部分尖晶石型氧化物对N2O的催化性能。
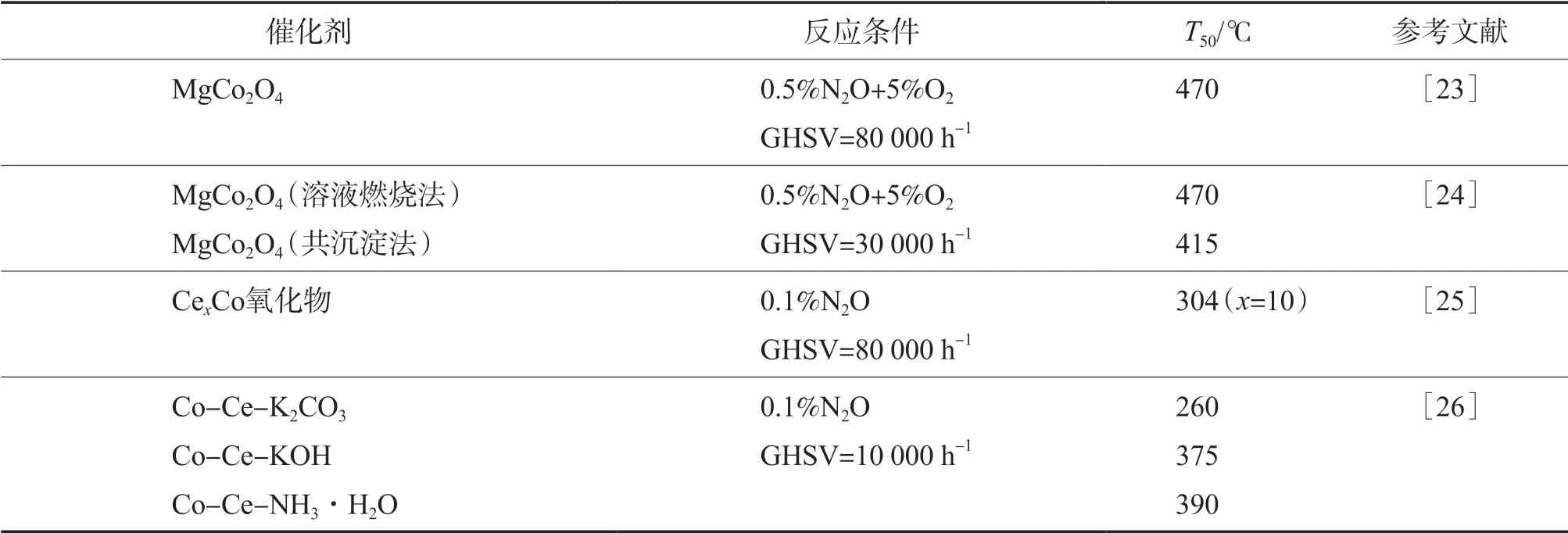
表 2 部分尖晶石型氧化物对N2O的催化性能
RUSSO等[23]通过溶液燃烧法制备了多种AB2O4尖晶石型催化剂,发现B位金属为Co的催化剂具有更好的催化活性,尤其是MgCo2O4,具有更大的形成表面空位的能力,在有O2的条件下T50仍低于500 ℃,由此可见钴基尖晶石具有很高的催化分解N2O的能力。之后ZAMUDIO等[24]采用共沉淀法和溶液燃烧法制备了MgCo2O4尖晶石型催化剂,发现共沉淀法制备的催化剂比表面积更大、分散度更好,在有氧和无氧条件下均具有很高的N2O分解活性。
有研究发现N2O预处理可以改变催化剂的表面性质,使催化剂的分解性能大大提高。YOU等[25]通过共沉淀法合成了一系列CexCo氧化物催化剂来探究经N2O预处理对催化剂分解性能的影响。他们通过H2-TPR和XPS发现,随着预处理温度的升高,CexCo氧化物催化剂表面的吸附氧(O*)也显著增加,原因在于CeO2具有较好的储氧能力,N2O解离产生的O*会沉积在CexCo氧化物的表面,其沉积量与CeO2的掺杂量呈正相关。较高温度下的N2O预处理会导致更多的O*,冷却后残留的O*会与气态N2O在CexCo氧化物上发生实质性的反应,从而提高了CexCo氧化物的分解活性。
催化剂表面活性位上O*的脱附是N2O催化分解反应的控速步骤,因此可在催化剂中加入电子助剂来弱化R—O化学键,使得O*的脱附变得更加容易,从而提高催化剂催化分解N2O的活性。WANG等[26]以K2CO3、KOH和NH3·H2O为沉淀剂制备出Co-Ce复合金属氧化物催化剂,研究发现以K2CO3为沉淀剂制备的催化剂具有更高的比表面积和更小的颗粒尺寸,同时拉曼光谱显示Co和Ce物种之间的相互作用也更强,推测原因是以K2CO3为沉淀剂制备的Co-Ce复合金属氧化物催化剂中残留的K+有利于表面O*的脱附和Co3+的还原,使得催化剂能够在320 ℃时就可将N2O完全催化分解。
在尖晶石型氧化物中,Co基尖晶石由于拥有最弱的M—O键,能够在较低温度下形成氧空位,从而具有优越的催化性能,是最具有工业应用前景的金属氧化物催化剂。因此目前针对Co基尖晶石型氧化物催化剂的开发研究较多。
2.2 类水滑石型氧化物
类水滑石型氧化物是由阳离子组成的主体层板和阴离子填充的层间构成的具有层状结构的新型材料,也称为层状双羟基复合氧化物(LDHs),其结构如图1[27]所示。类似于水镁石Mg(OH)2,类水滑石型氧化物的化学组成可以表示为其中M2+通常为Co2+,Mg2+,Cu2+,Ni2+等二价金属阳离子;M3+通常为Fe3+,Al3+,Cr3+等三价金属阳离子;An-通常为Cl-,NO3-,SO42-,CO32-等阴离子或基团[28-29]。表3总结了部分类水滑石型氧化物对N2O的催化性能。
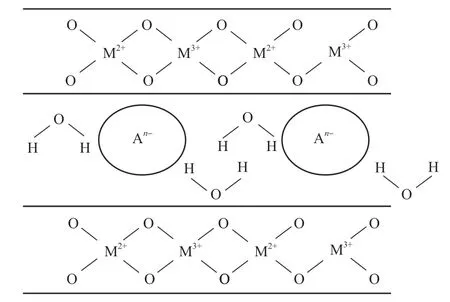
图1 类水滑石型氧化物结构示意

表3 部分类水滑石型氧化物对N2O的催化性能
水热处理对类水滑石催化分解N2O活性有显著影响。KOVANDA等[30]采用共沉淀法制备了Ni-Al摩尔比分别为2,3,4的类水滑石催化剂,考察了水热处理对其催化分解N2O的影响。研究发现水热处理后的催化剂中由于无定形组分的减少及NiO结构中Al阳离子掺杂量的増加,催化剂活性明显提高。
碱金属盐对水滑石类化合物的N2O催化活性具有一定的促进作用。OBALOVA等[31]制备了碱金属(Li,Na,K,Rb,Cs)改性的Co-Mn-Al水滑石,并测试了催化剂在惰性气体中的N2O分解情况。实验结果表明,碱金属对Co4MnAlOx混合氧化物N2O转化率促进作用的大小顺序依次为:Cs>Rb>K>Na=Co4MnAlOx>Li。通过XPS表征发现,向Co4MnAlOx混合氧化物中添加碱助剂会导致活性金属的电子性能和催化剂表面的酸碱功能发生改变,碱金属的促进作用与其电离势、电荷转移到催化剂以及所有催化剂组分(Co,Mn,Al,O)的结合能降低有关。武海鹏等[29]制备了碱金属(Na,K,Cs)改性的Ni-Al、Ni-Co-Al复合氧化物,均有利于提高N2O分解反应的催化活性,其中K的促进作用最明显。对于K的不同前驱物而言,K2CO3、CH3COOK、K2C2O4的加入均能有效提高催化剂的活性,而加入KNO3反而降低了催化剂活性。通过XPS谱图发现,K+的加入弱化了催化剂表面的Co—O、Ni—O化学键,促进了表面氧的脱附,从而提高了催化剂的活性和抗氧抗水性能。
关于过渡金属、稀土金属和碱金属三方面对水滑石类化合物直接分解N2O的协同作用也有相关报道。ZHANG等[32]采用共沉淀法制备了不同组成的Co-M-Al和Co-M-Ce-Al(M=Ni,Cu,Zn)水滑石混合氧化物催化剂,研究发现Co-Ni-Al催化分解N2O的活性最高,并且添加少量CeO2后催化活性得到明显提高,使T50的分解温度降低80 ℃,同时K+掺杂对Co-M-Ce-Al直接分解N2O的催化活性又有一定的促进作用,当K2O负载量为1.5%(w)时催化活性最高,分解温度T50降低约50 ℃。
由此可见,通过对类水滑石型氧化物进行改性,可显著提高催化剂在水蒸气和O2下的活性和稳定性。但该类催化剂高温易烧结,导致比表面积降低,影响其催化性能。
2.3 (类)钙钛矿型氧化物催化剂
钙钛矿型氧化物是一种独特的混合氧化物,其结构如图2[34]所示。类似于天然钙钛矿(CaTiO3),其化学组成可以用ABO3表示,其中A通常为半径较大的稀土金属离子,处于12个O原子组成的十四面体的中央,起稳定结构的作用;B通常为半径较小的过渡金属离子(Ni+、Co2+、Mn2+等),处于6个O原子组成的八面体中央,决定着钙钛矿的性质[35]。表4总结了部分(类)钙钛矿型催化剂对N2O的催化性能。
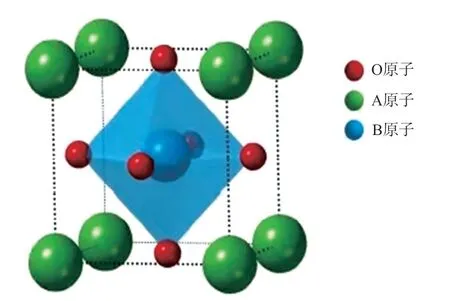
图2 钙钛矿型氧化物结构示意
关于A2BO4型类钙钛矿金属氧化物的报道相对较少,它由钙钛矿层(ABO3)和岩盐层(AO)相互交替构成,可通过调控A、B位的离子价态来改变催化剂的氧化还原性能。PAN等[36]研究发现在相同的操作条件下,3种类钙钛矿型催化剂的N2O分解率依次为La2NiO4>LaSrNiO4>La0.7Ce0.3SrNiO4。O2-TPD表征结果表明:La2NiO4的β氧解吸峰位于790 ℃,说明La2NiO4在790 ℃以下不易解吸,因此其活性中心不能再生,使用寿命较短;而LaSrNiO4和La0.7Ce0.3SrNiO4的β氧解吸峰明显位于较低的温度,这意味着LaSrNiO4和La0.7Ce0.3SrNiO4具有较好的氧迁移率,并且很容易从晶格中吸附氧;同时,La0.7Ce0.3SrNiO4对氧和水蒸气有较好的耐受性。
RUSSO等[37]通过溶液燃烧法制备了4种LaBO3(B=Cr,Mn,Fe,Co)钙钛矿催化剂,其中LaCoO3催化剂在N2O分解中表现出最佳的活性,在有O2的条件下,即使在相对较低的温度下仍具有较大的还原能力。之后DACQUIN等[38]采用反应研磨法、溶胶-凝胶法和模板法制备了LaCoO3钙钛矿催化剂,以此探究制备方法对LaCoO3钙钛矿催化剂催化N2O分解性能的影响,结果显示,反应研磨法制备的LaCoO3催化剂氧空位密度和比表面积最大,具有最高的N2O催化分解活性。
改变A、B位离子或对A、B位离子进行掺杂也可获得催化性能更加优良的钙钛矿型复合氧化物。KUMAR等[39]通过共沉淀-浸渍法制备了A位取代的Pr1−xBaxMnO3钙钛矿型催化剂,研究发现Ba取代提高了PrMnO3催化分解N2O的活性,最佳取代量为20%,在544 ℃下就能够将N2O完全分解。通过XPS、O2-TPD和H2-TPR表征发现,Ba取代提高了PrMnO3催化剂中Mn4+与Mn3+的比例,改善了PrMnO3的氧化还原性能。HUANG等[42]采用溶胶-凝胶法制备了一系列BaFe1-xSnxO3-δ催化剂,研究B位取代对钙钛矿型催化剂的影响。实验结果表明,随着Sn掺杂量的增加,催化剂中活性中心Fe3+—O5数量占比由原来的30%增加到68%,同时由于Fe—O—Sn结构的形成,使Fe—O键相互作用减弱,催化剂的氧迁移率大大提高,N2O活化能由241 kJ/mol降低至178 kJ/mol,同时与BaFeO3-δ催化剂相比,本征反应速率增加了近4倍。
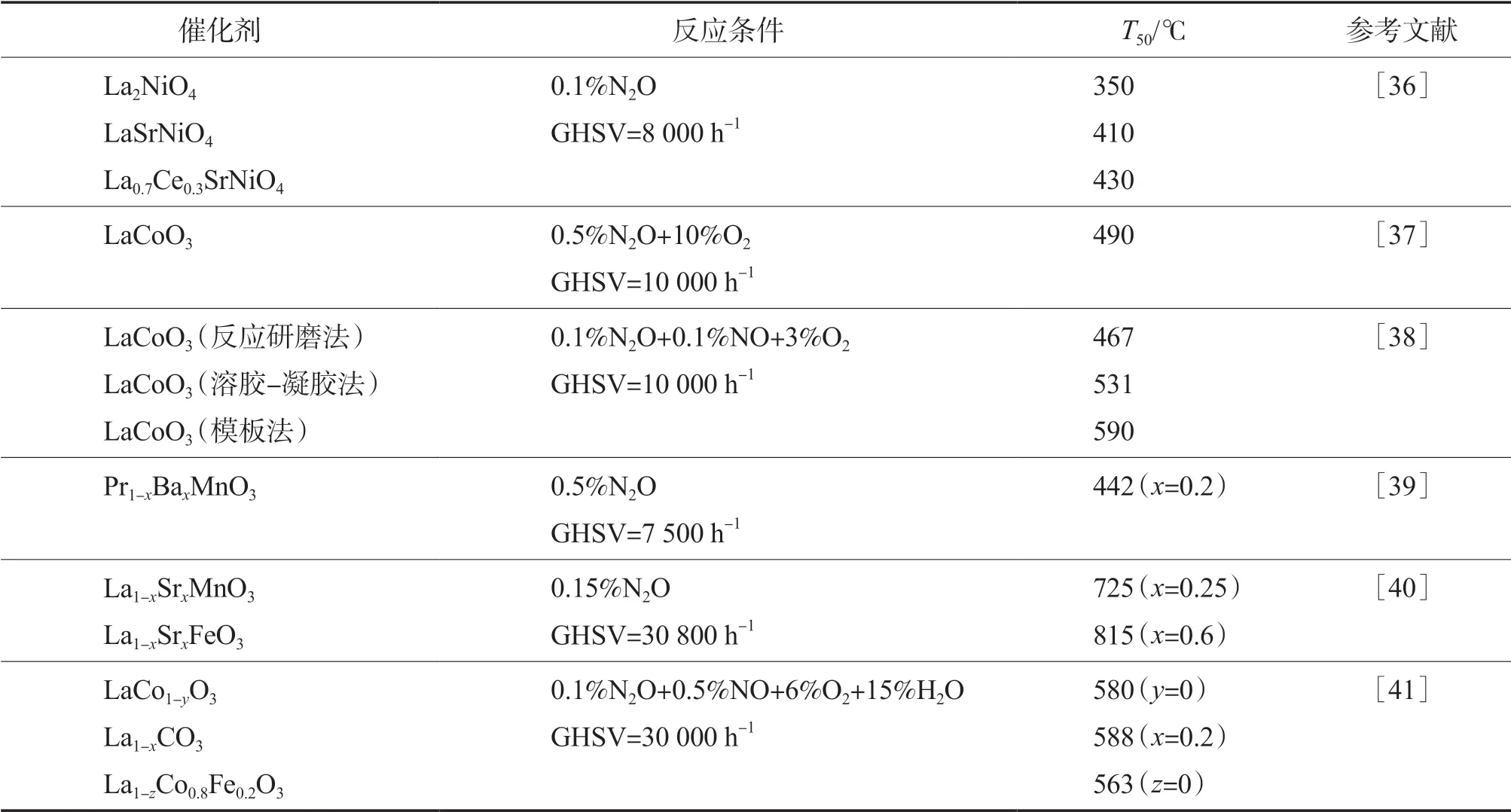
表4 部分(类)钙钛矿型催化剂对N2O的性能
通过对(类)钙钛矿型氧化物的A、B位离子的部分掺杂和替换,可以制备出具有不同氧化还原能力的材料,能够进一步提高其应用范围,这有助于实际应用的发展。
2.4 六铝酸盐型
六铝酸盐的化学式为AAl12O19,是由互成镜像的尖晶石结构单元和镜面交替堆积而成的具有六方层状结构的晶体,其中A是碱金属(K、Na等)、碱土金属(Ca、Mg、Ba等)或稀土金属(Pr、La、Nd等)等阳离子[43]。根据阳离子的离子半径和电荷的不同,六铝酸盐的晶体结构可分为β-Al2O3和磁铅石(MP)两种类型,如图3所示。晶格中的Al3+还可以被其他过渡金属离子部分或全部取代,从而达到活性组分镶嵌而骨架结构不变的目的。表 5总结了近几年部分六铝酸盐型催化剂的催化性能。
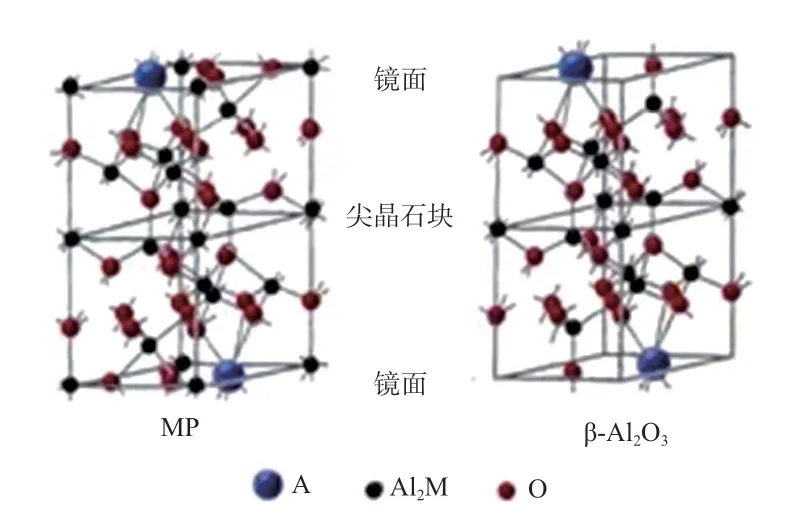
图 3 六铝酸盐结构示意
六铝酸盐型催化剂的活性基本不受结构中A阳离子的影响,因此研究者们更多关注B位取代对其催化分解N2O性能的影响。ZHANG等[44]通过共沉淀法制备了Fe3+取代的LaFexAl12-xO19六铝酸盐型催化剂,研究发现随着Fe3+浓度的增加,导致LaFeO3中间相的形成,LaFeO3中间相的八面体位置的Fe3+会优先容纳在镧六铝酸盐的镜面八面体Al(3)位置,催化剂的活性与该位点上Fe3+的占据率成正比。同时与以相同方法制备的具有相同Fe含量的钡六铝酸盐相比,Fe取代的镧六铝酸盐催化剂在500 ℃下表现出更高的N2O分解活性。

表 5 部分六铝酸盐型催化剂对N2O的性能
过渡金属取代的六铝酸盐催化剂只有在高于500 ℃的温度下才具有活性。在不影响催化性能的前提下,将贵金属加入到骨架中可以提高六铝酸盐型催化剂的活性。AMROUSSE等[45]首次制备了一种新型的Rh取代六铝酸盐催化剂BaRhxMn1−xAl11O19并用于N2O分解反应。实验结果表明,当Rh含量为x=0.3时,N2O在250 ℃时就已经开始分解,并在1 200 ℃的绝热温度下保持稳定性。经过4个反应周期后,由于沉积在骨架外的Rh部分氧化成Rh2O3,活性仅略有下降,表现出良好的可重复性。ZHU等[46]采用沉淀法成功合成了Ir取代的六铝酸盐用于催化分解高浓度N2O。研究发现只有少量Ir通过取代Al3+进入到六铝酸盐晶格中,使催化剂表现出高活性,大多数Ir物种以IrO2相存在,活性较低且高温容易烧结。Fe本身对N2O没有分解活性,但它促进了六铝酸盐的形成和Ir元素在六铝酸盐骨架中的结合。同时比较了BaIrxFe1-xAl11O19(IBFA)与Ir/Al2O3的催化性能,发现BaIrxFe1-xAl11O19在高温条件下比Ir/Al2O3具有更高的活性和稳定性。
由此可见,六铝酸盐型催化剂具有优异的抗烧结性能和抗热震性,同时在高温条件下仍具有较大的比表面积,是一种很好的高温热稳定材料,因此是最有前途的高温N2O分解催化剂,可应用于航天推进级N2O的催化分解。
2.5 负载型金属氧化物
将单组分金属氧化物负载到高比表面积的载体上,通过两者之间的相互作用能够显著提高催化剂的活性和稳定性,有利于催化剂的实际应用。常用的载体有:Al2O3、TiO2、CeO2、ZrO2、活性炭、分子筛等。
表6总结了部分负载型金属氧化物对N2O的催化性能。
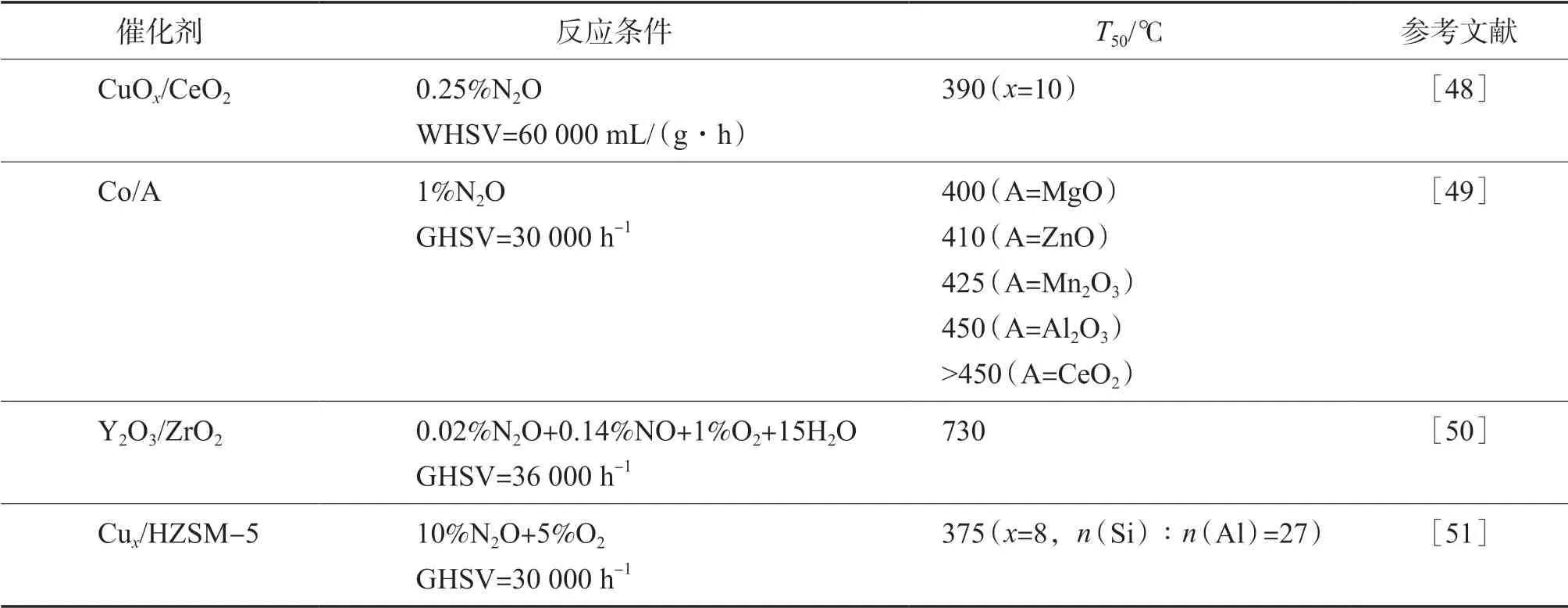
表 6 部分负载型催化剂对N2O的催化性能
GRZYBEK等[48]探究了不同类型的氧化铝载体(α-Al2O3,γ-Al2O3,θ-Al2O3,δ-Al2O3)对Co3O4催化分解N2O性能的影响,发现以α-Al2O3为载体时,催化剂的活性最高,且对H2O、O2和NO等杂质气体具有很好的耐受性,是制备钴基尖晶石催化剂时的良好载体,同时为开发基于钴尖晶石及其衍生物的低温N2O分解催化剂的实践提供了参考。赵丹等[49]制备了分别负载有K、Fe、Cu、Mg、Sr氧化物的活性炭纤维催化剂(M/ACF),并应用于N2O分解反应中。实验结果显示K2O/ACF催化剂具有最高的N2O分解活性,可在350 ℃时将N2O完全分解,其中K2O在低温下对N2O的分解有重要影响,起主要的活性作用。
CeO2通过Ce4+/Ce3+的氧化还原循环具有很高的储氧释放能力,与过渡金属的相互作用,能够提高氧化还原能力并提高催化性能,因此以CeO2为载体的负载型金属氧化物得到了广泛研究。ZABILSKIY等[50]通过浸渍法将铜负载到水热法合成的具有高比表面积的CeO2载体上。研究发现,负载量为10%(w)时,CuO/CeO2催化剂催化分解N2O的活性最好,在水蒸气或NO环境中会抑制催化剂活性,使完全分解温度上升65 ℃和10 ℃。此外以分子筛(ZSM系列、MCM系列、SBA系列、Hβ、MOR、FER等)为载体近几年来引起了广泛关注,尤其ZSM-5因较好的低温活性得到较多研究。徐庆生等[51]制备了负载型N2O直接分解催化剂Cu/HZSM-5,研究发现等体积浸渍法制备的催化剂活性优于离子交换法,且硅铝比越低催化活性越好,具有良好的水热稳定性。在寿命实验中,连续反应100 h,催化活性仍未降低。
3 结语
随着温室效应不断加剧,N2O的减排对控制全球变暖具有重要意义。纯金属氧化物因组成单一,催化性能较差,不适于N2O工业减排,但在经过组成、结构的调节后的复合金属氧化物,催化性能得到了明显改善,热稳定性有所提高,应用范围不断扩大。因此,复合金属氧化物是目前金属氧化物的主要研究方向,其中尖晶石型氧化物以优异的催化性能得到广泛的研究,六铝酸盐型氧化物是最有希望的高温N2O分解催化剂。
工业尾气通常除N2O外还含有O2、H2O、SO2和NOx等杂质气体,对金属氧化物催化剂活性具有一定的毒害作用,因此需要深入研究毒害机理,提高催化剂的抗毒能力。同时仍需要积极开发新型催化剂,例如氧化物气凝胶被广泛应用于吸附、催化等领域,但未有关于催化分解N2O的相关报道,值得后期进行相关研究。
