糖基化改性大豆蛋白溶解特性
2021-06-10卢亚东梁亚萍王愈陈振家
卢亚东,梁亚萍,王愈,陈振家
1. 山西农业大学食品科学与工程学院(晋中 030801);2. 山西农业大学校医院(晋中 030801)
大豆中蛋白质含量较高而且营养丰富,其蛋白质含量约为38%,是谷类的4~5倍,除糖类较低外,其他营养成分,如脂肪、钙、磷、铁和维生素B1、B2等人体必需的营养物质都明显高于谷类和薯类食物[1]。大豆蛋白含有8种人体必需氨基酸,且比例比较合理,只是赖氨酸含量相对稍高,而蛋氨酸和半胱氨酸含量较低[2]。大豆蛋白是一种重要的蛋白资源,特别是大豆分离蛋白,含蛋白质90%以上,是一种优良的食品原料[3]。用于大豆分离蛋白改性的方法很多,通过物理法、化学法或生物酶法可对大豆蛋白进行改性,经改性后的大豆蛋白功能特性得到改善,常用的是化学法,主要有酸作用、磷酸化、酯化、酰化和糖基化等。其中,糖基化修饰由于其具有自发进行,无需添加化学试剂,加热即可加速反应等优点而成为一种较为理想的改性方法[4]。试验的大豆蛋白糖基化改性是利用大豆蛋白自身糖分,使其氨基酸与多羟基化合物葡萄糖在碱性环境中发生美拉德反应(羰氨反应),生成葡萄糖-大豆分离蛋白复合物,促使蛋白结构和功能发生变化,提升大豆蛋白功能特性与营养价值[5-7]。
1 材料与方法
1.1 试验材料
1.1.1 试验原料
脱脂豆粕:山东山松生物制品有限公司(蛋白质≥51%)。
1.1.2 主要试剂
石油醚、无水乙醇、甲醇、氢氧化钠、氯化钠、盐酸、浓硫酸(均为分析纯,天津市凯通化学试剂有限公司);考马斯亮蓝G250、SDS、β-巯基乙醇、溴酚蓝、甲叉双丙烯酰胺、四甲基乙二胺、过硫酸铵、氢氧化钾、甘油、低分子量蛋白质Marker(北京索莱宝科技有限公司)。
1.1.3 试验仪器与设备
DYY-7C型电泳仪(北京市六一仪器厂);723可见分光光度计(上海菁华科技有限仪器公司);HH系列数显恒温水浴锅(金坛市科析仪器有限公司);RE-52AA旋转蒸发器(上海亚荣生化仪器厂);SHZ-III循环水真空泵(上海亚荣生化仪器厂);TS-2000多用脱色摇床(海门市其林贝尔仪器制造有限公司);HC-2064高速离心机(安徽中科中佳科学仪器有限公司)。
1.2 试验方法
1.2.1 大豆分离蛋白的提取
采用碱提酸沉法将脱脂大豆内的蛋白质溶解在稀碱溶液中,50 ℃恒温搅拌2 h,离心除去豆粕中的不溶物,用酸将大豆蛋白提取液的pH调至等电点,使大豆蛋白沉淀析出,再经分离水洗,回调pH至中性,冷冻干燥备用[2,8-9]。
1.2.2 糖基化改性大豆蛋白
采用碱提酸沉法将脱脂大豆内的蛋白质溶解在稀碱溶液中,50 ℃恒温搅拌2 h,离心除去豆粕中的不溶物,用酸将大豆蛋白提取液的pH调至等电点,使大豆蛋白沉淀析出,经分离水洗,按一定比例加入5%的葡萄糖,置于95 ℃水浴搅拌,反应一段时间后水浴冷却,调节pH至等电点,回调pH至中性,冷冻干燥备用[5]。
1.2.3 不同温度下的溶解度
配制1%蛋白溶液搅拌均匀后,于不同温度梯度(50,60,70,80,90和100 ℃)恒温水浴下加热1 h,调节至pH 7,取1 mL样液,离心后取上清液,采用考马斯亮蓝法测定上清液中蛋白浓度。
1.2.4 不同pH下的溶解度
配制1%蛋白溶液搅拌均匀后,调节pH(2,3,4,4.5,5,6,7,8,9,10,11和12),于不同梯度下取1 mL样液,离心后取上清液,采用考马斯亮蓝法测定上清液中蛋白浓度。
1.2.5 不同离子强度下的溶解度
配制1%的蛋白溶液搅拌均匀后,称取氯化钠以配备不同浓度(0.01,0.05,0.10,0.20,0.30,0.40,0.50,0.60,0.70,0.80,0.90和1.00 mol/L)的盐离子溶液,各取1 mL样液,离心后取上清液,采用考马斯亮蓝法测定上清液中蛋白浓度。
1.2.6 SDS-PAGE电泳
依照Laemmli[10]的方法。浓缩胶质量分数5%,分离胶质量分数12%,样品上样量5 μL。恒压电泳,电流16 mA,浓缩胶电压100 V,分离胶电压150 V。电泳结束后,电泳胶片先固定3 h后,染色,脱色结束后,用成像仪进行成像。
2 结果与分析
2.1 糖基化改性前后大豆蛋白的溶解度
2.1.1 温度对改性前后大豆蛋白溶解度的影响
由图1可知,温度70~90 ℃之间,未改性的大豆蛋白溶解度下降明显,这是由于热动能的增加破坏蛋白质分子内氢键,导致蛋白质结构的展开(变性),蛋白质内部的疏水基团暴露,促使蛋白质聚集沉淀。
90~100 ℃溶解性增加,可能是因为温度过高导致蛋白亚基和展开的肽链结构发生折叠,使上清液中的蛋白浓度略有增大[11-12]。
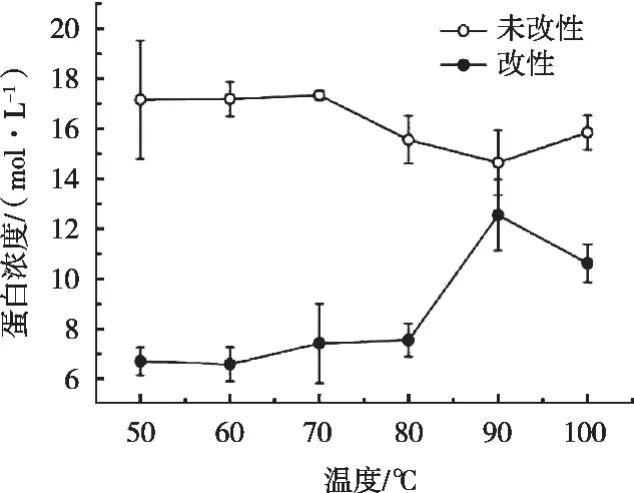
图1 温度对改性前后大豆蛋白溶解度的影响
糖基化改性大豆蛋白在50~90 ℃溶解性增加,80~90 ℃尤为明显。这是由于糖基化反应在大豆蛋白表面接枝糖分子并引入亲水性羟基,大豆蛋白与水分子之间的作用增强,且接枝的糖分子使蛋白质的空间结构增大并趋于稳定,阻碍蛋白质分子聚集,从而增大蛋白质的溶解度[12-14]。90~100 ℃溶解度降低,是由于糖基化使大豆蛋白部分分子结构得以展开,蛋白质分子内部的疏水基团暴露,使其数量增加,分子间的疏水作用增强,导致蛋白质分子相互聚集沉淀从而使溶解性降低[13]。
2.1.2 pH对改性前后大豆蛋白溶解度的影响
由图2可知,大豆分离蛋白的溶解度和溶液pH的变化有密切关系,成明显的U字型结构。pH在4.3等电点附近时大豆蛋白的溶解性最低,pH 2~4.3蛋白溶解度随pH升高而降低,pH 4.3~12之间蛋白溶解度随pH升高而升高,pH 12时达到最大。因为大豆蛋白分子含有氨基和羟基,是两性分子。在酸性介质中,蛋白质分子主要以正离子状态存在,电荷相互排斥,分子分散性好,溶解度较高;随着pH升高,蛋白质所带电荷被中和,由电荷引起的各残基之间的静电排斥力消失,蛋白质分子便紧密地排列在一起,降低与水分子的结合能力,此时蛋白质最不稳定;随着pH继续升高,大豆蛋白变为负离子,电荷相互排斥,溶解度升高[15]。

图2 pH对改性前后大豆蛋白溶解度的影响
改性后的大豆蛋白在等电点附近的溶解度略微高于未改性的大豆蛋白,但在其余两侧溶解性比未改性的大豆蛋白低。这是因为糖分子的还原末端与大豆蛋白的自由氨基发生反应,减少了大豆蛋白所带的正电荷,相对增加其所带的负电荷,使其在等电点处溶解性增强。
糖基化修饰使大豆蛋白在等电点区域具有了更好的亲水性,在等电点附近有较高的溶解度,这在食品加工中有很重要的应用。在偏离等电点的范围,糖基化改性大豆蛋白的溶解性表现出降低趋势。
2.1.3 离子强度对改性前后大豆蛋白溶解度的影响
由图3可知,离子强度0.01~0.05 mol/L时,未改性大豆蛋白溶解度降低,因为蛋白质溶液净电荷量增加,因此带上较厚的水化胶层导致大豆蛋白的溶解性下降;离子强度0.05~0.5 mol/L时,溶解度升高,是由于盐离子结合亲水基,增加蛋白质分子表面的电荷,从而增强蛋白质分子与水分子的作用,使蛋白质溶解度增大,这种现象称为盐溶;离子强度0.5~1.0 mol/L时,溶解度降低,是由于高浓度中性盐,破坏蛋白质的水化层和电荷,从而使蛋白质沉淀,这种现象称为盐析[16]。
改性后大豆蛋白在离子强度大于0.3 mol/L范围内溶解度不断升高,这是由于蛋白与糖分子的结合比较紧密,蛋白质基本不受高盐的影响。

图3 离子强度对改性前后大豆蛋白溶解性的影响
2.2 糖基化改性大豆蛋白组分SDS-PAGE分析
2.2.1 温度变化
由图4可知,非还原电泳图谱中浓缩胶顶端颜色较深条带在还原电泳中消失,而非还原电泳图谱中条带颜色很浅的B亚基和A3亚基在还原电泳中颜色变深,说明不同温度下糖基化大豆蛋白的B亚基和A3亚基通过分子间或分子内二硫键形成分子质量较大的可溶性聚集体。随着温度升高,浓缩胶顶端条带颜色加深,说明温度升高加剧B亚基的聚集。随着温度升高,糖基化大豆蛋白的非还原电泳图谱变化不大,而还原电泳图谱中分离胶顶端的条带颜色在100 ℃明显变浅,结合图1数据,说明这部分大分子亚基在温度从90 ℃到100 ℃的过程中变为不溶性聚集体,导致糖基化大豆蛋白溶解度出现大幅下降的结果[17]。

图4 糖基化改性大豆蛋白非还原(N)和还原(R)电泳图谱
2.2.2 pH变化
由图5可知,非还原电泳图谱中,等电点附近几乎没有条带,而在还原电泳图谱中虽能辨识α、A和B亚基,但颜色非常浅,与图2结果相符。非还原和还原电泳图谱中,pH 2的亚基条带中β亚基缺失,说明在酸性条件下β亚基的溶解性差。此外,非还原电泳图谱中随着等电点右侧pH升高,B亚基条带的颜色逐渐加深,说明碱性增强有助于B亚基聚集体二硫键的断裂。还原电泳图谱中,等电点右侧不同pH的亚基分布相似,说明随着pH升高,所有亚基的溶解度均有升高。

图5 糖基化改性大豆蛋白非还原(N)和还原(R)电泳图谱
2.2.3 离子强度变化
图6可知,对比温度条件和pH条件,非还原电泳图谱中浓缩胶顶端条带消失,说明离子强度增加导致这部分亚基发生聚集变为不可溶性聚集体。随离子强度增加,还原电泳图谱中分离胶顶端的亚基条带和B亚基逐渐消失又逐渐恢复,对照图3的结果分析可知,随着离子强度增加,分离胶顶端的亚基条带和B亚基的溶解度呈现先下降后上升趋势,这是造成糖基化大豆蛋白溶解度变化的主要原因。

图6 糖基化改性大豆蛋白非还原(N)和还原(R)电泳图谱
3 结论
糖基化改性大豆蛋白随着温度的升高呈现先增大后减小的趋势,在90 ℃达到最高;随着pH增大呈现先减小后增大趋势,pH在4.3等电点附近时大豆蛋白的溶解性最低;随着盐离子浓度增加,其溶解性先增大后减小再增大。SDS-PAGE结果表明,不同温度下糖基化大豆蛋白的B亚基和A3亚基通过分子间或分子内二硫键形成分子质量较大的可溶性聚集体,加入β-ME后,部分大分子亚基形成不溶性聚集体;酸性条件下糖基化大豆蛋白表现出β亚基的缺失,而碱性条件下则有利于B亚基聚集体二硫键的断裂从而提高溶解度;随着离子强度增加,糖基化大豆蛋白B亚基的溶解度呈现先下降后上升趋势。
