肠系膜上动脉栓塞的发生及预后危险因素分析
2021-06-08张树荣
肖 艳,张树荣
肠系膜上动脉栓塞(superior mesenteric artery embolism,SMAE)是急性肠系膜缺血的主要原因,近年来其发病率有上升趋势,但总体患病率仍处于较低水平,在急腹症占比不足1%,但其病死率却超过50%[1]。SMAE由于其临床表现、实验室资料缺少特征性,不易确诊,加之本病起病急、病情进展迅速,导致病死率较高。为提高临床医师对该病的认识,本研究对42例SMAE患者的临床资料进行回顾性分析,探讨影响SMAE发生及预后的危险因素,为临床诊治、预后评估提供更多依据。
1 资料与方法
1.1 研究对象 通过电子病历系统,收集某三甲医院2015年9月~2020年11月所有确诊为SMAE的患者共61例,经筛选后共42例纳入研究组,其中男性27例(64.3%),女性15例(35.7%),平均年龄(65.8±13.7)岁,6例为入院后行剖腹探查术确诊,其余36例为血管CT检查确诊。排除标准为:(1)因外伤所致的SMAE;(2)癌栓阻塞导致的SMAE;(3)肠系膜上动脉夹层动脉栓塞;(4)住院资料不全,未完成治疗自动出院病例。随机选取同期在该院住院诊断为慢性胃炎患者42例作为对照组,其中男性27例(64.3%),女性15例(35.7%),平均年龄(65.2±9.1)岁。研究组与对照组性别、年龄比较差异无统计学意义(P>0.05)。按照治疗结局,将研究组分为好转组与死亡组,其中好转组32例(76.2%),死亡组10例(23.8%)。
1.2 研究方法
1.2.1 资料收集 (1)病人基本情况,包括性别、年龄及烟酒史;(2)既往病史,包括高血压病、糖尿病、心脏疾病、房颤、动脉栓塞、腹部手术史等;(3)主要临床症状,如腹痛、恶心、呕吐、便血等;(4)实验室资料为患者入院后首次静脉血检测结果,包括血常规、血生化、血脂、凝血常规、肝肾功能等指标;(5)影像学检查包括腹部超声、CT及血管CT,外周血管超声等;(6)患者治疗方法及结果、住院天数等。
1.2.2 危险因素分析 (1)通过比较研究组与对照组患者基本情况、既往疾病史、血脂等,分析SMAE发生的危险因素;(2)比较好转组与死亡组患者基本情况、既往病史、临床症状、检查资料等,分析影响SMAE预后的危险因素。
1.3 统计学方法 应用SPSS 20.0软件进行数据分析。计数资料以频数和百分率表示,两组间比较采用χ2检验或Fisher精确检验;计量资料符合正态分布以±s表示,采用t检验进行两两比较;非正态分布采用M±Q表示,采用秩和检验;逐步线性回归法筛选变量,二元Logist ic回归进行危险因素分析。P<0.05为差异有统计学意义。
2 结果
2.1 SMAE的危险因素分析
2.1.1 既往史比较 研究组患有高血压病、房颤、动脉栓塞史、腹部手术史及动脉硬化均显著高于对照组(P<0.05),而烟酒史、糖尿病史、冠心病史两组比较差异无统计学意义(表1)。

表1 两分组基本情况、既往史比较[n(%)]
2.1.2 实验室指标比较 研究组纤维蛋白原、D-二聚体显著高于对照组(P<0.05),胆固醇、甘油三酯、低密度脂蛋白均高于对照组,但差异无统计学意义(表2)。

表2 观察组与对照组实验室指标比较
2.1.3 SMAE的危险因素分析 单因素分析显示,有高血压、房颤、栓塞史、动脉硬化、D-二聚体增高、纤维蛋白原增高与发生SMAE呈正相关(P<0.05),腹部手术史0.05<P<0.1(表3)。将单因素分析中P<0.1的7个变量纳入模型进行逐步回归法筛选,后进行多因素分析,结果显示,房颤、栓塞史、腹部手术史、动脉硬化、纤维蛋白原增高与发生SMAE呈正相关(P<0.05,表4)。
2.2 影响SMAE预后的危险因素分析
2.2.1 基本情况比较 死亡组年龄明显高于好转组(P<0.05),性别、吸烟饮酒情况比较差异无统计学意义(表1)。
2.2.2 既往史比较 死亡组存在心脏疾病较好转组多(P<0.05),高血压病、糖尿病、房颤、动脉栓塞史、腹部手术史及动脉硬化比较差异无统计学意义(表1)。
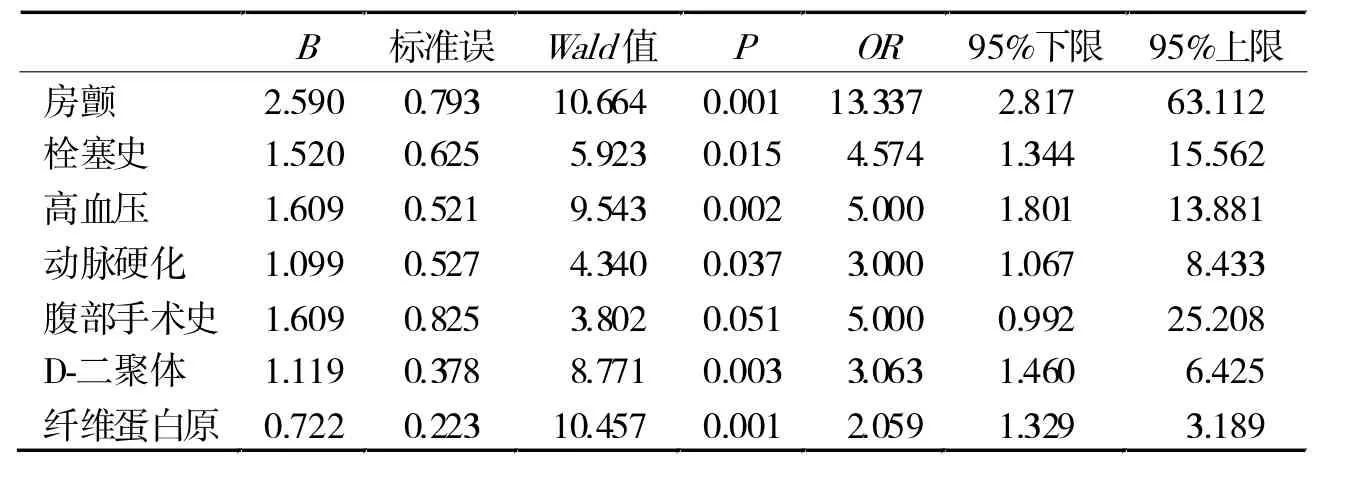
表3 SMAE危险因素单因素Logistic回归分析
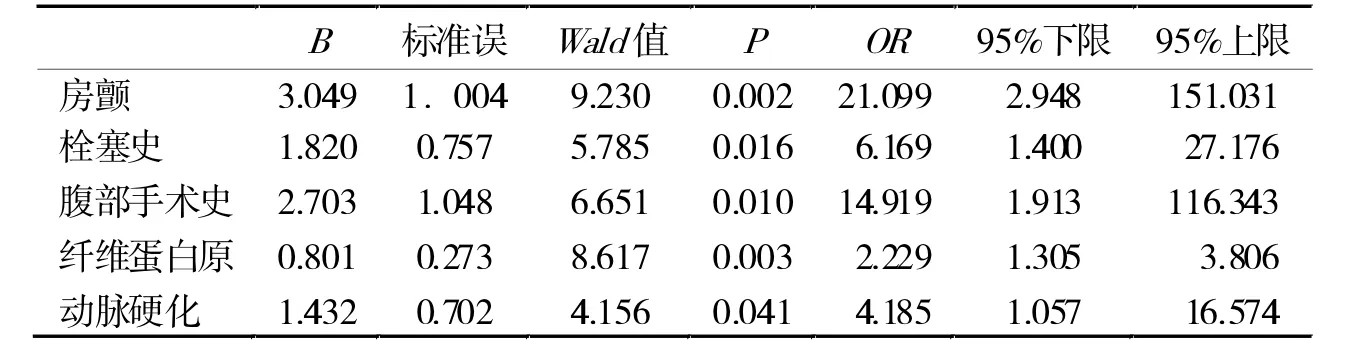
表4 SMAE危险因素多因素Logistic回归分析
2.2.3 症状体征、检查资料及治疗情况比较 两组在便血、肠坏死、腹膜刺激征方面差异无统计学意义。存在多处血管栓塞(栓塞血管≥2处)病例中,死亡组明显高于好转组(P<0.05,表5)。实验室指标比较显示,死亡组尿素氮高于好转组,而血小板明显低于好转组(P<0.05),其余指标差异无统计学意义(表6)。死亡组平均住院天数明显少于好转组(P<0.05),两组治疗方法选择差异无统计学意义(表5)。

表5 死亡组与好转组临床表现及治疗情况比较[n(%)]
2.2.4 影响SMAE预后的危险因素分析 单因素分析示存在心脏疾病、存在多处血管栓塞、年龄与SMAE患者死亡呈正相关,血小板与SMAE患者死亡呈负相关(P<0.05,表7)。将单因素分析中P<0.1变量使用逐步线性回归法筛选,最终多处血管栓塞、血小板纳入模型,多因素分析示血小板与SMAE患者死亡呈负相关(P<0.05),多处血管栓塞与SMAE患者死亡为可疑危险因素(0.05<P<0.1)(表8,图1,表9)。

图1 血小板ROC曲线

表6 死亡组与好转组实验室资料比较

表7 SMAE预后单因素Logistic回归分析

表8 SMAE预后多因素Logistic回归分析

表9 血小板ROC曲线相关指标
3 讨论
肠系膜上动脉主要为大部分空肠和回肠供血,SMAE因肠系膜上动脉血流突然中断,使其供血区域肠管骤然缺血而产生以剧烈腹痛为主的一系列临床急症。本病多发生于老年人,随着年龄的增长,患病率逐渐升高[5]。本病起病急,随着肠缺血时间的延长,发生肠坏死、肠梗阻、腹腔感染甚至脓毒血症的机会也随之增加[2],严重危及患者生命安全。
本研究结果显示房颤、栓塞史、腹部手术史、动脉硬化、纤维蛋白原增高是发生SMAE的危险因素。高水平的纤维蛋白原在凝血初始产生大量纤维蛋白、提高血液黏稠度、增加血小板聚集[3],促进动脉血栓形成。小部分肠系膜上动脉粥样硬化者,随着斑块的逐渐积累,出现管腔突然闭塞,另外动脉粥样硬化斑块脱落可产生栓子,腹部外科手术损伤血管内膜、术后患者制动也可产生血栓,造成栓塞。有研究提出房颤是动脉血栓形成一个重要的原因,大约75%的SMAE患者出现房颤,30%的患者存在栓塞史[4],也有文献指出肠系膜动脉栓塞的危险因素包括房颤、血栓、栓塞史[5],与本研究结果一致。
SMAE患者死亡率较高,本组患者病死率为23.8%。本研究结果显示血小板数量减少、多处血管栓塞、高龄、患有心脏疾病是SMAE患者死亡的危险因素。患有心脏疾病的老年人基础病多、体质弱,对疾病耐受程度及病后恢复不佳,预后往往较差。有学者也提到,60岁以下、无心脏疾病的急性肠系膜缺血患者其生存率相对较高[6]。当伴有肠系膜上动脉以外血管栓塞,尤其是重要器官血管栓塞时,可造成多器官缺血损伤,加重患者病情。血小板通过多种作用机制使整个凝血过程加速2×108倍[7],是机体止、凝血过程中最重要成员之一。然而,近年来越来越多的研究发现,血小板依靠自身携带的各种表面抗体、微粒参与机体多种细胞活动,成为机体炎症免疫反应中重要的一员[8-9]。栓塞性疾病早期血小板消耗多于生成,出现血小板减少,随着机体功能恢复,血小板可逐渐增多至正常。而当机体处于严重感染状态时,过度的炎症反应会抑制血小板生成[10]。低下的血小板水平,在疾病早期会抑制机体炎症反应[8],有数据表明,血小板减少与发生严重感染呈正相关,甚至可能成为独立危险因素[11],血小板数量减少与感染形成一个恶性循环。本研究中SMAE患者血小板数量均减少,死亡组血小板减少程度更是较好转组明显,可见死亡组血小板消耗或破坏过多,生成减少,而较低的血小板水平又加快感染的发生与发展,增加治疗难度,对预后产生不良影响。白奎等[12]也指出,对于严重感染性疾病,血小板减少明显患者预后更差。
虽然SMAE临床患病率较低,但通过详细查阅病史及相关检查检验资料,可以在很大程度上提高本病的确诊率,对于怀疑肠系膜上动脉栓塞的患者,及时完善针对性检查,缩短进入治疗时间,可提高治愈好转率及减少病死率。另外,通过分析患者临床资料,可以预判患者预后。但因本研究病例数偏少,进行危险因素分析时可能不尽全面,在后期的研究中将继续增加样本量,使数据更完善。
