骨组织模型3D 打印建模中CT 图像序列选择的策略分析
2021-06-03李修往吴家昌叶灼峰吴铭杰庄伟达赵仁礼桑宏勋
李修往 吴家昌 叶灼峰 吴铭杰 庄伟达 赵仁礼 桑宏勋* 王 琼
1(南方医科大学深圳医院骨科中心 深圳 518000)
2(中国科学院深圳先进技术研究院 深圳 518055)
1 引 言
3D 打印在医疗领域的应用已成为数字医学发展的一个重要趋势,特别是在骨外科领域的应用越来越普遍。美国食品及药物管理局(FDA)于 2021 年 2 月 17 日宣布批准了 Additive Orthopaedics 公司的个性化 3D 打印距骨植入物用于人道主义用途。其中,特制距骨垫片是世界首个,也是同类首个替代距骨(连接腿和脚的踝关节中的骨骼)的植入物,可用于治疗踝关节缺血性坏死(Avascular Necrosis,AVN)。AVN 是一种严重的进展性疾病,该部位因缺乏血液供应而导致骨组织死亡。采用外科手术治疗晚期 AVN可能导致患者踝关节无法运动,而采用植入物进行治疗则可避免这一副作用。特制距骨垫片是一种 3D 打印的植入物,可用于距骨置换手术中。其中距骨垫片是根据计算机断层扫描(CT)成像为每个患者单独制作的、适合患者的特定解剖结构。置换手术则是将患者的距骨取下并用钴铬合金制成的植入物代替。若患者病情恶化需要融合手术,则使用特制距骨垫片进行距骨置换手术可以使患者的踝关节保留运动能力[1]。
采用 3D 打印技术在术前通过打印患者的等比例骨组织模型可以进行手术方案的精确规划[2];术中通过等比例骨组织模型的观察可以确保手术的定位精准度[3],从而缩短手术时间,减少病人出血量,减小创口以及术中反复透视的辐射剂量[4-5];术后可以通过打印模型评估手术效果[6-7]。在骨组织的 3D 打印建模中,CT 图像是公认的最佳建模数据,其由于较高的空间分辨率和组织分辨率,成为骨组织建模以及后续力学有限元分析、3D打印的最佳选择[8-10]。但打印出等比例的、与患者完全匹配的、精确的骨组织模型涉及术前 CT影像扫描、3D 建模、3D 打印及打印后处理一系列的流程。前期的 CT 影像扫描和 3D 建模的质量直接影响后续打印出模型的质量和精度,故选择何种序列的 CT 图像进行 3D 打印仍是值得研究的问题。以 GE Revolution CT 为例,该 CT提供的主要常规重建算法包括 SOFT、STND、DETAIL、CHEST、LUNG、BONE、BONE+ 以及 EDGE。根据检查目的不同,这些算法对空间分辨力和密度分辨力各有侧重。在实际应用中,重建方法分为低分辨重建算法和高分辨重建算法。其中,低分辨重建算法主要表现低对比度的软组织细节,密度分辨力较高,可用于增强扫描,包括 SOFT、STND、DETAIL 及 CHEST;高分辨重建算法主要表现空间分辨力,用于展现骨边缘等细节信息,密度分辨力偏低,一般不用于增强扫描,包括 LUNG、BONE、BONE+ 及EDGE。而现有的文献还没有对不同 CT 序列图像骨组织模型建模效果进行对比研究。本研究在多年的骨组织模型 3D 打印中发现不同 CT 图像序列重建的骨组织模型有一定差异,特别是骨窗序列常被默认为重建骨组织模型的序列,而通过笔者对比发现,在三维建模的效果上骨窗序列并不是最佳选择。
2 实 验
2.1 实验材料和工具
选择骨病患者中的 10 例作为研究对象,其中颈胸椎、腰椎、骨盆、四肢、足踝各 2 例。该研究获得南方医科大学深圳医院伦理委员会批准(批准号 NYSZYYEC20180002)以及患者的知情同意。根据不同临床应用领域的需求,CT 设备的厂家提供了不同的 CT 图像序列,本团队采用的是 GE 医疗 Discovery CT750 HD,将患者的手术部位进行 CT 扫描,扫描数据以 Dicom 3.0 格式存储于光盘。扫描参数如下:管电压 120 kV,管电流 349 mA,层厚 0.625 mm,无间隔容积扫描,扫描矩阵为 512 像素×512 像素,层内像素尺寸为 0.54 mm,机架倾角为 0°,图像序列包含标准窗(STND)序列和骨窗(BONE)序列。三维建模软件采用 Mimics Medical 21.0 医用设计软件(Materialise 公司,比利时)。建模后采用微软的 3D 查看器 V7.2 查看模型参数及效果。
2.2 实验方法
将 10 例骨病患者 CT 扫描后输出的原始Dicom 3.0 数据拷贝到 Mimics 图像工作站,点击图像工作站上 Mimics Medical 21.0 医用设计软件菜单栏的“New Project”新建病人项目,选择并导入 STND 扫描序列和 BONE 扫描序列,选择软件 Segment 菜单下的“New mask”中的“Bone(CT)”预置分割阈值,提取出骨骼组织的 Mask,随后右键点击分割出的骨骼组织Mask,再右键菜单栏选择“Calculate Part”即可将分割出的骨骼组织重建为三维结构,并显示于软件视窗右下角视图内。可通过工具栏或右键菜单选择不同的工具对重建的三维结构进行旋转、平移、缩放、半透明、拆分、切割、合并和修饰等操作,以调整重建模型达到要求,模拟手术切除范围。随后分别将 STND 扫描序列和 BONE 扫描序列的重建结果通过软件“STL+”功能导出 STL格式的建模数据,用于后续的分析和 3D 打印。
通过微软的 3D 查看器 V7.2 对 Mimics 21.0软件输出的 10 例患者(颈胸椎、腰椎、骨盆、四肢、足踝各 2 例)的骨组织 3D 建模的 STL 文件结果进行对比分析。其中,重点对建模阶段选择CT 影像的骨窗图像序列和标准窗图像序列进行比较——在软件中输入选定的 CT 序列图像后,采用相同分割参数和重建算法的前提下对建模效果和打印效果进行对比。具体地,对比相同条件参数下的重建构成三角形面片数量(表 1)和三角形顶点数量(表 2)、三维显示的效果、重建结果的吻合度和医生目测观察结果(图 1)。目测观察实验由 5 名具有 10 年以上工作经验的骨科医师对建模图像进行主观评价,采取盲法,同一台 Mimics 图像工作站,每位医师阅片时房间亮度和屏幕亮度均一致,每评完 1 组图像闭目休息20 s,以避免因视觉疲劳而产生误差。
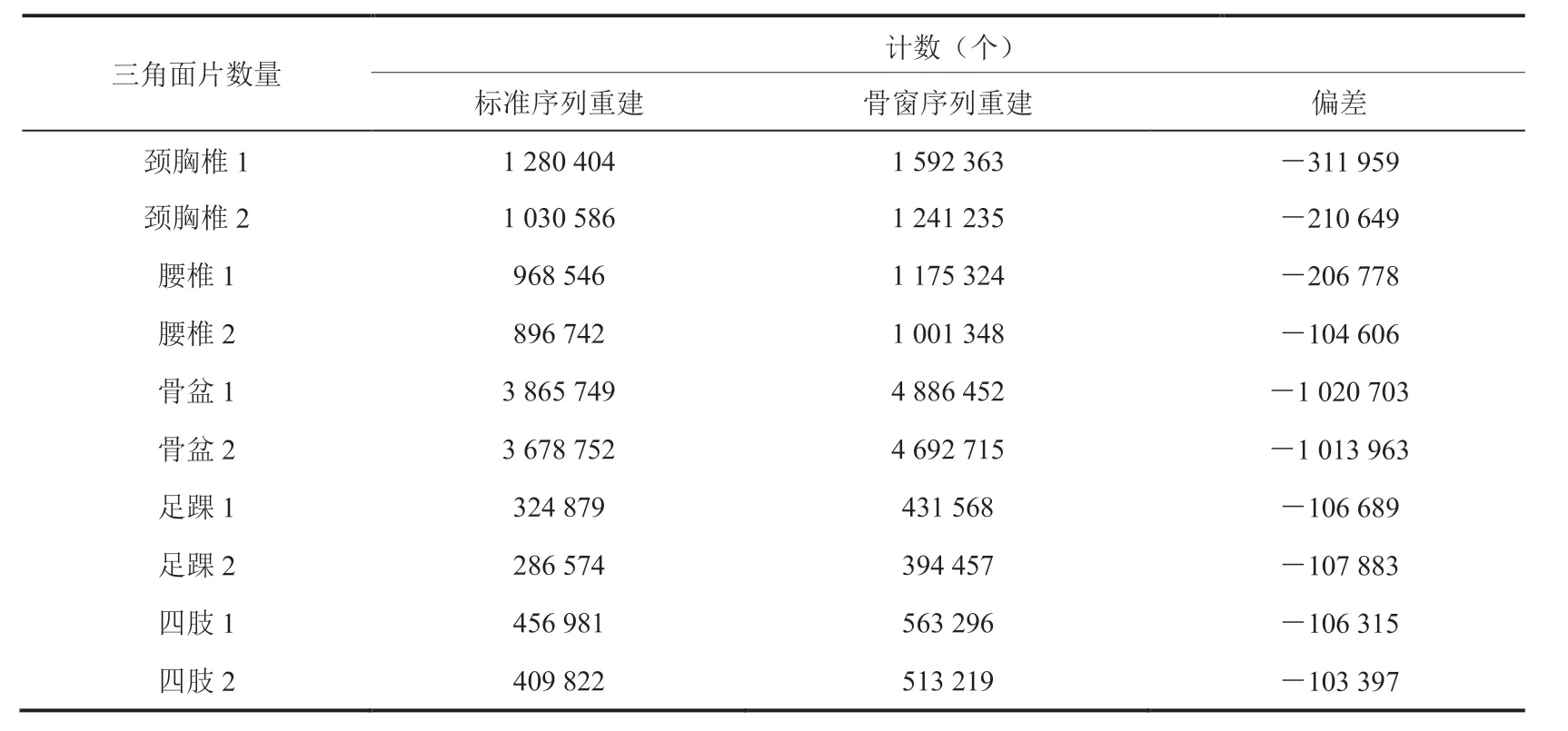
表1 10 例患者重建数据三角面片数量对比Table 1 3D reconstruction triangles numbers comparison of 10 patients
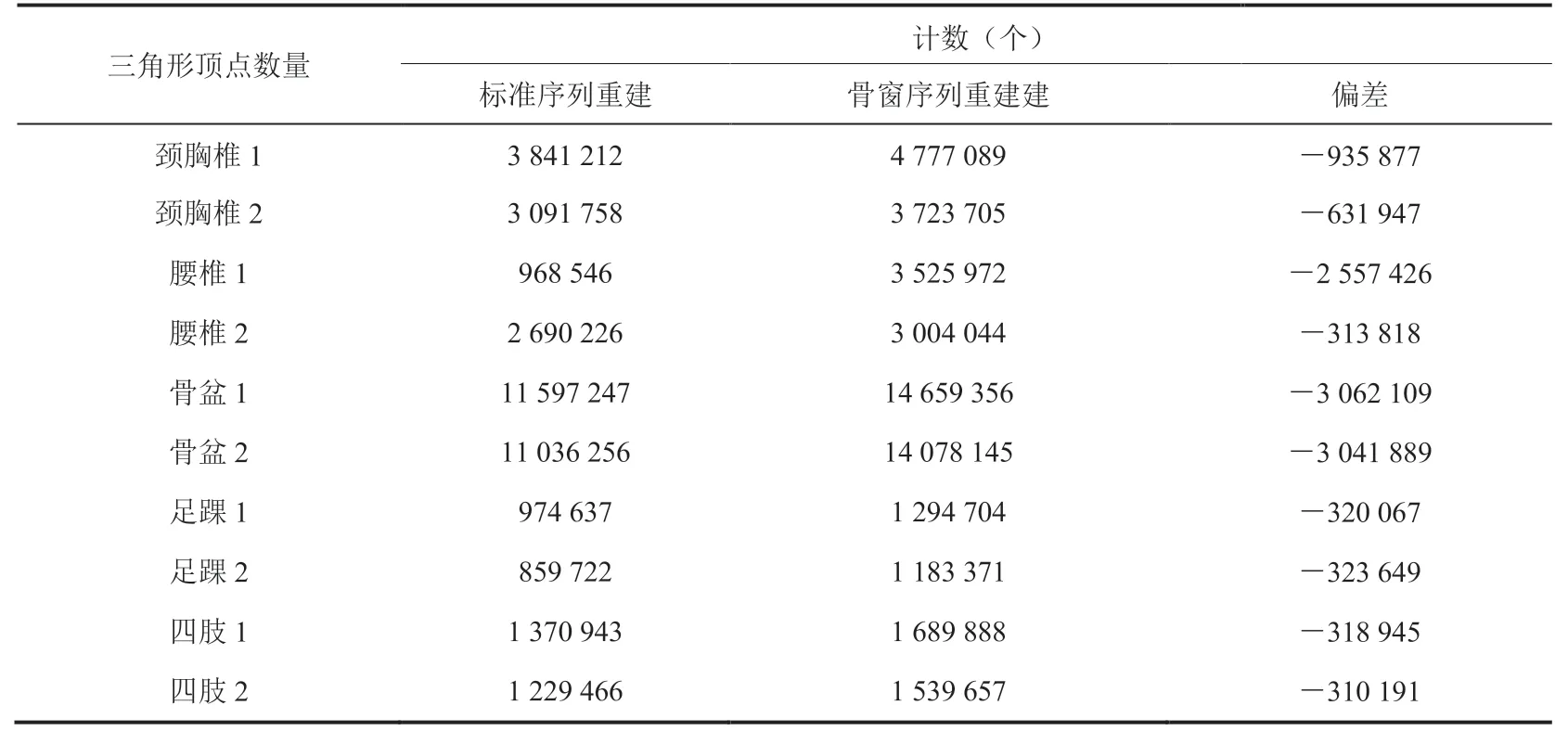
表2 10 例患者重建数据三角形顶点数量对比Table 2 3D reconstruction triangles vertex numbers comparison of 10 patients

图1 结果比较:(a)重建吻合度比较,(b)局部细节比较,(c)三角面片构成比较Fig. 1 Comparison of results: (a) 3D reconstruction coincide, (b) local details, (c) triangle facets
对于需要 3D 打印的模型,首先将重建的建模 STL 文件导入 iSLA450 树脂 3D 打印机(中瑞科技有限公司)进行打印前支撑设计和打印格式转换;然后,采用光固化立体造型工艺(材料为中瑞科技光敏树脂,型号 ZR710)进行实物打印(打印结果见图 2);最后,去除模型支撑和清洗模型上残留树脂,并用紫外光固化(99 min)完成打印模型后处理。
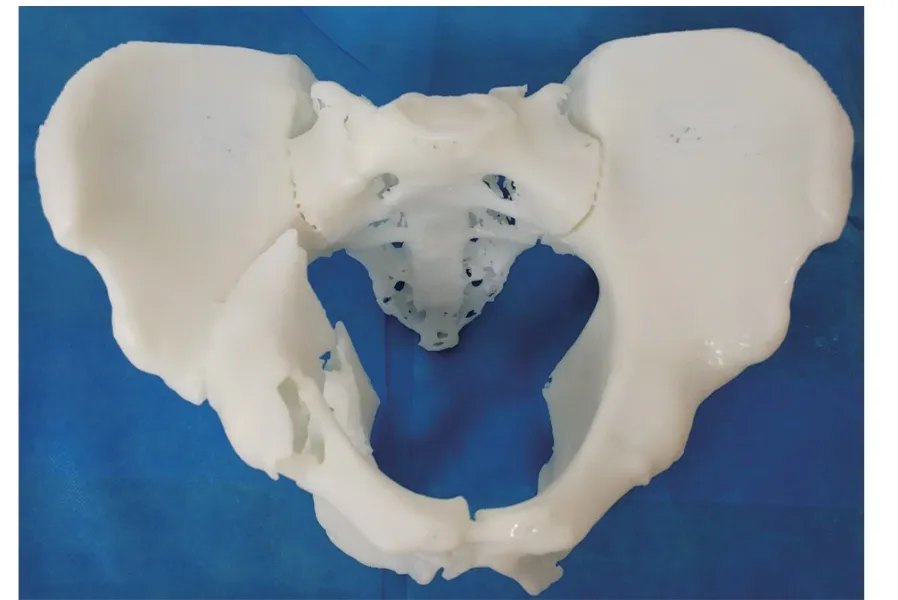
图2 标准序列重建骨盆打印结果Fig. 2 3D printed pelvis reconstructed from standard CT image series
3 实验结果
通过对 10 例骨组织模型的建模数据采用软件算法分析发现,采用标准窗序列的建模和打印效果优于采用骨窗序列的。其中,标准窗序列的建模结果中三角面片的数量和三角形顶点数量显著少于骨窗序列。推测骨窗序列的建模效果和质量下降的原因:CT 厂家在把标准窗的图像序列转化为骨窗图像序列时做了图像锐化处理[11-12],该处理降低了骨组织周围相邻组织(如软骨、肌腱、肌肉等)的灰度值[13-14],通过该处理后在二维断层图像上骨组织的对比度有显著提升[15-16](图 3),便于阅片期间对骨组织病变的快速识别[17-18]。但在 3D 建模中,建模的效果是通过三角面片顶点的相邻图像像素的灰度梯度先计算出法向量,再将该法向量代入计算机图形学的光照模型方程计算得到,而锐化后的图像相邻像素的灰度梯度过大,导致建模效果上出现明显的颗粒状失真。标准窗由于能够准确地反映骨组织和邻近组织(如软骨、肌腱、肌肉等)的真实灰度梯度过渡关系,在重建中的法向量计算中能准确体现骨组织和周围组织的真实关系,建模效果与真实一致,其重建和打印出的模型在质量和精度上都优于骨窗的。
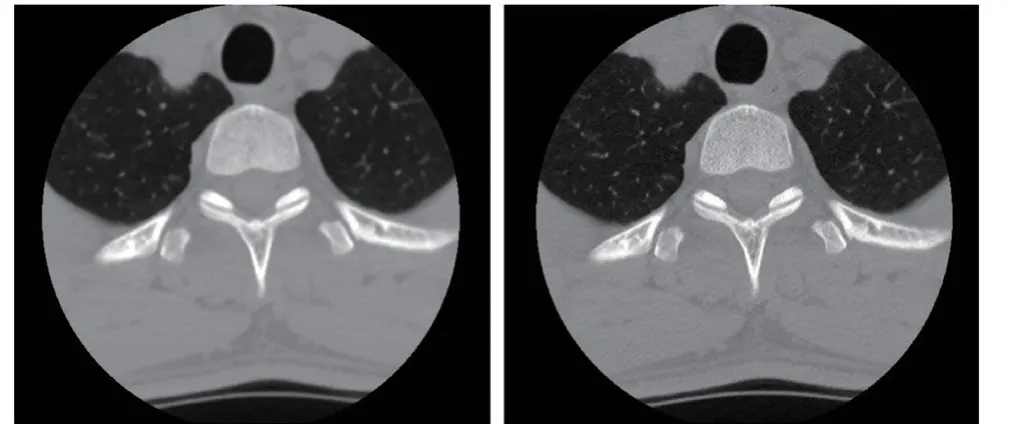
图3 标准序列(左)与骨窗序列 2D(右)对比Fig. 3 Comparison between STND(left) and bone(right) series
4 结 论
CT 图像的不同序列来源于扫描阶段采用的不同重建算法改变图像噪声的频段,目的是方便不同组织结构的阅片。其中,低分辨重建算法可提高各个噪声点之间的相关性,降低噪声频段,噪声结构趋于平滑,如标准序列;而高分辨重建算法可提高各噪声点之间的差异,提高噪声频段,噪声结构趋于锐利,如骨窗序列。因而低分辨重建算法往往降低噪声,提高密度分辨力,降低空间分辨力;高分辨重建算法提高噪声,降低密度分辨力,提高空间分辨力。根据检查目的合理地运用重建算法可以有效提升二维图像质量,提高疾病检出率。但目前缺乏不同序列对骨组织三维建模效果影响的相关研究。本研究结果表明,骨组织的 3D 打印建模阶段应选择标准窗的CT 扫描序列图像作为输入图像,如选择骨窗序列图像作为建模的输入图像则会导致最终打印模型的质量和精度下降(图 4、图 5)。本研究可为从事医疗领域骨组织 3D 打印相关业务在建模阶段选择序列的 CT 图像提供科学依据,避免在骨组织的 3D 打印建模阶段陷入选择骨窗序列的误区。

图4 重建效果(前视图)Fig. 4 3D reconstruction view (Anterior)
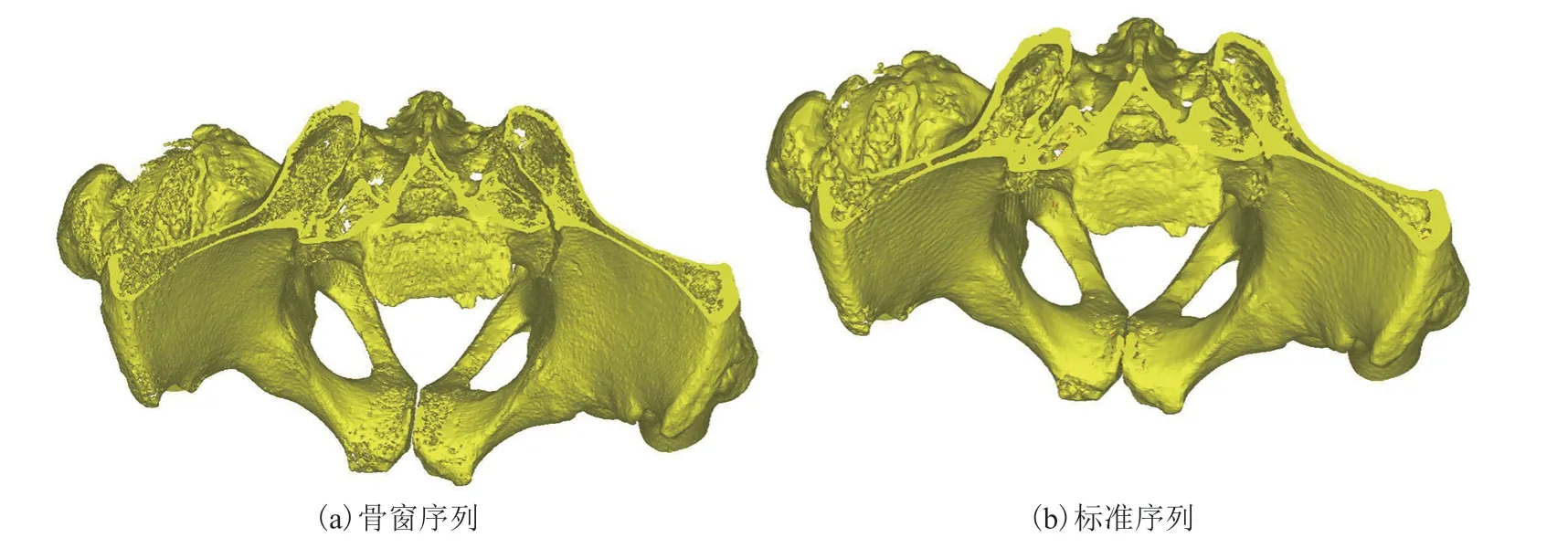
图5 重建效果(顶视图)Fig. 5 3D reconstruction view (Top)
