微/纳米机器人在生物医学中的应用进展
2021-06-03吴宏亮施雪涛
吴宏亮 施雪涛
1(华南理工大学生物医学科学与工程学院 广州 510006)
2(广州市再生医学与健康广东省实验室 广州 510005)
1 引 言
1959 年,费曼在演讲中指出,机器小型化到微/纳米尺度将开启一个新的技术时代[1]。此后,纳米技术的发展推动了微型机器人在不同领域的应用,其中一个重要的应用领域就是生物医学。微/纳米机器人可以触及到传统医学难以触及的部分,为药物治疗、手术、诊断和医学成像等的发展提供新的可能。
例如,在药物输送方面,一种基于金属-有机框架的生物可降解微型机器人已被确定为该领域有前景的载体,它能够在细胞培养物中实现磁控运动、药物递送和选择性降解。在癌细胞培养物中进行的药物递送研究显示,在递送抗癌药物阿霉素(DOX)后的短时间内,癌细胞的活力明显降低[2]。这种递送方法可能解决被动递送方法的低定位问题,在保持治疗效果的同时减少副作用。在手术治疗方面,一种由复合材料制造的毛刺状的多孔球形结构的微型机器人能够将治疗性细胞运输至靶位点。从微型机器人中释放工程干细胞可以显著抑制裸鼠肝脏肿瘤的生长,此方法相较于传统的细胞疗法有很大的优势。除此之外,利用实时光声成像技术的高时空分辨率、高分子对比度和深度穿透进行辅助,可以定位和导航深层血管组织中的微型机器人,方便医生以高精度、灵活性和可控性执行各种微创手术,不仅能为癌症等疾病的精确治疗提供参考,还能够减少患者的不适以及缩短术后恢复时间[3]。在医疗诊断方面,通过多孔天然孢子的逐步封装和功能化可快速合成廉价的荧光磁性孢子微型机器人,它可以在几十分钟内检测到细菌培养基甚至临床粪便样本中不同梭菌毒素的存在。微型机器人简单、快速、实时的监测诊断优势将有助于临床医生在患者感染初期选择有效的治疗方案[4]。
微/纳米机器人的出现为现代生物医学的创新、发展提供了新的思路,它能够以微创的方式进入人体,这是任何传统医疗技术都无法实现的。然而,尽管医疗微/纳米机器人在过去十年取得了一定的进步,但该领域尚未成熟的技术要求如微型机器人的驱动和集群控制等,限制了这些工具在临床中的广泛应用,且同时驱动一定数量的微/纳米机器人通常需要繁琐的程序和先进的仪器。
因此,本文简要概述了微/纳米机器人的制造和动力基础,总结了微/纳米机器人研究的最新趋势,重点阐述了它们在精密医学中的应用,如运输货物、外科手术、医疗诊断和医学成像等。文章最后明确了医学微型机器人从实验室向临床应用转移的主要挑战和潜在风险,并指出微/纳米机器人未来的发展方向。
2 微/纳米机器人的制造、驱动和降解
制造、驱动和降解是微/纳米机器人应用的基础。在微纳米尺度内,微型机器人的运动受低雷诺数和布朗运动两种因素的影响,它的运动必须考虑环境效应,因此设计微/纳米机器人主要是使其能够产生连续不断的运动,并要求其具有足够的动力来克服环境的阻力[5]。例如,可以使用催化材料制造微型机器人,并在 H2O2中利用催化反应产生气泡的方法推进其定向运动;赋予有螺旋结构的微型机器人磁性,利用磁场引起螺旋自身的旋转,进而推动螺旋的直线运动;对于具有不对称结构的微/纳米机器人,可以施加超声波产生压力梯度来推动它们运动[6-8]。不同种类的微纳米机器人有着不同的制造方法和驱动方式,而微/纳米机器人的无毒降解对生物体的安全而言也十分重要。
2.1 微/纳米机器人的制造
在模板上使用薄膜涂层产生不对称结构的方法也已经被用于微/纳米机器人的制造。Janus 微型机器人就是利用电子束或溅射沉积法产生不对称结构制造而成的。例如,将锌(Zn)微粒部分浸入液态金属镓(Ga)中,Zn 微粒的顶面部分被 Ga覆盖,形成不对称的 Ga/Zn 微结构,这种微结构能在模拟胃酸中进行推进[10]。如图 1(a)所示,一种不对称改性的 Mg/Pt-聚(N-异丙基丙烯酰胺)(PNIPAM) Janus 微型机器人能够在没有引入任何添加剂或燃料的情况下,在模拟体液和血浆中自主运动并通过调节温度来控制药物输送[11]。
对一些结构比较复杂的微/纳米机器人则使用更加先进的制造方法。例如,用来运输细胞的具有螺旋结构的微/纳米机器人(图 1(b)),它是使用高精度的双光子聚合 3D 打印方法制造的[7]。虽然双光子聚合 3D 打印允许人们按照自己的想法设计特定结构的微/纳米机器人,但这种制造方法需要使用昂贵的仪器和特殊的材料。
自组装是一种制造微/纳米机器人的常用方法。一种生物混合磁性精子机器人的自组装制造以静电学为基础,依靠表面相反电荷的吸附作用,使牛精子细胞和赤铁矿纳米粒子结合到一起。它能够通过超声图像进行定位,并通过磁场可控地操纵其沿着预设轨迹运动[9]。
具有管状结构的微/纳米机器人常用自卷曲技术制造。此种自卷曲制造方法利用了材料内部的应变梯度,通过蚀刻牺牲层来释放预应变的纳米膜,并使其卷曲成管状结构[12],如图 1(c)所示。
2.2 微/纳米机器人的驱动

图1 不同类型的微纳米机器人[7,11-12]Fig. 1 Different types of micro/nanorobots[7,11-12]
微/纳米机器人既可以单独运动又可以集群运动。其驱动方式很大程度上会影响其运动速度、受控难易程度和生物相容性等,进而影响它们在生物系统中的应用。微/纳米机器人的驱动方式主要包括:由局部化学、生物化学能量(如H2O2、尿素等)驱动的化学驱动方式,由外部场(如光、超声波或磁场等)驱动的物理场驱动方式和由微生物或细胞(如精子等)驱动的生物驱动方式。
2.2.1 化学驱动
化学驱动的微/纳米机器人通常由催化剂(如活泼金属)和惰性材料组成。其中,催化剂的作用是在机器人表面与燃料发生化学反应,而惰性材料用于构建不对称结构。H2O2是最早也是研究最广泛的燃料。在 H2O2中,微/纳米机器人可以产生自电泳机制而驱动或利用自身的铂金(Pt)等材料催化分解 H2O2产生气泡,推动自身的运动[13-14]。但高浓度的 H2O2氧化作用强,与生物体不相容。故为实现实际应用,特别是在生物系统中采用化学驱动的方式驱动微/纳米机器人时,需要确定除 H2O2之外的新的原位燃料,即原料应该是生物流体中的自然物质,而不是由外部添加。例如,使用可生物降解的 Zn 或 Mg,通过与胃的酸性环境发生反应产生氢气来实现自推进,并在使用后留下无毒的产物[15];利用酶取代Pt 进行催化反应,这样就可以把燃料替换为各种生物分子,如葡萄糖或尿素[16]。
2.2.2 外部场驱动
外部场驱动的微/纳米机器人大多不需要燃料,因此其是生物相容和可持续的,主要包括光、超声波或磁场驱动等。与化学驱动的微/纳米机器人相比,它们在控制运动方面更加灵活。
建立声学条件是比较容易的,声波能够通过固体、液体和空气介质传播,故可深入穿透生物组织,从外部触发微/纳米机器人的推进,而不会对人体造成损害。超声波驱动一种纳米棒状的微型机器人的机制是在超声波的作用下,不对称纳米棒表面上局部声流应力产生了运动的驱动力[17]。一种用金纳米线包裹着红细胞膜和血小板膜组成的仿生纳米机器人,在全血中显示出快速而有效的长时间声学推进,并且可以模仿自然活动的细胞运动。这种推进机制增强了微型机器人对病原体和毒素的结合能力,提高了解毒效率[18]。除此之外,还可以利用高强度聚焦超声波来诱导化学燃料的快速蒸发,产生子弹运动状态的管状微型机器人。这种微管能以非常高的平均速度运动,凭借强大的推力穿透组织[19]。
光驱动的微/纳米机器人由光活性材料构成,主要包括光催化材料、光致变色材料和光热材料等。在光的照射下,这些光活性材料能够吸收光能,分别引发光催化反应、光异构化反应和光热转化反应等。光驱动的方法操作简单、响应速度快[20]。例如,一种利用聚吡咯(Polypyrrole,PPy)纳米粒子制造的新型光驱动片状微型机器人,当其被近红外光照射时,产生马兰戈尼效应并显示出受控的平移运动。这种效应通过改变入射光的角度来调节,从而精确控制微型机器人的运动过程,使其能够以理想的方式输送和释放吸附的有效载荷[21]。除了提供驱动力之外,近红外光还具有光学成像的潜力,可以跟踪体内微/纳米机器人的运动[22]。
磁场驱动的微/纳米机器人同样可以在没有任何燃料添加的情况下被驱动,而对人体没有任何伤害。磁场驱动的条件是使用磁性材料构建微/纳米机器人来响应外部磁场。其中,外部磁场分为旋转磁场、梯度磁场、振荡磁场等。例如,三维磁性管状机器人的远程可控性和精确运动可以通过外部磁场来实现,这些管状机器人在二氧化硅微粒的捕获、靶向递送和释放方面有着良好的能力[23]。再比如运动金属有机框架(MOF)是环境修复、靶向药物输送和纳米外科手术中小型机器人平台的潜在候选者。Wang 等[24]制备的具有生物相容性和 pH 响应特征的螺旋微型机器人,就是由 Zn 基 MOF 和沸石咪唑骨架 8(ZIF-8)包覆的。这种高度集成的多功能微型机器人可以在弱旋转磁场的控制下沿着预先设计的轨道运动,并在复杂的微流体通道网络内部实现货物的有效输送。除此之外,磁场还可以与其他物理场一起控制微/纳米机器人的运动。例如,Xu 等[25]提出了一种可靠的推进方法,在建立了一个电磁线圈系统来驱动螺旋机器人的前提下,通过额外施加超声波将微型机器人悬浮在基板上,以此来减少整个运动过程中多余的横向漂移,这是进一步改善运动控制的一种新颖而有效的策略。
2.2.3 生物驱动
生物驱动的微/纳米机器人主要是指生物混合微型机器人,它是由活动的微生物(细胞)和人工材料组成的。像细菌和精子这些通过鞭毛推动自身运动的微生物可以当作推进生物混合微型机器人的引擎,其中精子还有与体细胞融合的独特能力,这会显著提高微/纳米机器人的生物相容性和安全性。例如,一种由运动性精子细胞作为动力源和药物载体的生物混合微型机器人系统,包括 3D 打印的具有四个臂的磁性管状微结构。与纯合成微型机器人或其他载体相比,这种精子杂交微型机器人可以将高浓度的药物封装在精子膜内,从而保护其免受体液稀释和酶降解的影响[26]。
总之,化学或生物驱动的微/纳米机器人利用的是内置的能量转换,或是微生物的自主能动性,而外场驱动的微/纳米机器人的运动是外部场、机器人的构造和其所处的介质之间相互作用的结果。因此,每种驱动方式都具有独特的优势。其中,利用外场还可以诱导微型机器人的集群行为。例如,超顺磁性的 Pt-微型机器人,它们能够在化学燃料存在的前提下,利用磁场的作用协同推进,并能够形成链状结构,提高药物的释放效率。除此之外,对于微型机器人的集群运动,还可以使用计算机设计算法来控制。如 Villa 等[27]设计的粒子群算法具有调整参数少、内存占用少的优点,可以应用于微/纳米机器人的协调控制或其他物理用途,如将其运用到伤口止血,治疗一些病人的血小板数量及功能紊乱。其中,人造血小板止血过程为:首先,使用粒子群算法来控制微型机器人群沿着血管移动,寻找伤口,附着在受损部位;然后,释放信号激活其他部位;最后,微型机器人之间相互连接。这种止血的治疗方法避免了使用药物、血小板输注或脾切除术治疗带来的副作用,也对短时间内处理大量负载提供了可能[28]。
2.3 微/纳米机器人的降解
所用材料的降解性是微/纳米机器人降解的基础,良好的降解性能够省去微型机器人使用后的操作。例如,利用可生物降解的聚合物来制造微型机器人,结合激光直写控制形状,在细胞培养中具有很大的优势[2];利用水溶性聚合物聚乙烯醇等,能够快速并大规模生产许多已经含有药物的可生物降解的微型机器人[29]。将明胶、壳聚糖等天然聚合物与磁性纳米颗粒共同使用制造的磁性靶向生物可降解微型机器人,可以在适当的磁场作用下达到靶向缺陷位点,并在微型机器人降解后释放细胞。其中,被释放的细胞可以运动到其作用位点并发挥相应的作用[30]。
3 微/纳米机器人在生物医学中的应用
3.1 运输作用
制造微/纳米机器人的一个重要目的就是使其能够装载“货物”并到达所需的地方。这些“货物”主要包括药品、试剂和细胞等。
3.1.1 运载药物和生物试剂
药物对于疾病的治疗效果通常受到多种因素的影响。在传统治疗方法下,如果想达到期望的治疗效果,一般方法是高剂量的重复给药,但这很可能会增大毒性和副作用。微/纳米机器人在目标区域精确的运送潜力有望解决药物用量过大而导致的毒性问题。
一种治疗胃细菌感染的载药微/纳米机器人的核心由平均尺寸约为 20 μm 的 Mg 微粒制成,其治疗过程如图 2 所示。它拥有高效推进的能力,在体外模拟胃液(pH=1.3)中测试的平均速度约为 120 μm/s。对幽门螺杆菌的体外杀菌活性试验表明,在研究中使用的整个浓度范围内,载药机器人显示出与游离药物溶液相当的杀菌活性,微型机器人可以被有效推动并分布在活小鼠的整个胃中,显著减少了幽门螺杆菌的数量。体内毒性研究证明了微型机器人在治疗小鼠模型中的安全性。与被动药物载体相比,在胃介质中推进载药 Mg-微型机器人可以更高效地递送抗生素。除此之外,自主推进所需要利用的酸-Mg 反应也会消耗胃液中的质子,从而中和胃的 pH 值[31]。类似地,另一种以 Zn 为基体的微/纳米机器人在胃药物输送方面,同样具有高动力推进、高负载能力、有效载荷的自主释放和无毒的自我降解,与口服给药的普通被动扩散和分散相比,其有效载荷在胃内壁中的保留情况得到了显著改善[15]。除了胃酸之外,还可以用尿素来驱动微/纳米机器人。鉴于尿液中尿素浓度较高,该机器人的一种直接体内应用可能是通过膀胱内给药来治疗膀胱癌或感染[32]。
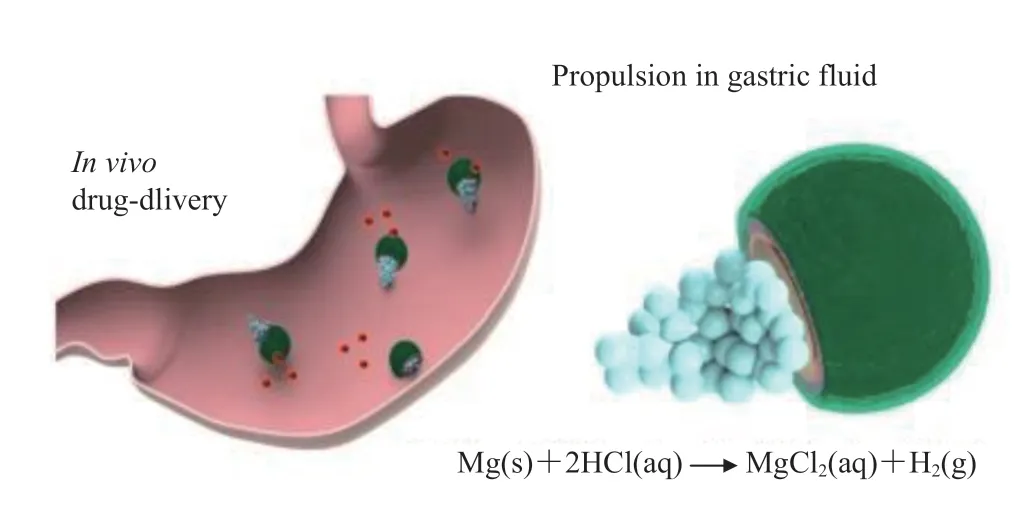
图2 Mg-微型机器人治疗胃部细菌感染[31]Fig. 2 Magnesium-micro/nanorobots treats bacterial infections in the stomach[31]
金属有机框架(MOF)可以通过 pH 响应控制药物释放,它能够在细胞培养物中实现磁性运动、药物递送,其所有成分都能够降解[2]。进一步地,Wang 等[33]在室温下,通过超声辅助湿化学法合成制备了一种基于多孔沸石咪唑盐骨架-67(ZIF-67)的新型催化微型机器人。这些多孔微型机器人在 H2O2中显示出有效的自主运动和长达 90 min 的持久运动寿命。其结合 DOX 后载药量可高达 682 μg/mg。如图 3(a)所示,该微型机器人由于具有多孔性、高表面积,以及基于H2O2的催化反应和 H2O 溶剂效应的双重刺激,在外磁场下显示出优异的药物递送性能。与传统基于 pH 响应释放机制的多孔膜载体相比,双重刺激诱导的多孔 ZIF-67 微型机器人的药物释放更加直接和及时。
磁场可以精确控制磁性微/纳米机器人,但Ni 等磁性材料的有害性限制了这类微型机器人在药物输送方面的应用。基于此,Park 等[34]开发了具有 3D 螺旋结构的可降解热疗微型机器人,并将其用于主动控制药物输送、释放和热疗。该微型机器人由聚乙二醇二丙烯酸酯(PEGDA)和季戊四醇三丙烯酸酯(PETA)制成,包含磁性 Fe3O4纳米粒子和抗癌药物 5-氟尿嘧啶(5-FU)。在电磁驱动系统产生的旋转磁场的远程精确控制下,5-FU 可以从微/纳米机器人中释放。对此种机器人进一步的研究发现,其对声能的响应更高,在超声下对药物的释放如图 3(b)所示。通过改变超声束的条件,发现机器人对药物的释放有自然释放、爆发模式和恒定释放 3 种模式,体外试验结果显示每种释放模式有着不同的治疗结果。其中,在爆发和恒定释放模式中观察到癌细胞的生存力大幅度降低,证实了超声可以通过增加药物浓度和声孔作用来增强治疗效果。超声介导治疗可以减少药物的副作用,这是由于微型机器人可以被精确地操纵到目标位置,并且装载的药物可以通过超声聚焦选择性的释放。即使在操作过程中一些药物转运蛋白发生偏移,通过仅在目标位置使用聚焦超声主动释放药物也可以将药物损失降至最小[35]。
微/纳米机器人同样可以运送生物制剂(如病毒疫苗),用于治疗腹腔中的转移性肿瘤(如卵巢癌)。其在小鼠肿瘤模型中递送病毒疫苗的示意图如图 4 所示。体外细胞研究表明,微/纳米机器人可以延长纳米颗粒和巨噬细胞之间的相互作用时间,从而更有效地激活巨噬细胞,引起免疫刺激的增强,进而提高小鼠的存活率。这解决了被动治疗由于大的腹膜空间和快速排泄而需要多次注射的问题。在免疫治疗方向,主动递送在治疗不同类型的原发性和转移性腹膜腔肿瘤方面具有广阔的前景[36]。
3.1.2 递送细胞

图3 微/纳米机器人对药物的输送[33,35]Fig. 3 Drug delivery by micro/nanorobots[33,35]

图4 微/纳米机器人在小鼠肿瘤模型中递送病毒疫苗[36]Fig. 4 Micro/nanorobots deliver virus vaccines in mouse tumor models[36]
运用微/纳米机器人将活细胞直接输送到目标区域可以提高它们的保留率和存活率。例如,球形和螺旋形的磁性微/纳米机器人被开发用于三维培养和体外、离体和体内干细胞的精确输送。该类微型机器人通过 3D 打印技术制造,在外加旋转磁场条件下表现出滚动和螺旋运动,这比由磁场梯度拉动的机器人有着更高的推进效率,更适用于生物流体。海马神经干细胞可以在其上增殖并分化为星形胶质细胞、少突胶质细胞和神经元。此外,微型机器人可以在体外将直肠癌细胞转移到肝肿瘤微芯片上的肿瘤微组织中。这些结果表明,微型机器人在各种体外、离体和体内生理流体环境中进行靶向干细胞运输和移植是可行的[37]。另外,一种超顺磁性/催化微型机器人能够像单个机器人一样移动,并在弱磁场的作用下“组队”,形成链状球形结构,这样的结构可以有效地装载运输癌细胞。在装载 DOX后,它们还能够捕获乳腺癌细胞,同时通过扩散释放药物[27]。
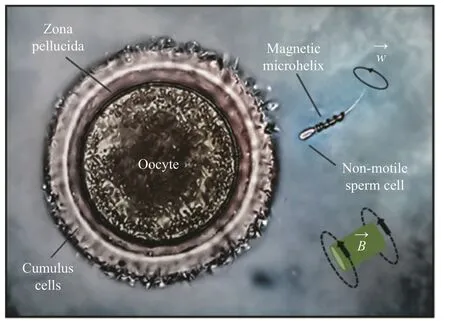
图5 微/纳米机器人协助受精过程[38]Fig. 5 Micro/nanorobots assist in the fertilization process[38]
除了用于干细胞移植,微/纳米机器人还可以用作精子的载体来协助完成受精过程。针对有些精子细胞因缺陷活动力低或无法移动,Medina-Sánchez 等[38]设计了金属涂层-聚合物微螺旋机器人来运输运动障碍的精子细胞,以帮助它们实现自然受精的功能,该过程如图 5 所示。他们设法模拟生理条件的流体通道,在其中捕获、运输和释放单个不活动的活精子,并成功地将单个精子细胞输送到卵母细胞的细胞壁。除了用螺旋微型机器人之外,他们还设计利用管状的微型机器人来捕捉运送精子[39]。这种新受精方法的优势在于其潜在的体内适用性,因为如果能够在卵母细胞的自然环境中对其进行靶向受精,就没有必要将卵母细胞移植和再移植。但人工输送精子到卵母细胞受精似乎还有很长的路要走。
3.2 外科手术
传统的手术没有微/纳米尺度的手术工具,这限制了在这种小尺度下操作的能力。小型化的微/纳米机器人尺寸小,如果能被用作外科手术工具,那么其能够到达导管和刀片不能到达的区域,具有明显的优势。此外,它们将有可能降低感染风险和缩短恢复时间,并提高外科手术的精确度和控制力。
3.2.1 消灭细菌和癌细胞
利用外加物理场以及材料本身的特性,微/纳米机器人可以直接杀死肿瘤部位的癌细胞。Chen 等[40]通过聚焦磁场操纵趋磁细菌-微型机器人来定向杀死病原体。他们首先在微流控芯片中引导趋磁细菌-微型机器人,然后操纵微型机器人靶向附着在金黄色葡萄球菌上,当微型机器人与金黄色葡萄球菌结合时,施加摆动磁场可使金黄色葡萄球菌生存力显著下降。虽然磁性靶向装置可以杀死金黄色葡萄球菌,但不能杀死简单的混合物或仅含金黄色葡萄球菌的溶液中的金黄色葡萄球菌。这些结果表明,使用磁性靶向装置是微型机器人靶向治疗的一种有前景的方法。未来的研究需要探寻脉动血流、红细胞、摩擦对趋磁细菌-微型机器人控制的影响以及趋磁细菌在人体内的安全性。
抵抗细菌还可以依靠微机器人自身的作用,如将 Ga/Zn 微/纳米机器人降解产生的 Ga 阳离子用作内置抗生素。与被动使用的 Ga 微粒相比,该方法改善了 Ga 离子的扩散,使抗幽门螺杆菌的抗菌效率显著提高,其制造和抗菌过程如图 6所示[10]。
与正常细胞相比,癌细胞对热更敏感,在大于 40 ℃ 环境下就会遭受不可逆的热损伤,42~45 ℃ 的温度就足以杀死癌细胞。因此,可以利用可降解热疗微型机器人在交变磁场作用下将电磁能转化为热能,通过升高温度来降低癌细胞的生存能力。在体外使用癌细胞系证明了这种介导靶向热疗的可行性,这种杀死癌细胞的方式在最大程度上降低了对身体的损伤[34]。
3.2.2 眼科手术
在玻璃体内注射治疗剂方法的应用有望推动眼科医学的发展。传统的递送方法依赖于分子的随机、被动扩散,不能将浓缩的药物快速递送到眼睛后的限定区域,而且包括玻璃体在内的大多数组织都有一种紧密的大分子基质作为屏障,阻止颗粒的渗透。而通过磁驱动的螺旋微/纳米机器人可以主动穿过玻璃体液到达视网膜。其中,螺旋的直径与玻璃体的生物聚合物网络的网孔尺寸相当,并且用全氟化碳进行表面涂层功能化,该涂层使螺旋与生物聚合物(包括玻璃体中的胶原束)的相互作用最小化,最大限度地减少对周围生物聚合物网络的黏附。在外部磁场的无线激励下,螺旋微/纳米机器人的大群体可以被驱动穿过眼球几厘米的距离,并可以在 30 min 内到达视网膜,输送时间缩短为原来的 1/10。整个系统用标准光学相干断层扫描成像。完整的操作程序包括玻璃体内注射、远程自我推进和无创监测[41]。
为了提高微/纳米机器人的生物相容性,将微/纳米机器人在进入眼部时产生的炎症反应降到最低,Pokki 等[42]研究了 PPy 在镀金/钴/镍微型机器人上的应用。他们将与多种细胞具有良好的长期生物相容性的 PPy 用作微结构上的保形功能涂层,并将带有涂层的微型机器人注入兔眼内。结果显示,通过使用 PPy 涂层,微/纳米机器人的生物相容性增强;与未涂覆 PPy 涂层的对照物相比,涂覆后的炎症反应最小。微型机器人在视网膜静脉阻塞的药物输送和视网膜前膜的剥离手术中显示出潜在的适用性。
3.3 医学诊断
微型机器人可以与流体混合并诱导靶受体产生相互作用,这为医学诊断提供了可能性。微型机器人可以选择性地识别金属离子、细菌毒素、蛋白质、细胞等[4,43-44],为疾病治疗提供治疗前的准确分析。
3.3.1 检测离子和毒素

图6 Ga/Zn Janus 微电机的制造和抗菌过程示意图[10]Fig. 6 Schematic illustration of the fabrication and antibacterial process of Ga/Zn Janus micromotors[10]
微/纳米机器人可以检测血液中的金属离子,防止离子浓度过高而严重影响人体健康。例如,一种新型磁性介孔的二氧化硅/硫化锌锰/金/四乙烯五胺/肝素-微型机器人可以直接检测和去除血液中过量的铜。该微型机器人可以加速溶质的扩散,并与目标充分混合,其磁性介孔二氧化硅微管为活性物质四乙烯五胺(TEPA)的吸附提供了丰富的负载空间,从而对 Cu2+表现出良好的吸附能力和短的处理时间。由于介孔结构、吸附性官能团和良好的移动能力的协同作用,血铜离子的去除率高达 74.1%。同时,该微型机器人可以根据从血液中分离后荧光信号的变化选择性地监测血液中的铜离子浓度。整个自混合过程可以通过微型机器人的自主运动实现,无需搅拌或超声波。磁性 Fe3O4可以实现微型机器人在去除血液中 Cu2+后的快速分离。这一研究成果将为血液中毒素的检测和去除的一体化提供一定的支持,并解决传统治疗方法治疗周期长、费用高、诊疗分离、治疗效果有限的问题[43]。合成微型机器人和去除/检测血液中 Cu2+的示意图见图 7。
为了在脓毒症的早期对其进行诊断,Molinero-Fernandez 等[44]开发了一种基于微型机器人的荧光免疫测定法并将其用于降钙素原(PCT)的测定。这种微型机器人的 PPy 层有着高结合能力的特异性抗体,通过磁导向和催化产生气泡的推动来主动识别 PCT 抗原。该测定法在临床相关浓度范围内使用少量样品,就可以对疑似败血症的、极低体重的新生儿临床样品进行PCT 水平测定。
3.3.2 生物传感
微/纳米机器人作为生物传感器,在智能传感和驱动系统中具有巨大的潜力。Kong 等[45]开发了一种能够自我更新表面的 Mg/Pt Janus 微型机器人。在 Mg/Pt Janus 微型机器人的辅助下,无需额外的有毒燃料或表面活性剂,就可以提高对人血清中葡萄糖的电化学检测能力,如图 8 所示。他们的研究显示,在人体血清中的葡萄糖为毫摩尔浓度的情况下,Mg/Pt Janus 微型机器人的快速运动增强了电流信号且电流信号随着引入的微型机器人数量的增加而增加,检测信号得到了改善,且微型机器人的加入在电流信号与葡萄糖浓度之间建立了线性关系。
与合成传感器相比,红细胞生物传感器和微型机器人在生物系统中具有高度的生物相容性、灵活性和无创性[46]。Li 等[47]使用体内红细胞波导构建了活体生物传感器和微型机器人,该波导被光学梯度力限制在两根锥形光纤的光轴内。红细胞波导可以作为微型机器人连续旋转,从而在血液中可控地输送微粒。该红细胞波导管已经在斑马鱼血管中成功组装并工作,其光传播模式对周围环境敏感,又与红细胞形态有关,而红细胞形态取决于血液的 pH 值,因此该红细胞波导可用于人体的酸碱度传感,检测由酸碱度引起的血液疾病,可测量的 pH 值为 5.0~9.0。

图7 合成微型机器人并去除/检测血液中的 Cu2+[43]Fig. 7 Synthesize micro robots and remove/detect Cu2+ in blood[43]
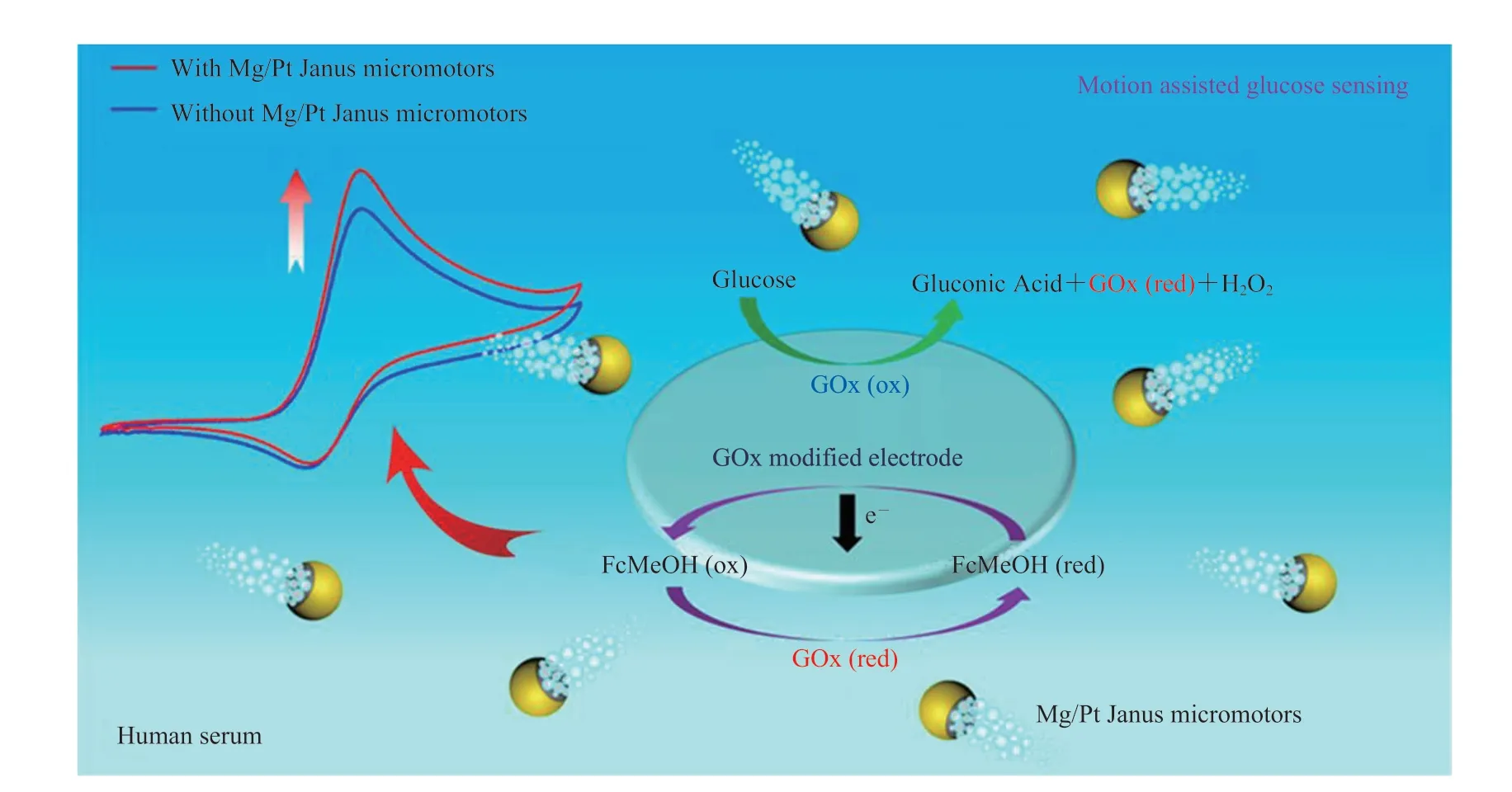
图8 Mg/Pt Janus 微型机器人对人血清中葡萄糖的检测[45]Fig. 8 Detection of glucose in human serum by Mg/Pt Janus micro-robot[45]
3.4 医学成像
医疗微/纳米机器人在临床中的一个关键应用是依靠个体或群体进行监测。它们可以容易地在体内定位和引导,甚至发送信号以诱导触发释放,因此在医学成像方面的潜力也不可忽视。例如,利用光学相干断层扫描成像在小鼠静脉中监测微型机器人的实时位置,反馈微型机器人在体内的运动。与以往的成像方法相比,光学相干断层扫描成像方法在实时成像、与梯度磁操纵系统的兼容性好、高成像分辨率和对身体的伤害小等方面显示出令人满意的效果。微型机器人在2 mm 穿透深度的体内环境中能被很好地检测到,但此穿透深度需进一步提高[48]。另外,还有一种方式是将光声计算机断层扫描(PACT)引导的活体肠道微型机器人设计为成像造影剂和可控药物载体。其中,该微型机器人具有功能性多层涂层,其金层被用来增强光吸收并提高推进的速率,明胶水凝胶层用于扩大不同功能成分的负载能力,聚对二甲苯层用于在推进过程中保持微型机器人的几何形状。由于 PACT 具有高时空分辨率、非侵入性、高分子对比度和强深度穿透性,故可以实时观察到微型机器人胶囊向目标区域的迁移[49]。Iacovacci 等[50]提出了一种由热响应双层水凝胶制成的磁驱动治疗微型机器人。这种微型机器人包含磁性纳米粒子和放射性化合物,在水凝胶框架中充当成像剂。磁性纳米粒子可用于远程驱动并触发微设备的形状转换,而成像剂可以在体内监控微型机器人。对小鼠进行皮下注射的离体成像如图 9 所示,在注射后进行单光子发射断层扫描,在小鼠腹部可以清楚地检测到微型机器人。该研究首次表明,当使用直径低至 100 μm 的水凝胶结构时,可以进行单个微型机器人的成像,这为未来单机器人闭环控制的发展打下了基础。
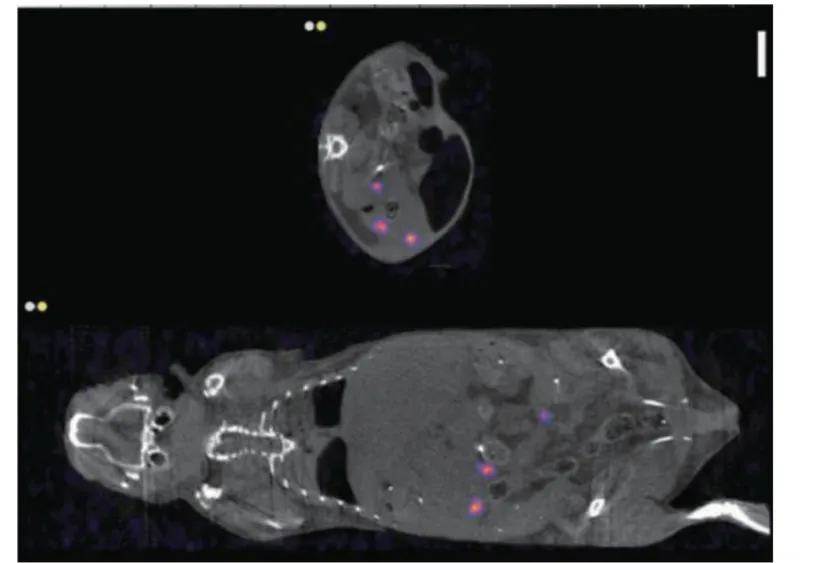
图9 利用微/纳米机器人进行医学成像[50]Fig. 9 Medical imaging of micro/nanorobots[50]
除了光声成像之外,微/纳米机器人还可以利用磁共振成像。通过简单的浸涂工艺,在磁铁矿悬浮液中利用螺旋微藻制备的螺旋微锥机器人具有超顺磁性。由于微藻具有允许体内荧光成像的固有特性,该螺旋机器人不需要任何表面修饰就能显示出内在荧光、磁共振信号、天然降解性和理想的细胞毒性,能够在各种生物流体中进行稳健的导航,并且能够通过自体荧光、磁共振成像在浅表组织或深层器官中进行无创跟踪。对小鼠进行皮下注射和腹腔注射后,通过磁共振成像,在小鼠的胃中观察到了微型机器人群[51]。另一种微型机器人可以在带有附加梯度线圈的磁共振成像设备中导航,并允许在单轴磁场下线性组装[52]。
4 总结与展望
总体来说,在过去十年中,微型机器人在精密医学中的研究在不同领域均取得了一定程度的突破,其应用包括:作为运输工具负载和运送药物、生物试剂及活细胞等;作为手术工具检查组织、消灭癌细胞和细菌等;作为诊断工具,检测人体中的离子含量并进行生物传感;作为成像工具,依靠光、声、磁等方式进行体内和体外成像。
虽然目前已有很多在动物试验上进行靶向给药的研究。但在微/纳米机器人转化为临床应用之前,仍然面临着安全、技术、监管和市场等诸多方面的挑战。例如,目前微/纳米机器人的应用尚未在人体内进行试验,其对人类健康的影响还未进行评估;在技术层面上,虽然 3D 打印技术的出现能够对微/纳米机器人进行大规模制造,但是其对设备有严格要求以及需要高昂的成本,此外,微/纳米机器人的驱动方法仍需要继续优化;最后,目前还没有微/纳米机器人在商业领域的大量需求,缺乏验证医用微型机器人的市场。
尽管距离微/纳米机器人的大规模临床应用还有很长的路要走,但在精密医学中使用微型机器人进行诊断和治疗疾病的潜力是巨大的。一旦微/纳米机器人在人类受试者中取得初步的验证,可以帮助精确医疗、降低成本、减轻外科手术的痛苦,那么它就会极大地推动现代生物医学的发展,并在很大程度上改变人类的生活。
