三种新型冠状病毒抗体检测系统一致性评价
2021-05-27张华耿亚松王倩付东鹤唐洪影杨玲董莉真吴高鹏李桂柃李天宁袁玉华
张华,耿亚松,王倩,付东鹤,唐洪影,杨玲,董莉真,吴高鹏,李桂柃,李天宁,袁玉华
天津医科大学总医院空港医院,天津300308
2019年12月以来,全球各地陆续发现不明原因引起的肺炎病例,通过对患者呼吸道标本病毒全基因组测序、核酸检测等多种方法证实,该病毒是一种从未在人体内发现的β属冠状病毒新毒株[1],WHO将其命名为新型冠状病毒(SARS-CoV-2)。目前全球累计新型冠状病毒肺炎确诊病例超过1亿例,死亡人数逼近300万,已经发展为全球性公共安全卫生事件[2]。实时荧光定量PCR核酸检测是诊断SARS-CoV-2感染的金标准,但仍存在一定的局限性[3],临床中可能出现影像学诊断、临床表现与核酸检测结果不相符的现象[4]。同时核酸检测存在方法学局限性,目前无法进行定量检测,不能对病情发展进行动态监测。血液样本易获取、稳定、可定量检测,因此血清IgM/IgG抗体检测可弥补核酸检测的不足,避免因采样原因造成的假阴性,可与核酸联合检测用于疑似患者的确诊[5-6]。目前对于SARSCoV-2抗体血清学的发生发展机制尚不明确。龙泉鑫等[7]分析了新型冠状病毒感染机体后抗体的变化规律,在症状发作后19 d内,所有患者特异性IgG抗体检测均呈阳性,表明抗体检测对疾病的诊断和监测具有重要意义。为进一步落实对病例的早发现、早报告、早隔离、早治疗的防控政策,全国将进行重点人群核酸检测、抗体检测,因此抗体检测系统的能力与质量尤为重要。我们收集了本院2020年3~4月的SARS-CoV-2抗体检测数据,对三种化学发光系统IgM/IgG检测结果进行一致性评价,将定性结果与临床诊断结果进行验证,探讨新型冠状病毒IgM/IgG抗体检测的临床价值,为新型冠状病毒感染的诊断与预后提供参考。
1 材料与方法
1.1 材料
1.1.1 标本来源 收集天津医科大学总医院空港医院收治的入境筛查者的血清样本。其中SARSCoV-2核酸检测阳性23例,符合《新型冠状病毒肺炎诊疗方案(第七版)》中的诊断标准[8],确诊为SARSCoV-2感染;核酸检测阴性23例,来自同期健康人群,均无临床症状,无其他基础疾病。
1.1.2 仪器与试剂 重庆博奥塞斯Axceed260化学发光测定仪及其配套试剂(IgM批号G202004313,IgG批号G202004313),深圳亚辉龙iModules化学发光测定仪及其配套试剂(IgM批号20200202,IgG批号20200202),天津丹娜生物Smart 500S化学发光测定仪及其配套试剂(IgM批号20200401,IgG批号20200401)。
1.2 检测方法 采集受试者静脉血3 mL,置于含分离胶的真空采血管,3 500 r/min离心10 min,56℃水浴箱中灭活30 min。将上述3个化学发光测定系统(包括仪器与其配套试剂)随机编号为A、B、C,使用3个系统分别对46份样本进行SARS-CoV-2 IgM和IgG抗体检测,严格按照仪器和试剂说明书操作。根据样本的S/CO值进行结果判断,S/CO值=样本发光值/cut-off值。S/CO值<1.0判定为阴性,≥1.0判定为阳性。
1.3 精密度验证 采用各检测系统厂家提供的配套SARS-CoV-2质控品进行精密度验证。参考美国临床实验室标准化协会(CLSI)EP15-A3方案,使用A、B、C系统分别检测高、低水平的质控品,每天5次,连续5天,计算各水平的批间精密度,并与试剂说明书中厂家声明的产品性能指标进行对照。
1.4 方法学比对 参考CLSI EP9-A3方案[9-10],用Medcalc18.0软件对A、B、C 3个系统SARS-CoV-2 IgG、IgM检测结果进行离群值检验,使用passingbablok回归模型对3个检测系统结果两两比较(AvsB、AvsC、BvsC),显示回归方程y=a+bx,并计算各组合的相关系数(r)、截距、斜率及95%C I;将3个系统检测IgG、IgM定性结果分别与鼻/咽拭子核酸检测结果进行比对,采用χ2检验对定性结果与临床最终诊断结果进行差异性分析,以(真阴性+真阳性)/总例数计算抗体检测结果与核酸检测结果的符合率。
2 结果
2.1 三种系统抗体检测精密度验证结果 A、B、C系统检测IgG抗体的精密度分别为4.59%~5.08%、4.40%~4.91%、4.25%~8.09%,符合厂家声明的检测结果变异系数<15%、<10%、<15%;检测IgM抗体精密度分别为4.92%~5.39%、3.97%~4.19%、4.18%~8.44%,符合厂家声明的检测结果变异系数<15%、<10%、<15%。
2.2 抗体定量检测比对结果
2.2.1 IgG抗体定量检测比对结果 对三种系统IgG抗体的检测结果进行passing-bablok回归分析,回归方程分别为AvsB:y=0.0253+0.173x、AvsC:y=0.0172+0.0338x、BvsC:y=0.194+0.761x,两两比对,A系统与B系统的相关性最佳(r=0.871,P<0.05)。见表1。
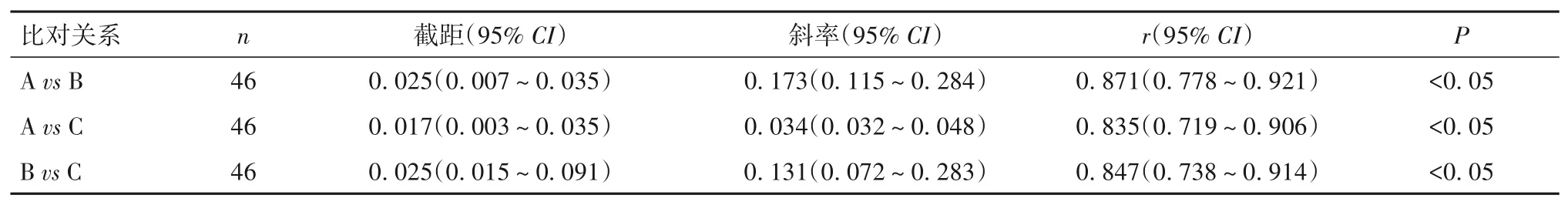
表1 三种系统检测IgG抗体的passing-bablok回归分析结果
2.2.2 IgM抗体定量检测比对结果 对三种系统IgM抗体结果进行passing-bablok回归分析,回归方程 分 别 为AvsB:y=0.025 3+0.194x、AvsC:y=0.006 9+0.098 5x、BvsC:y=0.091 9+0.44x。两两比对,A系统与C系统的相关性最佳(r=0.885,P<0.05)。见表2。

表2 三种系统检测IgM抗体的passing-bablok回归分析结果
2.3 抗体定性检测比对结果
2.3.1 IgG抗体定性检测比对结果 三种系统IgG抗体定性检测结果与核酸检测结果符合率为91.3%~95.6%,三种系统与核酸检测结果差异均无统计学意义(P均>0.05)。见表3。
2.3.2 IgM抗体定性检测比对结果 三种系统IgM抗体定性检测结果与核酸检测结果符合率为65.2%~86.9%,A系统、C系统与核酸检测结果存在明显差异(P均<0.05),B系统与核酸检测结果无明显差异(P>0.05)。见表4。

表3 三种系统IgG抗体定性检测结果与核酸检测结果一致性比对[例(%)]
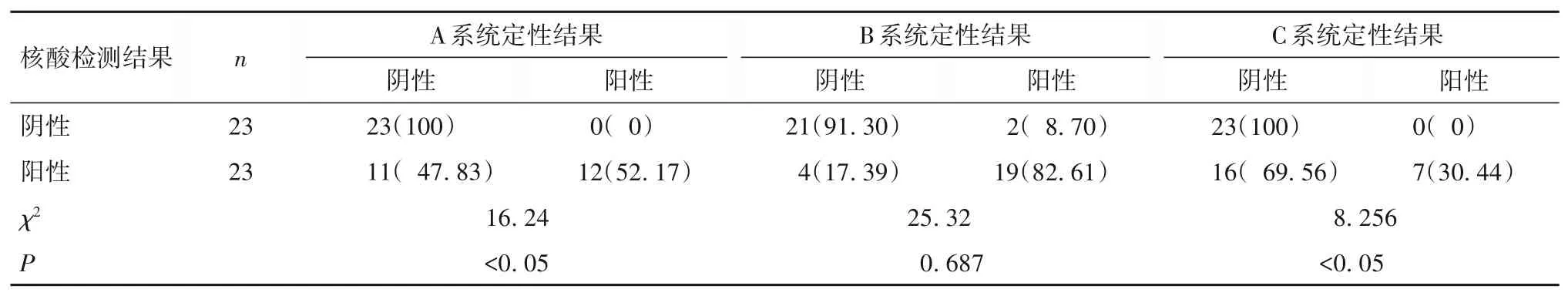
表4 三种系统IgM抗体定性检测结果与核酸检测结果一致性比对[例(%)]
3 讨论
《新型冠状病毒感染的肺炎诊疗方案(第七版)》中提出,确诊病例应包含以下三者之一:①实时荧光定量PCR检测新型冠状病毒核酸阳性;②病毒基因测序与已知的新型冠状病毒高度同源;③血清新型冠状病毒特异性IgG、IgM抗体阳性[8]。《新型冠状病毒感染的肺炎诊疗方案(第八版)》将特异性IgM抗体阳性作为疑似病例诊断依据之一[11],SARS-CoV-2特异性抗体检测有着不可替代的重要临床和公共卫生价值[12]。
本研究中的三种检测系统均采用磁微粒化学发光法,结果显示三种系统检测SARS-CoV-2特异性IgG、IgM抗体的精密度均符合厂家声明的生物医学变异范围,可保证检测结果的重复性。对三种系统特异性IgG抗体定量结果进行passing-bablok回归分析,回归方程的r为0.835~0.871,截距为0.017~0.025,斜率为0.034~0.173,r均大于0.8,表明三种系统的结果两两比较均高度相关,其中A系统与B系统间相关性最佳;同时三种系统特异性IgG抗体定性结果与核酸检测结果符合率为91.3%~95.6%;对三种系统特异性IgM抗体定量结果进行passing-bablok回归分析,各回归方程r为0.671~0.885,截 距 为-0.09~0.025,斜 率 为0.098~0.437,三种系统结果两两之间相关性良好,以A系统与C系统的相关性最佳;三种系统SARS-CoV-2特异性IgM抗体定性结果与核酸检测结果符合率为65.2%~86.9%。
本研究结果显示,三种系统IgG检测结果一致性良好,与临床诊断符合率高;而IgM各系统间检测结果一致性并不理想,与最终临床诊断也存在差异。其原因可能与以下因素有关:①试剂盒抗原质量、包被质量、标记物包被质量等都会对检测结果产生影响[13];②试剂包被抗原点位的选择不同可导致不同品牌试剂检测结果存在差异;③IgM抗体是病毒感染后首先产生的抗体,本身维持时间短,存在检测的空窗期,导致在感染早期或末期可能无法测出;④不同厂家采用的原理不同,检测灵敏度也不同。
由于抗原抗体反应的特殊性,难免会出现假阳性结果,对临床诊断造成一定的困扰。结合本实验室工作实际,假阳性结果与以下因素有关:①阳性预判值设定过低。阳性判断值一般是通过测定大量的阴性人群和一定数量的已知阳性人群标本,对结果进行统计后得到阳性预判值,由于统计学方法的局限性,不可避免地会有一部分弱阳性结果实际上为假阳性。同时,由于不同厂家的灵敏度和特异度存在差异,阳性预判值的设定原则也不相同,也会造成不同仪器检测结果间的差异。②血清中存在内源性的干扰物质,如类风湿因子、嗜异性抗体、溶菌酶、补体和因使用鼠抗体治疗而产生的抗鼠抗体等,均可能产生非特异性的结合,造成假阳性结果。③外源性干扰物质,如标本溶血、细菌污染、标本贮存时间过长、标本凝固不全等,可能影响化学发光反应过程,造成假阳性。④环境因素:因生物安全的要求,在日常工作中检验科要用到含氯消毒剂喷洒或过氧化氢喷雾,空气中存在强氧化剂,可能干扰底物发光反应过程,造成假阳性。
SARS-CoV-2是一种新发病原体,目前对该病毒检测方法性能的了解仍有限,需要更多的临床研究以提高不同检测方法的效能。血清学检测目前不单独作为SARS-CoV-2感染的诊断依据,化学发光法检测SARS-CoV-2抗体可以提供较高的灵敏度和特异度,是SARS-CoV-2感染筛查、诊断、疗效监测及流行病学调查的重要检测手段[14-15]。
