静电纺短纤维的制备及其生物医学应用
2021-05-27张蓓蕾沈明武史向阳
张蓓蕾, 沈明武, 史向阳
(东华大学 化学化工与生物工程学院, 上海 201620)
随着纳米技术的发展以及高分子材料的出现,合成纳米纤维逐渐被人们熟知并被广泛应用于催化、能源、生物医学等领域。在众多合成纳米纤维的制备方法中,静电纺丝以其简单快捷、经济高效的特点被重视起来。该技术通过在设定的参数条件下对高分子聚合物进行加工从而得到具有纳米级尺寸的纤维支架,主要具有以下优点:设备成本低,装置简单,易于操作;可实现纤维取向、结构、形貌调控;可一步合成复合/多功能纳米纤维材料。典型的静电纺装置主要由高压电源、注射泵、喷丝头和接收器组成[1]。在静电纺丝过程中,喷丝头与接收器之间会存在一个高压静电场,从注射泵推出的聚合物液体(或熔体)经过喷丝头时,液体表面产生的静电排斥作用会克服表面张力使得液体被拉伸为圆锥状,形成射流。射流在喷发进程中直径减小、溶剂挥发,最终固化为非织造纤维毡收集在接收器上。
大多具有良好生物相容性和可降解的合成聚合物如聚己内酯(PCL)、聚乳酸(PLA)和聚乳酸-羟基乙酸(PLGA),以及天然生物聚合物如丝素蛋白、壳聚糖、海藻酸盐、胶原蛋白(collagen)和明胶(gelatin)等,都可用来制备静电纺纳米纤维。通过静电纺丝成功制备出的聚合物纳米纤维性能是由溶剂、聚合物溶液、环境条件和电压、流速、接收距离等工艺参数共同决定的[2]。
由于具有比表面积大、孔隙率高、易于修饰等优良特性,静电纺纳米纤维最早被用作过滤材料以捕获溶胶粒子[3],现如今在生物医学领域引起极大关注,并且在药物控释、组织工程及癌症研究等方面得到了很好的应用[4-5]。例如,Hu等[6]制备出聚癸二酸甘油酯-聚甲基丙烯酸甲酯(PGS-PMMA)/gelatin静电纺复合纳米纤维膜,再将大鼠PC12细胞接种到纳米纤维上,研究其对神经再生的潜力,发现PGS-PMMA/gelatin静电纺复合纳米纤维能够促进细胞增殖,诱导神经干细胞的突起生长。Qiu等[7]制备的聚电解质表面活性剂复合物(PESCs)/PCL静电纺复合纳米纤维膜作为一种新型伤口敷料,具有良好的抗菌活性和细胞相容性,强度高,能满足临床应用的需求。Zhao等[8]研发的经透明质酸(HA)修饰的静电纺聚乙烯醇/聚乙烯亚胺(PVA/PEI)纳米纤维膜具有特异性捕获CD44受体过表达癌细胞的卓越能力,还能够用于捕获癌细胞以达到早期肿瘤诊断的目的。
尽管这些静电纺纳米纤维膜在生物医学领域已有所贡献,但其较小的孔径尺寸限制了氧气和营养物质的扩散,阻碍了细胞的渗透,传统单一的二维结构无法完全模拟允许细胞生存的三维立体微环境[9]。其次,在癌症治疗等方面也难以达到微创治疗的效果。为了解决以上缺陷,研究者们试图通过直接调节静电纺的工艺参数,如电压、流速、聚合物溶液浓度,或者通过后续处理的方式开发出更多的新型纳米纤维材料。近年来,静电纺短纤维被广泛用于构建可注射药物载体[10]、纳米纤维气凝胶[11]以及三维细胞模型[12]等多种仿生材料,在组织工程、癌症治疗等方面都具备无限的发展潜力;但是人们对短纤维的认知不够系统和全面,本文结合国内外相关文献综述了静电纺短纤维的制备及其功能化的方法,分类介绍了功能化短纤维在生物医学领域中的应用,并结合静电纺短纤维当前的发展,分析了其在生物医学领域应用中所面临的挑战和发展前景。
1 制备方法
静电纺短纤维可通过一步电喷和后续工艺处理获得,后续工艺包括均质处理、超声破碎和冷冻切片3种。在制备短纤维时,要根据纳米纤维的力学强度、短纤维长度、静电纺溶液所用溶剂来选取最适用的方法。
1.1 一步法
聚合物的相对分子质量、浓度、溶剂会影响聚合物溶液的黏度,而黏度是影响静电纺纤维形态的重要因素。在静电纺过程中,当聚合物溶液的黏度低于一定程度,溶液无法延展为连续且细长的纤维,而是以电喷雾的形式断裂为短纤维或者球形颗粒[13],并且可通过调节电压、流速、收集距离等参数改变短纤维的长度。Fathona等[14]通过简单的一步静电纺丝直接制备聚合物短纤维,并且研究了聚合物溶液浓度、外加电压和流速对短纤维制备的影响。通过对不同浓度纤维素醋酸酯溶液进行电喷,发现聚合物溶液质量分数在13%~15%之间时能够得到长度为50~150 μm的短纤维,而低于或高于这一浓度范围得到的分别是串珠纤维和连续纤维,并且短纤维的长度随着流速的增加而增加,随着电压的增加而减小。Luo等[15]研究了在短纤维制备过程中不同溶剂体系对短纤维尺寸的影响,在其他纺丝条件相同的情况下,以丙酮、乙酸甲酯/环己酮和甲醇作为聚甲基硅倍半氧烷的溶剂体系,分别得到了连续纤维、串珠纤维和长径比小于200的短纤维。
虽然这种方法不经过后续二次加工,但是在电喷过程中变量较多,纤维的形貌和尺寸难以控制,往往会伴随串珠纤维、水滴状颗粒或者球形颗粒的产生;因而需要从多个方面不断优化工艺条件。
1.2 后续工艺
1.2.1 均质处理
均质处理是借助均质刀头在高速运转时产生的机械剪切力将纳米纤维膜破碎为一定长度的短纤维。Li等[16]利用此方法获得了Fe3O4/PLGA短纤维。首先,将Fe3O4/PLGA静电纺纳米纤维膜剪成为1 cm×1 cm大小的碎片,然后浸泡在乙二醇溶液中,在16 000 r/min转速下均质处理30 min,最后得到平均长度为(11.90±2.03) μm的短纤维。Li等[17]将0.83 mg边长为0.5 cm的聚酰胺酰亚胺/双马来酰亚胺(PAI/BMI)正方形纤维碎片浸在100 mL水/正丁醇混合溶液里,在1 500 r/min转速下均质处理20 min后得到平均长度为41.8 μm的短纤维。均质处理的转速越高、时间越长,得到的短纤维也越均匀。除此之外,影响短纤维尺寸和形貌的因素还包括分散液种类以及纤维材料的亲疏水性。Yoshikawa等[18]分别对接枝和不接枝亲水聚苯乙烯磺酸钠(PSSNa)的苯乙烯和4-乙烯基苄醇的无规共聚物(poly(ST-r-VBP))纳米纤维进行均质处理,最终发现,后者在均质过程中因纤维的疏水特性使其能够逃离水溶液然后聚集在水-气界面,而含有PSSNa的纤维在机械剪切3 h后获得了分散均匀的短纤维乳状液。综上,在均质处理疏水性纤维时,需要在水分散液中加入具有密度差的亲油性物质如己烷,纤维碎片会聚集在形成的水-油界面而无法避开机械剪切作用力,促进了对纳米纤维的切割。
总的来说,均质处理虽然难以获得尺寸均一的短纤维,但其操作简单,成本较低,产率较高,在数量上可满足后续对短纤维进行一系列改性和物理组装的要求。
1.2.2 超声破碎
利用超声破碎法制备静电纺短纤维的原理是超声探头刺激液体介质产生密集的小气泡,小气泡立即爆破,释放出的能量可将静电纺纳米纤维膜破碎成微米长度的短纤维。超声破碎的参数包括振幅、频率和时间,振幅和时间的增加有利于制备长度更短的短纤维。需要注意的是,在超声过程中,温度会逐渐升高,功率越大,温度上升的越快。温度的升高会对材料的力学性能或者化学性质产生影响,所以通常都是在冰浴条件下进行超声。Boda等[19]制备了PLGA/gelatin静电纺纳米纤维,剪成小块后在振幅为20%的超声条件下冰浴破碎20 min,获得了长度分布在20~80 μm之间的短纤维。
文献[20]研究表明,静电纺纳米纤维膜的韧性是影响短纤维制备的主要因素。对于脆性纳米纤维如聚苯乙烯(PS),在超声60 s后便得到了(10.5±6.2) μm长度的短纤维。韧性越强的纳米纤维越能够抵抗超声波处理过程中产生的变形,无法直接有效地获得短纤维,因此,在超声破碎之前需要对具有良好延展性的纤维进行额外处理,即制造纤维的受力薄弱点。Friedemann等[21]所采取的策略是将PS颗粒作为孔洞前驱体加入到PVA/SiO2纤维中,高温煅烧后的纤维在PS颗粒嵌入处出现孔洞,在超声破碎时有利于纤维断裂。Zhang等[10]也采用了类似的策略,用NaCl颗粒作为前驱体来制造纤维孔洞,经超声破碎后可获得(8.6±2.0) μm 长度的短纤维,且NaCl颗粒含量越高,短纤维的长度越短。
超声破碎的作用力对于固态且具有一定韧性的纤维来说作用力较弱。在进行额外处理时,作为空隙前驱体的纳米颗粒在纤维基体的分散性和均匀性也不易把控,得到的短纤维长短不一,因此超声破碎也存在一定的局限性。
1.2.3 冷冻切片
冷冻切片是将取向的纤维膜沿着垂直于纤维取向的方向折叠为1~2 cm的宽度,将折叠好的纤维冻存在有包埋剂的容器中,然后在冷冻切片机中固定并沿着垂直于纤维取向的方向切割成一定厚度的薄片,最后将其分散在溶液中,从而获得短纤维[22]。相比于前2种方法而言,冷冻切片最大的优势在于能够设置短纤维切割的长度,因此可以得到尺寸均一的短纤维。Wei等[23]为了建立HepG2体外肿瘤模型,首先在高速转动的滚筒上收集取向PMSA(聚苯乙烯-马来酸酐)/PS纳米纤维膜,然后通过冷冻切片法获得长度分别为20、50和80 μm的短纤维。Omidinia-Anarkoli等[24]使用跨度为2 cm宽的平行板收集到取向PLGA纳米纤维膜,用通过冷冻切片后得到的短纤维来制备混合水凝胶。
一般而言,所用原料的玻璃化转变温度低于常温的纤维膜会较多采用此方法来制备短纤维,超声和简单的机械剪切力不足以克服纤维所具有的黏弹力而使它破碎[19]。比如,John等[25]通过静电纺丝制备了PCL/gelatin取向纳米纤维,而PCL的玻璃化转变温度为-50 ℃,于是在-20 ℃的环境下通过冷冻切片获得短纤维。
冷冻切片法所有的流程操作相比于前2种方法而言更耗时耗力,成本较高。通过冷冻切片得到的短纤维会出现分散性不好的情况,这就对取向纳米纤维的厚度、力学强度、润湿性有一定的要求,需要进一步探索和优化条件。
2 功能化
纳米短纤维由于其特有的尺寸及形貌,不仅能够用于微创治疗,还被用来组装三维支架材料应用于组织工程。微创治疗充分利用了短纤维独特的可注射性,在治疗的同时避免二次创伤以减轻患者痛苦。多孔三维支架结构可模拟结构复杂的组织原生微环境,为体外细胞的培养提供良好的生长增殖环境,然而,仅仅依靠单一的聚合物纤维材料不能够满足生物医学应用中的多个需求,如靶向识别,局部缓释药物以及指导细胞的行为;因此,研究人员想办法对短纤维进行功能化以发掘短纤维更多的功能,其方法主要有物理掺杂、化学键合和综合改性3种。
2.1 物理掺杂
物理掺杂是将纳米颗粒、化合物等物质与聚合物溶液共混,在不发生化学反应的情况下通过静电纺丝就能够将功能化物质包覆在纤维中,从而获得功能化的短纤维。例如,Omidinia-Anarkoli等[24]在静电纺丝之前于PLGA溶液中混合平均直径为5.2 nm的超顺磁氧化铁纳米颗粒(SPION),通过测试可知SPION均匀地分布在PLGA纤维内部,所获得纤维的平均直径不受SPION掺入的影响,随后通过超声处理获得具有磁响应的短纤维,最后将其分散在水凝胶前体溶液中,向该混合物施加低磁场(300 mT),在水凝胶交联之前诱导短纤维取向,从而获得具有各向异性以及具有骨髓修复功能的水凝胶。热重分析表明,在短纤维生产过程中,SPION包封效率为78%。除此之外,Feng等[26]在掺杂Fe3O4纳米颗粒的同时还向聚丙烯腈(PAN)静电纺溶液中加入氧化石墨烯(GO),GO的亲水性含氧基团赋予其与蛋白质相互作用的能力,具有良好的生物效应,可引导细胞行为,通过对PAN纳米纤维的均质处理,最终获得生物安全性高且能够指导细胞行为的功能化短纤维。另一项研究中,Weng等[11]制备了由静电纺PLGA-collagen-gelatin(PCG)纤维和生物活性玻璃(BG)纤维组成的超轻三维杂化纳米纤维气凝胶。在纺丝之前向BG电纺溶液中加入特定质量的Sr(NO3)2和特定体积的CuCl2水溶液,Sr2+和Cu2+的引入使得BG短纤维具有促进新骨和血管形成的功能。将PCG短纤维与功能化的BG短纤维在超声破碎时混合,最后通过冷冻浇注法获得纳米纤维杂化气凝胶。
除了赋予短纤维指导细胞行为的功能,还可通过与化疗药物物理掺杂使短纤维具有局部治疗效果。短纤维对药物来说是一种良好的载体,通过原位注射将药物递送到受损或病变部位,实现药物的局部释放以及缓释作用。例如,Wei等[27]将质量比为50∶1的聚乳酸聚乙二醇(PELA)与羟基喜树碱(HCPT)的混合溶液先静电纺丝为纳米纤维膜,然后通过冷冻切片制备出具有抗肿瘤功能的短纤维。在另一项研究中,Zhang等[10]用同样的方法制备了载有阿霉素(DOX)的短纤维,并验证了载有DOX短纤维比载有DOX微球的抗肿瘤效果更为显著。为了进一步提高短纤维对肿瘤的杀伤力,He等[28]制备出一种同时具有靶向识别与双重刺激响应功能的短纤维,将喜树碱(CPT)共轭胶束聚合物(PMCPT)与CDM (2-丙-3-甲基马来酸酐)/PELA聚合物溶液共混,得到包覆PMCPT的短纤维。PMCPT在肿瘤酸性微环境中经释放后会自组装为胶束(MCPT),经靶向识别和刺激响应后释放抗癌药物CPT。
物理掺杂的优点是简单易操作,方便快捷,包封率高,而且不要求纳米纤维材料具有某些特定的官能团,因此选择性多;但此方法首先得到的是包覆有功能化物质的纤维膜,因此在制备短纤维的后续处理中难免会有损失。
2.2 化学改性
化学改性是聚合物或纳米纤维与修饰物所具有的官能团之间发生化学反应形成新的化学键,从而将功能化物质固定在纤维表面,最终得到功能化短纤维。例如,Chen等[29]为了合成双亲性聚合物(PMCPT)结合的短纤维,首先通过PLA本体的开环聚合、末端叔丁氧羰基脱保护以及酰化反应合成了2-丙-3-甲基马来酸酐(PLA-cdm),再采用标准EDC/NHS(1-(3-二甲基氨基丙基)-3-乙基碳二亚胺盐酸盐/羟基琥珀酰亚胺)化学方法将PMCPT与PLA-cdm偶联,合成了PLA-cdm-PMCPT共聚物,经静电纺丝和冷冻切片后得到了PLA-cdm-PMCPT短纤维,其在肿瘤治疗中发挥了双重响应功效,提高了对肿瘤细胞的杀伤力。Wang等[30]将聚L-乳酸(PLLA)短纤维在含有体积分数为0.5%乙二胺的异丙醇溶液中于20 ℃氨解15 min,再通过短纤维表面的氨基连接磺基-4-(N-马来酰亚胺甲基)环己烷-1-羧酸,将其作为交联剂连接神经胶质衍生的神经营养因子(GDNF,一种能促进细胞存活和轴突生长的蛋白),最后将功能化短纤维与木葡聚糖混合形成具有显著改善受损脑部环境功能的复合凝胶。
相比于物理掺杂,化学键合对纳米纤维材料有一定的要求,需要纤维表面具有丰富的官能团以提供多个结合位点,并且在修饰过程中可能会需要催化剂、连接体来提高修饰物的上载率,过程较为复杂。
2.3 综合改性
在对短纤维赋予多种功能时,仅仅依靠物理掺杂或者化学键合是难以实现的,这就考虑到将物理掺杂与化学键合相结合来对短纤维进行修饰。在本文课题组的一项研究中,Xiao等[31]首先通过静电纺丝技术将Fe3O4/PEI纳米颗粒掺杂到PEI/PVA纳米纤维中,均质处理后得到磁性纳米短纤维(MSNFs)。MSNFs表面的氨基连接3-马来酰亚胺基丙酸N-羟基琥珀酰亚胺酯,作为中间连接体将特异性靶向上皮细胞黏附分子(EpCAM)的DNA适配体修饰在MSNFs表面,得到具有磁响应和靶向识别功能的aptamer-MSNFs。John等[25]将gelatin-甲基丙烯酰基(GelMA)与PCL/gelatin共混得到了表面带有甲基丙烯酸基团的PCL/gelatin/GelMA短纤维,短纤维上的甲基丙烯酸基团与修饰肽中的辛烯基丙氨酸(OCTAL)将骨形成蛋白-2(BMP-2)和血管内皮生长因子(VEGF)模拟肽QK通过光交联成功连接到短纤维上,GelMA提供了与OCTAL的共聚合结合位点。其中,BMP-2促进骨髓源性干细胞(BMSCs)的成骨分化,QK是一种VEGF模拟肽,可复制VEGF的功能,诱导血管生成。综上,功能化短纤维可开发仿生和可注射载体来有效指导细胞应答(成骨和血管生成)。表1为文中短纤维的制备及功能化方法梳理。
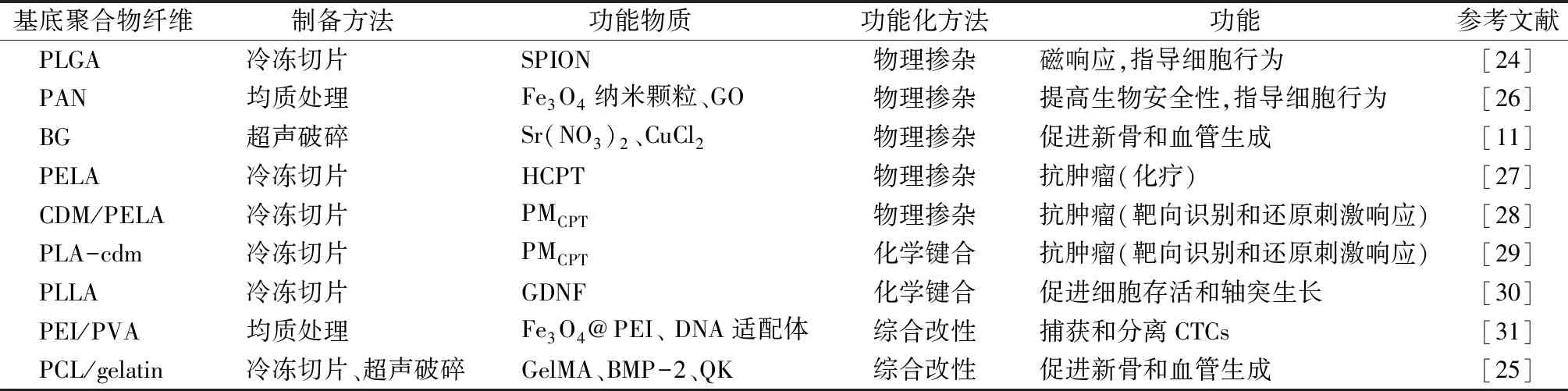
表1 静电纺短纤维的制备及功能化方法总结Tab.1 Summary of preparation and functionalization of electrospun short fibers
3 生物医学应用
3.1 诊断检测
循环肿瘤细胞(CTCs)指的是原位肿瘤发生脱落进入到血液循环系统中的癌细胞,其随着血液转移到身体的各个器官;而肿瘤转移是导致癌症患者死亡的主要原因,因此,外周血的检测与分析为癌症的诊断检测、早期治疗以及疗效评价等提供了一种有效途径[32-33]。然而,CTCs在大量血液细胞中的浓度极低(小于1.0×10-6),所以在血液样本中捕获到CTCs具有较大挑战性[34-35]。
建立一种能够对CTCs进行筛选和高效捕获的平台是提高确诊患者生存率的重要手段。目前,已经有大量研究表明静电纺纳米纤维凭借其多孔网络仿生结构以及靶向分子的表面可修饰性能够提高对CTCs特异性捕获的准确性与灵敏性[36-38]。与二维的纳米纤维毡相比,静电纺短纤维同样能够作为制备具有仿生结构的纳米支架基底材料并且进行表面功能化修饰。近年来,有研究者证实了以静电纺短纤维材料作为CTCs的捕获平台也可对癌细胞进行高效捕获与分离。例如,Xiao等[31]制备了具有磁响应和靶向识别功能的aptamer-MSNFs。通过对MCF-7细胞的捕获实验来评价aptamer-MSNFs的癌细胞捕获能力,结果表明aptamer-MSNFs能够有效捕获和快速磁性分离癌细胞,其捕获效率达到87%,而对白细胞的捕获效率仅有2%,这也说明aptamer-MSNFs的特异性捕获性能。另外通过对多种癌细胞(EpCAM阳性MCF-7、A549、HepG2细胞和EpCAM阴性HeLa细胞)的捕获验证了aptamer-MSNFs的普适性。在经过Benzonase®核酸酶对DNA适配体分解处理后,CTCs的释放效率高达90%,实现了CTCs无损释放,便于后续对CTCs进行监测分析。最后与商业磁珠(MBs)的对比研究表明aptamer-MSNFs的捕获效率(87%)与MBs(91%)的捕获效率相当,而aptamer-MSNFs对CTCs的释放效率显著高于MBs。
3.2 肿瘤治疗
在肿瘤治疗过程中,一直都存在化疗药物缺乏对肿瘤的靶向特异性选择、对人体健康组织及器官副作用大以及外科手术带来的创伤等问题。功能化载药短纤维不仅能实现对肿瘤的微创治疗,还可以将药物靶向递送到肿瘤部位并且缓慢释放,减小了全身副作用的同时还提高了抗肿瘤的治疗效果。
Chen等[29]制备了一种PLA-cdm-PMCPT短纤维。进行瘤内注射时,CDM在酸性条件下断裂而释放PMCPT,其由二硫键和HA片段构建而成,用于还原敏感释放和细胞选择性吸收。PMCPT释放之后自组装成以CPT为核、以HA为壳的MCPT。HA可识别肿瘤细胞表面过表达的CD44受体被肿瘤细胞吞噬,其次在谷胱甘肽刺激响应下二硫键断开而释放抗癌药物CPT。经体外细胞实验证实,瘤内注射短纤维可确保胶束在肿瘤组织内积聚3周以上。依靠负载PMCPT短纤维的靶向能力和双刺激响应性增强了抗癌药物对肿瘤的蓄积量以及生物利用度,显示出应对癌症化疗的治疗优势。在类似的一项研究中,He等[28]通过共混静电纺丝和冷冻切片得到载有PMCPT的短纤维。与上述不同的是,其纤维基质在肿瘤酸性微环境下分解而释放的聚合物再自组装为胶束后发生的是以叶酸介导的细胞吞噬。
3.3 组织工程
静电纺纳米纤维在组织工程领域的应用已经取得极大进展[39-41],而功能化静电纺短纤维的出现又为组织工程领域的发展提供了更多的可能性。由短纤维加工而来的微球能作为一种可注射的载体,填充不规则组织缺损。例如,John等[25]结合了静电纺丝、电喷雾和表面偶联技术将功能化短纤维加工为表面接有修饰肽BMP-2和QK的纳米纤维微球(NMs)。NMs模仿细胞外基质的特性为细胞黏附和增殖提供了一个特殊的微环境。将BMSCs分别与具有和不具有BMP-2缀合的NMs共同培养,通过对照实验证实了BMP-2多肽结合NMs在基因和蛋白水平上促进骨髓间充质干细胞的成骨分化;将HUVEC细胞分别与具有和不具有QK缀合的NMs共同培养,与没有QK的NMs相比,发现在QK偶联的NMs上形成了比没有QK的NMs更加致密、成熟的微血管网络。因此,结合修饰肽BMP-2和QK的NMs是一种先进且多功能的可注射载体,可通过微创手术将细胞输送到病变组织或组织缺损处。在另一项促进骨组织再生的研究中,Boda等[42]制备了单载阿仑膦酸钠(ALN)和ALN+E7-BMP-2的PCG矿化短纤维。ALN是一种氨基二膦酸盐,可抑制异位骨形成和软组织钙化;E7-BMP-2肽在下颌骨和颅骨缺损中诱导新骨形成。在对大鼠拔牙种植4周后,单载ALN和共载ALN-E7-BMP-2的PCG矿化短纤维的新骨体积分数和骨密度明显高于未填充的缺损,并且在新骨形成方面没有显著差异。这说明二者对临界尺寸(2 mm(直径)×2 mm(深度))的大鼠牙槽骨缺损有较好的愈合效果。有报道称高剂量的ALN可导致某些骨质疏松患者的颌骨坏死,小剂量的ALN单独使用或与E7-BMP-2肽联合使用可在手术4周后诱导适度的新骨形成。
Yu等[43]通过静电纺丝、均质处理、冷冻干燥及热处理4个步骤制备了PCL-PEG-PCL三维纳米纤维支架(TNSs),如图1所示。体外细胞实验表明,TNSs能促进L929细胞的黏附、增殖和迁移行为。TNSs的微米级多孔结构促进了氧气和营养物质在伤口和外界环境之间的渗透。在体内创面愈合实验中,TNSs的创面愈合面积在第14天缩小到7.8%,愈合速度比二维纳米纤维毡快,这也证实了细胞实验的结果,说明TNSs对创面修复有显著的促进作用。

注:(1)—采用静电纺丝法制备了PCL-PEG-PCL二维纳米纤维毡;(2)—采用高速机械切削法制备均匀短纤维溶液;(3)—冷冻 干燥后获得PCL-PEG-PCL TNSs;(4)—通过热处理 对合成的TNSs进行强化。图1 PCL-PEG-PCL TNSs 四步法制备示意图Fig.1 Schematic illustration of fabrication of PCL-PEG-PCL TNSs by a four-step process
对于疾病或创伤造成的中枢神经系统损伤修复,生物相容性良好的三维支架仿生材料可在体外促进细胞增殖、神经分化和轴突延伸,同时还影响完整大脑中宿主和嫁接神经元的存活和可塑性。除了为移植神经元提供必要的物理支持外,许多研究还强调了借助营养蛋白和引导因子来增加植入细胞存活和整合的能力。Wang等[30]制备了一种载有GDNF的短纤维与木葡聚糖的复合热敏性凝胶支架。体外细胞实验证实,该支架促进了腹侧中脑(VM)多巴胺祖细胞的生长,并持续递送GDNF,促进细胞存活和多巴胺能神经元轴突的生长。在以帕金森氏病小鼠为模型的动物实验中发现,该复合支架可提高VM移植物的存活和纹状体的神经支配,GDNF的输送可增强这种效果。综上所述,该功能化复合支架提供了一种显著改善受伤脑部环境的手段,从而能够提高植入脑细胞存活率和嫁接神经元的整合。此类复合支架的实用性,其他功能蛋白的掺入以及对多能干细胞来源的神经元的影响,将来可能会显著地促进细胞治疗,以治疗神经退行性疾病。
4 结束语
静电纺短纤维具有可注射性以及后续加工操作的灵活性,因此在生物医学领域得到了广泛的应用。在癌症研究方面,功能化短纤维可用于CTCs的特异性捕获与无损释放,为癌症患者的早期诊断、临床结果预测和治疗效果监测提供了一项有前景的新策略。其次,功能化短纤维能够在肿瘤治疗阶段以微创治疗的方式注入肿瘤部位,并发挥靶向识别、缓释给药等多重作用来抑制肿瘤生长。对于组织修复与再生而言,短纤维主要被用于制备仿生三维立体支架材料以填补组织缺损部位。与大多数自组装而成的支架材料相比,这种通过低温冷却剂将短纤维以物理聚集的方式形成多孔三维立体支架的方法更具有普适性。
相比于静电纺纳米纤维膜,短纤维在癌症研究和组织工程领域应用的探究还远远不够。为进一步提高对肿瘤细胞的杀伤力,应充分结合短纤维的3种功能化途径,将光疗、热疗以及化疗等多重治疗机制相结合。三维多孔仿生支架除了对缺损部位进行修复以外,还能够建立体外肿瘤模型,通过在体外分析肿瘤生理特性并对药物安全性及疗效进行评估,为药物筛选提供参考途径。
