经皮黄疸测定仪检测新生儿总胆红素水平的可靠性分析
2021-05-20黄循斌程国强丘惠娴
黄循斌,程国强,丘惠娴*
(1.深圳市龙岗中心医院新生儿科,广东深圳 518116;2.复旦大学附属儿科医院新生儿科,上海 201102)
新生儿高胆红素血症(neonatal hyperbilirubine⁃mia)是指由于疾病或某些致病因素所引起血清胆红素超过生理性黄疸的诊断标准,亦称为病理性黄疸,是新生儿最常见的疾病之一〔1-2〕。如果严重的高胆红素血症不积极治疗,过高的非结合胆红素可通过血脑屏障进入脑组织,主要累及基底核的神经核团,损害神经元的细胞膜及细胞内的各种生物膜,引发胆红素脑病,遗留锥体外系、注视障碍、听力损害、牙釉质发育不良等后遗症,严重者可导致死亡〔3-4〕。因此,快速、准确、动态监测胆红素水平对指导治疗非常重要。全自动生化分析仪检测血清总胆红素(serum total bilirubin,STB)具有准确性高、干扰因素少等优点,且能区分非结合胆红素和结合胆红素,但测量STB需要专业技术人员采血,并通过离心、特定仪器读数后才能得到结果,且为有创操作,增加了患儿的痛苦,不适宜快速、反复监测胆红素水平〔5-6〕。目前使用的日本美能达经皮黄疸测定仪(JM-103型)检测新生儿总胆红素(total bilirubin,TBIL)已广泛用于临床,因其具有无创、安全和方便的特点,深受临床医务工作者的欢迎〔7〕,但其检测TBIL的可靠性仍需进一步研究。本研究回顾性分析2017年6月至2019年6月在深圳市龙岗中心医院收治的新生儿高胆红素血症患儿,同步使用经皮黄疸测定仪和全自动生化分析仪检测TBIL值,评价其相关性和一致性。
1 方法
1.1 纳入标准 回顾性分析2017年6月至2019年6月在深圳市龙岗中心医院新生儿科住院的所有新生儿高胆红素血症患儿。入组标准:①胎龄≥35周;②黄种肤色患儿;③STB≥221µmol∕L。
1.2 排除标准 血清结合胆红素>34µmol∕L或结合胆红素超过血清总胆红素20%以上的患儿。
1.3 分组 2014年中华医学会儿科学分会新生儿学组既参考美国儿科学会2004年发表的“胎龄≥35周新生儿高胆红素血症处理指南”,又结合我国实际情况制定了“新生儿高胆红素血症诊断和治疗专家共识”。本研究根据指南将全自动生化分析仪检测的TBIL值分为3组,其中TBIL 221~342µmol∕L纳入中度黄疸组(即中度高胆红素血症组)、343~427µmol∕L纳入重度黄疸组(即重度高胆红素血症组)、>427µmol∕L纳入极重度黄疸组(即极重度高胆红素血症组)。
1.4 TBIL的检测 患儿入院后由新生儿科医生立即使用经皮黄疸测定仪检测TBIL,检测部位为前额两眉心、胸骨两部位,计算出其平均值。同时用促凝管采集外周静脉血2 mL,由生化室检测人员采用全自动生化分析仪(UniCel DxC 800 Synchron,贝克曼库尔特,美国)严格按照仪器说明书在2 h内检测TBIL。
1.5 资料收取 从电子病例系统中筛选符合纳入标准的新生儿高胆红素血症病例,调取入院当天首次同步使用经皮黄疸测定仪及全自动生化分析仪检测的TBIL值。
1.6 统计学分析 采用SPSS 22.0和MedCalc 12.1软件进行统计学分析。计量资料符合正态分布时以(xˉ±s)表示,计数资料采用[n(%)]表示。多组间比较采用单因素方差分析,经皮黄疸测定仪和全自动生化分析仪测定的TBIL值进行配对t检验。采用Spearman相关系数和Bland-Altman散点图分析评价两种检测方法所测TBIL的相关性和一致性。P<0.05为差异有统计学意义。
2 结果
2.1 一般情况 研究期间共收治新生儿高胆红素血症患儿508例,符合纳入标准383例,根据全自动生化分析仪检测的TBIL值分为3组,其中,中度黄疸组198例、重度黄疸组120例、极重度黄疸组65例。3组患儿的性别、胎龄、体质量、Apgar评分(新生儿评分)和入院日龄的差异均无统计学意义(P>0.05)。见表1。
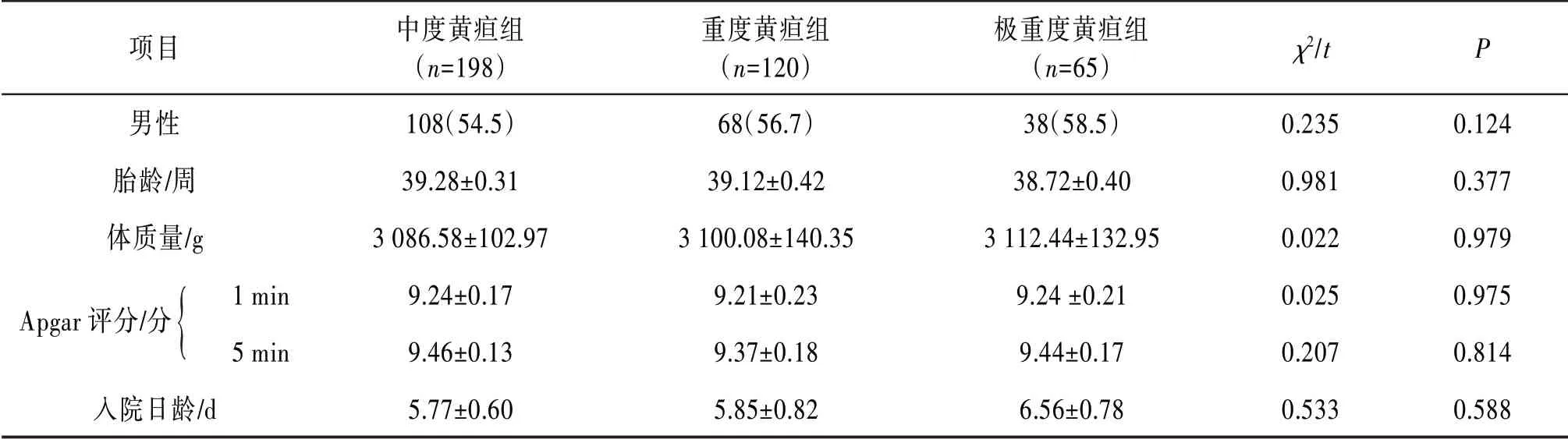
表1 不同组别高胆红素血症患儿的一般情况[n(%),xˉ±s]
2.2 经皮黄疸测定仪和全自动生化分析仪检测TBIL值比较 经皮黄疸测定仪检测TBIL值在中度黄疸组和重度黄疸组均高于全自动生化分析仪对应组的TBIL值,差异有统计学意义(P<0.01),在极重度黄疸组低于全自动生化分析仪,差异有统计学意义(P<0.01)。见表2。
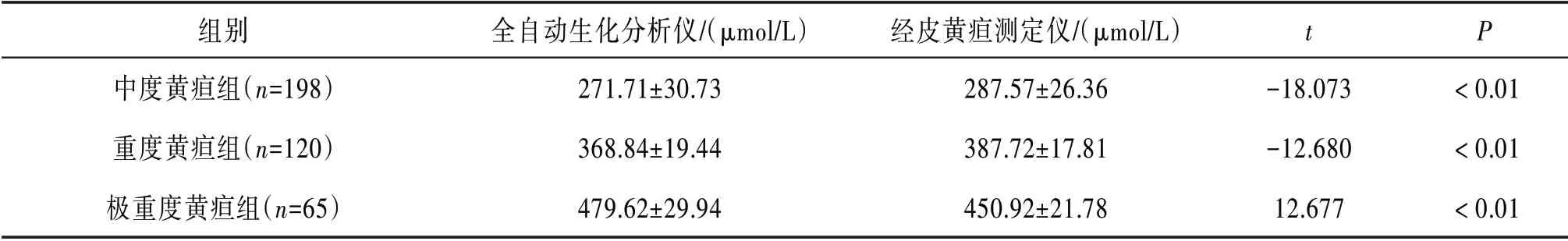
表2 两种检测方法测定的TBIL值比较(xˉ±s)
2.3 经皮黄疸测定仪和全自动生化分析仪检测TBIL值的相关性 经皮黄疸测定仪和全自动生化分析仪两种方法检测TBIL值呈显著正相关(r=0.973,P<0.01);中度黄疸组、重度黄疸组和极重度黄疸组两种方法检测TBIL值的相关系数分别为0.918、0.825和0.796(P均<0.01)。见图1。
采用MedCalc 12.1得到的Bland-Altman散点图分析经皮黄疸测定仪和全自动生化分析仪检测TBIL值的一致性,两种方法检测TBIL值的平均偏倚为(-7.10±22.58)µmol∕L,95%CI为(-51.6~36.9)µmol∕L,TBIL值在95%CI以外者占7.0%(27∕383);中度黄疸组、重度黄疸组和极重度黄疸组患儿的TBIL值平均偏倚分别为(-15.90±12.35)、(-12.90±11.12)和(28.70±18.27)µmol∕L,95%CI分别为(-40.1~8.3)、(-34.7~8.9)和(-7.1~64.5)µmol∕L,TBIL值在95%CI以外者分别占3.0%(6∕198)、7.5%(9∕120)和4.6%(3∕65)。见图2。
3 讨论
20世纪80年代起临床上开始应用经皮黄疸测定仪检测TBIL,其机理是根据皮肤颜色反射光线分别经过机器内的蓝光滤光器和绿光滤光器,被发光二极管转换为电讯号,故会受到肤色深浅、血红蛋白、黑色素、真皮厚度等因素的影响,可靠性不高。目前国内广泛使用的日本美能达经皮黄疸测定仪(JM-103型)改进了电路和光路,减少了肤色差异等因素对结果的影响,并且可以储存数据及随时求均值〔8〕,但其可靠性相关研究不多。

图1 两种检测方法测定的TBIL值线性回归图
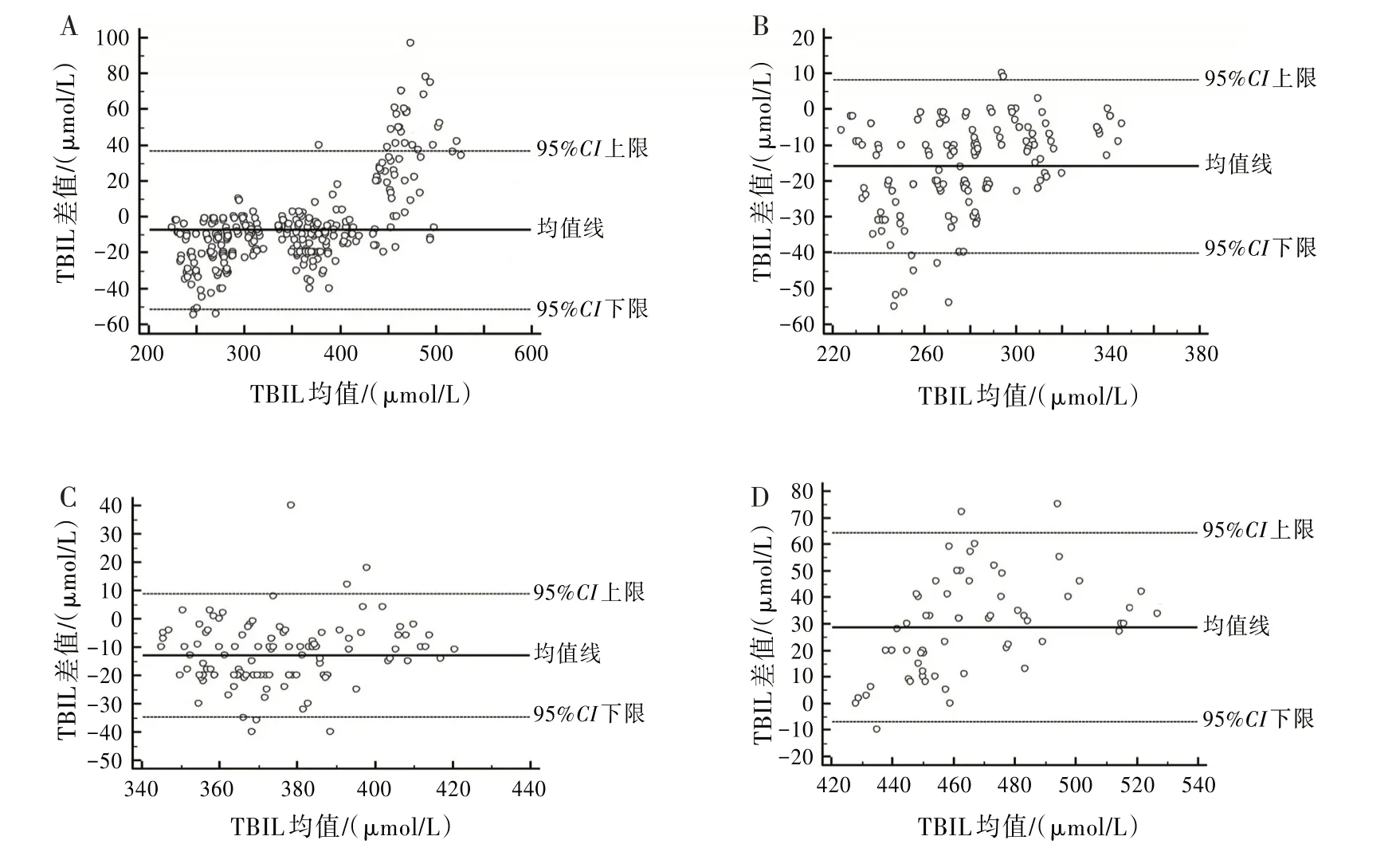
图2 Bland-Altman散点图
美国儿科学会相关指南提出经皮黄疸测定仪测定的TBIL百分位曲线图可代替足月新生儿小时STB百分位曲线图预测新生儿高胆红素血症及制定随访计划〔9-10〕。Yu等〔11〕采用系统评价的方法研究新生儿小时STB和经皮黄疸测定仪测定的TBIL,发现两种检测方法对新生儿高胆红素血症的预测价值相当(AUC分别为0.819、0.817)。Srinivas等〔12〕分析足月新生儿出生后(36±2)h的经皮胆红素(trans⁃cutaneous bilirubin,TCB)值和STB配对资料,发现92.8%(512∕552)的TCB值略高于STB。Taylor等〔13〕回顾性分析了足月新生儿出生后2周内TCB和STB配对资料,发现TCB均值略高于TSB,TCB-STB的平均差为(14.4±30.4)µmol∕L,两者的相关系数是0.78。Panburana等〔14〕测定了足月儿和近足月儿在出生后(57.85±22.15)h前额部位的TCB-STB的平均差为(7.5±20.0)µmol∕L,显示两者线性相关。本研究中,383例新生儿经皮黄疸测定仪测定TBIL值与全自动生化分析仪测定TBIL值具有显著正相关性,3组中比较中度黄疸组相关性最好,与Srinivas等〔12〕、Taylor等〔13〕和Panburana等〔14〕的研究结果相似。本研究同时考虑了黄疸程度因素的影响,即经皮黄疸测定仪测定TBIL值在中、重度黄疸组高于全自动生化分析仪检测TBIL值,而在极重度黄疸组低于全自动生化分析仪检测TBIL值。
既往研究的相关性分析仅考虑经皮黄疸测定仪和全自动生化分析仪测量结果的程度和方向,不能说明两种检测方法测量结果的一致性。本研究通过Bland-Altman散点图,分析两种检测方法测量结果的平均偏倚和95%CI来判断一致性,并以美国国会颁布的能力比对检测分析质量要求(CLIA'88)中规定的允许总误差为判断标准,若两种仪器检测TBIL的平均偏倚低于CLIA'88规定的允许总误差的1∕2,即±6.84µmol∕L,可认为这两种仪器检测方法测量结果有较好的一致性,提示可互换使用〔15〕。
Neocleous等〔16〕用BiliChek测定了足月新生儿TCB-STB的平均差为(12.5±24.9)µmol∕L,95%CI(-36.2~61.3)µmol∕L,提示两者检测方法的一致性较差。本研究中,经皮黄疸测定仪与全自动生化分析仪测定383例新生儿TBIL的平均偏倚为(-7.10±22.58)µmol∕L,95%CI为(-51.6~36.9)µmol∕L;中度黄疸组、重度黄疸组和极重度黄疸组患儿的TBIL平均偏倚分别为(-15.90±12.35)、(-12.90±11.12)和(28.70±18.27)µmol∕L,95%CI分别为(-40.1~8.3)、(-34.7~8.9)和(-7.1~64.5)µmol∕L,以上研究结果示两种仪器检测TBIL值的平均偏倚较大(尤其是极重度黄疸组),不在最大允许总误差范围内,表明本研究中两种仪器检测TBIL值的一致性较差;95%CI较广(尤其是极重度黄疸组),表明TBIL检测值的个体差异较大。因此,经皮黄疸测定仪不能代替全自动生化分析仪检测TBIL值,仅对单个患儿的纵向随访,观察其病情变化有一定的临床价值。
采用Bland-Altman散点图法进行一致性评价时,目前尚缺少公认的样本量估算方法,已有研究发现样本量越大,一致性(Limits of Agreement,LoA)CI范围越小,越容易得到一致性较好的结论〔17〕。Bland建议用Bland-Altman散点图法进行一致性评价时样本含量至少为100例〔18〕。因此,若本研究能进行多中心大样本量分析后得出的结论可靠性更好。
综上所述,经皮黄疸测定仪和全自动生化分析仪TBIL检测值具有较好的相关性,但随着TBIL值的升高(尤其是TBIL值大于427µmol∕L)一致性变差。因此认为,经皮黄疸测定仪可用于床旁快速、动态评估中、重度黄疸水平,但是对于极重度黄疸患儿不能仅仅根据TCB进行管理,需要动态监测STB。随着光谱技术的发展,未来可利用此技术无创、准确性测定皮下微循环中的胆红素水平。
