药用植物云南龙胆中的黄酮类化学成分研究
2021-05-20叶足约杨惠云王福生
王 甜,叶足约,杨惠云,王 乐,王福生
(大理大学药学院,云南大理 671000)
龙胆属(Gentiana)植物系龙胆科(Gentianaceae)的一个大属,全球约400种,我国有247种、41变种,其中,云南有125种,含6个变种〔1〕。龙胆属植物在我国民间有悠久的药用历史,具有抗高血压、抗菌、抗炎、抗肿瘤和保肝及神经保护等多种药理活性〔2〕。据文献〔3〕报道,龙胆属植物的化学成分主要有环烯醚萜类、黄酮类和三萜类等。云南龙胆(Gentiana yunnanensis Franch.)主要分布于云南昭通、巧家、东川、大理、洱源、丽江、香格里拉、宾川等地,作为民族药,具有清热解毒、止咳和润喉等功效〔4〕。
课题组前期对龙胆属植物微籽龙胆中的化学成分及其活性进行了研究,发现部分黄酮类成分具有明显的抗氧化活性〔5〕。课题组前期对云南龙胆的化学成分进行了研究,发现云南龙胆中含有木脂素苷类化合物〔6〕。除本课题组外,未见国内外其他学者对云南龙胆的化学成分和药理作用进行研究,为了进一步开发利用该药用植物资源,本实验对云南龙胆的化学成分进行了系统研究,从中分离鉴定了7个黄酮类化合物,分别为异荭草素(1)、牡荆素(2)、芹菜素-7-O-β-D-吡喃葡萄糖苷(3)、木樨草素-7-O-β-D-吡喃葡萄糖苷(4)、柚皮素(5)、山柰酚(6)和葛根素(7)。化合物1~7均为首次从该植物中分离得到,化合物4为首次从该属植物中分离得到,为该药用植物资源的开发利用提供了科学依据。化学结构见图1。
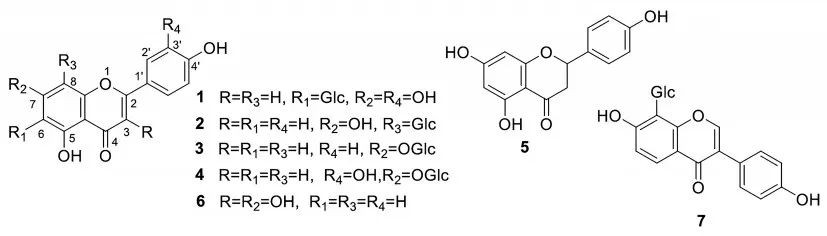
图1 化合物1~7的化学结构
1 实验仪器与材料
1.1 实验仪器 AvanceⅢ-400核磁共振波谱仪(德国布鲁克公司);干燥箱(深圳市澳德玛电子科技有限公司);RE-2000B旋转蒸发仪(上海亚荣生化仪器厂);分析天平(Sartourius);AB-8型大孔树脂(蚌埠市辽源新材料有限公司);Sephadex LH-20(美国GE公司);中压色谱分离凝胶(MCI)和十八烷基硅烷键合硅胶(ODS)(日本YMC公司);硅胶(青岛海洋化工厂分厂);薄层色谱硅胶板GF254(青岛海洋化工有限公司)。
1.2 实验材料 乙醇、甲醇、丙酮、石油醚、氯仿、乙酸乙酯、正丁醇均购自天津市大茂化学试剂厂;氘代甲醇、二甲基亚砜(DMSO)均购自阿拉丁。本实验所用植物云南龙胆药材采自于云南省大理市花甸坝,经大理大学段宝忠教授鉴定为龙胆科龙胆属植物云南龙胆(Gentiana yunnanensis Franch.)全草,植物标本号为WFS-2017823,保存于大理大学王福生教授课题组。
2 提取与分离
干燥云南龙胆全株5.0 kg,粉碎后依次用95%乙醇冷浸提取3次(3×30 L×24 h),提取液浓缩成浸膏(1.2 kg),将浸膏水溶后经AB-8型大孔树脂柱层析由甲醇-水(体积比0:1→1:0)洗脱,得到Fr.1~Fr.4 4个组分。其中Fr.3(287 g)经硅胶柱层析(氯仿-甲醇,体积比100:1→1:1)得到4个组分(Fr.3.1~Fr.3.4)。Fr.3.2组分反复经凝胶Sephadex LH-20柱层析(氯仿-甲醇,体积比1:1)、硅胶柱层析(氯仿-甲醇,体积比30:1→5:1),得到化合物2(20 mg)、3(5 mg)、5(20 mg)和7(10 mg)。Fr.4(529 g)经硅胶柱层析(氯仿-甲醇,体积比100:1→1:1)得到4个组分(Fr.4.1~Fr.4.4)。Fr.4.3和Fr.4.4反复经ODS(甲醇)、MCI(甲醇)、硅胶柱层析(氯仿-甲醇,体积比15:1→5:1)和凝胶Sephadex LH-20(甲醇)柱层析,得到化合物1(63 mg)、4(19 mg)和6(15 mg)。
3 结构鉴定
化 合 物1:黄 色 粉 末。1H-NMR(400 MHz,DMSO-d6)δ:6.70(1H,s,H-3),6.53(1H,s,H-8),7.47(1H,d,J=2.3 Hz,H-2'),6.79(1H,d,J=8.2 Hz,H-5'),7.39(1H,dd,J=8.2,2.3 Hz,H-6'),4.64(1H,d,J=9.9 Hz,H-1″);13C-NMR(100 MHz,DMSO-d6)δ:163.68(C-2),102.83(C-3),181.91(C-4),103.41(C-4a),160.73(C-5),108.90(C-6),163.28(C-7),93.53(C-8),156.23(C-8a),121.75(C-1'),112.98(C-2'),143.28(C-3'),149.99(C-4'),114.47(C-5'),119.01(C-6'),73.09(C-1″),71.19(C-2″),78.51(C-3″),71.28(C-4″),80.34(C-5″),62.34(C-6″)。上述数据与文献〔7〕报道基本一致,因此鉴定化合物1为异荭草素(isoorientin)。
化合物2:黄色粉末。1H-NMR(400 MHz,CD3OD)δ:6.78(1H,s,H-3),6.36(1H,s,H-6),7.97(2H,d,J=8.5 Hz,H-2',6'),6.90(2H,d,J=8.5 Hz,H-3',5'),4.84(1H,d,J=9.7 Hz,H-1″);13C-NMR(100 MHz,CD3OD)δ:165.87(C-2),103.76(C-3),183.88(C-4),103.45(C-4a),162.83(C-5),99.64(C-6),162.87(C-7),108.85(C-8),158.64(C-8a),123.25(H-1'),129.49(H-2',6'),117.35(C-3',5'),161.86(C-4'),75.78(C-1″),72.64(C-2″),78.75(C-3″),71.75(C-4″),80.14(C-5″),62.78(C-6″)。上述数据与文献〔8〕报道基本一致,因此鉴定化合物2为牡荆素(vitexin)。
化合物3:黄色粉末。1H-NMR(400 MHz,CD3OD)δ:6.77(1H,s,H-3),6.59(1H,d,J=2.1 Hz,H-6),6.63(1H,d,J=2.1 Hz,H-8),7.82(2H,d,J=8.5 Hz,H-2',6'),6.91(2H,d,J=8.5 Hz,H-3',5'),4.82(1H,d,J=7.9 Hz,H-1″);13C-NMR(100 MHz,CD3OD)δ:164.18(C-2),104.19(C-3),185.12(C-4),103.91(C-4a),165.43(C-5),98.12(C-6),164.32(C-7),100.01(C-8),158.78(C-8a),123.18(C-1'),132.10(C-2',6'),118.05(C-3',5'),161.96(C-4'),100.24(C-1″),74.77(C-2″),77.64(C-3″),71.21(C-4″),78.27(C-5″),62.41(C-6″)。上述数据与文献〔9〕报道基本一致,因此鉴定化合物3为芹菜素-7-O-β-D-吡喃葡萄糖苷(apigenin-7-O-β-D-glucopyranoside)。
化合物4:黄绿色粉末。1H-NMR(400 MHz,DMSO-d6)δ:6.69(1H,s,H-3),6.57(1H,d,J=2.1 Hz,H-6),6.85(1H,d,J=2.1 Hz,H-8),7.39(1H,d,J=2.2 Hz,H-2'),6.90(1H,d,J=8.2 Hz,H-5'),7.48(1H,dd,J=8.2,2.2 Hz,H-6'),4.96(1H,d,J=7.9 Hz,H-1″);13C-NMR(100 MHz,DMSO-d6)δ:164.23(C-2),103.40(C-3),182.97(C-4),105.71(C-4a),157.13(C-5),100.90(C-6),162.88(C-7),96.25(C-8),161.49(C-8a),120.61(C-1'),113.46(C-2'),153.24(C-3'),147.18(C-4'),115.98(C-5'),122.31(C-6'),100.78(C-1″),72.10(C-2″),76.18(C-3″),71.54(C-4″),78.10(C-5″),62.34(C-6″)。上述数据与文献〔10〕报道基本一致,因此鉴定化合物4为木樨草素-7-O-β-D-吡喃葡萄糖苷(luteolin-7-O-β-D-glucopyranoside)。
化合物5:淡黄色粉末。1H-NMR(400 MHz,DMSO-d6)δ:7.22(2H,m,H-2',6'),6.73(2H,m,H-3',5'),5.80(2H,q,J=2.2 Hz,H-6,8),5.22(1H,dd,J=13.0,2.7 Hz,H-2),3.01(1H,dd,J=17.1,12.8 Hz,H-3-trans),2.58(1H,dd,J=17.1,2.7 Hz,H-3-cis);13C-NMR(100 MHz,DMSO-d6)δ:80.45(C-2),44.01(C-3),197.76(C-4),103.29(C-4a),164.85(C-5),97.01(C-6),168.31(C-7),96.13(C-8),165.43(C-8a),129.05(C-1'),131.03(C-2',6'),116.28(C-3',5'),158.99(C-4')。上述数据与文献〔11〕报道基本一致,因此鉴定化合物5为柚皮素(naringenin)。
化合物6:黄色粉末。1H-NMR(400 MHz,DMSO-d6)δ:7.95(2H,d,J=8.9 Hz,H-2',6'),6.83(2H,d,J=8.9 Hz,H-3',5'),6.34(1H,d,J=2.0 Hz,H-8),6.09(1H,d,J=2.0 Hz,H-6);13C-NMR(100 MHz,DMSO-d6)δ:146.85(C-2),135.75(C-3),175.97(C-4),103.12(C-4a),160.78(C-5),98.27(C-6),163.94(C-7),93.56(C-8),156.24(C-8a),121.75(C-1'),129.60(C-2',6'),115.51(C-3',5'),159.25(C-4')。以上数据与文献〔12〕报道基本一致,故鉴定化合物6为山柰酚(kaempferol)。
化 合 物7:白 色 粉 末。1H-NMR(400 MHz,CD3OD)δ:8.09(1H,s,H-2),7.96(1H,d,J=8.9 Hz,H-5),6.93(1H,d,J=8.9 Hz,H-6),7.28(2H,m,H-2',6'),6.76(2H,m,H-3',5'),5.02(1H,d,J=9.9 Hz,H-1″);13C-NMR(100 MHz,CD3OD)δ:154.48(C-2),124.11(C-3),178.23(C-4),116.20(C-4a),125.43(C-5),116.20(C-6),162.99(C-7),113.08(C-8),158.64(C-8a),124.11(C-1'),131.34(C-2',6'),113.08(C-3',5'),154.48(C-4'),74.31(H-1″),71.62(H-2″),79.97(H-3″),70.34(H-4″),82.73(H-5″),62.38(H-6″)。以上数据与文献〔13〕报道基本一致,故鉴定化合物7为葛根素(puerarin)。
4 讨论
本文对云南龙胆95%乙醇提取物进行分离纯化,得到了7个黄酮类化合物,包括4个黄酮苷类化合物1~4、1个二氢黄酮类化合物5、1个黄酮醇类化合物6和1个异黄酮类化合物7。化合物1~7均首次从该药用植物中分离得到,化合物4为首次从该属植物中分离得到。
龙胆属植物中含有丰富的黄酮类成分,课题组前期实验发现化合物2、3和7对1,1-二苯基-2-三硝基苯肼(DPPH)自由基有明显的清除能力〔5〕。黄酮类化合物还具有抗胃溃疡、神经保护、抗心肌缺血、降压、改善学习记忆认知、保护生殖组织、抗炎、抗菌、抗病毒、抗肿瘤以及降血糖等药理活性〔14〕。因此,该实验为龙胆属植物的物质基础及药用植物资源开发利用提供一定的科学依据。龙胆属植物中黄酮类化合物的构效关系及量丰黄酮类化合物的结构优化有待进一步研究。
