老年脂代谢紊乱与糖尿病并发症及预后关系的探讨
2021-05-17赵颖王苏
赵颖 王苏
DM 是以糖代谢紊乱为主的慢性疾病,患者通常因“三多一少”而就诊,部分患者是通过体检发现患有DM,而DM 并发症是导致DM 患者死亡的主要原因,据相关流行病学研究,80%的DM 患者死于心血管疾病,且80%的DM 患者存在脂代谢紊乱现象,有些学者将DM 称之为“糖脂病”[1]。近些年,随着人们生活水平的提高,肥胖人群比例越来越高,而肥胖症成为DM 的前驱症状已经备受临床重视,肥胖患者的脂肪细胞肥大、胰岛素受体受损,容易产生胰岛素抵抗,使血糖升高,临床已经将脂代谢紊乱一起的肥胖、高脂血症、高血糖等称为胰岛素抵抗X 综合征。而脂代谢紊乱已经成为DM患者预后的关键性因素。有关临床研究表明,DM 未伴有并发症的患者10年内发生心血管疾病死亡率与非DM 但伴有陈旧性心肌梗死患者的死亡率相当。DM 患者发生急性心肌梗死较非DM 发生急性心肌梗死患者的近远期预后更差。因此,在对患者进行降糖治疗的同时,需重视DM 患者血脂异常等危险因素[2]。本文就探讨老年脂代谢紊乱与DM 并发症及预后的关系,现将研究结果报告如下。
1 资料与方法
1.1 一般资料 2017年8 月~2020年4 月本院收治的初诊DM 脂代谢正常的患者40 例作为对照组,另选取同期初诊DM 伴脂代谢紊乱的患者40 例作为观察组。观察组:男25 例,女15 例;年龄60~78 岁,平均年龄(69.45±5.27)岁。对照组:男24 例,女16 例;年龄62~76 岁,平均年龄(69.37±5.28)岁。两组患者性别、年龄等一般资料比较差异无统计学意义(P>0.05),具有可比性。纳入标准:患者符合《糖尿病诊断和分型标准》中空腹血糖≥7.0 mmol/L 的标准,餐后2 h 血糖>11.1 mmol/L;无DM 急性并发症;体重<80 kg;知情此研究;经本院伦理委员会批准。排除标准:伴有恶性肿瘤;服用降脂药物;急性感染者。
1.2 方法 生化指标测定:受试者禁食12 h,次晨起空腹,采取肘静脉血5 ml,测定TG、TC、LDL-C、HDL-C、VLDL-C,血糖采用日本OlympusAU600 自动生化分析仪测定。对两组患者使用饮食调节,采用双胍类或磺脲类降糖药物,部分患者使用胰岛素治疗。3 个月后进行疗效评价。
1.3 观察指标 ①比较两组治疗后的体重、腰围、臀围、BMI;②比较两组治疗后的血脂相关指标,包括TG、TC、LDL-C、HDL-C、VLDL-C;③比较两组并发症发生率。
1.4 统计学方法 采用SPSS24.0 统计学软件处理数据。计量资料以均数±标准差()表示,采用t检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 两组治疗后的体重、腰围、臀围、BMI 比较观察组的体重、腰围、臀围、BMI 均高于对照组,差异有统计学意义(P<0.05)。见表1。
2.2 两组血脂相关指标比较 观察组的TC、TG、LDL-C、VLDL-C 水平高于对照组,HDL-C 水平低于对照组,差异均有统计学意义(P<0.05)。见表2。
2.3 两组并发症发生率比较 观察组的糖尿病肾病、糖尿病视网膜病变、糖尿病周围神经病变、糖尿病足发生率均高于对照组,差异有统计学意义(P<0.05)。见表3。
表1 两组治疗后的体重、腰围、臀围、BMI 比较()
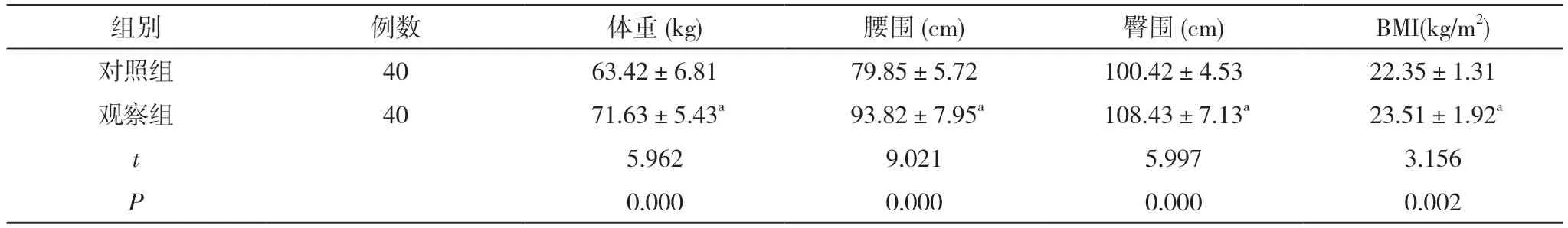
表1 两组治疗后的体重、腰围、臀围、BMI 比较()
注:与对照组比较,aP<0.05
表2 两组血脂相关指标比较(,mmol/L)
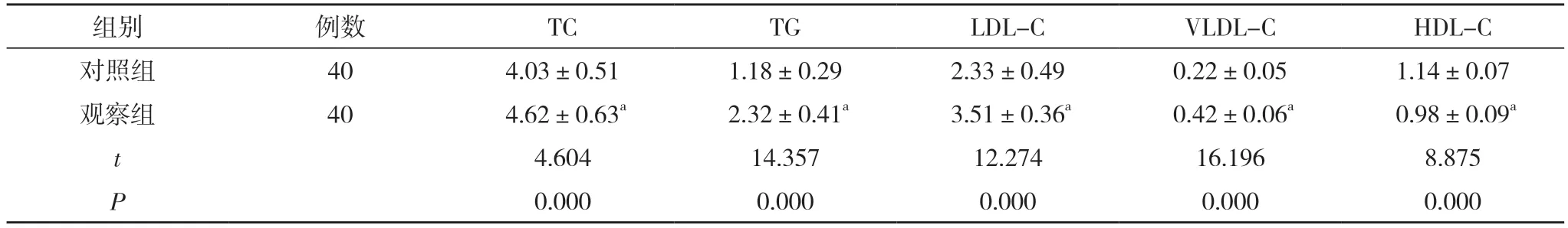
表2 两组血脂相关指标比较(,mmol/L)
注:与对照组比较,aP<0.05
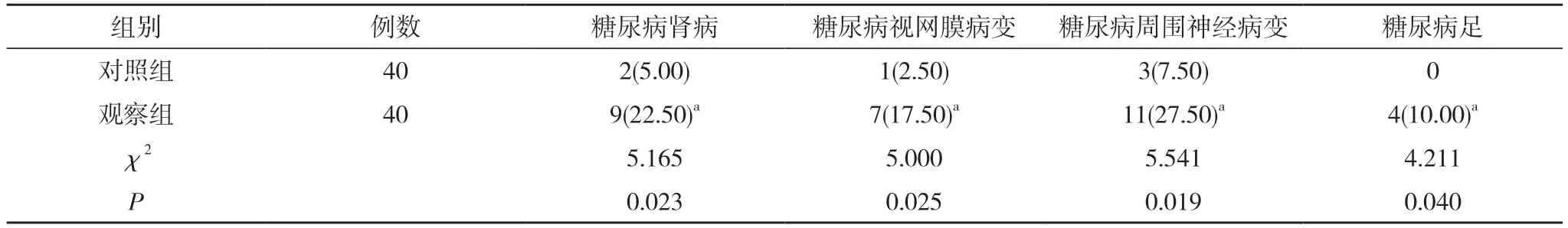
表3 两组并发症发生率比较[n(%)]
3 讨论
DM 是一种慢性代谢性疾病,临床证实,DM 患者以老年人群最多,老年DM 患者多伴有脂代谢紊乱现象,可能是DM 代谢紊乱,脂肪贮存体内所致,有关老年人血脂水平随着年龄的增长而升高的机制尚不明确,但老年DM 患者与健康人体内脂肪组织的合成和代谢处于动态平衡不同[3]。大量研究证实DM 伴并发症患者的动脉粥样硬化疾病的发生率显著高于DM 未伴脂代谢紊乱患者,且DM 伴脂代谢紊乱患者预后较差。DM 伴脂代谢紊乱患者比未伴脂代谢紊乱患者的并发症更多[4]。DM 伴并发症患者除了与肥胖、高血糖、高血脂、胰岛素抵抗以及高胰岛素血症等因素有关外,DM 所致的脂代谢紊乱也是导致并发症的明确且重要的危险因素。有研究证实[5],通过调节DM 伴脂代谢紊乱患者的异常血脂,可降低并发症的发生。因此,若能将患者的异常血脂调节正常,可降低并发症的发生,这对防治DM 并发症特别是血管合并症有着非常重要的作用。
DM 伴脂代谢紊乱患者病情控制不佳,是以极低密度脂蛋白(VLDL)以及TG 水平显著升高作为脂代谢紊乱的评价标准。DM 伴脂代谢紊乱患者除了VLDL、TG 水平升高,低密度脂蛋白(LDL)、TC、载脂蛋白B、E(ApoB、E)水平也会升高,部分患者乳糜微粒(CM)水平也会升高,而载脂蛋白A1(ApoA1)、高密度脂蛋白(HDL)水平降低。临床常将HDL 降低以及TG、LDL升高称为血脂异常三联症[6]。这症状是动脉粥样硬化的一种表现型,常伴随着早发的冠心病,而DM 患者血浆脂蛋白的改变和血糖控制情况以及胰岛素水平息息相关[7]。
轻度2 型DM 患者特别是肥胖患者,由于胰岛素抵抗所致糖代谢异常,会增加脂肪动员;重型2 型DM以及1 型DM 患者由于机体缺乏胰岛素,造成胰高血糖素浓度的上升,增强了动员脂肪的分级,升高了血中游离脂肪酸的浓度,为肝脏提供丰富的原料来合成更多的内源性TG,也就合成了更多的VLDL;机体缺乏胰岛素会降低脂蛋白酯酶(LPL)的活性,而LPL 是TG 的水解酶,LPL 活性下降,使TG 分解缓慢,因此含有TG 的VLDL 以及CM 分解代谢也缓慢。且DM 患者血中VLDL 转化成LDL 的途径遭到破坏,从而升高了TG、VLDL 在血中的浓度[8]。胆固醇的主要载体是血LDL,虽然HDL 也存在一定量的胆固醇,但3/4 左右的胆固醇以LDL-C 的形式存在。这是血浆胆固醇组成的不均一性,正是这种不均一性,导致LDL 在致动脉粥样硬化的关系上比胆固醇更具意义。LDL 的主要前身物质是VLDL,DM 患者VLDL 水平升高,为LDL的合成提供很多的原料,增加了LDL 的合成,而LDL的合成和分解与血浆胰岛素浓度有关。轻型或肥胖的2 型DM 患者有高胰岛素血症,使肝内3-羟基-3-甲基戊二酸单酰辅酶A(HMG-CoA)还原酶的活性激活,合成更多的TC;重型2 型DM 患者以及1 型DM 患者由于机体缺乏胰岛素,减少了纤维母细胞表面的LDL受体数量或降低了其活性,减少了LDL 与其受体的结合,使LDL 的分解降低。而DM 患者的高血糖使LDL糖化并被氧化,降低了LDL 与其受体结合的能量,上述原因均是导致TC 和LDL 浓度升高的原因。而TC的堆积形成泼墨细胞,加速脂质沉积在血管壁上,促进了动脉粥样硬化的发生和发展[9]。
关于DM 伴有脂代谢紊乱的防治有非药物和药物治疗两个方面,非药物治疗是饮食干预,合理的膳食对改善脂代谢紊乱有着很重要的作用,根据年龄、工作、体力活动、生活习惯预估每日需要摄入的总能量,根据有关脂肪、蛋白、碳水等摄入的比例进行分配[10]。适当多食用不饱和脂肪酸及纤维素,尽量少食用高胆固醇的肥肉、动物内脏、蛋黄、黄油、带鱼等,养成良好的饮食习惯对脂代谢紊乱有一定的改善作用。药物治疗常采用降脂药物,常用的有阴离子交换树脂、盐酸及其衍生物以及HMG-CoA 还原酶抑制剂等他汀类药物、抗氧化剂等。本研究结果显示,观察组的体重、腰围、臀围、BMI 均高于对照组,TC、TG、LDL-C、VLDL-C 水平高于对照组,HDL-C 水平低于对照组,糖尿病肾病、糖尿病视网膜病变、糖尿病周围神经病变、糖尿病足发生率均高于对照组,差异有统计学意义(P<0.05)。
由结果得知DM 患者伴有脂代谢紊乱会导致DM并发症的发生,DM 患者的脂代谢紊乱可作为DM 并发症的高危因素。杨晓艳等[11]研究结果表明DM 并发症的发生率在青壮年人群中较为少见,而在老年组DM患者中发生率非常多,DM 随着年龄和病程的增长,慢性并发症增多,而加重血糖、血脂的代谢紊乱。本研究对老年DM 伴脂代谢紊乱患者进行研究,也证实了,DM 伴随着脂代谢紊乱,并发症较多。
综上所述,老年脂代谢紊乱和DM 并发症及预后均有一定的关系,经分析,DM 未伴有并发症的血脂异常低于DM 伴有并发症的患者,因此,在降糖治疗的同时,应强化血脂的治疗。
