瑞舒伐他汀对2型糖尿病肾病患者氧化应激及mir-34a/SIRT1表达的影响
2021-04-30刘晓莉
刘晓莉
糖尿病肾病为2型糖尿病最严重的并发症,患者主要表现为血流动力学异常与代谢紊乱,是导致糖尿病患者晚期死亡的主要原因。糖尿病肾病的发生与炎性反应、氧化应激等多种途径所致的血管内皮细胞功能异常、细胞凋亡有关。随着临床对他汀药物研究的不断深入,已证实他汀类药物不仅具有血脂调节作用,还具有非依赖降脂的肾脏保护作用,能够减轻氧化应激损伤[1]。瑞舒伐他汀为强效羟甲基戊二酰辅酶A还原酶抑制剂,新型他汀类调脂药物,生物利用度高,且安全性高,患者耐受性良好。沉默信息调节因子1(silent information regulator 1,SIRT1)为调节机体代谢的重要因子,陶鹏宇等[2]研究指出,SIRT1降低可促进肾脏细胞凋亡。临床研究显示,microRNA存在于外周血细胞中,表达水平稳定,mir-34a为mir-34家族成员,具有抑制细胞增殖,促进细胞凋亡的作用[3]。胡豪飞等[4]研究表明,肾组织mir-34a表达与IgA肾病患者肾小球硬化相关,其过程可能与脂代谢紊乱有一定相关性。本研究中2型糖尿病肾病患者采用瑞舒伐他汀治疗,观察患者氧化应激状态与mir-34a/SIRT1表达水平,报道如下。
1 资料与方法
1.1 一般资料 选取2017年2月至2019年3月我院收治的2型糖尿病患者95例,采用随机字母表法分为观察组(n=47)与对照组(n=48)。观察组中,男21例,女26例;年龄39~67岁,平均年龄(48.78±9.46)岁;病程5~14年,平均病程(7.65±1.87)年;平均收缩压(133.48±10.25)mm Hg;平均舒张压(82.43±6.48)mm Hg;平均体重指数(BMI)(24.62±2.73)kg/m2。对照组中,男19例,女29例;年龄39~67岁,平均年龄(49.43±9.65)岁;病程5~15年,平均病程(7.71±1.53)年;平均收缩压(131.56±9.79)mm Hg;平均舒张压(83.36±6.77)mm Hg;平均BMI(24.53±2.89)kg/m2。2组患者一般资料比较差异无统计学意义(P>0.05)。本研究经我院伦理委员会批准同意。
1.2 纳入与排除标准
1.2.1 纳入标准:①糖尿病诊断均符合中华医学会糖尿病学分会制定的相关标准[5],且符合糖尿病肾病诊断[6],24 h尿微量白蛋白排泄率(UAER)>200 μg/min,常规尿检蛋白阳性;②患者均未合并急慢性感染性疾病、恶性肿瘤或急慢性肾炎;③近1个月内未服用他汀类调脂药物;④患者均知晓本研究详情并自愿参与。
1.2.2 排除标准:①合并严重肝脏、心脏疾病;②有重度吸烟、嗜酒;③合并自身免疫性疾病;④近1个月内发生糖尿病酮症酸中毒。
1.3 方法
1.3.1 对照组:采用常规治疗,给予患者降糖药物,指导患者适量运动、低蛋白饮食,控制血压,维持电解质、酸碱平衡等。
1.3.2 观察组:在对照组基础上给予瑞舒伐他汀(生产厂家:江苏南京正大天晴制药有限公司生产;国药准字 H20080670;规格:10 mg)治疗,口服,10 mg/次,1次/d。4周为1个疗程,连续治疗8周。
1.3.3 其他:研究期间2组患者均不给予其他降脂类药物。
1.4 观察指标 观察2组患者血脂水平、血清炎性因子水平、氧化应激指标与mir-34a、SIRT1表达水平。
1.4.1 血脂水平:治疗前后于清晨患者空腹状态下抽取静脉血3 ml,使用全自动生化分析仪检测低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)、总胆固醇(TC)、三酰甘油(TG)水平。
1.4.2 血清炎性因子水平:治疗前后于清晨患者空腹状态下抽取静脉血3 ml放入无菌离心管内,离心后取上清液,采用酶联免疫吸附法(ELISA)测定血清肿瘤坏死因子-α(TNF-α)、白介素-6(IL-6),采用速率散射比浊法测定超敏C-反应蛋白(hs-CRP)。
1.4.3 氧化应激指标:另取3 ml静脉血采用肝素抗凝,低温离心后取血浆,采用黄嘌呤氧化酶法测定超氧化物歧化酶(SOD)含量,采用硫代巴比妥酸显色法测定丙二醛(MAD)含量。
1.4.4 mir-34a、SIRT1表达水平:将抽取的3 ml静脉血放入无菌离心管内,室温状态下静置30 min,离心后取血清离心后取上清液,采用免疫印迹法测定SIRT1表达水平。采用Ambion公司提供的mirVana试剂盒从血清中提取RNA,采用ABI公司提供的TaqMan MicroRNA Assay试剂盒将血清RNA逆转录后行qPCR反应,将U6作为内部参照。
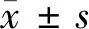
2 结果
2.1 2组患者血脂水平比较 治疗前,2组患者血脂水平比较差异无统计学意义(P>0.05)。治疗后,观察组LDL-C、TC、TG均较治疗前下降,且明显低于对照组(P<0.05),观察组HDL-C水平较治疗前升高,且明显高于对照组(P<0.05)。见表1。
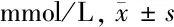
表1 2组患者血脂水平比较
2.2 2组患者血清炎性因子水平比较 治疗前,2组患者血清TNF-α、IL-6、hs-CRP水平比较差异无统计学意义(P>0.05)。治疗后,观察组血清TNF-α、IL-6、hs-CRP均较治疗前下降,且各指标水平均明显低于对照组,差异有统计学意义(P<0.05)。见表2。

表2 2组患者血清炎性因子水平比较
2.3 2组患者氧化应激指标比较 治疗前,2组患者SOD、MAD水平比较差异无统计学意义(P>0.05)。治疗后,观察组SOD较治疗前升高,且明显高于对照组(P<0.05),观察组MAD水平较治疗前降低,且明显低于对照组(P<0.05)。见表3。

表3 2组患者氧化应激指标比较
2.4 2组患者mir-34a、SIRT1表达水平比较 治疗前,2组患者mir-34a、SIRT1表达水平比较差异无统计学意义(P>0.05)。治疗后,观察组mir-34a表达水平较治疗前下降,且低于对照组(P<0.05),观察组SIRT1表达水平较治疗前升高,且显著高于对照组(P<0.05)。见表4。

表4 2组患者mir-34a、SIRT1表达水平比较
3 讨论
临床研究指出,血清TC尤其是LDL-C 水平升高是糖尿病肾病进展的独立危险因素[7]。血脂异常可导致神内脂肪酸结构发生改变,使肾内缩血管活性物质释放增多,肾小球血液流变学异常,从而使LDL-C糖化与氧化。Bahmani等[8]指出,防治糖尿病肾病应重视调节血脂水平。瑞舒伐他汀是临床治疗早期糖尿病肾病的药物,但在临床期的应用较少。本研究中糖尿病肾病患者采用瑞舒伐他汀治疗,结果显示观察组LDL-C、TC、TG水平明显低于对照组,HDL-C水平显著高于对照组,表明瑞舒伐他汀具有调节糖尿病肾病患者血脂作用。临床研究指出,过度分泌的TG粒子,血清TG水平与尿蛋白排泄率、肾小球滤过率下降具有明显相关性,可促进肾小球系膜细胞增生,加速肾炎进展,因此调节血脂水平有助于抑制肾脏疾病[9]。临床研究发现,瑞舒伐他汀不仅具有肾脏保护作用,还具有良好的抗炎作用[10]。CRP为急性时相反应蛋白,并参与炎性反应过程,IL-6与TNF-α为其合成的调节因子。临床研究已证实,IL-6与TNF-α水平与组织损伤程度呈正相关[11]。本研究结果显示,观察组血清TNF-α、IL-6、hs-CRP水平均明显低于对照组。这表明瑞舒伐他汀具有显著的抗炎作用,与相关临床研究[12]具有一致性。
氧化应激是引发心血管功能异常的一个重要因素,糖尿病肾病患者肾组织的一个病理变化是活性氧浓度升高,增加肾脏负担,并且能够引起机体氧化应激反应。研究发现,氧化应激反应增强可对机体造成损伤,加速糖尿病肾病进展[13]。SOD为自由基清除剂,是人体内很重要的抗氧化酶,其水平变化能够间接反映机体氧自由基清除能力的高低。MDA为脂质过氧化物,其水平可直接反映机体过氧化强度与组织损伤程度。因此评估上述指标,可评估机体氧化应激程度。郭英利等[14]研究指出,瑞舒伐他汀能够降低慢性心力衰竭患者氧化应激反应。本研究结果显示,观察组SOD水平明显高于对照组,MAD水平明显低于对照组。表明瑞舒伐他汀可提高糖尿病肾病患者抗氧化应激能力。
Tabuchi等[15]研究显示冠心病患者与非冠心病患者相比较,内皮祖细胞中miR-34a表达水平上调,而SIRT1表达水平下调,经阿托伐他汀治疗后,可在一定程度上下调冠心病患者miR-34a的非正常表达水平,并促进SIRT1正常表达。并指出,miR-34a靶向调控SIRT1蛋白细胞凋亡过程中起重要作用,他汀类药物能够调节二者表达。氧化应激损伤可引起miR-34a表达水平上调,SIRT1表达水平下调。SIRT1为miR-34a作用的靶基因之一,在细胞氧化应激过程中能够保护细胞,抑制细胞凋亡[16]。本研究结果显示,治疗前患者mir-34a表达升高,SIRT1下降,治疗后观察组mir-34a表达水平较治疗前下降,且低于对照组,SIRT1表达水平较治疗前升高,且显著高于对照组。表明瑞舒伐他汀能够调节miR-34a与SIRT1表达。推测瑞舒伐他汀可能通过减轻2型糖尿病肾病患者氧化应激损伤、调节脂代谢紊乱使miR-34a表达水平下调,SIRT1表达水平上调。
综上所述,瑞舒伐他汀治疗糖尿病肾病效果确切,可有效调节患者的血脂水平,降低炎性反应与氧化应激反应,并可在一定程度上调节mir-34a、SIRT1表达,而下调miR-34a表达,上调SIRT1表达反过来可减轻氧化应激损伤。但mir-34a是否通过 SIRT1通路参与氧化应激,本次未进行研究,此外,外周血细胞中miRNA的动态变化与血糖控制效果的关系也值得进一步探讨。
