经内科胸腔镜冷冻胸膜活检对不明原因胸腔积液诊断的有效性及安全性研究
2021-04-27付鹏龙发胡斯育黄文婷董洪波蒋慧龙亮胡凤波甘景帆
付鹏 龙发 胡斯育 黄文婷 董洪波 蒋慧 龙亮 胡凤波 甘景帆
胸腔积液是胸膜疾病最常见的临床表现,可原发于胸膜疾病,也可来源于肺部及全身性疾病[1]。经过全面的胸腔积液分析及效果欠佳的闭式胸膜活检,仍有多达25%的胸腔积液患者不能确诊[2]。内科胸腔镜是一项可操作的、安全、有效的微创诊疗技术,对胸腔积液和气胸等胸膜疾病的诊疗具有重要的临床应用价值[3]。有研究[4]表明,内科胸腔镜常规活检对渗出性胸腔积液的诊断率为94%,仍有部分患者无法确诊。冷冻活检技术因其活检组织标本大,诊断阳性率较高,手术安全性较好,已广泛用于肺组织的活检,具有较好的安全性和有效性[5]。我们拟通过冷冻胸膜活检对比常规活检方法,探讨经内科胸腔镜冷冻胸膜活检的安全性和有效性,为不明原因胸腔积液的诊断提供参考。
资料与方法
一、纳入及排除标准
本研究采用前瞻性自身对照研究方法,将2017年9月-2018年9月在中国科学院大学深圳医院呼吸内科住院的102例渗出性胸腔积液患者纳入本次研究。所有患者均需符合胸腔积液light诊断标准[6],因诊断不明,需要行内科胸腔镜胸膜活检检查。本研究经中国科学院大学深圳医院医学伦理委员会批准,所有患者均书面签署知情同意书。
纳入标准:年龄>18岁;术前经胸部CT或胸部超声证实有胸腔积液;心肺功能可以耐受基础麻醉,凝血功能正常。
排除标准:严重胸膜粘连者、凝血功能异常;血小板<50×109/L,严重心肺功能不全或血流动力学不稳定状态。
二、方法
1 设备 可弯曲电子胸腔镜(LTF-240,日本Olympus公司)、主机(日本Olympus公司)、活体取样钳、冷冻仪(Erbokyo CA,德国ERBE公司)及冷冻探头(直径1.9 mm,德国ERBE公司)(见图1)。
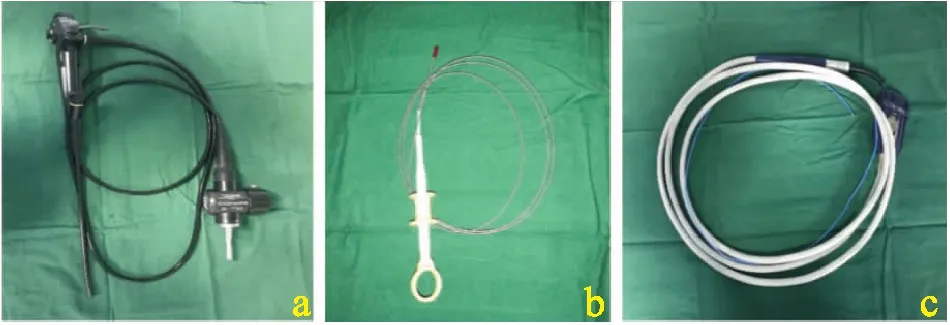
图1 a: 可弯曲电子胸腔镜;b:活体取样钳;c:冷冻探头
2 手术方法及分组 所有患者术前完善血常规、凝血功能、心电图、胸部CT、胸部超声等检查。所有患者均在胸腔镜室进行内科胸腔镜操作。术前行床边胸部超声检查,以确定最佳进入点。术中全程给予鼻导管吸氧(2~3 L/min),心电监护,检测心率、血压、血氧饱和度。患者取健侧卧位,患侧上肢上举于头顶,使肋间隙增宽,取患侧腋前线或腋中线第4~8肋间作为切口部位,常规消毒、铺无菌单及孔巾,静注咪达唑仑、舒芬太尼用于镇静镇痛,皮下注射2%利多卡因至壁层胸膜局麻,沿肋间隙作约1 cm切口,钝性分离至肌层,用带有穿刺鞘管针的外套管经切口处垂直插入胸腔。拔出针芯,将可弯曲胸腔镜插入套管并进入胸膜腔,吸引出胸水后,检查整个胸膜腔,在壁层胸膜可疑病变部位进行多点活检,首先用活检钳行钳夹活检,一共活检6次,记录活检标本大小、观察出血情况(设为常规活检组)。然后在相同部位依次行冷冻活检,经胸腔镜工作通道把探头送至需活检部位,使冷冻探头尖端接触活检部位,启动制冷3~5 s(温度-60 ℃)后将胸腔镜及冷冻探头一同拔出,待探头复温后取下活检标本,一共活检3次,记录活检标本大小、观察出血情况(设为冷冻活检组)。术毕,放置胸腔引流管,行胸腔闭式引流。
3 观察指标及评价方法 记录活检标本大小、观察出血情况。根据以下标准[7]对活检部位的出血情况进行评估:无出血或轻微,出血量<5 mL,无需用药;轻度出血,出血量5~10 mL,局部注射冰冻生理盐水、血管活性药物(肾上腺素1 ∶10 000);中重度出血,出血量>10 mL,使用电烧灼、氩等离子体干预或外科介入手术。
活检标本按组织病理学和免疫组织化学染色标准处理,由病理科医师作出最终的病理学诊断,比较经常规活检和冷冻活检获取组织的病理阳性率。
三、统计学分析

结 果
一、一般资料
102例患者中,男65例(63.7%),女37例(36.3%),年龄19~79岁,平均(40.3±14.8)岁,右侧胸腔积液52例,左侧胸腔积液49例,双侧胸腔积液1例。
二、两组活检获得标本直径比较
常规活检组活检总次数为612次(102×6),标本直径为(2.3±0.3)mm;冷冻活检组活检总次数306次(102×3),标本直径为(6.5±1.2)mm。统计结果显示,冷冻活检组标本直径明显大于常规活检组,差异有显著统计学意义(t=81.671,P<0.01)(见图2)。

图2 a为常规胸膜活检组织;b为冷冻胸膜活检组织
三、两组病理阳性率比较
共纳入102例,99例获得明确的病理诊断,其中恶性17例(16.7%)(腺癌12例、鳞癌2例、乳腺癌胸膜转移1例、卵巢癌胸膜转移1例、胸膜间皮瘤1例),结核75例(73.5%),炎症7例(6.9%)。常规活检病理阳性率为90.2%(92/102)[95%CI为0.843-0.961];冷冻活检病理阳性率为97.1%(99/102)[95%CI为0.937-1.004]。冷冻活检组阳性率明显高于常规活检组,差异有统计学意义(P<0.05)(见表1)。
常规活检组与冷冻活检组诊断结果一致性一般(Kappa=0.436,P<0.001),冷冻活检组的阳性率为97.1%,明显高于常规活检组(90.2%),差异具有统计学意义(P=0.016)。
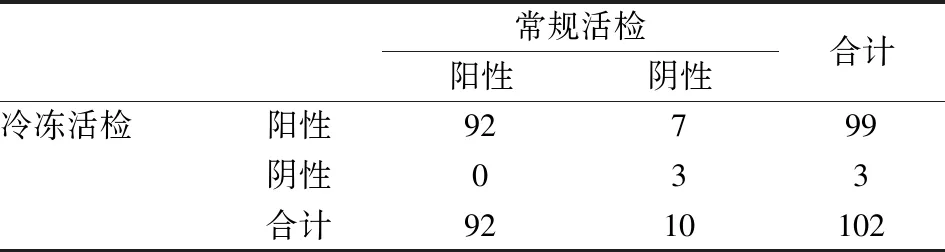
表1 两组病理结果比较(n)
四、两组合并出血情况比较
两组均无中重度出血发生,轻微出血无需用药,轻度出血经局部注射冰冻生理盐水或血管活性药物(肾上腺素1 ∶10 000)止血。统计结果显示,常规活检组无出血或轻微出血几率为92.2%,轻度出血几率为7.8%,冷冻活检组无出血或轻微出血几率为89.2%,轻度出血几率为10.8%,两组出血情况无统计学差异(P>0.05)(见表2)。

表2 两组患者出血情况比较(n)
讨 论
近年来,冷冻活检技术作为一种新型的诊断工具越来越受到学者们的关注。冷冻活检技术应用冷冻活检系统,当冷冻探头到达病灶处可冻滞局部组织,避免取材过程中组织滑动导致的取材失败,也降低了疾病的漏诊率和误诊率[8]。目前,国内外都有研究将经支气管镜冷冻肺活检应用于间质性肺疾病的临床诊断中,均取得了理想的效果,安全性较高[5,9-10],与传统的钳式活检相比,冷冻活检技术获得标本大小及病理诊断率方面具有明显的优势,安全性良好。
Wurps等[11]在研究中分析了内科胸腔镜常规活检联合冷冻活检对胸腔积液的诊断价值,结果发现,常规活检联合冷冻活检的总阳性率为95%,而常规活检的总阳性率为85.8%。说明内科胸腔镜常规胸膜活检联合冷冻活检可以达到更高的病理确诊率。Rozman等[12]在研究中分析了电子支气管镜进行胸膜活检联合壁层胸膜冷冻活检,对不明原因渗出性胸腔积液的诊断价值和安全性。结果发现,通过电子支气管镜进行胸膜活检对不明原因渗出性胸腔积液的确诊率接近90%,如果联合应用胸膜冷冻活检可以达到更高的病理学确诊率,且并发症轻微。
本研究为前瞻性、自身对照研究。对102例渗出性胸腔积液患者在壁层胸膜使用胸腔镜下常规钳式活检与冷冻活检的有效性与安全性进行比较。本研究发现,常规活检组对胸腔积液诊断的阳性率为90.20%,这与其他学者的研究结论基本一致。本研究中,经冷冻活检获取的组织标本,阳性率明显高于常规活检组(97.06%vs90.20%),且冷冻活检获取的组织标本直径明显大于常规活检获取的组织标本。以上说明,冷冻胸膜活检对比常规活检在获得标本大小方面有明显优势,且能提高对胸腔积液诊断的阳性率。
另外我们发现在病理诊断阳性结果中,常规活检和冷冻活检对于肿瘤及炎症的例数一致,而在75例结核患者中,常规活检有7例漏诊。我们在病理诊断中发现常规活检为纤维坏死物,而冷冻活检能明显看到干酪样坏死和郎罕斯巨细胞(图3、图4)。结核性胸膜炎多伴有大量的纤维素渗出,易造成胸膜粘连、胸膜增生。胡旭钢等[13]研究中表明在内科胸腔镜下结核性胸膜炎的表现主要有:胸膜上呈弥漫性分布的粟粒状结节、胸膜充血水肿、胸膜肥厚增生、脏壁层胸膜粘连、大量纤维素性渗出和黄白色干酪样坏死等。我们发现在部分病例中,由于大量纤维素性渗出导致胸膜粘连及显著增厚(图5),常规活检钳取深度不够,易滑脱,而冷冻活检取材深度够深范围够大,能获取完整理想的组织标本,这可能是冷冻胸膜活检技术在结核性胸膜炎病理诊断中更具优势的原因。

图3 常规胸膜活检标本病理 为纤维坏死物 HE×40
内科胸腔镜的并发症发生率报道不一,为3%-22.6%,但严重并发症较为少见,死亡率为0.01-0.6%[14]。出血为活检操作最常见的并发症,冷冻活检中取得的标本组织体积相对较大,因此所形成的创面也相对较大,出血发生时,可在胸腔镜下直视局部喷洒肾上腺素等进行止血。本研究中,在进行冷冻活检操作时尽量操作轻柔、准确,避免强行拉扯等粗暴行为。从本研究结果中表明冷冻活检获取的标本大小明显大于常规活检,因此在取样过程中能明显减少取样次数而获得满意的组织标本,显著减少因多次取样造成的胸膜创伤。并且研究结果表明两组均无中重度出血发生,出血情况无统计学差异。考虑可能是由于冷冻活检由于会降低创面周围组织的温度,导致创面周围血管收缩,且壁层胸膜的收缩性相对较好,因此术后出血的概率较小。

图4 冷冻胸膜活检标本病理 HE×40
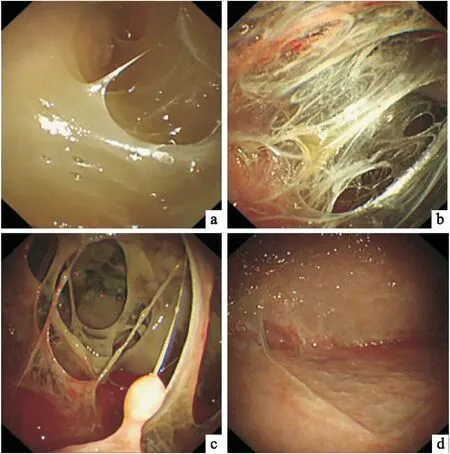
图5 胸腔镜所见大量纤维素样渗出导致胸膜粘连及增厚 a-c为胸膜粘连,d为胸膜增厚
终上所述,在不明原因胸腔积液的诊断中,内科胸腔镜是重要的检查手段,冷冻活检技术能获取较为完整的病理组织,显著减少取样次数,明显提高活检诊断阳性率,且安全性好,当常规活检技术无法取得满意的组织标本进行病理诊断时,可联合冷冻活检技术,以提高活检诊断的阳性率。
