复合益生菌发酵不同基料乳酸菌饮料中挥发性代谢物差异分析
2021-04-22韩之皓王月娇王记成张和平
韩之皓,郭 帅,黄 天,郑 岩,王月娇,白 梅,王记成,张和平
(内蒙古农业大学 乳品生物技术与工程教育部重点实验室 农业农村部奶制品加工重点实验室 呼和浩特010018)
乳酸菌饮料是指以乳或乳制品为原料,经化料、水合、杀菌,接种发酵剂所得发酵基料,按照一定比例混入水、食品添加剂(甜味剂、酸味剂、稳定剂)调配后制得的饮料。乳酸菌饮料作为健康饮品以其独特的风味和优质的保健功效赢得广大消费者的追捧。相关资料显示,近5年,世界乳酸菌饮料市场份额不断增加,其市场规模超过500 亿美元[1]。益生菌是一类能够改善宿主肠道菌群平衡并有效增强食用者身体健康水平的活性有益微生物,其具有改善便秘、缓解腹泻、抗肿瘤、保护口腔健康等重要生理功效[2];Buriti 等[3]应用L.rhamnosus LR-32 和B.lactis BB12 复配发酵山羊乳清饮料,并添加适量的膳食纤维,所得产品在贮藏期(4 ℃、24 d)内活菌数维持在1×108CFU/g 以上,膳食纤维的添加能够改善山羊乳清饮料的口感、风味并增进其功能特性,活性乳酸菌饮料将菌株的益生特性与乳制品的健康功效完美结合,同时乳酸菌在发酵过程中产生多种维生素、有机酸、抗菌肽等生物活性物质能够有效提高产品的功能特性。近年来,国内外学者主要针对基础发酵剂在发酵乳中的产香机理进行研究,而对于复合益生菌在发酵乳制品中的挥发性代谢物及产香机制研究较少。Karacali 等[4]研究开菲尔粒对双蛋白乳饮料(按牛奶与豆奶质量比17∶3 混合)挥发性风味物质的影响时发现,应用开菲尔粒发酵能够促进双蛋白饮料中双乙酰、乙偶姻等具有脂肪香、奶油气息等挥发性风味物质的产生,降低其(E)-2-己烯醛、1-己醇等致豆腥味挥发性风味物质的含量。固相微萃取-气相色谱质谱联用技术 (SPME-GCMS)具有操作简单、灵敏度高、分析范围广等特点,目前,该技术主要用于乳制品、肉制品以及发酵果蔬中风味物质的检测[5]。
本研究以含有8 株菌株的复合益生菌发酵3种基料的乳酸菌饮料为对象,应用SPME-GC-MS技术结合多元统计分析乳酸菌饮料发酵及贮藏期内挥发性代谢物的变化,通过OAV 值确定乳酸菌饮料中的关键挥发性风味物质,对3 种基料的乳酸菌饮料整体风味进行比较预测,为复合益生菌的商业化应用及活性乳酸菌饮料的研发提供理论依据。
1 材料与方法
1.1 试验材料与仪器
1.1.1 试验菌株 本试验所用益生菌(见表1)直投式发酵剂由内蒙古农业大学“乳品生物技术与工程”教育部重点实验室提供。

表1 菌株信息Table 1 Information of strains
1.1.2 仪器与试剂 SRH60-70 高压均质机,上海申鹿均质机有限公司;电热恒温水浴锅,上海一恒科技有限公司;气相色谱-质谱联用仪(Agilent 7890B GC system-5977A MSD),赛默飞世尔科技有限公司;色谱柱 (HP-5 毛细管柱30 m×0.25 mm,0.25 μm),赛默飞世尔科技有限公司;手动固相微萃取(SPME)进样手柄(USA,SUP-ELCO),赛默飞世尔科技有限公司;固定搭载装置及50/30 μm 二乙基苯/碳分子筛/聚二甲基硅氧烷(divinylbenzene/carboxen/polydimethylsiloxane,DVB/CAR/PDMS)萃取头,赛默飞世尔科技有限公司;陶瓷加热磁力搅拌器 (Corning),美国Agilent 公司;脱脂乳粉(蛋白质含量33%),新西兰NZMP;浓缩乳清蛋白粉 (蛋白质含量80%),美国HILMAR 公司;大豆分离蛋白粉 (蛋白质含量95%,富吉普乐200),吉林不二蛋白有限公司;C3-C9 正构烷烃混标(AccuStandard,USA)、C10-C25 正构烷烃混标(AccuStandard,USA)、丙酮(色谱纯)、甲醇(色谱纯)、1,2-二氯苯(色谱纯)等均购于美国Sigma 公司。
1.2 试验方法
1.2.1 乳酸菌饮料的制备 分别将脱脂乳粉(12.1%)、乳清蛋白粉(5.0%)、大豆分离蛋白粉(4.2%)与葡萄糖(2%)混合溶解于预热至55 ℃的蒸馏水中,水合30 min,85 ℃杀菌15 min,冷却至37 ℃,将复合菌株按照总接种量5×106CFU/g 接入3 种不同发酵基料中,具体接种量如表2所示,3种发酵基料蛋白质含量均为4%,然后置于37 ℃恒温培养箱中发酵,待到达发酵终点得发酵基料(复合益生菌在3 种基料中生长至稳定期);将发酵基料与预先溶解并冷却的稳定剂、甜味剂混合,调配,20 MPa 均质,所得样品(蛋白质含量均为1%)即为发酵基料不同的3 种乳酸菌饮料。
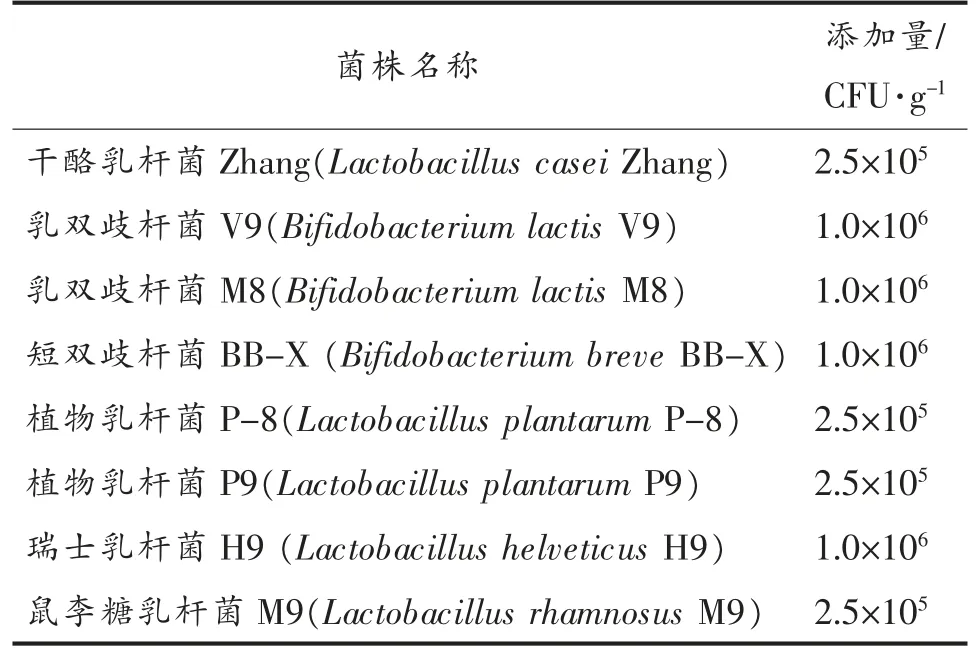
表2 样品中菌株添加量Table 2 The addition of strain in samples
1.2.2 发酵前及贮藏期内挥发性风味物质的测定 采用50/30 μm DVB/CAR/PDMS 萃取头,对发酵前及发酵结束后贮藏0,14,28 d 的脱脂乳饮料、豆乳饮料、乳清饮料进行富集,每组3 个平行,随后应用GC-MS 技术对其挥发性风味物质进行检测分析。
1.2.3 挥发性风味物质的萃取条件与测定条件
1)色谱条件 载气为He,流速1.0 mL/min;不分流进样,进样口温度250 ℃。程序升温方式,起始温度为35 ℃,保持5 min 后以5 ℃/min 的速率上升至140 ℃,保持2 min,再以10 ℃/min 的速率上升至250 ℃,保持3 min。
2)质谱条件 全扫描模式;EI 离子源;电子能量70 eV;离子源温度230 ℃;质量扫描范围m/z 35~500;无溶剂延迟。
3)SPME 萃取条件 50 ℃平衡60 min。
4)解吸附条件 250 ℃条件下解吸附3 min。
1.2.4 定性、定量分析 定性方法:利用随机携带Masshunter 工作站NIST 11 标准库进行自动比对,挑选匹配率≥85%的物质作为鉴定结果,同时依据Vandendool 等[6]的方法测定保留指数(retention indices,RI),根据文献报道的RI 值对发酵乳样品中的挥发性风味物质进行再次鉴定,RI 值计算公式如下:

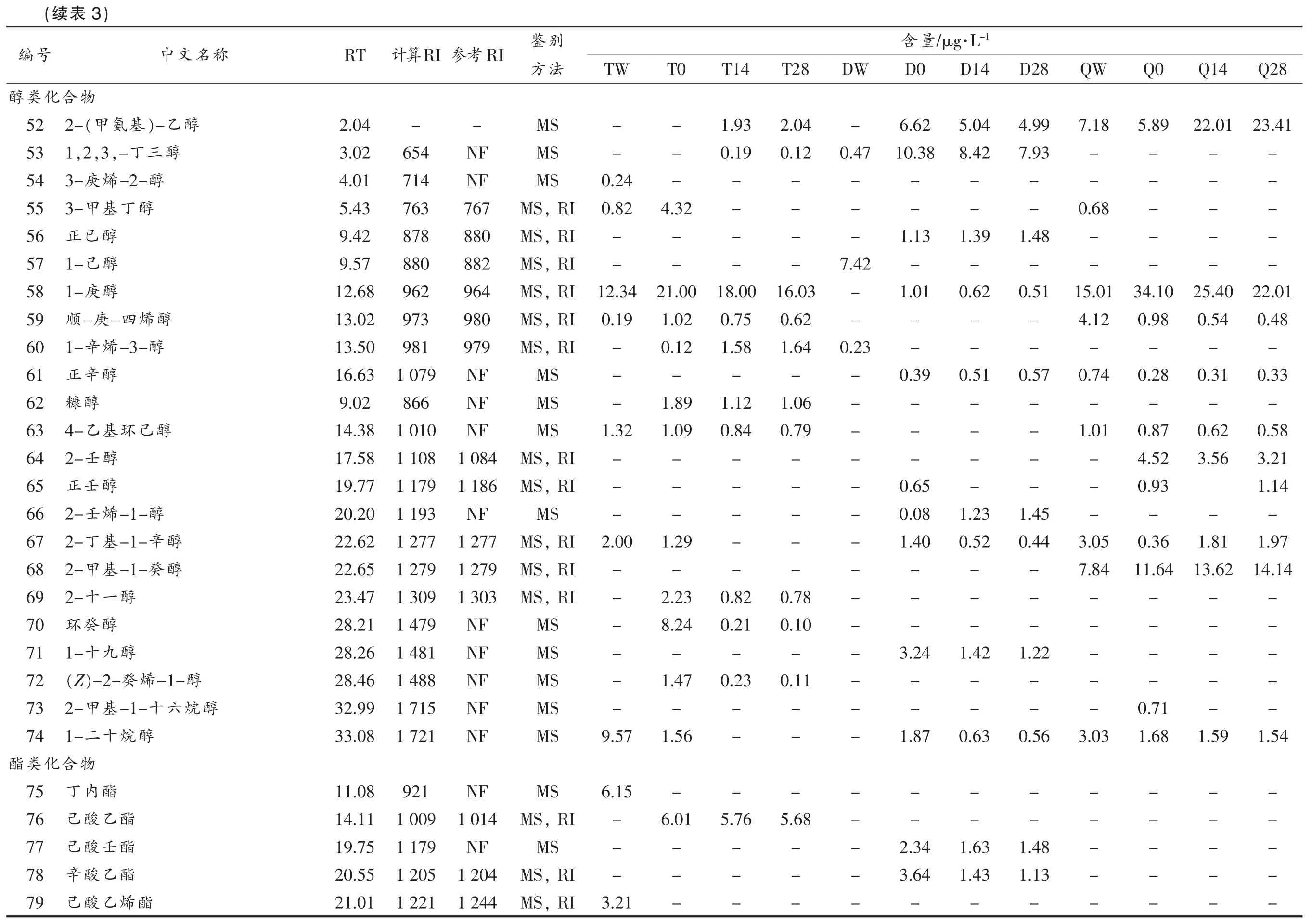
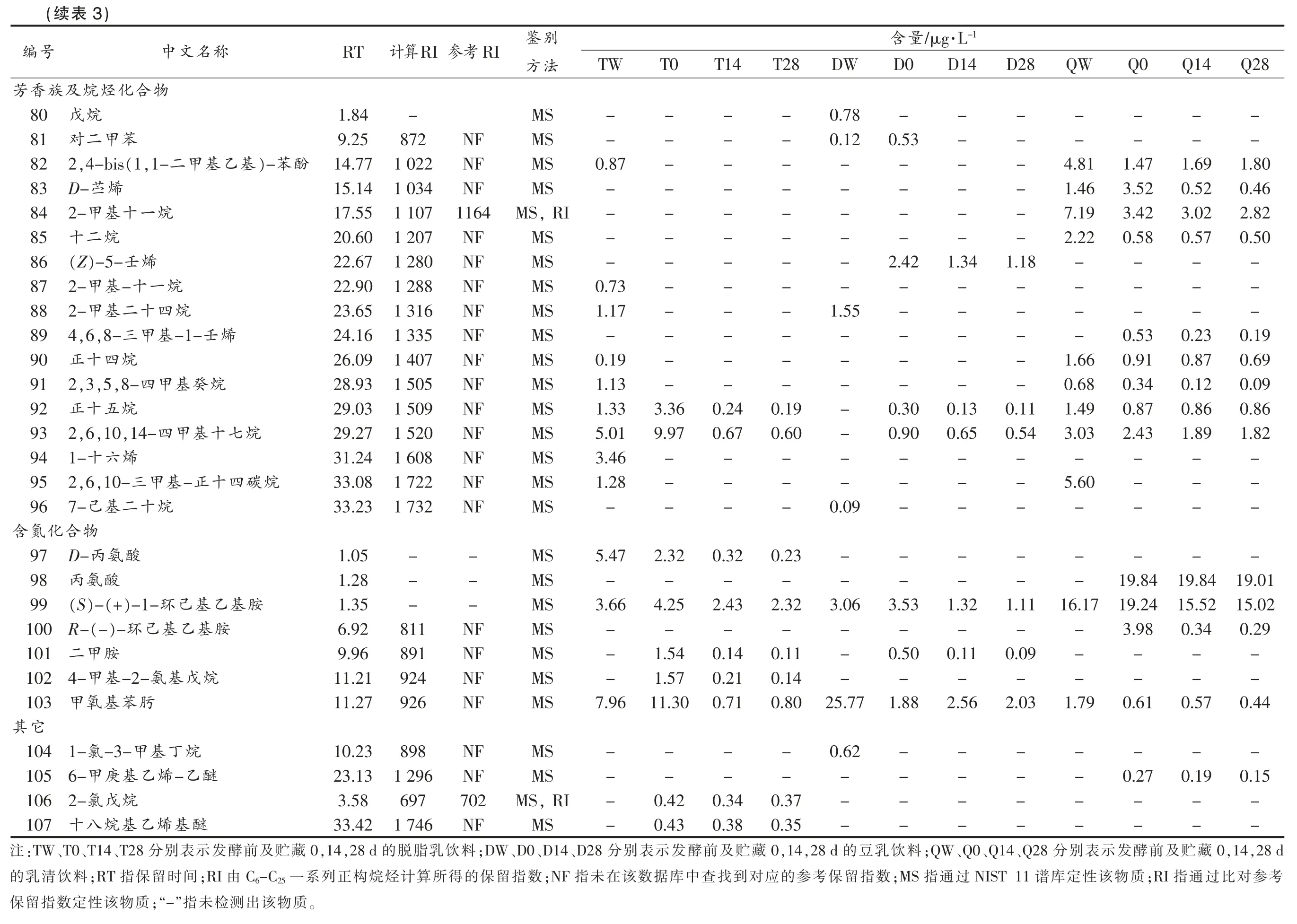
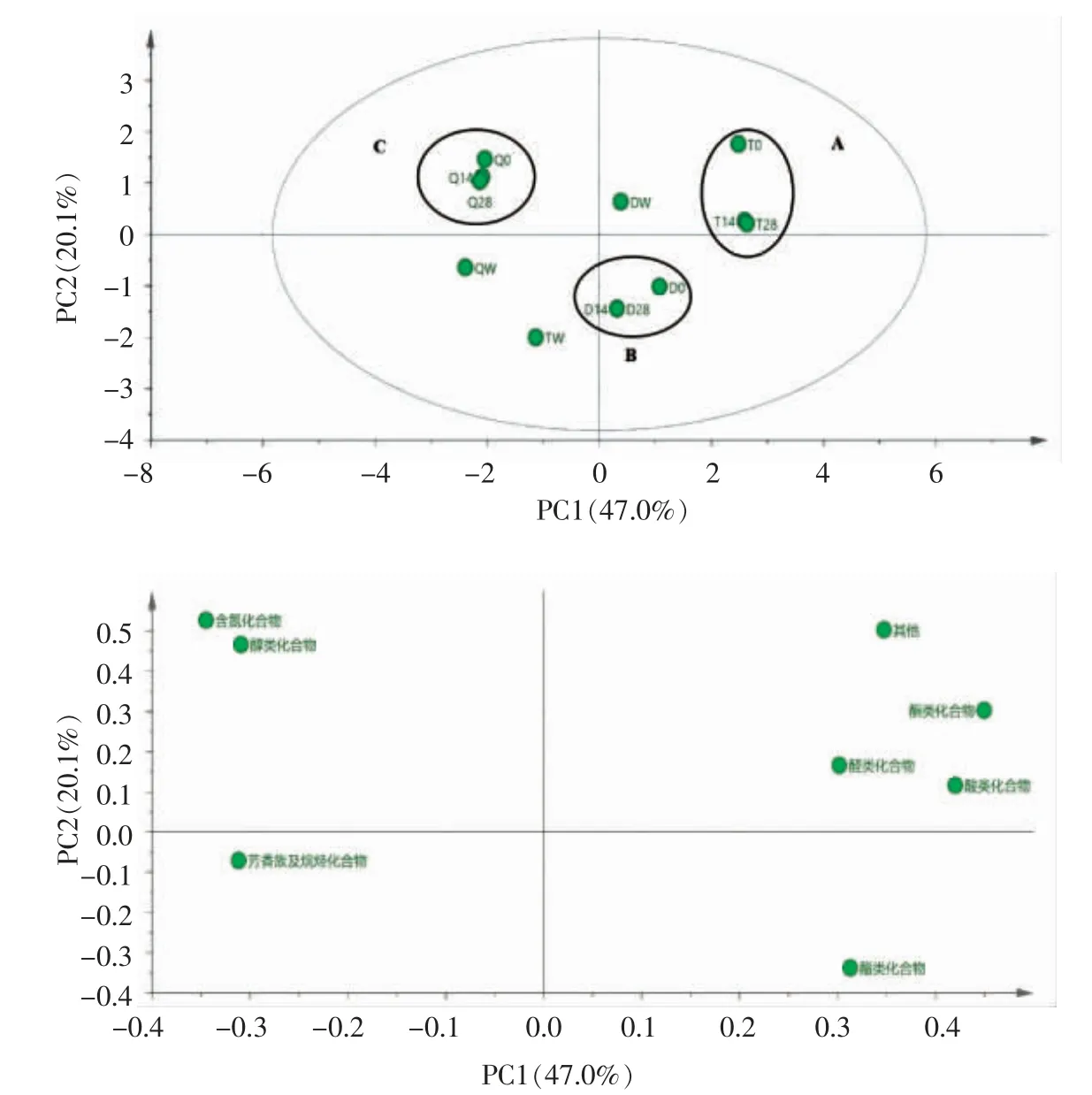
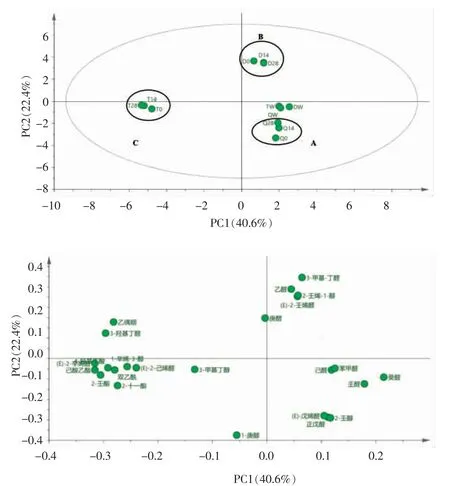
式中:RT(z)、RT(z+1)和RT(x)分别为正构烷烃碳原子数为Z、Z+1 和待测物x 的保留时间,且RT(z) 定量方法:在5 mL 发酵样品中添加质量浓度为0.01 μg/L 的内标物1,2-二氯苯溶液50 μL,样品中各组分风味物质的浓度可代入公式(2)计算: 式中:Ci——待测样品中各风味化合物质量浓度,μg/L;Cs——1,2-二氯苯质量浓度,μg/L;Ai——样品中待测物质对应的色谱峰面积;As——内标物色谱峰面积。 1.2.5 香气活度值评价法 在对乳酸菌饮料中挥发性风味化合物定量的基础上,以各风味化合物在水中的风味阈值作为参考,计算能表征风味化合物贡献率的物理量——香气活度值(odor activity value,OAV)[7-8]。可代入公式(2)计算: 式中:OAVi——风味化合物i 的香气活度值;Ci——乳酸菌饮料中挥发性风味化合物质量浓度,μg/L;OTi——所测风味化合物在水中的气味阈值。 应用SPSS 21.0 软件进行显著性、主成分分析处理,使用Origin lab 2017、SIMCA-P 14.1作图。 结合表3与图1可知,除了萃取头带来的少量硅氧烷类杂质,3 种不同基料的乳酸菌饮料在发酵前、发酵结束及贮藏过程中总计12 组样品共检测出107 种挥发性物质,其中包括21 种醛类、17 种酮类、13 种酸类、23 种醇类、5 种酯类、17 种芳香族及烷烃类、7 种含氮化合物、4 种其它化合物。发酵前的脱脂乳饮料、豆乳饮料、乳清饮料中分别检测出31,29,27 种挥发性物质,发酵结束时挥发性物质的数量分别为46,46,41 种,贮藏结束时挥发性物质的数量为43,45,39 种;乳制品在发酵过程中,乳酸菌及其产生的酶类通过分解代谢碳水化合物、蛋白质等一系列生物化学过程形成挥发性副产物,其中在糖酵解途径中,乳酸菌将葡萄糖转化为丙酮酸,进而通过柠檬酸代谢等多种代谢途径产生醛类、酮类、酸类和醇类化合物,在蛋白质水解途径中,其通过蛋白酶分解蛋白质形成肽类和氨基酸等多种代谢物,其中部分氨基酸等小分子物质进一步形成挥发性芳香化合物,而这一系列挥发性副产物的形成对发酵乳制品的滋气味和风味起到决定性的作用[9-12]。 以脱脂乳为发酵基料的乳酸菌饮料经发酵后,酮类化合物、酸类化合物和醇类化合物发生显著变化(P<0.05),其中,乙偶姻、双乙酰、2-壬酮、2-十一酮等酮类化合物在脱脂乳发酵过程中产生,贮藏期内,2-壬酮、2-十一酮含量逐渐降低,乙偶姻含量由4.72 μg/L 增加至8.02 μg/L,双乙酰由9.26 μg/L 降至3.96 μg/L,在乳糖代谢过程中,α-乙酰乳酸合成酶催化丙酮酸形成α-乙酰乳酸,随后α-乙酰乳酸脱羧酶作用于α-乙酰乳酸合成乙偶姻,同时部分α-乙酰乳酸通过化学氧化脱羧合成双乙酰,双乙酰通过双乙酰还原酶同样能够形成乙偶姻[13-14],这可能是贮藏期内两种重要的酮类化合物含量变化的主要原因;乳酸菌在脱脂乳中的生长过程中,乳酸、乙酸等酸类化合物含量不断增加,乳酸能够通过EMP 途径、HMP 途径及HK途径产生,当乳酸菌生长在葡萄糖受限的情况下,通过丙酮酸代谢产生乙酸,在贮藏过程中,随着活性乳酸菌饮料酸度不断增加,发酵菌株产酸活力减弱,后期酸类化合物含量逐渐开始下降;1-庚醇、糠醇、2-十一醇等醇类化合物在脱脂乳发酵过程中不断增加,贮藏期间逐渐降低。 豆乳饮料发酵前后主要在醛类化合物、酮类化合物、酸类化合物和醇类化合物上存在显著差异(P<0.05),其中己醛、苯甲醛、(E)-2-己烯醛等挥发性代谢物在豆乳发酵及贮藏过程中含量不断降低,己醛是亚油酸的一级氧化产物[15],苯甲醛由苯丙氨酸降解形成[16],乙醛、3-甲基丁醛在豆乳发酵过程中不断增加,贮藏期间其含量逐渐下降,乳酸菌能够通过丙酮酸脱羧、苏氨酸代谢等多条代谢途径产生乙醛,其中苏氨酸在苏氨酸醛缩酶的作用下降解产生乙醛是其主要代谢途径,豆乳饮料在贮藏过程中乙醛含量逐渐降低可能是因为部分乙醛在乙醛还原酶的作用下形成乙醇引起的[17-18],在氨基酸的分解代谢过程中,亮氨酸的转氨化形成α-酮异己酸,随后α-酮异己酸在α-酮酸脱氢酶的作用下通过非氧化性脱羧合成3-甲基丁醛[19];乙偶姻、2-羟基-3-戊酮、2-十三烷酮、4-甲基-3-庚酮等酮类化合物于豆乳发酵过程中产生,随着贮藏时间的增加其含量逐渐下降;辛酸、己酸、正癸酸等酸类化合物及正已醇、正辛醇、2-壬烯-1-醇等醇类化合物在豆乳发酵及贮藏过程中含量不断增加。 图1 乳酸菌饮料样品挥发性风味物质含量及数量Fig.1 Content and quantity of volatile flavor compounds in Lactobacillus beverages Q28 Q14------7.92 8.71--0.21 0.41 0.76 0.72------------1.34 1.21 1.46 1.42 0.22 0.32--------------3.06 3.21--0.86 0.84果结析GC-MS 分质物味风性发挥中程过藏贮及前酵发料饮菌酸乳3表Analysis of volatile flavor compounds in Lactobacillus beverages before fermentation and during storage by GC-MS-1·L/μg量含别鉴RI参考RI计算RT Q0 QW D28 D14 D0 DW T28 T14 T0 TW法方--3.09 3.21 8.92-----MS--2.32--1.36 1.54 2.84 0.52 3.91 4.01 4.98-MS NF 638 2.81-----1.24----MS NF 688 3.45 14.01---------,RI MS 702 702 3.68--1.39 1.48 1.69 0.11----,RI MS 697 704 3.74 0.65---------MS,RI 750 722 5.12 0.41 2.86 0.25 0.32 0.41 8.42 0.20 0.23 0.37 1.07,RI MS 809 808 6.66-----8.72 22.40 21.30 2.03-,RI MS 862 863 8.92----19.17 3.74 0.19 0.28 4.42-,RI MS 910 908 10.60-1.10---3.98---2.70,RI MS 970 970 13.21--0.18 0.21 0.01-----MS,RI 1 139 1 065 16.18--0.13 0.15 0.65-4.86 4.26 3.32-,RI MS 1 067 1 065 16.19-1.61--------MS NF 1 099 17.30 0.63 2.88 0.11 0.14 0.18 4.91---2.13,RI MS 1 119 1 111 17.70 0.09 1.86 0.37 0.43 0.52 2.82---1.65 MS,RI 1 204 1 214 20.79 1.26---------,RI MS 1 181 1 222 21.02------0.92 0.96 1.74-MS NF 1 233 21.35 0.33---------,RI MS 1 242 1 280 22.66--0.71 0.79 0.93 1.36----MS NF 1 372 25.15------0.16 0.19 2.19 3.22 MS NF 1 415 26.34--0.43 0.52 0.86-----MS NF 1 481 28.26------3.96 4.32 9.26-MS--2.26----5.72-----MS NF 641 2.85 3.72 1.23--------,RI MS 685 681 3.37--3.43 3.72 4.80-8.02 7.78 4.72-,RI MS 706 707 3.83 0.76---------,RI MS 733 732 4.55 Table 3 称名文中物合醛乙醛丁基3-羟醛烯二己,4-)-2,E(E醛戊正醛丁基甲3-醛烯(E)-戊醛己醛烯己)-2-(E醛庚醛甲苯醛烯(E)-2-壬醛烯辛)-2-(E醛一十-基甲2-醛壬醛癸醛甲苯基甲二,4-2醛糠基甲羟5-醛烯癸)-2-(E醛桃醛烷二十醛桂月物合酰乙双酮-3-庚基4-甲酮戊2-姻偶乙酮丁异基甲号编化类醛1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21化类酮22 23 24 25 26 Q28 Q14 Q0 QW D28----2.36----0.28----6.04----0.64-----0.27 0.29 0.35------2.97-----1.21 1.31 2.19-0.65 4.71 4.98 5.23-1.00 5.76 5.97 6.62 1.02 3.96----------2.01 1.98 1.03-2.41-------------------0.41----1.23----11.41 0.23 0.16--0.27 2.25 2.13 1.84-15.62----0.43----0.53--0.24-0.59-1·L/μg量含D14 D0 2.96 3.38 0.32 0.44 6.32 6.51 0.74 0.28----3.84 5.24--0.59 0.42 0.58 0.50 4.32 5.68----2.25 1.43------0.38 0.21 1.02 0.78 10.97 5.30 0.24 0.32 13.96 6.49 0.37-0.45-0.51-DW T28 T14 T0 TW-0.69 0.78 1.21-0.05----5.95 7.01 7.16 8.22 5.32 5.03-----1.48 1.32 1.25 0.72-----0.03---0.37 1.57 2.62 2.78 3.52 1.73 3.61 14.97 15.32 18.03-3.58 13.98 14.56 26.07-------0.34 0.47 0.87----17.18 2.54 0.92 2.69 2.84 31.88-2.32--3.21--3.25 3.56 4.13--28.41 26.32 9.27-------1.42 1.34 0.99--0.25 0.37 1.27--0.11 0.06-----0.94------------0.13 0.21 0.79-别鉴法方,RI MS MS MS,RI MS,RI MS,RI MS MS MS,RI,RI MS MS,RI MS MS MS MS MS MS MS MS,RI MS,RI MS,RI MS MS MS MS MS RI参考RI计算RT 821 822 7.36 NF 891 9.97 889 889 10.19 NF 897 10.20 962 951 12.21 1 003 999 14.01 NF 1 036 15.21 1 046 1 041 15.41 1 088 1 099 17.32 NF 1 301 23.27 1 491 1 488 28.54 NF 1 688 32.58--1.75--1.97 NF 783 6.02 NF 891 9.98 NF 923 11.16 1 020 1 017 13.64 NF 1 173 19.58 1 178 1 193 20.20 1 226 1 276 22.54 NF 1 380 25.35 NF 1 403 25.99 NF 1 693 32.66 NF 2 176 38.15酸羧-)3表(续称名文中号编酮戊-3-基羟2-27酮丁-2-基甲)-3-(S 28酮2-庚29酮已-基甲5-30酮庚-3-基甲5-31酮辛2-32酮-2-烯庚-3-基甲5-33-2-酮烯3-辛34酮壬2-35酮一十2-36酮烷三十2-37酮烷五十环38物合化类酸酮醇-3-三,5-,4-1醇己环39酸乙40酸酮丙41酸乳42酸丁基羟4-43酸己44酸甲苯45酸辛46酸壬47酸癸正48酸辛基7-氧49酸烯四十-9-基甲Z-8-50酸烷八十51 Q28 23.41-----22.01 0.48-0.33-0.58 3.21 1.14-1.97 14.14-----1.54-----Q14 22.01-----25.40 0.54-0.31-0.62 3.56-1.81 13.62-----1.59-----Q0 QW D28 5.89 7.18 4.99--7.93----0.68---1.48---34.10 15.01 0.51 0.98 4.12----0.28 0.74 0.57---0.87 1.01-4.52--0.93----1.45 0.36 3.05 0.44 11.64 7.84---------1.22---0.71--1.68 3.03 0.56--------1.48--1.13----1·L/μg量含D14 D0 5.04 6.62 8.42 10.38----1.39 1.13--0.62 1.01----0.51 0.39-------0.65 1.23 0.08 0.52 1.40------1.42 3.24----0.63 1.87----1.63 2.34 1.43 3.64--DW T28 T14 T0 TW-2.04 1.93--0.47 0.12 0.19------0.24---4.32 0.82-----7.42-----16.03 18.00 21.00 12.34-0.62 0.75 1.02 0.19 0.23 1.64 1.58 0.12-------1.06 1.12 1.89--0.79 0.84 1.09 1.32------------------1.29 2.00------0.78 0.82 2.23--0.10 0.21 8.24-------0.11 0.23 1.47---------1.56 9.57----6.15-5.68 5.76 6.01---------------3.21别鉴法方MS MS MS,RI MS,RI MS MS,RI,RI MS,RI MS MS,RI MS MS MS MS,RI,RI MS MS MS,RI,RI MS,RI MS MS MS MS MS MS MS,RI MS MS,RI MS,RI MS RI RI 参考计算RT--2.04 NF 654 3.02 NF 714 4.01 767 763 5.43 880 878 9.42 882 880 9.57 964 962 12.68 980 973 13.02 979 981 13.50 NF 1 079 16.63 NF 866 9.02 NF 1 010 14.38 1 084 1 108 17.58 1 186 1 179 19.77 NF 1 193 20.20 1 277 1 277 22.62 1 279 1 279 22.65 1 303 1 309 23.47 NF 1 479 28.21 NF 1 481 28.26 NF 1 488 28.46 NF 1 715 32.99 NF 1 721 33.08 NF 921 11.08 1 014 1 009 14.11 NF 1 179 19.75 1 204 1 205 20.55 1 244 1 221 21.01)3表(续称名文中号编物合化类醇醇乙)-基氨(甲2-52醇三丁,-,3,2 1 53醇-2-烯庚3-54醇丁基甲3-55醇已正56醇1-己57醇庚1-58醇烯四-庚-顺59-3-醇烯1-辛60醇辛正61醇糠62醇己环基乙4-63醇2-壬64醇壬正65醇-1-烯壬2-66醇-1-辛基2-丁67醇癸-1-基甲2-68醇一十2-69醇癸环70醇九十1-71醇-1-烯癸)-2-(Z 72醇烷六十-1-基甲2-73醇烷十1-二74物合化类酯酯内丁75酯乙酸己76酯壬酸己77酯乙酸辛78酯烯乙酸己79 -1·L/μg量含Q28 Q14 Q0 QW D28 D14 D0-------------0.53 1.80 1.69 1.47 4.81---0.46 0.52 3.52 1.46---2.82 3.02 3.42 7.19---0.50 0.57 0.58 2.22-------1.18 1.34 2.42--------------0.19 0.23 0.53----0.69 0.87 0.91 1.66---0.09 0.12 0.34 0.68---0.86 0.86 0.87 1.49 0.11 0.13 0.30 1.82 1.89 2.43 3.03 0.54 0.65 0.90----------5.60-----------------19.01 19.84 19.84----15.02 15.52 19.24 16.17 1.11 1.32 3.53 0.29 0.34 3.98--------0.09 0.11 0.50-------0.44 0.57 0.61 1.79 2.03 2.56 1.88-------0.15 0.19 0.27------------------,28 d,14 0藏贮及前酵发示表别分、Q28、Q14、Q0;QW料饮乳考参对比过通指;RI质物该性定库谱NIST 11过通指;MS数DW T28 T14 T0 0.78---0.12---------------------------1.55----------------0.19 0.24 3.36-0.60 0.67 9.97--------0.09----0.23 0.32 2.32----3.06 2.32 2.43 4.25-----0.11 0.14 1.54-0.14 0.21 1.57 25.77 0.80 0.71 11.30 0.62--------0.37 0.34 0.42-0.35 0.38 0.43豆的,28 d,14 0藏贮及前酵发示表指留保考参的应对到找查中库据数)3表(续别鉴RI参考RI计算RT称名文中号编TW法方物合化烃烷及族香芳-MS-1.84烷戊80-MS NF 872 9.25苯甲二对81 0.87 MS NF 1 022 14.77酚苯)-基乙基甲二,1-(1,4-bis 2 82-MS NF 1 034 15.14烯D-苎83-,RI MS 1164 1 107 17.55烷一十基甲2-84-MS NF 1 207 20.60烷二十85-MS NF 1 280 22.67烯壬)-5-(Z 86 0.73 MS NF 1 288 22.90烷一十-基甲2-87 1.17 MS NF 1 316 23.65烷四十二基甲2-88-MS NF 1 335 24.16烯壬-1-基甲三,8-,6 4 89 0.19 MS NF 1 407 26.09烷四十正90 1.13 MS NF 1 505 28.93烷癸基甲四,8-,5,3 2 91 1.33 MS NF 1 509 29.03烷五十正92 5.01 MS NF 1 520 29.27烷七十基甲四,14-,10,6 2 93 3.46 MS NF 1 608 31.24烯六十1-94 1.28 MS NF 1 722 33.08烷碳四十正-基甲三,10-,6 2 95-MS NF 1 732 33.23烷十二基7-己96物合化氮含5.47 MS--1.05酸氨丙D-97-MS--1.28酸氨丙98 3.66 MS--1.35胺基乙基己环)-1-(+)-(S 99-MS NF 811 6.92胺基乙基己100 R-(-)-环-MS NF 891 9.96胺甲二101-MS NF 924 11.21烷戊基氨-2-基甲102 4-7.96 MS NF 926 11.27肟苯基氧甲103-MS NF 898 10.23烷丁基甲-3-它氯104 1-其-MS NF 1 296 23.13醚乙-烯乙基庚甲105 6--,RI MS 702 697 3.58烷戊氯106 2--MS NF 1 746 33.42醚基烯乙基烷八十107别分、D28、D14、D0;DW料饮乳脂脱的,28 d,14 0藏贮及前酵发示表别分、T28、T14、T0:TW注该在未指;NF数指留保的得所算计烃烷构正列系一-C 25 C 6由;RI间时留保指;RT料饮清乳的。质物该出测检未”指;“-质物该性定数指留保 乳清饮料发酵前后主要在酮类化合物、醇类化合物、芳香族及烷烃化合物和含氮化合物上存在显著差异(P<0.05);2-戊酮、2-辛酮、2-壬酮、2-十一酮、2-十三烷酮等酮类化合物及1-庚醇、2-壬醇等醇类化合物在乳清发酵过程中不断增加,在贮藏过程中,随着贮藏时间的推移其含量逐渐降低,其中,2-壬酮由辛酸的β-氧化和癸酸的脱羧反应生成[20];2-甲基十一烷、十二烷、正十四烷、正十五烷等烷烃化合物及丙氨酸、甲氧基苯肟等含氮化合物在乳清发酵及贮藏过程中其含量逐渐降低。 对发酵前,发酵结束及贮藏期间乳酸菌饮料中所检测到的8 类挥发性风味物质进行主成分分析,结果如图2所示:3 种不同基料的乳酸菌饮料区分明显,而相同基料的乳酸菌饮料在贮藏期内分布接近,以上结果表明:不同基料的乳酸菌饮料经复合益生菌发酵后,挥发性代谢物明显不同,而相同基料的乳酸菌饮料在贮藏期间 (T14-T28、D14-D28、Q14-Q28)挥发性代谢物变化较小;以脱脂乳为发酵基料的乳酸菌饮料中,酮类化合物、醛类化合物、酸类化合物聚集在第一,二主成分正向端,且贡献较大,酮类化合物通过糖酵解、部分氨基酸的降解、脂肪酸的氧化以及相关微生物的代谢形成,具有甜香、清香和脂肪的油腻气息[21-22],醛类化合物多为中间体化合物,化学性质活泼,是发酵乳制品中重要的呈味物质[23],酸类化合物一般为C2-C10的饱和脂肪酸,主要形成于蛋白质和脂肪的水解代谢途径,对乳酸菌饮料的滋味产生影响并赋予其清爽口感[24-25]。以豆乳为发酵基料的乳酸菌饮料中,酯类化合物聚集在第一主成分正向端,且贡献较大,发酵乳制品中的酯类物质是由酸类物质和醇类物质发生酯化反应或环化反应形成的,由于其阈值较低,对发酵乳制品的风味影响较为明显,能够赋予其奶酪香和花香[26-28];以乳清为发酵基料的乳酸菌饮料中,醇类化合物、含氮化合物聚集在第二主成分正向端,且贡献较大,醇类化合物的形成与甲基酮还原、亚油酸降解及碳水化合物的代谢有关,其能够与乳香平衡,更好地改善发酵乳制品的口感[29],含氮化合物阈值较高,对发酵乳制品的整体风味影响相对较小[30]。 图2 乳酸菌饮料主成分得分图和挥发性风味物质主成分载荷图Fig.2 Score scatter plot and loading scatter plot of volatile flavor components in Lactobacillus beverages 活性乳酸菌饮料中各挥发性物质的种类、含量及阈值共同决定其整体风味,香气活性值(OAV)是指香气组分浓度与其在水中香味阈值的比值,能够准确评价单一香气组分对整体风味的贡献程度[31]。不同基料乳酸菌饮料发酵前、发酵结束及贮藏期间主要风味物质的OAV 值见表4。通常将OAV≥1 的物质认定为样品中的关键风味化合物,对整体风味有重要贡献作用,而0.1≤OAV<1 的组分对样品的整体风味有重要修饰作用[32]。本研究对OAV≥0.1 的24 种主要挥发性代谢物进行主成分分析,由图4可知,3 种不同基料的乳酸菌饮料区别明显,而相同基料的乳酸菌饮料在贮藏期间分布接近,以上结果表明,不同基料的乳饮料经复合益生菌发酵后,主要挥发性代谢物明显不同而相同基料的乳酸菌饮料在贮藏期间主要挥发性代谢物变化较小。 脱脂乳饮料在发酵后及贮藏期与乙偶姻、3-羟基丁醛、双乙酰、2-壬酮、2-十一酮、(E)-2-辛烯醛、(E)-2-己烯醛、4-羟基丁酸、3-甲基-1-丁醇、己酸乙酯等10 种OAV≥0.1 的挥发性物质有较强相关性。乙偶姻作为发酵乳制品中常见的风味物质具有令人愉快的弱奶油香味,略带甜味,双乙酰赋予发酵乳制品较重的奶油香味、类似坚果仁的风味[13-14],3-羟基丁醛、庚醛、2-壬酮、2-十一酮等具有果香、脂肪香、奶甜味,(E)-2-辛烯醛、(E)-2-己烯醛等烯醛类化合物具有类似橘子皮的风味[33],3-甲基-1-丁醇能够赋予发酵乳制品麦芽香、花香的风味[34]。 图3 乳酸菌饮料主成分得分图和关键挥发性风味物质主成分载荷图Fig.3 Score scatter plot and loading scatter plot of key volatile flavor components in Lactobacillus beverages Q28 Q14 Q0------0.66 0.73 1.17---0.18 0.34 0.54 0.17 0.16 0.09---------------1.34 1.21 0.63 1.46 1.42 0.09--1.08------0.0014 0.0015 0.0017------0.0054 0.006 0.007值OAV应对及质物味风性键关中料饮菌酸乳4表Key flavor substances and corresponding OAV values in lactic acid bacteria beverages Table 4 OAV觉感QW D28 D14 D0 DW T28 T14 T0 TW a值阈-0.36 0.37 1.03-----8.7-0.05 0.06 0.11 0.02 0.14 0.15 0.18-27---------12-1.16 1.23 1.41 0.09----1.2---------1.2 0.63 0.06 0.07 0.09 1.87 0.04 0.05 0.08 0.24 4.5----0.05 0.12 0.11 0.01-190---6.39 1.25 0.06 0.09 1.47-3 0.37---1.33---0.90 3-2.22 2.63 0.06-----0.08-0.04 0.05 0.22-1.62 1.42 1.11-3 2.88 0.11 0.14 0.18 4.91---2.13 1 1.86 0.37 0.43 0.52 2.82---1.65 1---------0.3-----1.72 1.88 4.03-2.3---1.06-----5.4 0.0006--------2150-0.06 0.07 0.09-0.15 0.14 0.09-55-0.04 0.05 0.05 0.04 0.05 0.05 0.06 0.04 140---------50称名文中物合化类醛醛乙醛丁基羟3-醛戊正醛丁基甲3-醛烯戊)-(E醛己醛烯己)-2-(E醛庚醛甲苯醛烯壬)-2-(E醛烯(E)-2-辛醛壬醛癸醛烯癸)-2-(E物合化类酮酰乙双酮庚-3-基甲4-酮戊2-姻偶乙酮庚2-酮辛2- Q28 Q14 Q0 QW D28 0.24 0.26 0.44-0.13 0.02 0.02 0.02-0.003 0.00009 0.00009 0.00005-0.0001---------0.0001----0.02 0.00007 0.00005--0.00009 0.0008 0.0007 0.0006-0.05---0.17------0.07 0.08 0.10 0.05 0.002----------0.13 0.14 0.18------1.45 0.002 0.001 0.0003 0.002 0.0003----------OAV D14 D0 0.12 0.08 0.002 0.002 0.0001 0.00007--0.0001 0.00007 0.02 0.01 0.00008 0.0001 0.005 0.002----0.002 0.003------1.23 0.08 0.0004 0.001---0.002 DW T28 T14 T0 0.72 2.99 3.06 3.61 0.01 0.05 0.06 0.10 0.00004 0.0001 0.0001 0.001-0.12 0.11 0.04-----0.0005 0.0007 0.003-0.00004 0.00002----0.0003---1.08 0.03----0.05 0.05 0.06 0.15 1.09 1.05 0.08-0.0002 0.0002 0.0004-----------0.0009-0.41 0.41 0.43 0.0006---。TW--------0.21-0.04----0.002--质物的出测觉感a值阈5 255 22 000 240 3 000 500 3 000 3 000 4 250 330 1.5 5 000 25 1 1 300 14 200检未分部;“-”指值)4表(续称名文中酮壬2-酮一十2-物合化类酸酸乙酸丁基4-羟酸己酸辛酸壬酸癸正物合化类醇醇丁基3-甲醇己1-醇庚1-醇-3-烯辛1-醇糠醇壬2-醇-1-烯壬2-醇辛-1-基丁2-物合化类酯酯乙酸己物合化烃烷及族香芳苯甲二对阈的中水在质物各a 指:注 豆乳饮料在发酵后及贮藏期与乙醛、3-甲基丁醛、庚醛、(E)-2-壬烯醛、2-壬烯-1-醇等5 种OAV≥0.1 的挥发性物质有较强的正相关性。乙醛是发酵乳制品中重要的风味化合物之一,具有果香、清香味,适量的乙醛能够提供给发酵乳制品较好的风味[17-18]。相关研究表明,豆乳中的豆腥味主要来源于脂肪氧化酶催化亚油酸、亚麻酸等不饱和脂肪酸形成各类挥发性呈味物质,己醛、苯甲醛、戊醇、1-己醇、(E,E)-2,4-癸二烯醛等风味化合物呈现青草味、生味、磨茹、辛辣味,被定义为豆腥味化合物,乳酸菌发酵能够有效降低并去除豆腥味[35-36];由表3可知,以豆乳为发酵基料的乳酸菌饮料经复合益生菌发酵后,己醛、苯甲醛、1-己醇等致豆腥味挥发性物质的含量显著降低 (P<0.05),同时产生3-甲基丁醛、(E)-2-壬烯醛等赋予发酵乳制品巧克力、青草香的风味物质[37]。 乳清饮料在发酵后及贮藏期与正戊醛、(E)-戊烯醛、2-壬醇、壬醛、癸醛、1-庚醇等6 种OAV≥0.1 的挥发性物质有较强的相关性,正戊醛、壬醛、癸醛等醛类化合物具有清爽的芳香味、脂肪气息,1-庚醇具有土质、油质的风味[38]。 本研究以8 株分离源明确,有良好益生特性的益生菌为发酵菌株,研究复合益生菌对3 种基料(脱脂乳粉、浓缩乳清蛋白粉和大豆分离蛋白粉)的乳酸菌饮料挥发性代谢物的影响。利用SPME-GC-MS 技术定性定量分析乳酸菌饮料发酵前、发酵结束及贮藏过程中挥发性风味物质的变化,共检测出107 种挥发性物质,其中包括21种醛类、17 种酮类、13 种酸类、23 种醇类、5 种酯类、17 种芳香族及烷烃类、7 种含氮化合物、4 种其它化合物。对挥发性代谢物成分的主成分分析结果表明:不同基料的乳酸菌饮料经复合益生菌发酵后,挥发性代谢物明显不同,相同基料的乳酸菌饮料在贮藏期间挥发性代谢物变化较小。对主要挥发性风味物质(OAV≥0.1)进行主成分分析结果表明:在贮藏期的脱脂乳饮料中,乙偶姻、3-羟基丁醛、双乙酰、2-壬酮、2-十一酮、(E)-2-辛烯醛、(E)-2-己烯醛、4-羟基丁酸、3-甲基-1-丁醇、己酸乙酯等10 种挥发性物质贡献较大;在贮藏期的豆乳饮料中,乙醛、3-甲基丁醛、庚醛、(E)-2-壬烯醛、2-壬烯-1-醇等5 种挥发性物质贡献较大并呈正相关性,且发酵后的豆乳饮料中己醛、苯甲醛等致豆腥味挥发性物质的含量显著降低(P<0.05),同时产生3-甲基丁醛、(E)-2-壬烯醛等赋予豆乳饮料良好风味的挥发性物质;在贮藏期的乳清饮料中,正戊醛、(E)-戊烯醛、2-壬醇、壬醛、癸醛、1-庚醇等6 种OAV≥0.1 的挥发性物质贡献较大。本研究为复合益生菌的商业化应用及活性乳酸菌饮料的研制开发提供理论依据和指导。

1.3 数据处理
2 结果分析
2.1 活性乳酸菌饮料挥发性代谢物分析



2.2 活性乳酸菌饮料挥发性代谢物主成分分析
2.3 活性乳酸菌饮料主要挥发性代谢物的主成分分析


3 结论
