氟喹诺酮类药物残留限量及检测技术研究进展
2021-04-21张运尚杜加茹王伟东樊剑鸣
张运尚,杜加茹,王伟东,樊剑鸣
(郑州大学公共卫生学院,河南郑州 450001)
氟喹诺酮类药物(Fluoroquinolones,FQS)是第3 代喹诺酮药物,其化学结构是在喹啉环的6 位上加入了氟原子,7 位上连有哌嗪基的一类衍生物,此特点使得原本亲脂性的吡酮类药物增加了适度的亲水性,同时降低了蛋白结合率,提高生物利用度[1-2]。该类药物通过抑制细菌的DNA 和RNA 合成从而达到抑菌作用[3]。相比第1 代及第2 代喹诺酮药物,FQS 的抗菌活性明显增加,抗菌谱显著扩大,对革兰氏阳性菌(金葡球菌、链球菌、肺炎球菌)和革兰氏阴性菌(肠杆菌科、流感杆菌和奈瑟菌属)[4]以及一些衣原体、支原体和螺旋体均有抗菌作用[5],因此被广泛应用在临床上治疗细菌感染性疾病。FQS 代表药物主要包括恩诺沙星(Enrofloxacin,ENR)、环丙沙星(Ciprofloxacin,CIP)、诺氟沙星(Norfloxacin,NOR)、达氟沙星(Danofloxacin,DAN)、氟罗沙星(Flero xacin,FLE)、沙拉沙星(Saraflaxacin,SFX)、依诺沙星(Enoxacin,EX)等。由于养殖业对食品中兽药残留的意识不足,存在大量不规范使用兽药、抗生素及违禁药品和不严格执行休药期规定等诸多问题,使得动物性产品中兽药残留超标[6]。随着我国居民生活水平提高,对动物性食品的需求也不断增加。当人们过多食用了含有药物残留的动物性食品后,通常不表现为急性毒性,而是药物在人体蓄积[7-8],对人体多个系统(如中枢神经系统、循环系统、消化系统、泌尿系统、呼吸系统等)造成损害[9-13]。更为严重的是,FQS 的不合理使用容易诱导人类致病菌对其耐药性的增强,不利于该类药物对人类疾病的治疗[14-17]。本文综述了FQS 在动物源性食品中残留的检测标准和3 种检测FQS 的常用方法,以期为在不同检测条件下选择最适的检测方法提供理论依据。
1 FQS 残留限量
FQS 残留存在诸多不良反应,逐渐引起世界各国的广泛关注。为了监控兽药在动物性食品中的残留,联合国粮农组织和世界卫生组织食品添加剂联席专家委员会(JECFA)早在1987 年第32 次会议中报告了相关兽药的残留毒性;从1997 年8 月20 日起,美国禁止将FQS 作为非限制性药物使用;美国联邦法规(21CFRS530,41)规定的禁用兽药品种(不能使用于供食用的动物)也包括FQS 类药物[18];欧盟(EC)于2009 年12 月22 日发布了37/20210 号法,其中关于动物性食品及其产品中兽药残留(B 类)制定最高残留限量(MRLs)包括喹诺酮类药物[19]。日本于2003 年7 月1 日起对进口生鳗鱼及其制品进行氧氟沙星、诺氟沙星、环丙沙星、恩诺沙星残留检测,并规定最大残留限量为50 µg/kg[20];我国颁布的首批绿色畜产品论证准则《绿色食品—兽药使用准则》也取消了FQS 在肉用动物上的使用。我国农业部兽药残留专家委员会在参考JECFA 及美国(CFR)和EC 有关标准的基础上,制定了恩诺沙星(Enrofloxacin)、二氟沙星(Difloxacin)、达氟沙星(Danofloxacin)在动物性食品中最大残留限量的国家标准[21],具体见表1。
2 FQS 残留检测方法
目前,针对FQS 的检测方法主要有高效液相色谱法(HPLC)、液相色谱-质谱联用法(HPLC-MS/MS)、酶联免疫分析法(ELISA)等。不同分析方法对FQS 的检测结果优缺点见表2。
2.1 HPLC 色谱法原理是利用样品中各个组分的物理化学性质差异(如分子大小及形状、亲和力、分配系数和吸附力等),使各组分在固定相和流动相中的分布程度不同,从而以不同的速度移动而达到分离样品的目的。高效液相色谱法又称“高分离度液相色谱”,是色谱法的一个重要分支。HPLC 利用高压输液系统将不同极性的液体流动相泵入装有固定相的色谱柱,流动相的各个组成成分在色谱柱内被分离开后,进入检测器得到不同的峰信号,最后通过分析对比这些信号判断待测样品所含物质。根据检测器的种类可以将HPLC 分为不同的方法,如高效液相色谱-紫外吸收检测法(HPLC-UV/DAD)、高效液相色谱-荧光检测法(HPLC-FLD)、高效液相色谱-固相萃取(HPLC-SPE)。HPLC 法具有应用范围广、分离能力强、测定灵敏度高、样品易回收等特点。
方永卫等[22]利用HPLC 法建立动物性产品中3 种FQS(麻保沙星、环丙沙星、恩诺沙星)含量的方法,设置波长为278~299 nm,采用流动相为A 液为0.05 mol/L磷酸0.5%三乙胺溶液,B 液为乙腈,进行梯度洗脱,得到最佳色谱分离图,表明3 种目标药物的标准曲线的相关系数均大于0.99,3 种药物的检测限为0.5 μg/mL。样品的添加回收率均在82.0%~105.6%,证明该方法用于动物性食品提取方法的可靠性较好,可以用于检测动物性食品中的FQS 残留。

表1 兽用氟喹诺酮药物在动物源性食品中最大残留限量 µg/kg

表2 几种分析方法对不同FQS 药物的检测结果优缺点比较
Vakh 等[23]使用Zr-Fe-C 磁性纳米粒子作为吸附剂进行自动磁分散微固相萃取,测定肉类婴儿食品中的氟喹诺酮类抗菌药物(氟罗沙星、诺氟沙星和氧氟沙星)含量。该方法将样品溶液注入流化反应器中,然后基于流化床策略使用磁性纳米颗粒从样品基质中在线分离分析物,并使用高效液相色谱系统洗脱和测定分析物。在实验最佳条件下,3 种药物的浓度为5~1 000 μg/L,相关系数均大于0.99。计算得出的检出限为氟罗沙星3.0 μg/L,诺氟沙星和氧氟沙星1.5 μg/L。所有分析物的回收率均在86%~122%。该方法检出限低于国家标准,可以用于测定肉类婴儿食品中的FQS 含量。
2.2 超高效液相色谱-串联质谱法(HPLC-MS/MS)质谱法原理是将样品的分子进行电离,不同质量的电子在电场或磁场中,按照质荷比的大小和相对强度进行分离和排序,形成有规则的质谱,从而对物质进行结构鉴定和定量分析。HPLC-MS/MS 法是常见的一种色谱-质谱连用技术,首先将样品中的分析物经过液相色谱柱分离后输送至质谱,根据特定的质荷比(m/z)离子进行选择,所选择的母离子可以产生具有特定结构信息的离子产物,进而可以对目标化合物进行选择性的定量分析。相比于HPLC,HPLC-MS 分离能力更强,分析结果具有更高的可靠性。
曹骞等[24]利用HPLC-MS/MS 建立了鸡蛋中8 种喹诺酮类药物残留检测方法,该方法对鸡蛋中各类化合物的检出限为0.3 μg/kg,定量限为1.0 μg/kg,线性范围为1~100 μg/L,相关系数均大于0.996 7。在空白鸡蛋样品中添加20 ng/mL 的8 种喹诺酮类药物进行回收试验,平均回收率范围为83.0%~108.5%。该方法灵敏度较高,可以用于检测鸡蛋中FQS 残留。
不同样品基质中FQS 液相检测方法见表3。可以看出HPLC 具有分离度高、灵敏度好及准确度高等特点,是目前检测FQS 残留使用较多的方法,但其对样品的前处理时间较长,检测过程较为复杂,不能满足大批量检测的需求,同时还存在溶剂消耗较大、对环境有较大污染等弊端。而相比于HPLC,HPLC-MS/MS 不仅具有色谱法的分离能力,还具有质谱法的灵敏度、选择性和识别能力,对于某些分子量大、极性强、稳定性差的样品有较好的分离检测和定性分析能力。利用HPLC-MS/MS 针对FQS 残留的检出限和定量限均高于HPLC,MS 提供了检测组织提取物中FQS 所需的特异性,该方法适合用于FQS 残留的确证。但是,该方法需要的仪器设备昂贵,对样品的前处理较复杂,对操作人员的要求也较高,导致该方法难以在基层工作中普及。
2.3 ELISA 酶联免疫吸附技术的基本原理是将抗原或抗体固定在特殊材料上,与其酶标的抗体或抗原发生特异性的反应,在高效的酶促反应下,达到扩大免疫反应的作用。利用FQS 中的羧基与载体蛋白质游离氨基的缩合反应,将FQS 与载体连接合成人工抗原,该方法简单,快速,且不需要昂贵的仪器设备,适用于大量样品的快速检测[32]。同时该方法具有特异性强、灵敏度高、操作简便等优点,可用于现场样品的检测,因此近年来国内外应用ELISA 法测定抗生素残留的研究越来越多。我国也在2008 年发布了《动物性食品中氟喹诺酮类药物残留检测-酶联免疫吸附法》(农业部1025号公告-8-2008)标准,该标准规定了在动物性食品中FQS 残留量检测的制样和酶联免疫吸附法,适用于动物源性食品中猪和鸡的肌肉、蜂蜜、鸡蛋和虾中恩诺沙星、环丙沙星、氧氟沙星、诺氟沙星等FQS 残留量的检测。
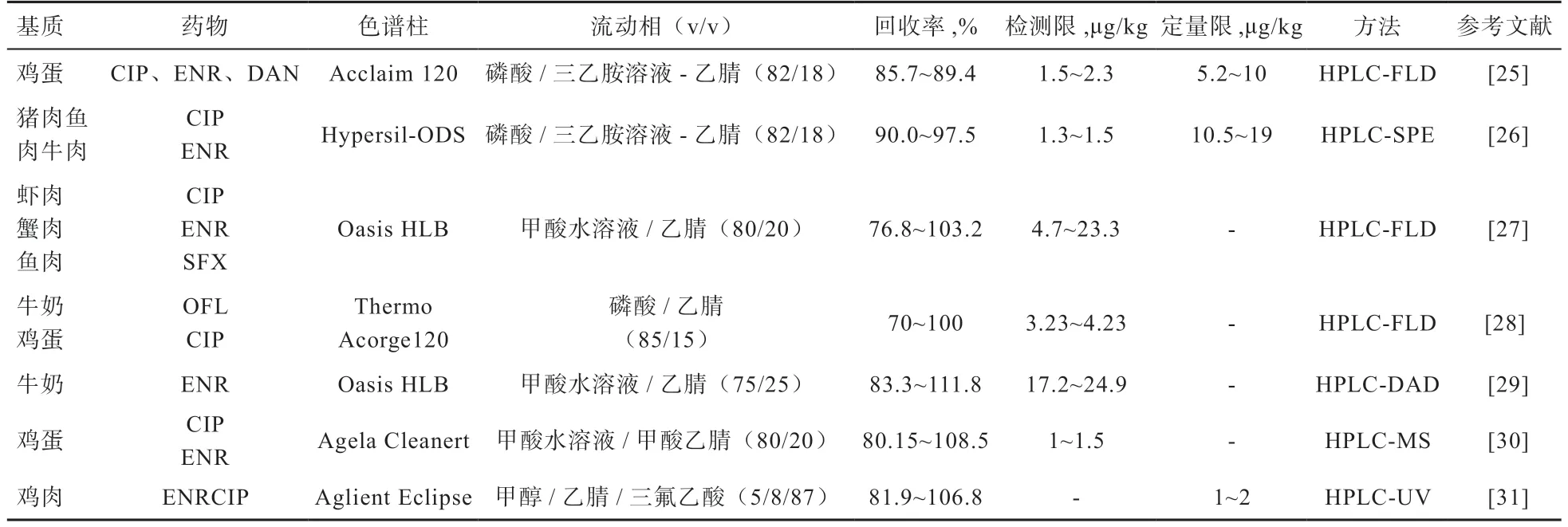
表3 不同样品基质中FQS 类药物液相检测方法的比较
李建鲲等[33]利用酶联免疫吸附法快速测定肉制品中FQS 残留,计算50%抑制浓度(IC50 值)可知FQS酶联免疫试剂盒的相关系数R 为0.997 6,百分吸光率标准曲线中4 次零浓度的标准液的IC50 介于0.306~0.351 ng/g,表明FQS 的浓度与百分吸光率呈负相关。在0~ 400 ng/g 时,添加回收率在81.8%~100.3%,相对标准偏差(Relative standard deviation,RSD) 在0.4%~12%,说明ELISA 法检测牛肉、羊肉、猪肉和鸡肉中FQS 准确、可靠,且重复性好、精密度高。
李燕君等[34]利用ELISA 法同时检测牛奶中环丙沙星、恩诺沙星、诺氟沙星等6 种FQS 残留,该方法的IC50 范围在0.254~0.361 μg/L,最低检测限为1.48 μg/L,在牛奶中添加5 μg/L 环丙沙星、恩诺沙星、诺氟沙星等6 种FQS 类药物时,回收率为87.20%~115.92%;同一批内的变异系数均小于15.0%,不同批间的变异系数均小于16.0%。该方法的精密度(变异系数)、回收率和最低检测限等均符合兽药残留试验技术规范的要求,且回收率和最低检测限与高效液相色谱法相接近,具有较高的灵敏度和准确度,并且操作相对简单,容易在基层工作中推广普及,适合进行大批量样本的快速检测。
孙晓峥等[35]用间接竞争ELISA(ci-ELISA)试验成功地检测了肉鸡组织中环丙沙星(CIP)的残留,将敏感性强的单抗与胶体金颗粒标记作为金标垫,以CIP-BSA 偶联蛋白为检测线,以兔抗鼠IgG 作为质控线,组装了检测FQS 药物的胶体金免疫层析试纸条,检测肉鸡中CIP 的残留,结果表明该方法对10 种FQS 检测均为阳性,而检测的4 种常见药物均为阴性。对环丙沙星、培氟沙星、达氟沙星的检测限为3.2 ng/mL,对沙拉沙星、二氟沙星、麻保沙星的检测限为6.4 ng/mL。该方法操作简单,检测所需时间短、灵敏度较高、特异性较强,为大量样品的筛选和快速检测提供了一种可靠的方法。
Yuan等[36]利用一种基于等离子体银纳米棱镜(AgNPR)氧化蚀刻的酶联免疫吸附法(pELISA),用于达氟沙星的定性和定量检测。该方法以AgNPR 作为信号转换器,通过引入生物素标记的单克隆抗体、链霉亲和素和生物素化葡萄糖氧化酶构建间接竞争的pELISA,催化H2O2的生成来刻蚀AgNPR。该方法对牛奶中达氟沙星的定量检出限为0.24 ng/mL,定性检测限为0.32 ng/mL,平均回收率为103%~121%,变异系数为0.6%~3.41%。用液相色谱-串联质谱法进一步证实了上述回收结果。根据结果可知,AgNPR 蚀刻pELISA法对牛奶中达氟沙星的定量和定性检测具有较高灵敏度、准确性和可靠性,可以用作牛奶中氟喹诺酮类药物的残留检测。
不同分析方法对FQS 的检测结果优缺点见表3。尽管相比于HPLC 和HPLC-MS,ELISA 的检出限和定量限较高,但仍远低于国家限量标准。该方法具有操作简单,所需时间短、成本低等诸多优势,适用于作为食品中FQS 类药物残留的初步检测。近年来,ELISA 为FQS 残留检测提供了诸多便利。随着科学发展,基于免疫法的检测方法不断创新,灵敏度不断提高,今后的研究重点可侧重于提高该方法的稳定性和特异性。
3 展 望
随着分析技术和新型材料的快速发展,HPLC、HPLC-MS/MS、ELISA 等方法被广泛应用于FQS 残留的检测。目前常用的HPLC 法虽然准确度高、重现性好,但所需仪器昂贵、操作复杂、对样品的前处理繁琐等。随着免疫技术的不断发展,使用ELISA 法检测FQS 残留的研究越来越多,该方法灵敏度较高、特异性强,相比于HPLC 法具有简便、快捷等优势,适用于对样品的初步残留检测。因此,可以预测ELISA 法将会在快速筛选大批量样品的FQS 残留中发挥重要作用。
