气相色谱法测定乳酸左氧氟沙星中三种有机溶剂的残留量
2021-04-15王杰刘绪平段和祥鄢雷娜肖钦钦陈希
王杰,刘绪平,段和祥,鄢雷娜,肖钦钦,陈希
江西省药品检验检测研究院,国家药品监督管理局中成药质量评价重点实验室,江西省药品与医疗器械质量工程技术研究中心,江西 南昌 330029
药物中残留的有机溶剂不仅没有疗效,还可能增加药物的毒副作用,影响药物的稳定性,为了保护患者免受药物中残留有机溶剂的伤害[1],人用药品注册技术规范国际协调会(ICH)规定,必须对药物中的残留溶剂进行检测,以保障用药安全[2]。左氧氟沙星是新一代喹诺酮类合成抗菌药,适用于敏感菌所致的呼吸、消化、泌尿、生殖系统、皮肤软组织及外科、耳鼻喉科、眼科、口腔科的各种急、慢性细菌感染[3]。根据原料药生产企业提供的工艺资料,获知其工艺过程中使用甲醇、乙醇、三氯甲烷,参考《中国药典》2015 年版四部通则0861“残留溶剂测定法”[4],采用气相色谱顶空进样程序升温法同时测定样品中三种有机溶剂的残留量,并进行了方法学考察[5]。
1 仪器与试药
Agilent 7890B 型气相色谱仪[氢火焰离子化(FID)检测器,7697A 顶空进样器];MS205DU 型电子天平(美国Mettler 公司);甲醇、乙醇、三氯甲烷、二甲基亚砜均为色谱纯(美国 Sigma-Aldrich 公司)。
乳酸左氧氟沙星原料(厂家A 批号:018C225- 190901;厂家B 批号:DK24-1806171-Ⅵ;厂家C批号:2018C225-190901)。
2 方法与结果
2.1 色谱条件
色谱柱:DB-WAX(30 m×0.53 mm×1.0 μm)石英毛细管柱;柱温:初始温度60 ℃,保持4 min,以20 ℃/min 升温至200 ℃,保持2 min;进样口温度:230 ℃;FID 检测器温度:240 ℃;载气:氮气(N2);恒流流速:3.0 mL/min;分流比3∶1;顶空瓶平衡温度85 ℃,平衡时间30 min,进样量1 mL。
2.2 溶液配制
2.2.1 空白溶液精密量取0.1%二甲基亚砜5 mL,置20 mL 顶空瓶中,密封,作为空白溶液。
2.2.2 对照品溶液精密称取三氯甲烷61.85 mg,置10 mL 量瓶中,用二甲基亚砜稀释至刻度,摇匀,作为三氯甲烷储备液;精密称取甲醇306.1 mg、乙醇500.4 mg,置10 mL 量瓶中,精密加入三氯甲烷储备液1 mL,加水定容至刻度,摇匀,作为混合对照品储备液;精密量取混合对照品储备液1 mL,置100 mL 量瓶中,用水稀释至刻度,摇匀,精密量取5 mL,置20 mL 顶空瓶中,密封,作为对照品溶液。
2.2.3 供试品溶液精密称取乳酸左氧氟沙星原料药(批号:018C225-190901)约0.5 g,置20 mL 顶空瓶中,精密加0.1%二甲基亚砜5 mL,摇匀,密封,作为供试品溶液。
2.3 系统适用性试验
取空白溶液、对照品溶液、供试品溶液,按“2.1”项下色谱条件,记录色谱图。结果空白溶剂无干扰,供试品中无杂峰影响测定:甲醇、乙醇、三氯甲烷在该色谱条件下分离度好,分离效能较高。详见图1。

图1 系统适用性图谱
2.4 线性试验
精密量取“2.2.2”项下混合对照品储备液0.1、0.2、0.4、0.6、0.8、1.0、1.2 mL,分别置100 mL量瓶中,用水稀释至刻度,摇匀,精密量取5 mL,置20 mL 顶空瓶中,密封,按“2.1”项下色谱条件,记录色谱图,以浓度(C)为横坐标,以峰面积(A)为纵坐标进行线性回归。结果表明,在所示各线性范围内,甲醇、乙醇和三氯甲烷的线性关系良好。结果见表1。
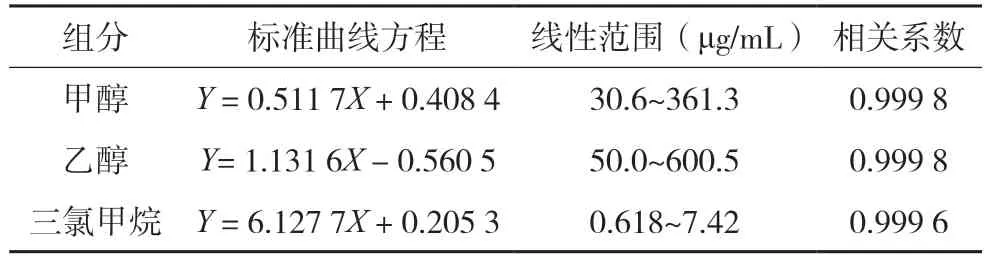
表1 线性回归结果表
2.5 检测限与定量限
取“2.2.2”项下对照品溶液,以水为溶剂逐步稀释,按“2.1”项下色谱条件,记录色谱图,以信噪比3∶1 确定检测限,以信噪比10∶1 确定定量限。得甲醇、乙醇和三氯甲烷的定量限分别为1.43、0.62和0.077 μg/mL,检测限分别为0.43、0.19 和0.023 μg/mL。均远小于ICH Q3C 最大限度的30%。
2.6 精密度试验
精密量取“2.2.2”项下对照品溶液,共6 份,分别置20 mL 顶空瓶中,密封,按“2.1”项下色谱条件,重复进样6 次,记录色谱图。计算测得峰面积,考察精密度。结果甲醇、乙醇、三氯甲烷的RSD 分别为2.7%、1.6%、2.4%。
2.7 重复性试验
精密称取乳酸左氧氟沙星约0.5 g,共6 份,分别置20 mL 顶空瓶中中,精密加0.1%二甲基亚砜5 mL,摇匀,密封,按“2.1”项下色谱条件,记色谱图,甲醇、乙醇、三氯甲烷均未检出。结果表明方法重复性良好。
2.8 回收率试验
取混合对照储备液0.8、1.0、1.2 mL,分别置100 mL 量瓶中,制成相当于对照品溶液浓度的80%、100%、120% 的溶液。精密称取乳酸左氧氟沙星约0.5 g,共9 份,置20 mL 顶空瓶中,分别精密加入80%、100%、120% 的溶液5 mL,每个浓度平行制备3 份,按“2.1”项下色谱条件,记录色谱图,根据峰面积计算回收率,平均回收率分别为100.7%、99.2%、100.6%,RSD 分别为0.5%、0.4%、0.9%,结果均符合规定。
2.9 样品测定
分别精密称取不同厂家的乳酸左氧氟沙星约0.5 g,按“2.2.3”制备供试品溶液,并按“2.1”项下色谱条件,记录色谱图,测定有机溶剂残留量,按外标法以峰面积计算,三个厂家乳酸左氧氟沙星中甲醇、乙醇、三氯甲烷均未检出。
3 讨论
采用顶空进样法可增加有机物检出的灵敏度和准确度[6],从而更加严格地控制药物中有机溶剂的残留量,提高药品质量。乳酸左氧氟沙星在水中的溶解度较好,由于三氯甲烷不溶于水,因此配制三氯甲烷对照品溶液时,第一步用DMSO 作为溶剂,后续配制以水做溶剂,从而增加三氯甲烷的溶解性。且本法中加0.1%二甲基亚砜不影响待测有机溶剂的检测,故选以0.1%二甲基亚砜作溶剂。由于本实验中的待测溶剂的沸点均低于80 ℃,并且溶剂为0.1%二甲基亚砜,因此确定顶空瓶平衡温度为80 ℃;对顶空瓶平衡时间进行筛选,实验表明平衡30 min 后顶空瓶内可以达到气液平衡,待测溶剂峰面积基本保持不变,因此选80 ℃下平衡30 min;三种待测溶剂以DB-WAX 为色谱柱,进行程序升温,分离度良好,故选用DB-WAX 为色谱柱。
药品中有机溶剂残留种类因生产工艺不同而异。参照人用药品注册技术规范国际协调组织(ICH)[7]和我国药典[4]规定,三氯甲烷为I 类有机溶剂,甲醇、乙醇为Ⅲ类有机溶剂,安全限度分别为0.3%和0.5%、0.006% 。从测定结果看,3 批样品均符合2015 年版《中国药典》四部的限度要求。
