分析新辅助化疗联合腹腔镜辅助胃癌根治术治疗进展期胃癌的效果
2021-04-14韩怡茹乌新林
韩怡茹,乌新林
(内蒙古医科大学附属医院胃肠外科,内蒙古 呼和浩特 010050)
进展期胃癌患者常表现出腹痛、恶心呕吐、呕血、食欲减退等症状,对患者的生活及生存质量均造成恶劣影响[1]。目前,临床上多采用腹腔镜辅助胃癌根治术治疗该病,但是单一手术治疗会增加复发及癌组织转移的风险,致使手术效果较理想预期相差甚远[2]。新辅助化疗可以有效缩小病变的癌组织,但临床上对于进展期胃癌患者行新辅助化疗联合腹腔镜辅助胃癌根治术进行治疗的效果尚有争议。基于此,本研究旨在分析针对进展期胃癌患者应用新辅助化疗联合腹腔镜辅助胃癌根治术进行治疗的临床效果,现报道如下。
1 资料与方法
1.1 临床资料 回顾分析2017年6月至2019年6月本院收治的90 例进展期胃癌患者的临床资料,将行腹腔镜辅助胃癌根治术治疗的45 例患者临床资料归为对照组,将应用新辅助化疗联合腹腔镜辅助胃癌根治术治疗的45例患者临床资料归为观察组。对照组男27例,女18例;年龄34~76岁,平均年龄(55.54±3.49)岁;体质量43~80 kg,平均体质量(56.57±4.22)kg。观察组男26 例,女19 例;年龄32~76岁,平均年龄(54.73±4.12)岁;体质量44~79 kg,平均体质量(56.77±4.16)kg。两组临床资料比较差异无统计学意义,具有可比性。
1.2 纳入及排除标准 纳入标准:经病理诊断确诊为进展期胃癌者;具备手术指征者;精神及认知功能正常者;未发生远处转移者;临床资料完整者。排除标准:凝血功能障碍者;既往有放化疗治疗史者;重要脏器(心、肾等)功能障碍者;化疗耐受性极差者。
1.3 方法 对照组行腹腔镜辅助胃癌根治术治疗:取截石位,气管插管全麻,常规消毒铺巾后建立人工气腹,气腹压力为10~14 mmHg。观察孔:于脐孔下缘做10 mm 左右的切口,主操作孔:在左腋前线肋缘下做12 mm左右的切口,辅助操作孔:在右锁骨中线肋缘下和剑突下做5 mm的穿刺孔。在腹腔镜辅助下探查病变组织的体积、位置等情况,将胃结肠韧带、相关静脉、横断大网膜、肝胃韧带应用超声刀进行游离、切断后,进行淋巴结清扫,在患者的上腹部正中位置做5 cm长度的切口,荷包包埋并将十二指肠肠端清除后,行远端胃切除,并将剩余胃组织与近端空肠进行BillrothⅡ式重建后,冲洗腹腔并放置引流管后关腹。观察组在对照组的基础上应用新辅助化疗,选择XELOX方案,患者入院第1天给予奥沙利铂[费森尤斯卡比(武汉)医药有限公司,国药准字H20093892],静脉滴注,85 mg/m2,每2 周重复1 次;入院1~14 d 内给予卡他培滨(上海罗氏制药有限公司,国药准字H20073024),口服,1 250 mg/m2,每天2 次,治疗2 周后停药1周,3周为1个疗程,化疗结束后14 d内行腹腔镜辅助胃癌根治术治疗。两组术后均给予胃肠减压及抗感染治疗。
1.4 观察指标 ①观察并记录两组手术相关指标(下床活动时间、淋巴结清扫数目、肛门排气时间)。②在术前及术后3 个月应用Karnofsky 功能状态量表(KPS)评估患者的健康状况,共11 项条目,百分制,KPS 评分越高表示健康状况越好。③记录两组术后相关并发症(肺部感染、胸腔积液、肠梗阻)发生情况。
1.5 统计学方法 采用SPSS 25.0软件进行数据处理,计量资料以“±s”表示,比较采用t 检验,计数资料用[n(%)]表示,比较采用χ2检验,以P<0.05为差异具有统计学意义。
2 结果
2.1 两组患者手术相关指标比较 观察组淋巴结清扫数目、下床活动时间、肛门排气时间均小于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组患者手术相关指标比较(±s)Table 1 Comparison of surgical indicators between the two groups(±s)

表1 两组患者手术相关指标比较(±s)Table 1 Comparison of surgical indicators between the two groups(±s)
肛门排气时间(d)3.97±1.24 3.42±1.12 2.208 0.030组别对照组(n=45)观察组(n=45)t值P值淋巴结清扫数目(个)20.69±5.74 17.89±5.23 2.419 0.018下床活动时间(d)3.41±0.56 2.93±0.77 3.382 0.001
2.2 两组患者术前及术后3个月KPS评分比较 术后,两组KPS 评分均高于术前,且观察组高于对照组,差异有统计学意义(P<0.05),见表2。
2.3 两组术后相关并发症发生率比较 观察组术后并发症发生率(6.67%)低于对照组(24.44%),差异有统计学意义(P<0.05),见表3。
表2 两组患者术前及术后3个月KPS评分比较(±s,分)Table 2 Comparison of preoperative and postoperative KPS scores between the two groups(±s,scores)
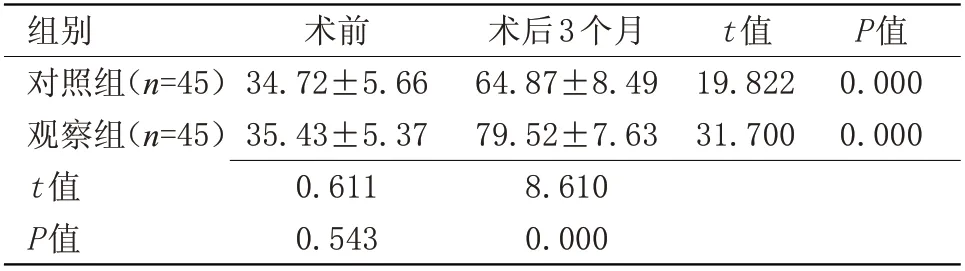
表2 两组患者术前及术后3个月KPS评分比较(±s,分)Table 2 Comparison of preoperative and postoperative KPS scores between the two groups(±s,scores)
组别对照组(n=45)观察组(n=45)t值P值术前34.72±5.66 35.43±5.37 0.611 0.543术后3个月64.87±8.49 79.52±7.63 8.610 0.000 t值19.822 31.700 P值0.000 0.000
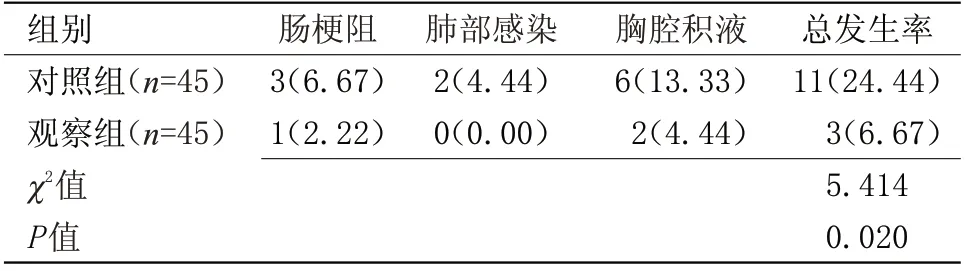
表3 两组术后相关并发症发生率比较[n(%)]Table 3 Comparison of incidence of postoperative complications between the two groups[n(%)]
3 讨论
近年来,胃癌的发病率较高且逐年增长,严重降低患者的生活及生存质量。目前,临床上针对胃癌患者多采用手术进行治疗,既往的开腹胃癌根治术存在创面大、感染率高等问题,应用存在一定的局限性[3]。而随着腹腔镜技术的发展与成熟,其也逐渐应用至胃癌根治术中,腹腔镜辅助胃癌根治术具有微创、易恢复等特点而逐渐被患者青睐,且该术式在早期胃癌治疗中具有良好的疗效。然而进展期胃癌患者往往存在淋巴结转移等情况,仅给予腹腔镜辅助胃癌根治术进行治疗,患者术后存在复发、转移的风险较高,治疗较预期有所差异[4-5]。
新辅助化疗可以促进肿瘤细胞凋亡,可以起到杀伤作用,进而可以缩小肿瘤;同时新辅助化疗可以有效抑制肿瘤细胞的转移活性,改善病变组织与周围的粘连情况,当新辅助化疗联合腹腔镜辅助胃癌根治术治疗时,可以有效提高病变组织的切除率[6]。此外,新辅助化疗可以有效降低术后患者的复发率及病死率,进而可以有效提升患者的生存质量[7-8]。但有研究指出,新辅助化疗会增加患者胃周组织纤维瘢痕增生的风险,会在一定程度上增加手术风险[9]。本研究结果显示,观察组淋巴结清扫数目、下床活动及肛门排气时间小于对照组,术后,两组KPS评分均高于术前,且观察组高于对照组,观察组术后并发症发生率低于对照组,表明应用新辅助化疗联合腹腔镜辅助胃癌根治术治疗的效果较好,可以改善患者的健康状况,降低术后并发症的发生风险,缩短患者的恢复时间。分析两种方式认为,相较单一的手术治疗,新辅助化疗可以杀伤患者机体内的病灶组织,致使其体积减小,抑制病变组织的转移活性,有助于腹腔镜辅助胃癌根治术治疗的顺利进行,进而可以提高手术效果,准确切除病灶,利于患者术后转归,降低复发率及病变组织出现转移的风险,有效提高患者5年存活率[10]。
综上所述,新辅助化疗联合腹腔镜辅助胃癌根治术可缩短进展期胃癌患者术后恢复时间,改善其术后健康状况,减少术后并发症的发生。
