胰十二指肠切除术150例围手术期并发症临床分析
2021-04-14贺卓王进峰罗建红欧阳永忠谢江波康安定黄波白飞肖科尹彬邓顺罗宇航左朝晖
贺卓,王进峰,罗建红,欧阳永忠,谢江波,康安定,黄波,白飞,肖科,尹彬,邓顺,罗宇航,左朝晖
(中南大学湘雅医学院附属肿瘤医院暨湖南省肿瘤医院 胃十二指肠胰腺外科/湖南省肿瘤防治研究所/肝癌转化医学联合研究中心和消化道肿瘤实验室,湖南 长沙 410013)
胰十二指肠切除术(pancreatoduodenectomy,PD)已成为胆管下段癌、胰头癌、十二指肠癌、壶腹癌、巨块型十二指肠间质瘤恶性肿瘤、十二指肠神经内分泌肿瘤、侵犯十二指肠降部和胰头的胃癌和胰腺头部囊腺瘤[9]等肿瘤的主要术式[1-9],对有临床症状的肿块型胰腺炎,PD术也是手术方式之一[10]。PD术切除的脏器多、手术时间长、术后并发症发生率高,其切除和重建都极富有挑战性,是腹部外科极限的手术之一[11]。虽医学发展虽突飞猛进,但其术后高并发症发生的相关因素及围手术期的处理方法仍是困忧外科医师的难题,减小术后并发症的发生和提高疗效一直临床探讨的热点。本文采用回顾分析9年期间150 例PD患者的临床资料,分析了并发症发生的可能因素、处理方法和疗效,以便更好指导临床,现报告如下。
1 资料与方法
1.1 一般资料
研究对象为2011年1月—2020年1月9年期间湖南省肿瘤医院暨中南大学湘雅医学院附属肿瘤医院腹部外科150例接受PD术的患者,其中男 99例,女51例;平均年龄51(28~72)岁。病理类型包括:胆管下段癌(44例)、胰头癌(35例)、十二指肠癌(32 例)、壶腹癌(20 例)、十二指肠间质瘤(4 例)、十二指肠神经内分泌肿瘤 (2例)、胰腺实性假乳头状瘤(2例)、胰腺囊腺瘤(3例)、壶腹部绒毛管状腺瘤(3例)、肿块型胰腺炎(2例)、进展期胃癌(2例)、胆囊癌(1例)。
1.2 手术前减黄标准及方法
术前TBIL水平(84.5±59.1)μmol/L,其中87例≤180 μmol/L,63例>180 μmol/L,术前ALT(128.1±48.2)U/L,术前AST(156.5 ± 58.2)U/L,术前白蛋白(38.4±5.9)g/L,其中ALT≥160 U/L和TBIL≥180 μmol/L,伴有梗阻性黄疸的31例患者予以减黄,对有胆道感染和凝血功能异常时,可能导致术后出血,予以急诊减黄。其中2例行逆行性胰胆管造影+鼻胆管引流(ERCP+ENBD),4例行逆行性胰胆管造影+胆道内支架引流(ERCP+ERBD),25例在B超引导下行经皮肝穿刺胆管引流(PTCD)引流。减黄时间7~124 d,平均9.4d。
1.3 手术方法及要点
1.3.1 基本术中处理全麻下取仰卧位行PD 术,术后均常规应用生长抑素、质子泵抑制剂、全静脉营养及抗生素治疗,6 d 后再根据患者情况予以调整。使用经十二指肠水平部与Kocher 联合入路:先暴露横结肠系膜根部,显露十二指肠水平部,沿其下缘切开后腹膜,游离十二指肠后方,显露并游离肠系膜上静脉,再于横结肠上方取Kocher 切口将胰头十二指肠完全游离。将十二指肠与下腔静脉分离,切断胃结肠韧带和切除大网膜进入显露网膜囊后壁(胰腺前缘),从横结肠系膜前叶间隙清扫淋巴结并切除胰腺背膜,顺着胰腺下缘的肠系膜上静脉或动脉在胰腺后侧贯穿分离,显露出门静脉;于拟断胃处切断胃,沿十二指肠第一段和胰腺上缘切开肝十二指肠韧带的前层腹膜,解剖肠系膜上静脉-门静脉系统和肠系膜上动脉-腹腔干系统。游离胆总管下段和肝固有动脉、肝总动脉,清除胰头周围、肝总动脉旁和腹腔动脉周围淋巴结,在胰腺上缘切断胆总管下端并向上牵引,清除肝动脉和门静脉周围的淋巴、神经、纤维脂肪组织,整块切除,直至左右肝门;并充分骨骼化肝十二指肠韧带,术中完整切除胰腺钩突,对腹腔干、门静脉、肝总动脉、肝固有动脉和肠系膜上静脉进行脉络化(图1),并对胰腺周围的淋巴结探查。
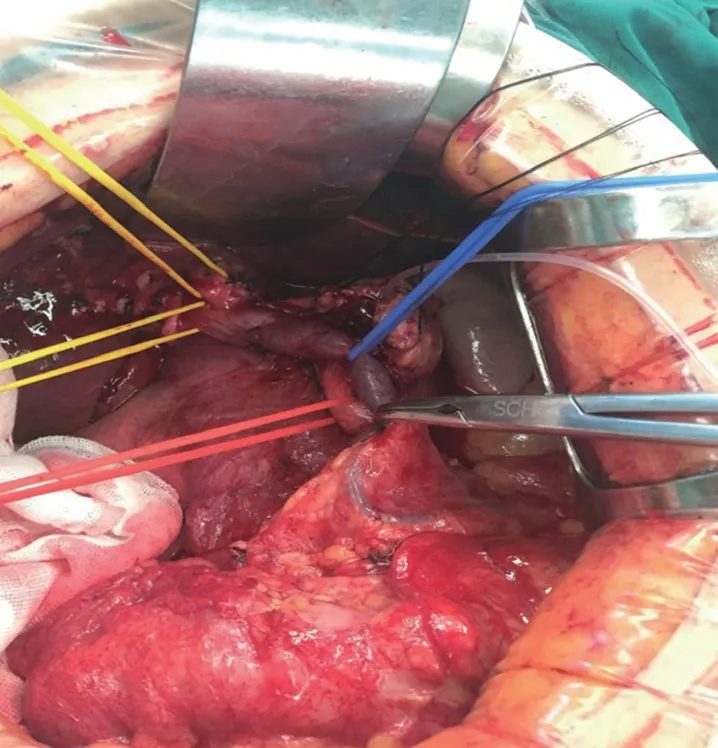
图1 术中显露Hen 干、显露肠系膜上动静脉、门静脉、肝动脉
1.3.2 消化道重建消化道重建方法为Child 法(即胰、胆、胃顺序),胰肠吻合方式选择根据胰管粗细及术者经验决定:游离胰腺残端2~3 cm,必须找到主胰管,术前根据CT 等影像学检查测定胰管大小,术中挤压胰腺断端观察胰液的溢出。寻找细小胰管一定要有耐心,对细小胰管的胰颈离断靠近胰管时用超声刀夹碎胰腺实质,用剪刀离断胰管;插入剪成斜面带2~3 个小孔与胰管匹配的胰液引流管至胰管,使其紧贴胰管内壁,予以4-0可吸收线贯穿胰管腹侧、胰液引流管腹侧、背侧、胰管背侧缝合,并封闭缝合胰液引流管与胰管存在空隙;根据胰腺断端的情况选择胰肠端侧套入式、改良式端侧胰管肠黏膜式和端端套入式等吻 合法。
1.3.3 其他处理为了减少胰瘘,简化改良了胰肠吻合,对于胰管扩张者(≥4 mm)行胰管空肠黏膜吻合,于胰腺上下缘距胰腺断端约2 cm 予以3-0 可吸收线从腹侧向背侧贯穿胰腺缝合1 针(边缘血管有效缝合),即从腹侧向背侧贯穿胰腺进针,环绕胰管“U”字贯穿胰腺实质缝合。如胰腺断端止血不满意,即用不可吸收线褥式或间断缝合胰腺断端3~5 针。距胰腺断端约1 cm,于胰腺上缘处应用带大针3-0 Prolene 线贯穿胰腺和空肠浆肌层“8”字缝合打结,继而在胰管对应处空肠切一小孔,应用4-0 可吸收线4-0 全层缝合荷包缝合后,将胰液引流管置入空肠袢远端,荷包缝线打结并靠拢空肠与胰腺断端,最后又在胰腺上缘处应用带大针3-0 Prolene 线贯穿胰腺和空肠浆肌层“8”字缝合2 针打结,即完成“改良的胰管空肠黏膜吻合”(4 针法缝合)。对于胰管不扩张(直径<4 mm),笔者改良了胰- 空肠端侧套入式吻合,首先对应胰腺断端切开空肠全层约3 cm,可吸收线“8”字缝合胰腺后切缘和空肠后壁全层 2 针,继而“8”字缝合空肠前壁全层与胰腺前切缘2 针,逐一打结;再间断缝合胰腺侧被膜和前被膜与空肠侧壁和前壁浆肌层,共4 针,即完成了“改良胰肠端侧套入式吻合”(4 针法缝合)。以游离大网膜衬垫于胰肠吻合口后方,覆盖肝总动脉、门静脉、肠系膜上静脉及肠系膜上动脉等,能防止胰液等消化液对脉络血管的腐蚀作用(游离大网膜围脖包绕隔离法)。对改良的胰肠吻合(modified pancreaticojejunostomy,MPJ),笔者主张“宽松稀”,吻合应选择简单和安全的方法。
胆肠吻合根据胆管直径选择手工或吻合器吻合,4-0或3-0可吸收线或倒刺线连续缝合后壁,前壁予以间断缝合。胃肠吻合采用Roux-en-Y式和Billroth II式,其中Roux-en-Y式优于Billroth II式吻合,远端空肠与残胃大弯侧行端端吻合。快速康复者术后麻醉苏醒前拔除胃管,术后第1天置鼻肠管灌注糖盐水300 mL,术后第2~3天进行肠内营养,逐步增量;未置鼻肠管者,术后1 d进水,术后2~3 d进流质,术后4~5 d进半流质。
1.4 手术后并发症诊断标准
腹腔引流管拔除标准:引流液淀粉酶<1000 U/L,单根引流量<50 mL/d,胰瘘、胆瘘、乳糜瘘、术后出血、胃潴留按国际相关协会并发症标准[12]。
1.5 术后随访
按术后病理分期给予术后观察或术后辅助治疗,并定期随访,最后1次随访日期为2020年6月30日。术后第1年,每3个月随访1次;第2~3年,每3~6个月随访1次;之后每6个月随访1次。
2 结 果
2.1 术中情况
150例PD患者,平均手术时间5.5(3.5~9.0)h,术中出血量 500(120 ~3000)m L,术后住院时间为16(8~62)d。胰肠吻合方式为改良端侧套入式59例,改良式端侧胰管对黏膜吻合57例,端端套入式吻合34 例。改良端侧套入式组胰肠吻合平均时间(13.4±1.85)min、改良黏膜式组(22.7±2.01)min、胰肠端端套入式组(20±1.98)min。
2.2 术后总并发症和围手术期死亡情况
150例PD术患者中,50例(33.3%)发生术后并发症,围手术期死亡5例(3.3%)(表1)。
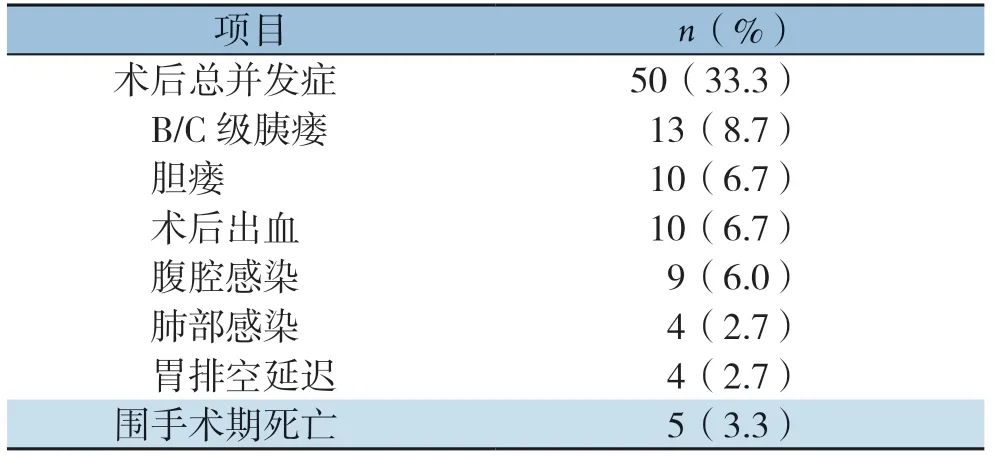
表1 150 例PD 术后并发症和围手术期死亡情况
2.3 胰瘘及胆瘘发生情况及处理
A级胰瘘65例,B/C级胰瘘13 例,其中B级 9例(6.0%),C级胰瘘4例(2.7%)。A级胰瘘对患者的预后及治疗方案无任何影响,B/C级胰瘘严重影响患者的预后,均给予治疗性干预,2例80岁以上的患者术后B/C级胰瘘合并多器官功能衰竭于4周死亡。术后胆瘘10例(6.7%),分析结果显示,胆管直径较细或扩张达2 cm以上者,胆瘘发生率较高。
2.4 术后出血和腹腔感染的发生情况及处理
术后出血10例,其中腹腔出血7例(4.7%),消化道出血3例(2.0%)。术后予以患者常规使用生长抑素(6 mg维持24 h),连续7 d,对术后消化液瘘和出血有一定效果。本研究仅1例应激性溃疡出血,经保守治疗痊愈。1例PD术后29 d胃肠吻合口溃疡出血,经2次内镜予以血管夹止血痊愈出院。于胰肠吻合和胆肠吻合处即文氏孔周围置2根引流管充分引流并予以药敏抗生素预防感染。全组术后仅发生9例腹腔感染。
2.5 胃排空延迟的发生情况及处理
4例(2.70%)出现胃排空延迟,均经非手术治疗治愈。1例胃空肠延迟持续时间较长,通过胃镜置入肠内营养管给予肠内营养支持治疗,改善患者营养状况后经非手术治疗治愈。
2.6 不同吻合方式及减黄与否患者的术后病死率情况
改良式端侧胰管对黏膜吻合57例中死亡1例(1.8%,1/57),胰肠端端套入式吻合34例中死亡2例(5.9%,2/34),胰肠端侧套入式吻合59例中死亡2例(3.4%,2/59)。31例减黄患者的围手术期病死率3.2%(1/31),119例未减黄患者的围手术期病死率3.4%(4/119)。
3 讨 论
PD术不但是壶腹部周围癌的首选手术方式,也是胰头囊腺瘤、侵犯周围的胃窦癌、十二指肠间质瘤和神经内分泌肿瘤等肿瘤的主要术式。PD术是技术要求最高、最具挑战性的手术之一。虽然随着手术技术要求的提高以及外科团队学习曲线的优化,其病死率下降,但目前围手术期的术后并发症的发生率仍然较高,尤其是有黄疸的胰头癌、胆总管下端癌、十二指肠乳头癌[13]等恶性肿瘤。德国Homeyer等[14]报道245例壶腹部癌PD术的并发症发生率30.7%,围手术期病死率6.7%。本组资料显示,PD术后并发症的发生率为33.3%,围手术期病死率为3.3%。其中主要并发症为胰瘘、胆瘘、腹腔感染和出血。笔者认为术后胰瘘、腹腔感染以及迟发性出血三者相互影响,胰瘘作为始动因素,进一步发展为腹腔感染,继而腐蚀胃十二指肠动脉残端或邻近血管而导致术后迟发性出血。
胰瘘是PD术后最严重、病死率最高的并发症。胰瘘的发生率为15%~40%,严重的胰瘘会导致腹腔内感染和出血的发生,总的胰瘘导致的病死率为1%,然而合并C级胰瘘患者的病死率可达25%[15]。目前公认的2016年国际胰腺外科研究组(ISGPS)胰瘘诊断标准[16]:术后3 d以上引流液淀粉酶含量>血清淀粉酶正常值上限3倍,且与临床治疗预后相关。胰瘘分级为B级,其临床表现发热、呕吐、腹痛腹胀,影像学示胰周积液;C级的临床表现为病情危重,生命体征不平稳。原来分级中的A级胰瘘变更为生化漏,即无临床症状,影像学无变化,一般在3周内消失。胰瘘的原因很多,有全身因素、局部因素以及手术因素。全身因素包括术前营养状况、年龄、总胆红素、白蛋白、糖尿病、贫血等;局部因素包括胰腺质地、胰管直径和疾病种类;手术因素包含胰肠吻合方式及胰腺周围充分有效的引流等。本组2例80岁以上的患者术后胰瘘合并多器官功能衰竭于4周死亡。笔者经验认为糖尿病不是胰瘘的危险因素,Malleo等[17]也通过临床回顾性研究发现,糖尿病并不会增加胰腺部分切除术后胰瘘的发生率;术前减黄可引起胆道逆行感染等并发症和延误了手术时机,术前常规不推荐减黄治疗,但对合并急性胆管炎、拟行新辅助治疗及全身一般状态极差者可选择减黄。
正常胰腺质地柔软、脆弱、纤维化较轻,吻合时易出血,缝合不当时极易出现胰瘘;而胰腺实质较硬时,胰腺创面不易出血,胰肠吻合较安全。十二指肠乳头癌、胆总管下段癌和壶腹部癌的患者胰腺与正常胰腺相似,分泌功能较好,较多的胰液易导致吻合口瘘。杨尹默等[18]认为若肿瘤位于胰腺部位的胰腺癌,可引起胰腺纤维化及外分泌功能降低,吻合操作方便,术后胰肠吻合口瘘发生率相对较低。目前临床常用的胰肠吻合方法有胰腺空肠端端套入式吻合、胰腺空肠端侧吻合、胰管-空肠黏膜吻合、捆绑式胰腺空肠吻合和胰胃吻合等。目前,尚没有任何一种胰肠吻合方式被公认为最佳的吻合方式。应该讲,吻合质量要比选择吻合方式更为重要。术者在选择吻合方式时,“因地制胰”很关键,根据胰腺质地和条件选择合适的吻合方式,并注重个体化原则。在行胰肠吻合时选择针线一体缝合线,避免引起针眼渗漏;缝合时选择可吸收缝线,避免引起吻合口周围炎症反应及肉芽增生;缝合时可选择如Vicrylplus控释针设计的“8”针线,因针线一体损伤较小;连续缝合时可选择如PDS的单针线,避免对组织拖拽而造成损伤;打结收线时用力轻柔,符合深部打结的要素,而且还应向相对固定、脆弱的胰腺组织靠拢,避免对胰腺的切割造成胰瘘及出血。“改良的胰肠吻合”简化了胰管-空肠黏膜吻合的术式,很大程度减少胰瘘的发生。本研究显示胰肠端端套入式组和改良端侧套入式组围术期病死率相仿,而改良端侧套入式组围术期病死率低于改良黏膜式组与胰肠端端套入式组。改良端侧套入式组手术平均时间亦少于改良黏膜式组和胰肠端端套入式组。
大网膜具有耐腐蚀、抗感染、吸收腹腔积液、再生血管、修复组织缺损等功能,将大网膜衬垫于胰肠吻合口后方,可封闭吻合口后壁,填塞潜在腔隙避免术区积液,覆盖吻合口周围血管以免被腐蚀出血,同时促进血管再生,改善吻合口血供,修复潜在的吻合口瘘。Shah等[19]在PD术后各种吻合口周围应用游离的网膜瓣可减少胰瘘、胆瘘、胰切除后出血和胃排空延迟的发生率,该手术简单有效,可降低PD术后的总发病率。本研究中150例患者发生C级胰瘘4例,B级胰瘘9例,A级胰瘘65例。胰瘘发生率低得益于“游离大网膜围脖包绕隔离法”,本组64例PD患者利用游离大网膜围脖包绕隔离法将吻合口和后方廓清后的血管分隔开,仅有C 级胰瘘6 例(9.4%)发生。笔者经验提示完成消化道重建后,将大网膜在吻合口后方平铺,使之将胰肠吻合口和门静脉、肝动脉分隔开,术后腹腔出血率和腹腔感染。垫高胰肠吻合口使得腐蚀性的胰液或腹腔积液即使未经胆肠侧引流管充分引流出,也易向左侧聚集在脾胃前方和胰体下缘的无血管区,继而经胰肠侧引流管流出。笔者认为对B级胰瘘,术中游离大网膜围脖包绕胰肠吻合口隔离法、术引流通畅、营养支持、抗生素和生长抑素的合理应用常可取得满意的效果。Andreasi等[20]认为将大网膜覆盖于PD术区的血管上能减少假性动脉瘤的形成。本研究认为将网膜组织衬垫于吻合口后方可减少胰瘘发生,即便发生胰瘘,也可有效控制胰瘘诱发的术后迟发性出血和腹腔感染等相关并发症。
PD术后胆瘘发生率各家报道不一,通常胆瘘发生率低于胰瘘。本组150例中胆瘘10例,发生率6.7%,高于Chen等[21]报道胆瘘发生率的5.0%左右的报道。临床上有诸多因素可能导致胰胆瘘发生,其发生与吻合口血供、吻合技术、胆管扩张程度及纤维化增厚等有关。Wang等[22]认为胆管直径是影响胆瘘发生的独立危险因素,胆管扩张、管壁增厚者胆瘘发生率低,正常胆管则发生率较高。而笔者经验提示胆管直径较细或扩张达2 cm以上,胆瘘发生率较高。在行胆肠吻合时,应避免过度游离胆总管,保证无张力吻合和充分的血运,并做确切的空肠和胆管黏膜对黏膜吻合,而且吻合口不要扭转,胰肠与胆肠吻合口间距要适当。一般用3-0或4-0可吸收缝线连续缝合胆肠吻合后壁,前壁予以间断缝合。该方法方便、快捷,且缝合后吻合口内没有线结,适用于任何口径的胆管吻合。胆管横断的位置应该尽可能靠近肝门部,以保证根治的彻底性和良好的血运。如果胆管壁菲薄,吻合时可将肝门板组织和胆管壁一并与肠壁吻合以增加吻合强度,并间断缝合浆肌层以减少张力,常规放置T管引流,对于胆管不扩张者宜同时置T管于肝总管中,短臂通过吻合口。为了避免早期胆汁和胰液的混合,胰液应该通过引流管越过胆肠吻合口远端引流至体外,避免胰液腐蚀胆肠吻合口。
腹腔感染是PD术后严重并发症之一,Karim等[23]报道胆瘘发生率为12.2%,胰瘘和胆瘘与腹腔感染互为因果,降低胰瘘和胆瘘的发生率可有效避免腹腔感染的发生。其原因包括全身因素和局部因素,全身因素考虑患者的免疫功能低下,对细菌的抵抗力减弱,如高龄、营养障碍、低蛋白血症和合并糖尿病等。Sun等[24]也证实了高龄是PD术后感染的独立危险因素,术中的大量出血和输血量(600 mL以上)是术后感染的危险因素,此外,机体针对输入大量异体血液成分会产生免疫反应或免疫障碍,从而增加感染的机会[25]。而局部因素与腹腔出现胰瘘和胆瘘后引流不畅发生感染,各种渗出液的潴留,残留胰腺钩突分泌胰液及术中腹腔消化液未被完全清除有关易致腹腔感染。对腹腔感染的治疗包括非手术治疗和手术治疗,首先加强全身营养支持治疗和早期使用抗生素,并根据药敏结果及时调整抗菌药物种类。当严重腹腔感染保守治疗无缓解,应尽早外科干预,推荐采用超声或CT 引导下经皮穿刺置管引流。但对重要吻合口瘘引起的严重腹腔感染,必要行手术外引流或消化道造瘘治疗。腹腔感染的最好的预防方法是手术后充分引流和药敏后抗生素的选择,常于胰肠吻合和胆肠吻合处即文氏孔周围置2根引流管引流。Yang等[26]也证实了PD术后腹腔感染充分引流和抗生素使用的重要性。
PD术后出血是PD术后最严重的并发症之一[27],本研究中PD术后出血患者10例(6.7%),其中腹腔出血7例(4.7%),消化道出血3例(2.0%)。早期腹腔和消化道出血多与手术操作相关,血管结扎不牢固、结扎线脱落及术野创面广泛渗血是主要原因。迟发性腹腔内出血多与胰瘘、胆瘘和腹腔感染等腐蚀胃十二指肠动脉等血管残端症相关,而迟发性消化道出血主要与应激性溃疡相关,随着抑酸剂和生长抑素在临床中的应用,可有效地抑制胰腺外分泌功能,减少胰液分泌,同时抑制胃泌素、胃酸及胃蛋白酶的分泌,近年来应激性溃疡出血很少见[28]。笔者术后患者常规使用生长抑素(6 mg维持24 h),连续7 d,还可减少内脏器官血流灌注且不引起动脉血压大幅波动,对术后消化液瘘和出血的防治取得了非常好的效果。对于术前是否需要减黄来降低术后出血等并发症发生率,目前尚无定论[29]。笔者经验认为对PD术前黄疸的壶腹部周围癌的患者应改善肝肾功能及补充凝血因子,精细的手术操作。对于已骨骼化的血管,可用游离的大网膜包绕覆盖吻合口(游离大网膜围脖包绕隔离法),同时关闭系膜间隙,使胆肠、胰肠吻合于右上腹隔离区,降低腐蚀血管的风险。在合并严重胰瘘或腹腔感染患者中,出现前哨出血时应更加重视,积极抗感染,保持引流通畅,甚至行内镜或DSA检查,如发现有假性动脉瘤则同时行栓塞治疗。是肠腔外还是肠腔内出血,多数可以通过腹腔引流管或胃肠减压管及临床表现进行明确诊断。但大量出血有时可表现为肠腔内和肠腔外同时出血,这种情况往往发生在合并有吻合口瘘基础上的迟发性出血,瘘口成为血液双向流动的通道。Floortje等[30]研究表明,术后出血患者的预后与出血发生距手术时间有明显相关性,间隔时间越长,患者死亡风险越高。出血距手术6~7 d是临床预后的明显分界点,这对术后出血早晚期分界有一定意义。本组出现1例PD术后29 d胃肠吻合口溃疡出血,经 2次内镜予以血管夹止血痊愈出院。
PD术后常见胃排空延迟发生率为7%~36%,严重影响患者的生活质量,同时导致住院时间延长、住院费用增加[31],本组4例(2.70%)出现胃排空延迟。目前临床对PD术后常见胃排空延迟并无统一的诊断标准,较公认的是ISGPS诊断标准,即排除机械性梗阻等其他问题,术后鼻胃管留置时间>3 d或拔出鼻胃管后重新插入以及进食固体食物的时间>7 d 可诊断为胃排空延迟。同时,据此将胃排空延迟分为A、B和C 3级,A级无需治疗[32]。相比常规的胃肠道手术后胃排空延迟,PD术后患者因切除胰头和胆总管而加行胰肠及胆肠吻合口,若机体的营养状况不良,同时合并胰瘘、胆瘘和腹腔感染均将一步加重胃排空延迟。故重视PD术后胃排空延迟有重要的临床意义。目前其机制如下:PD术破坏胃的正常生理结构及胃泌素和胃动素等兴奋性肽类激素水平降低使胃正常蠕动和排空均受到抑制,淋巴结清扫时很可能损伤迷走神经分支,减弱胃窦部研磨食物的蠕动性收缩[33]。笔者经验认为PD术后胃排空延迟首选的是非手术治疗,首先是禁食、禁水,持续胃肠减压,同时高渗温盐水洗胃,静滴氢化考的松或地塞米松减轻吻合口水肿;其次是维持水、电解质和酸碱平衡,并加强营养支持治疗,使用甲氧氯普胺和多潘立酮或西沙比利促进胃肠动力,也可使用红霉素减轻胃潴留;必要时通过胃镜置入肠内营养管给予肠内营养支持治疗,胃镜本身也能刺激胃壁促进胃的蠕动。PD术后胃排空延迟的预防因从多方面入手,术中应轻柔操作,选择术者熟练的消化道重建及吻合方式,笔者胃肠吻合采用Roux-en-Y式和Billroth II式,其中Roux-en-Y式优于Billroth II式吻合,远端空肠与残胃大弯侧行端端吻合,Billroth II式吻合并加空肠侧侧Braun吻合;适当延长胰管、T管及腹腔引流管的放置的时间,降低消化液漏和腹腔感染发生。
PD手术复杂,术后并发症预防要贯穿于术前、术中及术后,通过多学科、多角度模式加以干预。防治胰瘘、胆瘘、腹腔感染与出血则是围术期治疗的重中之重。根据具体情况选择合理的干预方式,可降低围手术期病死率并改善患者预后。
