磷铁合金精炼脱钛、锰、钒热力学分析
2021-04-14王海娟
常 朝 王海娟 王 勇
(1.中国科学院赣江创新研究院; 2.北京科技大学冶金与生态工程学院; 3.中国科学院过程工程研究所)
0 引言
磷铁是磷酸生产行业的副产物,其磷量在20 wt%~26 wt%,且含有少量钛、锰、钒、硅等元素;在钢铁铸造行业中,磷铁可改变钢的抗蚀性和切屑性,其磷铁中的磷含量在15 wt%~20 wt%[1]。而随着钢铁质量要求的不断提高,对于杂质含量的要求也越来越高[2]。铁水中含钛量高会降低材料的疲劳寿命[3],实际生产中,不同型号钢铁的含钛量有明确的规定,例如硅钢中要求wTi<0.04%;风电生铁和低钛生铁要求wTi<0.02%;铸造用高纯生铁要求wTi<0.01%[4]。现阶段对于铁水脱钛多采用加入氧化剂的方式,如气体吹炼[5]或固体氧化剂精炼[6]。两种工艺均有实践应用,脱钛效率均可达70%以上,但对于特定生产要求,需选择合理的脱钛除杂工艺。传统吹氧精炼[7]可将铁水中的杂质元素脱除,但对于磷铁合金体系来说,精炼时会造成大量的磷挥发而污染环境。喻爱国[8]对低钛低钒铁水的生产实践进行探究,生产出了低钛铁水。黄飞[9]对铁水脱锰工艺及生产实践进行研究,得到了纯净低锰特种钢。吴巍[5]等人采用吹炼法且加入固体氧化剂进行铁水脱钛研究,结果表明终点钛含量可降低至0.008 2 wt%,脱钛率可达71.3%。李闯[10]等人对铁水精炼脱钛硅锰的工艺进行了探究。刘壮壮[3]等人对铁水脱钛工艺进行了系统研究,同时对热力学进行了分析。但现阶段对于磷铁合金精炼过程的热力学分析尚未有明确的探究。
笔者为寻求更好的合金精炼方法,对精炼过程进行了热力学计算和试验分析。由于CaO 的加入可改善回钛现象[11],因此考虑在精炼过程中采用吹氧精炼辅助加入含CaO-MgO-SiO2[12]的渣系,探究各杂质元素的氧化程度、先后顺序及精炼时杂质元素之间的相互平衡关系,通过所得理论结果和分析为合金精炼脱钛、锰、钒实验提供指导。
1 合金成分分析
以磷铁合金为研究对象,其化学成分分析结果见表1。

表1 样品化学成分
2 合金精炼的热力学分析
合金精炼过程可采用气体氧化剂和固体氧化剂等,本文以吹氧精炼为例,对其反应热力学进行了分析研究。磷铁合金中元素与氧气反应的标准吉布斯自由能见表2。

表2 铁水中各元素氧化的反应式[13-14]
吹氧精炼需要考虑氧分压对反应的影响,以钛氧化为例,计算过程:

其中:(TiO2)选取纯物质为标准态,[Ti]选符合亨利定律的1 wt%溶液假想状态为标准状态。取温度为1 600 K,则式(1)的吉布斯自由能:

合金中Ti 组元的活度系数可依据相互作用系数计算,具体见表3。
表3 1 873 K 下铁水相关组元的活度相互作用系数

表3 1 873 K 下铁水相关组元的活度相互作用系数
组元 Ti Mn V P Ti0.013 00.004 3—-0.006 4 Mn0.019 20.000 0—-0.003 5 V——0.022 0 -0.041 0 P 0.040 00.000 0—0.062 0
将表3 中的数据代入公式[15]

可以计算出1 600 K 下相关组元的活度相互作用系数,结果见表4。
表4 1 600 K 下铁水相关组元的活度相互作用系数

表4 1 600 K 下铁水相关组元的活度相互作用系数
组元 Ti Mn V P Ti 0.015 2 0.005 0--0.007 5 Mn 0.022 5 0.000 0--0.004 1 V--0.024 6 -0.048 0 P 0.046 8 0.000 0-0.072 6
将表4 中的数据代入公式[15]

可以计算出Ti 元素的活度系数,相同方法计算各组元活度系数,并以ΔG—P(O2)/Pθ作图,如图1 所示。

图1 氧分压对各元素氧化的ΔG-P(O2)/Pθ(1 600 K)
从图1 可以看出,合金组分在1 600 K 吹炼条件下,氧分压对各元素氧化反应的自由能影响差异较大。随着氧分压的升高,各元素氧化反应的自由能降低,反应越易发生,但磷氧化反应趋势优先于钛、钒、锰。氧分压的存在是磷氧化的关键,若只采用固体氧化剂,则磷氧化反应不易发生。因此,精炼方式应考虑目标产物的元素含量,合理选择气体氧化剂或固体氧化剂,后续以吹氧加渣为例进行热力学分析。
3 添加渣系后的热力学分析
为防止渣相出现回钛现象,在吹氧精炼过程进行的同时加入含CaO 渣系,由于生成渣系中杂质元素的存在形式不一,进而可能会影响其脱除效率,因此需对加入CaO 渣系后的热力学进行分析。
采用空气吹炼的方式,则:

3.1 含钛渣系生成的热力学分析
由于所加渣系中的CaO 熔点较高(2 845 K),因此需辅助加入MgO 及SiO2,渣系配比可通过相图决定[7]。精炼时,铁水中的钛与氧气反应,生成(TiO2)进入渣相,并与精炼渣系反应生成共熔渣系,具体见表5。渣系的加入会影响(TiO2)活度,进而会影响反应平衡,则反应吉布斯自由能为:
假设渣相中(TiO2)的活度系数为1,在不同反应温度条件下,以ΔG-x(TiO2)作图,如图2 所示。
从图2 可以看出,随着温度的增加,ΔG 逐渐增加;随着渣系中(TiO2)含量的增加,ΔG 逐渐升高,但ΔG 的变化量对反应平衡的影响不明显。 (TiO2)含量较低时ΔG 变化较大,该现象表明,脱钛反应在初期时的反应速率较快,刘壮壮[3]等人的实验结论也验证了该结果。

表5 含钛渣系生成的反应式[16]

图2 渣系中(TiO2)含量对ΔG 的影响
3.2 锰、钒渣系生成的热力学分析
对铁水中的杂质元素锰和钒的精炼过程进行分析,探究不同精炼温度和两种渣系活度相差较大的条件下,反应平衡随温度变化的变化,分析结果如图3 所示。

图3 不同渣相活度下ΔG 随温度变化的变化
从图3 可以看出,随着温度的增加,ΔG 均逐渐增加,在熔炼温度范围内,ΔG 的变化均较小,这表明温度对精炼平衡的影响较小。当渣系中(MnO)和(V2O3)活度分别为0.01 和1 时,ΔG 的变化较小,这表明渣相中(MnO)和(V2O3)的含量对于精炼平衡无明显影响。同时,从ΔG 变化上可以看出,在a=1 时,反应2 和反应3 的ΔG 差别较小,因此推测合金精炼时[Mn]和[V]两元素之间可能存在平衡关系,需对杂质元素间的平衡关系进行分析。
3.3 精炼时[Ti]和[Mn]的平衡关系
以上分析表明,在合金精炼过程中,杂质元素之间可能存在平衡关系,因此对杂质元素间的平衡关系进行了分析。
精炼过程中钛和锰的氧化过程的平衡计算,将反应1 和反应2 结合可以得到:

将式(2)的标准吉布斯自由能计算公式进一步整理,可得:

该反应的吉布斯自由能可以写成:
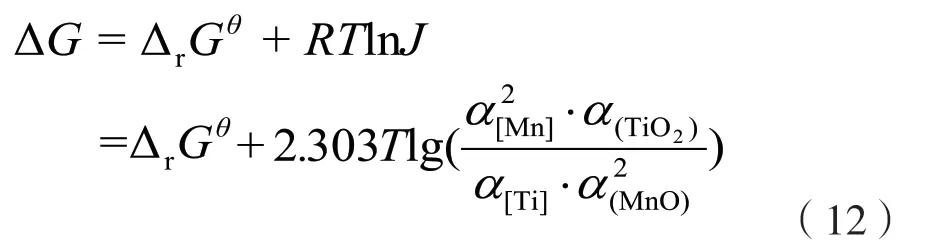
其中,熔体中锰和钛的活度计算公式为:

铁水中[Ti]和[Mn]均以假想纯物质仍符合亨利定律为标准态,以理想稀溶液为参考态;渣相中以纯物质为标准态。反应达到平衡时,ΔG=0,并定义:

则式(12)可写成:
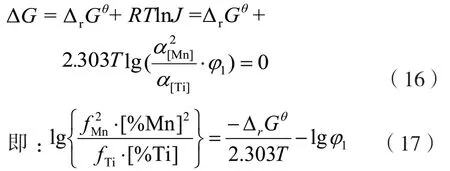
式中:fMn——合金中锰元素的活度系数;fTi——合金中钛元素的活度系数;[%Mn] ——合金中锰的质量分数,wt%;[%Ti] ——合金中钛的质量分数,wt%。设定值分别为0.1、1、2。温度为1 600 K 时,计算钛、锰两元素间的平衡关系,如图4所示。

图4 合金精炼中钛锰平衡关系
从图4 可以看出,精炼达到平衡时,虽然[Ti]含量随[Mn]含量的减少而减少,但两者含量存在数量级的差别。因此,式(9)中(MnO)的存在对于铁水中[Ti]的含量影响较小,且钛和锰含量之间不存在平衡关系。
3.4 精炼时[Mn]和[V]的平衡关系
精炼过程中钒和锰的氧化过程的平衡计算,将反应2 和反应3 结合可以得到:

该反应的吉布斯自由能可以写成:
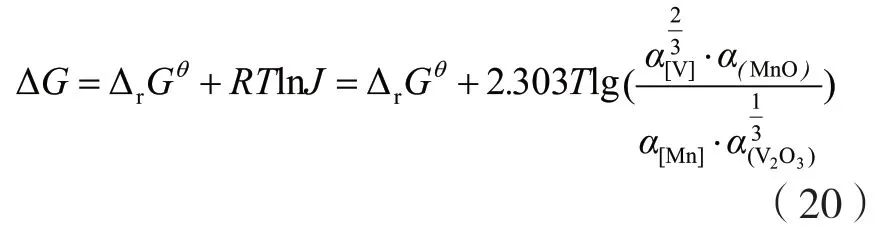
反应达到平衡时,ΔG=0,并定义:

即:


图5 合金精炼中钒锰平衡关系
从图5 可以看出,随着锰含量的降低,钒含量随之降低,同时的大小对于平衡结果影响较大,这表明锰钒两元素间存在平衡关系。由此可知,精炼时需对渣系中氧化物的组分和含量进行合理控制。
4 结论
通过对吹气精炼过程中合金中钛、锰、钒元素氧化的热力学分析及杂质元素之间的相互作用计算,可以得出:
(1)采用气体吹炼法可以有效地将合金中的杂质脱除,且在1 500~ 1 700 K 温度区间内,温度越低越利于钛的脱除,同时可以去除锰和钒元素。
(2)精炼时氧分压对于磷的氧化影响较大,合理控制氧分压或改变氧化剂类型可以有效控制磷含量。
(3)CaO-MgO-SiO2渣系的加入可以提高反应初期的脱钛速率。
(4)渣相活度大小影响锰元素的脱除,但对于钒元素的脱除影响较小。
(5)钛和锰含量之间不存在平衡关系;锰和钒含量之间存在平衡关系,因此精炼时需对于渣系中氧化物的组分、含量合理的控制。
