舌下脱敏疗法在儿童变应性鼻炎中的临床应用
2021-04-13陆振益崔忆旋赵报王文忠
陆振益 崔忆旋 赵报 王文忠
蚌埠医学院第一附属医院耳鼻咽喉头颈外科学(安徽蚌埠233000)
过敏性鼻炎(allergic rhinitis,AR)又称为变应性鼻炎,是由于患者在接触相应变应原后产生的一种慢性炎症反应[1]。全世界AR 患者约有5 亿,人群平均发病率在10%~25%。近30年来我国的AR 患病率显著增加[2],由最初的局部地区报告为11.1%到现在多地区报告的17.6%[3-4]。其中儿童的患病率也在快速增加[5]。AR 的主要症状为鼻痒、鼻塞、流鼻涕、打喷嚏以及眼痒等,随着病程进展还有可能诱发鼻息肉、鼻窦炎等一系列并发症[6],并且能够增加远期支气管哮喘发作的风险[7-8],虽不会为患儿带来生命危险,但病情迁延,易对患儿身心健康产生极大的危害。因此,如何彻底治疗AR 在临床中显得极为重要,传统的治疗方法多采用局部应用喷鼻剂、口服抗过敏药物或激素,患者症状多能得到有效缓解,但伴随而来的是长期用药的不良并发症[9],以及病情反复发作的痛苦。长期临床研究显示,儿童AR 患者经常规抗过敏治疗后,3 个月内复发率超过15%[10]。而舌下脱敏疗法(SLIT)是目前较新型的免疫治疗方法,其安全性好,用药方便[11]。目前虽有研究表明SLIT 治疗儿童过敏性鼻炎有效,但对SLIT 疗法的起效时间的研究相对较少。本研究主要探讨SLIT 治疗在儿童过敏性鼻炎中的短期治疗效果以及其显效时间的判定,以期为儿童过敏性鼻炎患者增加治疗选择方案,使患者减少药物依赖,增强治疗信心,改善患者身心健康。
1 资料与方法
1.1 一般资料本次研究选择2019年4-9月期间就诊于蚌埠医学院第一附属医院耳鼻喉科的儿童过敏性鼻炎患者共计151 例,其中男性患儿67 例,女性患儿84 例,年龄6 ~14 岁,平均(9.93 ±2.23)岁。所有入选患者均符合AR 诊断标准[11]。
纳入标准:(1)患者尘螨点刺实验++及以上;(2)治疗期生命体征平稳,包括体温、呼吸、心率、血压未见异常;(3)4 周内未参加任何其他药物临床实验。
排除标准[12]:(1)有胃肠道及肝肾等疾病或明显的心血管疾病;(2)恶性肿瘤;(3)有心理障碍,无法配合治疗;(4)合并过敏性哮喘;(5)正在应用β受体阻滞剂治疗者;(6)研究者认为不适合参加临床研究的情况。
本研究符合临床研究伦理准则,并获得医院伦理委员会的许可。在入组前,已取得患者及其家属的知情同意。
治疗方法上依据患者及家属治疗意愿分为两组,其中对照组79 例,观察组72 例。对照组采用传统方法治疗(盐酸西替利嗪+盐酸氮卓斯汀喷鼻剂),每周1 疗程,治疗4 周。观察组在对照组的基础上加用畅迪舌下脱敏治疗。观察患者治疗后3、6、12 个月的症状体征及用药改善情况。按照症状评分量表、体征评分量表以及用药评分量表综合评分。
1.2 研究方法对照组使用盐酸氮卓斯汀鼻喷雾剂(生产企业:VIATRIS GmbH Co.KG,规格:10 mg:10 mL)喷鼻,1 喷∕次,2 次∕d(相当于0.56 mg 氮卓斯汀),加用盐酸西替利嗪(生产企业:苏州东瑞制药有限公司,规格:10 mg×12片∕盒)口服,10 mg∕次,1 次∕d,治疗4 周,4 周后根据患者复诊情况及临床症状酌情增减药物用量。观察组在对照组基础上联合使用粉尘螨滴剂1 ~4 号(生产企业:浙江我武生物科技有限公司,规格:2 mL,国药准字国药准字S20060012)滴至舌下,含化2 min 后吞服(总蛋白浓度分别为1、10、100、333 μg∕mL),治疗周期为2年,每天给药1 次,疗程结束时防止病情反弹采用降低频率逐步减量方法停药,由每天1 次降为2 天1 次,1 周2 次,直至完全停药。观察组用药剂量见表1。

表1 观察组舌下脱敏用药剂量表Tab.1 Sublingual desensitization medication dosage table of observation group
1.3 疗效评估分别对AR 患儿SLIT 治疗前1 天、治疗3、6、12 个月后的临床效果进行疗效评估,主要从临床症状、体征、药物总评分三个方面进行评估,评分细则采用《变应性鼻炎诊断和治疗指南》中的评分标准进行制定[11]。(1)症状评分:包括鼻痒、打喷嚏、流涕和鼻塞四个症状,各症状分别采用4 分法计分,其中0 分为无症状,1 分为轻度症状(症状轻微,发作频率较低,易于耐受),2 分为中度症状(症状明显,发作频率较高,但可以忍受),3 分为重度症状(症状严重,影响日常生活或睡眠)。所有症状评分累计总分即为鼻部症状总评分(total nasal symptoms score,TNSS);(2)体征评分:按照鼻甲和鼻中隔黏膜改变进行评分。0 分为鼻甲粘膜无肿胀,鼻中隔、鼻甲可见;1 分为鼻甲轻度肿胀,鼻中隔、中鼻甲尚可见;2 分为下鼻甲与鼻中隔(或鼻底)紧靠,下鼻甲与鼻底(或鼻中隔)之间尚有小缝隙;3 分为下鼻甲与鼻中隔、鼻底紧靠,见不到中鼻甲,或中鼻甲黏膜息肉样变,息肉形成。(3)药物评分:根据患儿每日用药情况评估患儿对症药物的使用情况,采用标准化用药记分,每天喷一次鼻用抗组胺药记为1 分,喷用2 次记为2分,每日口服1 次抗组胺药记为1 分,初始剂量对照组和观察组均为每日两次喷鼻,1 次口服,共记分3 分。所有药物使用记录的累积分即为药物总评分(total medication score,TMS)。
1.4 统计学方法所有统计数据均使用SPSS 20.0 软件进行统计分析。计量资料以均数±标准差表示,组间比较采用独立样本t检验,组内比较采用配对样本t检验,计数资料比较用χ2检验。P<0.05 为差异有统计学意义。
2 结果
随访期间严密监视患者病情,记录患者体征变化及用药变化。其中对照组2 例因更换号码失访,未进行复查。观察组5 例因观察过程中拒绝继续治疗终止观察,其中有2 例考虑经济因素后拒绝进一步治疗,3 例因患儿依从性差拒绝配合用药终止治疗;观察组3 例因更换号码失访,坚持临床治疗的对照组和观察组分别为77、64 例。
2.1 疗效分析研究表明,对照组及观察组在治疗后3、6、12 个月较治疗前的TNSS 评分及体征评分均下降。(1)TNSS 比较:用药3 个月时,对照组和观察组的TNSS 比较差异无统计学意义;用药6、12 个月后观察组的TNSS 均小于对照组,差异有统计学意义(P<0.05)。同时,观察组在3、6、12 个月的TNSS 组内比较差异有统计学意义(P<0.05)。表明患者应用SLIT 疗法3 个月时与对照组相比疗效无明显优势;但治疗6 个月后效果突出,与同时段对照组相比,差异有统计学意义,且在1年内随着用药时间增加,疗效逐渐增强。(2)体征评分比较:用药3 个月时,对照组和观察组的体征评分差异无统计学意义,表明观察组在3 个月时与对照组相比,对体征改善程度没有明显提高。但用药6、12 个月时,对照组的体征评分均大于观察组的体征评分,差异有统计学意义(P<0.05)。同时,观察组在3、6、12 个月时体征评分相较于治疗前相比差异均有统计学意义(P<0.05)。表明患者应用舌下脱敏后对体征改善有效果,其中6、12 个月时效果改善明显。(3)TMS 评分比较:初始用药时两组均按照规范疗程用药,TMS 评分均为3分。用药3 个月时,对照组和观察组的TMS 评分相较于初始用药均有明显下降,差异具有统计学意义,说明两组治疗均有效。但两组间TMS 评分比较差异无统计学意义(P>0.05)。观察组6、12 个月的TMS 相较于对照组明显下降(P<0.05)。表明SLIT 治疗有助于减少药物使用,同时在治疗12 个月时,观察组有43 例(67.2%)完全脱离用药,而对照组仅3 例(3.8%)完全脱离药物治疗。见表2。
表2 治疗前后临床疗效对比Tab.2 Comparison of clinical efficacy before and after treatment±s
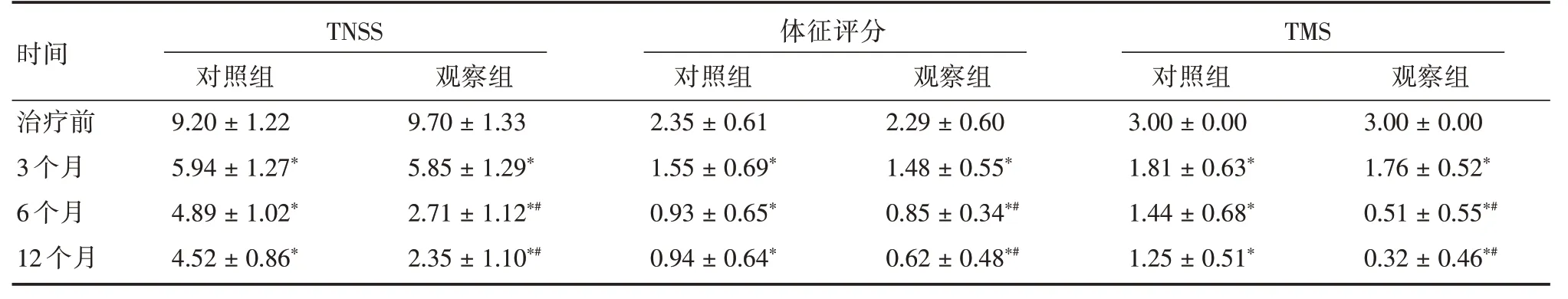
表2 治疗前后临床疗效对比Tab.2 Comparison of clinical efficacy before and after treatment±s
注:与同组治疗前相比,*P <0.05;相同时间点,观察组与对照组相比,#P <0.05
S 体征评分TMS 时间治疗前3 个月6 个月12 个月TNS对照组9.20±1.22 5.94±1.27*4.89±1.02*4.52±0.86*观察组9.70±1.33 5.85±1.29*2.71±1.12*#2.35±1.10*#对照组2.35±0.61 1.55±0.69*0.93±0.65*0.94±0.64*观察组2.29±0.60 1.48±0.55*0.85±0.34*#0.62±0.48*#对照组3.00±0.00 1.81±0.63*1.44±0.68*1.25±0.51*观察组3.00±0.00 1.76±0.52*0.51±0.55*#0.32±0.46*#
2.2 安全性分析观察组64 例中仅3 例出现口腔粘膜瘙痒症状,未予特殊处理,随疗程治疗后自行好转,1 人出现一过性胃肠道不适,共出现2 次,未予特殊处理自行改善,未出现过敏性休克等严重不良反应。同时为防止发生“过敏反跳”现象,对患者进行宣教,如患者拒绝继续脱敏治疗告知患者采用药量频率递减,2 周内逐步停药。
3 讨论
目前认为AR 的机制是机体针对环境变应原产生过量的特异性IgE 而诱发的免疫及炎性反应。吸入物变应原可诱导特异性IgE 产生并与IgE 受体相结合,导致组胺和白三烯等炎性介质释放从而引起鼻痒、打喷嚏、清水样涕等症状,同时组胺等炎性介质的释放还可诱导分泌细胞因子等,募集和活化嗜酸粒细胞及Th2 淋巴细胞等免疫细胞,导致炎性介质如白三烯等的进一步释放,炎性反应加重,鼻黏膜出现明显组织水肿导致鼻塞[13-14]。
变应原特异性免疫治疗被认为是目前惟一可能会改变变应性疾病自然进程的治疗方法[15]。特异性免疫治疗的主要治疗方法包括两种,其中皮下免疫治疗已在临床应用一百余年,疗效优异[16]。但近年来有文献表明其治疗过程中可能会诱发严重的过敏反应,故临床使用中受到限制[17],而舌下脱敏治疗因其更方便的使用方法,极小的不良反应发生率,近年来在临床上应用逐渐增多[18-19]。SLIT 疗法是一种免疫治疗,通过改善患者免疫反应,对参与疾病的多种细胞因子改变提高机体抗炎促炎能力,其作用机制主要为低剂量抗原被抗原提呈细胞处理而诱导T 辅助细胞分化,纠正机体Th1∕Th2 细胞因子的失衡[20],从而达到治疗疾病的目的,这种治疗方法不仅干预疾病进程而且可以预防新的致敏。
此次研究通过两种方法对AR 患者进行治疗,提示SLIT 治疗儿童AR 效果良好,能够有效改善患儿临床症状及减少药物使用。在1年的观察随访中,对照组和观察组相比,用药3 个月时两者差异无统计学意义,SLIT 相对对照组无明显优势;观察组的临床疗效在6 个月时开始优于对照组,表现在症状体征评分的下降,以及对症药物的减少使用,特别是在1年时观察组有43 例(67.2%)可停用对症药物治疗,而对照组仅3 例(3.8%)完全脱离药物治疗。PARK 等[21]统计了112 例15 岁以下亚洲儿童采用舌下含服粉尘螨滴剂特异性免疫治疗,观察1年,药物评分及症状评分明显比治疗前低,生存质量提高。YONEKURA 等[22]的研究显示SLIT 的疗效与患者最佳耐受剂量、时间有密切关系,多数患者半年起效,明显疗效要经过30 周的治疗方能达到。本次研究也发现SLIT 治疗起效较慢,一般在6 个月时方出现较佳的治疗效果,1年时效果明显,与YONEKURA 的研究相符。这给临床医师在SLIT 治疗上提供了指导依据,即临床治疗中需要注意对患者及家属教育,告知患者脱敏治疗的起效时间及药物起效规律,以增强患者的治疗信心,防止患者在早期治疗中自觉症状无明显改善而停药。
本次研究显示在第6 个月时两组差异明显,受限于门诊患者随访时间的限定,无法对患者进行每月随访,是本次实验的不足。同时根据药物使用说明,一般脱敏治疗周期建议治疗2年以上,本次临床研究目前仅随访了患者1年的治疗效果,旨在评估患者1年内的治疗疗效及显现良好效果的时间,同时在后续的治疗研究中将会对患者继续治疗并长期随访,主要随访患者用药2年及停药后的疗效,评估脱敏治疗的长期疗效及疗效时间。目前临床SLIT 治疗儿童过敏性鼻炎疗程为2 ~3年,治疗时间长、费用高,这也是许多患者无法用药的重要原因之一,但如果考虑疾病导致生产力的损失以及停用对症药物使用等间接费用,与单纯的药物治疗相比,SLIT 的优越性更加凸显[23]。
在安全性方面,本次研究中观察组64 例仅1 例患者出现轻度不良反应,后期自行好转,在1年的治疗过程中未出现诸如过敏性休克等严重不良反应,因此SLIT 疗法的安全性也在研究中得到了验证。
综上,SLIT 治疗起效较慢,但效果好,安全性强,用药方便,避免了反复医院就诊的麻烦,且患者依从性较好,能够有效改善患者临床症状,减少患者临床用药,给广大儿童变应性鼻炎患者的治疗提供了较好的治疗思路,有望在临床中进行广泛应用。
