PSEN1基因变异致早发性阿尔茨海默病两例报道并文献复习
2021-04-12张源孙梦凡贾紫嫣姜季委王艳丽徐俊
张源 孙梦凡 贾紫嫣 姜季委 王艳丽 徐俊
阿尔茨海默病是一种起病隐匿、进行性加重的神经变性病。2000-2019年,阿尔茨海默病死亡病例数增加145%[1]。有5%~10%的患者发病年龄<65岁[2],称为早发性阿尔茨海默病(EOAD),其中仅10%~15%与已知基因变异相关[2],呈家族聚集性。APP、PSEN1和PSEN2基因是早发性家族性阿尔茨海默病(EOFAD)最常见的3种致病基因,其变异均可能增加β-淀粉样蛋白(Aβ)的产生和沉积,其中PSEN1遗传变异约占上述3种致病性突变总数的75%[3]。目前已报道的PSEN1致病性突变位点有300余种(https://www.alzforum.org/mutations)。本研究报道2020年12月至2021年1月在首都医科大学附属北京天坛医院神经病学中心认知障碍科门诊就诊的2例早发性家族性阿尔茨海默病患者,并结合国内已报道的相关文献,总结疾病临床特点及基因诊断价值。
病例资料
例1先证者(Ⅲ2),男性,47岁,初中学历,右利手。主因记忆力下降2年、症状加重6个月,于2021年1月7日至我院认知障碍科门诊就诊。患者2年前无明显诱因出现近记忆力减退,主要表现为忘记他人说过的话、忘记与他人的约定等,未予特殊处理;近6个月记忆力减退加重,始终重复语言,情绪急躁,易激惹,精神行为无明显异常,日常生活基本自理。患者自发病以来,情绪较为低落,轻度焦虑、抑郁,入睡稍困难,夜间易醒,饮食尚可,大小便正常,体重无明显变化。既往身体健康;吸烟史20年、平均20支/d,饮酒史20年、500 g/次、3次/周,已戒酒1年。先证者祖父、母亲均有痴呆表现,其祖父(Ⅰ2)45岁时出现记忆力减退,晚年生活不能自理,70岁时死亡(死因不详);其母(Ⅱ2)47岁时出现记忆力减退,逐渐加重至不认识子女,生活不能自理,76岁时死亡(死因不详);其余家族成员目前无记忆力减退症状。体格检查:神志清楚,语言流利,记忆力、计算力、执行力欠佳,时间定向力差,空间定向力尚保留,脑神经查体未见异常,肌力、肌张力正常,腱反射对称,感觉及共济运动无特殊,病理征呈阴性。实验室检查指标均于正常值范围。神经心理学测验:简易智能状态检查量表(MMSE)评分为21,提示近记忆力、计算力、时间定向力和视空间能力下降;蒙特利尔认知评价量表(MoCA)北京版评分为18;徐俊Cog-12问卷调查系统(简称Cog-12)评分为7;汉密尔顿抑郁量表(HAMD)评分为9,提示轻度抑郁;汉密尔顿焦虑量表(HAMA)评分为6;日常生活活动能力量表20项(ADL-20)评分为21,匹兹堡睡眠质量指数(PSQI)评分为7,提示睡眠障碍。影像学检查:头部MRI显示全脑皮质及双侧海马轻度萎缩,内侧颞叶萎缩评定量表(MTA)为1级(图1),脑医生智能影像诊断平台(Dr.Brain)定量分析提示灰质和海马体积及其所占比例位于正常参考值下限,灰质总体积为585.22 cm3、占比40.11%(正常参考值:38.33%~47.06%),左侧海马体积为2.55 cm3、占比0.17%(正常参考值:0.17%~0.23%),右侧海马体积为2.78 cm3、占比0.19%(0.19%~0.26%);动脉自旋标记(ASL)定量分析显示双侧大脑皮质和海马血流量降低,右侧杏仁核血流量较左侧降低(图2)。基因检测:晨起采集先证者肘静脉血5 ml,送检北京金准医学检验实验室有限公司,进行高通量测序,结果显示,PSEN1基因编码区外显子6 c.488A>G(p.His163Arg)错义突变(图3);根据遗传变异分类的证据联合标准规则,该突变位点在人类基因突变数据库(HGMD)专业版已报道为致病性突变。结合先证者临床表现、家族史、神经心理学测验、影像学检查及基因检测结果,明确诊断为PSEN1基因变异致早发性家族性阿尔茨海默病,该家系明确为早发性家族性阿尔茨海默病家系(图4)。予以美金刚10 mg/d规律口服和利斯的明贴剂1贴/晚,随访至今病情稳定。
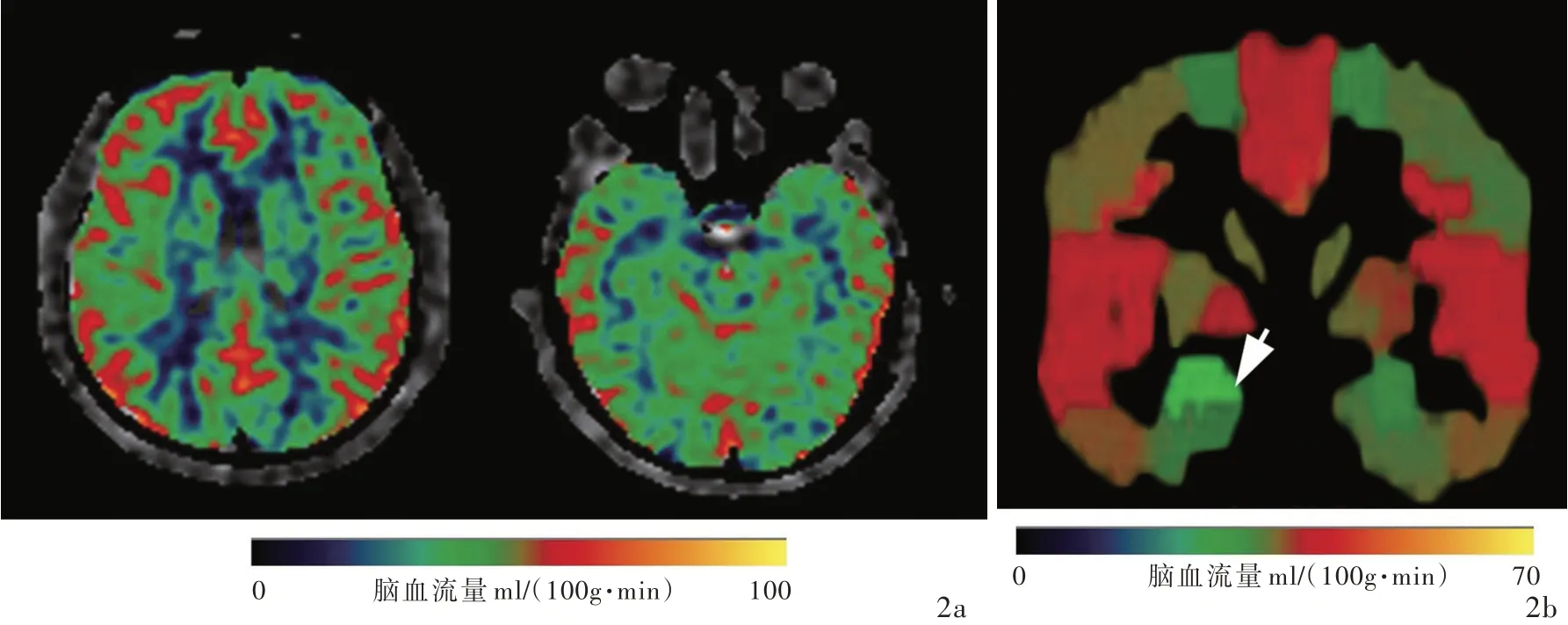
图2 例1头部ASL所见 2a 横断面ASL显示,额颞顶叶皮质(左图)和海马层面(右图)血流量降低 2b 冠状位ASL显示,右侧杏仁核血流量较左侧降低(箭头所示)Figur e 2 Head axial and coronal ASL showed low CBF in the bilateral cerebral cortex and hippocampus and reduced perfusion in the right amygdala(arrow indicates).Frontal,temporal and parietal cortex(left)and hippocampus(right,Panel 2a).Amygdala(Panel 2b).

图3 例1基因检测显示,PSEN1基因外显子6 c.488A>G(p.His163Arg)突变(红色圆圈所示)Figur e 3 The gene detection result of the proband of Case 1 was c.488A>G(p.His163Arg)in the exon 6 of PSEN1 gene(red circle indicates).
例2先证者(Ⅲ3),女性,44岁,小学学历,从事棉花检验工作,右利手。因记忆力下降1年余,于2020年12月31日至我院认知障碍科门诊就诊。患者1年余前无明显诱因出现记忆力减退,主要表现为不能胜任工作,情感淡漠,做家务懒散,无明显情绪及行为异常,无幻视,日常生活基本自理,睡眠一般,饮食尚可,大小便正常,体重无明显变化。既往身体健康,无吸烟、饮酒史。先证者外祖母(Ⅰ1)、母亲(Ⅱ5)、三姨母(Ⅱ3)、二舅父(Ⅱ2)、二兄(Ⅲ2)均有痴呆表现,且表现为记忆力减退,其母于53岁死亡(死因不详),其三姨母(60岁)和二舅父(59岁)仍可工作,其二兄48岁,职业为司机,目前已无法胜任工作,其余家庭成员尚无认知功能障碍症状。体格检查:神志清楚,语言流利,记忆力、计算力、执行功能、定向力欠佳,反应迟钝,理解力差,脑神经检查未见异常,肌力、肌张力正常,腱反射对称,感觉及共济运动无特殊,病理征阴性。实验室检查指标均于正常值范围。神经心理学测验:MMSE评分为11,提示近记忆力、定向力、计算力、语言功能和视空间能力下降;MoCA北京版评分为5;Cog-12评分为17;HAMD评分为2;HAMA评分为1;ADL-20评分为28;PSQI评分为5。影像学检查:头部MRI显示全脑皮质萎缩,双侧海马萎缩,以左侧显著(图5);脑医生智能影像诊断平台定量分析提示灰质和海马体积及其所占比例显著降低,灰质总体积为489.42 cm3、占比34.69%(37.62%~48.09%),左侧海马体积为1.63 cm3、占比0.12%(0.16%~0.24%),右侧海马体积为2.10 cm3、占比0.15%(0.18%~0.27%);ASL定量分析显示左侧大脑皮质及海马血流量显著低于右侧(图6)。基因检测:晨起采集先证者肘静脉血5 ml,送检北京金准医学检验实验室有限公司,进行高通量测序,结果显示,PSEN1基因编码区外显子5 c.344A>G(p.Tyr115Cys)错义突变(图7);根据遗传变异分类的证据联合标准规则,该突变位点在HGMD数据库专业版已报道为致病性突变,但为国内首次报道。结合先证者临床表现、家族史、神经心理学测验、影像学检查和基因检测结果,明确诊断为PSEN1基因变异致早发性家族性阿尔茨海默病,该家系明确为早发性家族性阿尔茨海默病家系(图8)。规律予以重酒石酸卡巴拉汀胶囊3 mg/d口服,随访至今病情较前无明显变化。
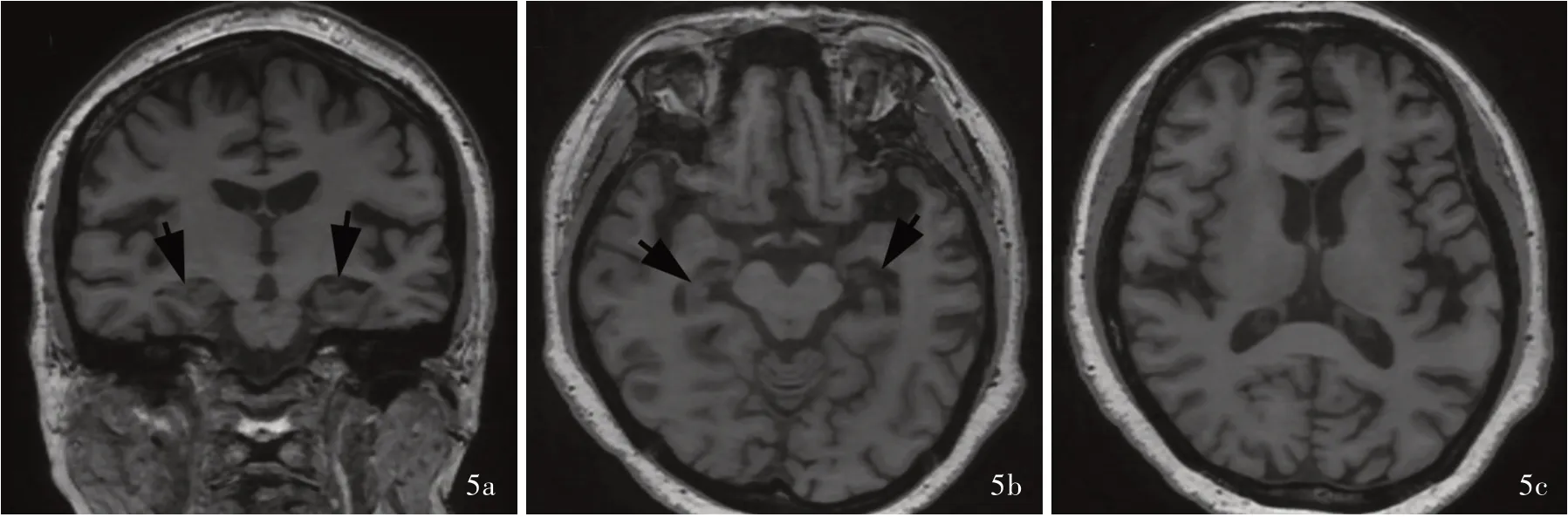
图5 例2头部MRI显示全脑皮质萎缩,双侧海马萎缩,以左侧显著(左侧MTA分级2级、右侧1级,箭头所示) 5a 冠状位T1WI(海马层面) 5b 横断面T1WI(海马层面) 5c 横断面T1WI(额颞顶叶皮质层面)Figure 5 Head MRI findings of the proband of Case 2 showed whole cerebral cortical atrophy and bilateral hippocampal atrophy,obviously on the left side(MTA 2 for the left,MTA 1 for the right;arrows indicate).Coronal T1WI(hippocampus,Panel 5a).Axial T1WI(hippocampus,Panel 5b).Axial T1WI(frontal,temporal and parietal cortex;Panel 5c).
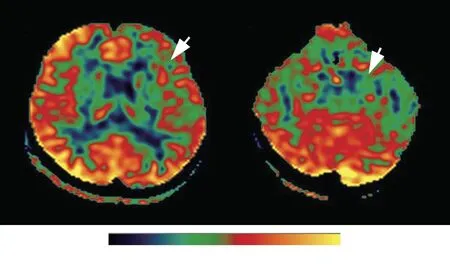
图6 例2头部横断面ASL显示左侧大脑皮质及海马血流量显著低于右侧(箭头所示;左图为额颞顶叶皮质层面,右图为海马层面)Figure 6 The head axial ASL findings of the proband of Case 2 showed significantly reduced perfusion in the left cortex and hippocampus(arrows indicate;frontal,temporal and parietal cortex for left and hippocampus for right).
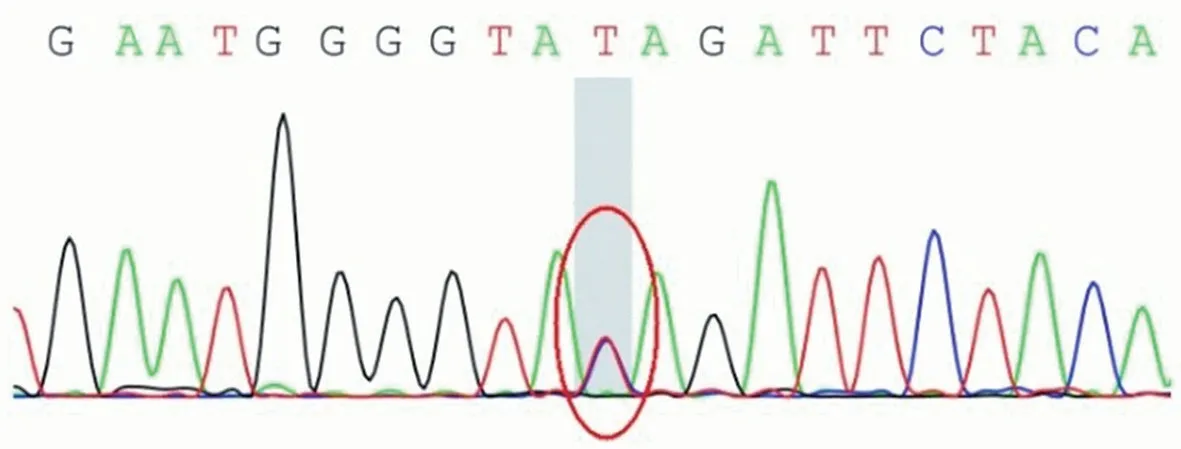
图7 例2基因检测显示,PSEN1基因外显子5 c.344A>G(p.Tyr115Cys)突变(红色圆圈所示)Figur e 7 The gene detection result of the proband of Case 2 was c.344A>G(p.Tyr115Cys)in the exon 5 of PSEN1 gene(red circle indicates).

图8 例2早发性家族性阿尔茨海默病家系图Figure 8 EOFAD pedigree of Case 2.
讨 论
阿尔茨海默病为痴呆最常见病因,占全部痴呆的60%~80%[1]。高龄是阿尔茨海默病的主要危险因素之一,据此分类可以分为早发性阿尔茨海默病和晚发性阿尔茨海默病(LOAD)。阿尔茨海默病典型临床特征为进行性记忆力损害,进而累及视空间、执行、语言等认知域,最终导致全面认知功能障碍。然而部分早发性家族性阿尔茨海默病患者可存在记忆功能相对保留的非典型表现,而以语言障碍、视空间能力或执行功能障碍更突出。
笔者以“早老素1”、“家族性”、“阿尔兹/茨海默病 ”、“presenilin 1”、“Chinese early-onset Alzheimer's disease”等作为关键词检索1995年7月1日至2021年4月1日万方数据知识服务平台、中国知网中国知识基础设施工程(CNKI)、维普中文数据库及美国国立医学图书馆生物医学文献数据库(PubMed)发表的中国PSEN1基因变异致早发性家族性阿尔茨海默病家系,剔除同一机构、作者的重复报道,并增加本研究两家系,最终纳入40家系(表1)[4-33]。PSEN1基因与早发性家族性阿尔茨海默病密切相关。目前已报道中国PSEN1基因变异致早发性家族性阿尔茨海默病共40家系,其中有2个重复报道的突变位点(c.488A>G和c.1133G>A),致病突变位点共38个,分别位于外显子4~12,其中外显子7变异率最高。发病年龄为21~62岁,病程4~者(家系7)以儿童期癫发作发病,35岁时出现记忆力减退,先证者祖母以精神障碍发病,家系中其10年,进展迅速,最终导致重度痴呆、卧床、生活无法自理,甚至合并肺部感染等并发症而死亡。详细报道(包括本研究两家系)的PSEN1基因变异致早发性家族性阿尔茨海默病家系中,35例先证者均以进行性记忆力减退为首发症状,其中1例c.1292C>T位点突变患者(家系34)有路易体痴呆样表现,即认知功能障碍、幻视及帕金森综合征,但其认知症状波动性不明显,家系中其余患者亦多呈路易体痴呆样表现[31]。1例c.677T>G位点突变患者(家系20)以语言障碍发病,表现为言语不清,除先证者母亲因死亡时间较早发病不详外,家系中其余患者均表现为相似症状[21-22]。1例c.346G>A位点突变患余患者均以记忆障碍发病[12]。1例c.1300G>A位点突变患者(家系37)以精神行为异常发病,主要表现为幻觉、妄想[10]。2例c.407C>G和c.1300A>C位点突变患者(家系8和家系36)临床表现不详。随着病情进展,早发性家族性阿尔茨海默病患者迅速出现定向力、计算力障碍,性格改变,行为异常,幻视以及日常生活活动能力下降等多认知域损害表现,精神行为异常主要表现为暴躁易怒、易激惹,也可表现为抑郁、淡漠等。疾病进程中,9例c.313T>G、c.346G>A、c.488A>G、c.497-499delTTA、c.604A>T、c.766T>A、c.786G>T、c.1133G>A和c.1292C>T位点突变家系(家系4、7、11、12、15、25、26、31、34)部分患者合并锥体外系症状,主要临床表现为步态异常、肌阵挛、静止及活动性震颤、行动迟 缓 等[6,10,12,15,17-19,28,31],4例c.488A>G、c.697A>C、c.766T>A和c.1156T>A位点突变家系(家系11、21、25、32)部 分 患 者 出现癫发 作[15,18-19,23,29]。2例伴有耳部症状,1例c.6519T>A位点突变家系(家系38)部分患者合并耳聋[33],1例c.313T>C位点突变家系(家系3)除病史无法采集者,余患者均伴蝉鸣样耳鸣[7-8]。

表1 中国PSEN1基因变异致早发性家族性阿尔茨海默病家系临床及遗传学特点Table 1. The clinical presentation and genotype characteristics of EOFAD caused by PSEN1 gene mutation in China
国内关于PSEN1基因变异致早发性家族性阿尔茨海默病的报道相对较少,随着基因检测技术的逐步成熟,国内相关病例报道逐年增多。本文报道的两家系均表现为以记忆力减退为首发症状的遗忘相关综合征,例2突变位点为国内首次报道。2例先证者目前尚未出现严重精神行为异常及认知功能障碍,进而影响基本日常生活活动能力。但早发性家族性阿尔茨海默病患者多进展迅速,平均5年即可进展至重度痴呆,尤其是遭受急性应激打击后,症状可呈断崖式恶化。早期干预能否延缓疾病进程尚不明确,仍待后续随访观察。除典型认知相关表现外,少数患者晚期可伴肌张力增高、肌阵挛、痉挛性截瘫等锥体外系表现及癫发作等,应注意识别。此外,少数患者发病症状不典型如言语障碍、癫发作等,易与额颞叶痴呆、原发性进行性失语(PPA)等混淆,造成早期误诊。
PSEN1基因变异致早发性家族性阿尔茨海默病患者在出现临床症状前即已发生阿尔茨海默病病理生理学改变,动物和体外研究显示,PSEN1M139T突变使γ分泌酶羧肽酶样活性降低,使Aβ42生成相对增加,Aβ43和Aβ40生成减少[34]。亦有研究显示,基因变异干扰Aβ生成和沉积是痴呆的先决条件,但并不能决定痴呆严重程度,而磷酸化tau蛋白病理改变是痴呆严重程度的主要决定因素[35]。基因变异改变相关tau蛋白激酶如细胞外信号调节激酶(ERK)活性和蛋白分解代谢,影响导致tau蛋白磷酸化的蛋白降解,从而加速疾病进展。临床表现多样性可能与致病基因变异相关。有研究显示,家族性阿尔茨海默病患者出现痉挛性截瘫可能提示存在PSEN1基因变异以及所谓的“棉毛斑(cotton wool plaque)”异常沉积[36]。“棉毛斑”主要由氨基末端(N-端)截断形式的Aβ组成,表明不同长度Aβ的产生和沉积可能造成不同的Aβ沉积形态,从而产生不同毒性作用。目前,PSEN1基因变异导致不典型临床表现的具体机制尚不明确。此外,有研究显示,早发性阿尔茨海默病亦有散发性患者,此类患者无明确家族史,可能为环境因素导致的新发变异,也可能与家庭成员未行基因检测或去世过早相关。Lanoiselée等[37]对129例发病年龄<51岁的早发性散发性阿尔茨海默病患者行基因检测,共发现9种PSEN1基因新发变异。既往报道的PSEN1基因新发变异较少,可能因目前基因检测多侧重家系病例,存在选择偏倚有关。因此,对于临床早发或症状不典型患者,无论是否存在可疑家族史,对患者及其亲属均建议行全外显子组或全基因组测序,有助于明确诊断。
本研究的不足之处在于,两家系仅对先证者进行基因检测,其余患者因死亡、联系困难、不愿配合等未进行家系成员验证。今后将尽可能完善家系验证,能够进一步明确突变位点及遗传学特征,早期发现无症状基因变异携带者,以指导临床诊断与治疗。
利益冲突无
