肾衰六君子方联合阿托伐他汀对维持性血液透析患者营养不良-炎症-动脉粥样硬化综合征的影响
2021-04-10潘红梅郭维毅张宏颖杜立建马金荣张林燕
潘红梅,郭维毅,张宏颖,杜立建,马金荣,张林燕
(1. 河北省沧州中西医结合医院,河北 沧州 061000;2. 石家庄市中医院,河北 石家庄 050000)
维持性血液透析(MHD)作为一种肾脏替代治疗方式,不仅可减轻机体水负荷,还能有效清除机体内毒性代谢产物,从而显著延长患者生存期[1]。然而,MHD患者在治疗过程中发生的营养不良-炎症-动脉粥样硬化综合征(MIAS)不容忽视,MIAS各个因素之间相互促进、相互影响,可形成恶性循环,显著增加患者病死率[2-4]。目前,针对本病的治疗仍以西医对症治疗为主,但综合疗效仍未达到预期。近些年,在MHD的同时辅以中医药治疗已受到了临床的青睐,中医药能够通过抑制炎症反应,调节机体代谢紊乱等多环节途径,从而发挥防治血液透析相关并发症的作用[5]。本研究探讨了肾衰六君子方联合阿托伐他汀对MHD患者MIAS的影响,现报道如下。
1 资料与方法
1.1一般资料 选择2017年1月—2019年4月河北省沧州中西医结合医院收治的MHD伴有MIAS患者64例,年龄>18岁,透析龄≥3个月,MIAS的诊断参照《临床血液透析学》[6]标准:同时存在营养不良[血清白蛋白(ALB)<35 g/L,或其余营养指标异常]、微炎症反应[高敏C反应蛋白(hs-CRP)>3 mg/L]和动脉粥样硬化[颈总动脉或分叉处内膜中层厚度(IMT)≥1.0 mm]。排除纳入前3个月发生感染者,合并风湿性疾病、自身免疫性疾病、恶性肿瘤、各类肝炎或消化道器质性疾病、心脑血管疾病(冠心病、心力衰竭、脑卒中等)者。将纳入的64例患者随机分为2组:对照组32例,男19例,女13例;年龄32~72(58.6±9.3)岁;透析时间(45.21±18.70)个月;原发疾病:慢性肾小球肾炎16例,糖尿病肾病6例,高血压肾病5例,狼疮肾炎3例,多囊肾2例。观察组32例,男17例,女15例;年龄30~71(57.4±8.4)岁;透析时间(43.87±16.40)个月;原发疾病:慢性肾小球肾炎17例,糖尿病肾病7例,高血压肾病4例,狼疮肾炎2例,多囊肾2例。2组性别、年龄、透析时间、原发疾病比较差异无统计学意义(P均>0.05),具有可比性。本研究经河北省沧州中西医结合医院医学伦理委员会审核通过(2016048)。
1.2治疗方法 2组均继续接受既往的血液透析治疗,均采用碳酸氢盐透析液,透析膜面积为1.3~1.8 m2;透析液速度、血流量分别设置为500 mL/min和200~300 mL/min,每周透析3次,每次4 h。此外给予低盐、低磷、优质低蛋白饮食,控制血糖血压,纠正贫血与电解质紊乱、代谢性酸中毒。对照组同时给予阿托伐他汀钙片(辉瑞制药有限公司,国药准字J20070060)20 mg每晚口服。观察组在对照组治疗基础上加用肾衰六君子汤,组方:人参20 g、黄芪20 g、山药15 g、白术12 g、党参12 g、茯苓12 g、半夏10 g、陈皮10 g、砂仁9 g、木香9 g、桃仁12 g、丹参12 g、炙甘草6 g。随症加减:血虚明显者加阿胶9 g、熟地12 g;湿热明显者加茵陈9 g、白术12 g;痞满腹胀明显者加槟榔和青皮各12 g。水煎煮200 mL,每日1剂,分早晚2次口服,2组疗程均为12周。
1.3观察指标
1.3.1营养不良-炎症评分(MIS) 该评分涵盖4个大项(病史、体检、体质指数与实验室检查),包括10个条目,每个条目分为4个等级[0(正常)~3分(严重)],总分值为30分,总分按照严重程度分为轻度(1~7分)、中度(8~18分)、重度(19~30分)[7]。
1.3.2营养学指标 记录2组干预前后ALB、血红蛋白(Hb)、转铁蛋白(TRF)、上臂围(MAC)、肱三头肌皮褶厚度(TSF)。
1.3.3炎性反应指标 抽取清晨空腹静脉血标本,离心后分别采用免疫比浊法、ELISA法测定2组干预前后血清hs-CRP、肿瘤坏死因子-α(TNF-α)与白细胞介素-6(IL-6)水平。
1.3.4动脉粥样硬化相关指标 干预前后采用飞利浦IE33型超声多普勒检测仪进行颈动脉超声检查,记录2组颈动脉分叉、IMT,其中IMT>1.0 mm则评定为颈动脉粥样硬化[8]。
1.3.5临床疗效 2组12周疗程结束后进行疗效评定。临床控制:ALB、hs-CRP和颈动脉IMT均恢复正常范围;显效:ALB、hs-CRP和颈动脉IMT均显著改善,且至少有2个指标恢复正常范围;有效:ALB、hs-CRP和颈动脉IMT均有所改善,且至少有1个指标恢复正常范围;无效:未达到上述标准。总有效率= (临床控制+显效+有效)例数/总例数×100%。

2 结 果
2.12组治疗前后MIS比较 与治疗前比较,治疗后2组MIS评分均明显降低(P均<0.05),且治疗后观察组评分明显低于对照组(P<0.05)。见表1。
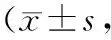
表1 2组MHD伴MIAS患者治疗前后MIS比较分)
2.22组治疗前后营养学指标比较 与治疗前比较,治疗后2组血清ALB、Hb、TRF水平,MAC、TSF均明显增加(P均<0.05),且治疗后观察组上述指标均高于对照组(P均<0.05)。见表2。
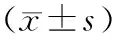
表2 2组MHD伴MIAS患者治疗前后营养学指标比较
2.32组治疗前后炎症反应指标比较 与治疗前比较,治疗后2组血清hs-CRP、TNF-α与IL-6水平均明显降低(P均<0.05),且治疗后观察组上述指标均低于对照组(P均<0.05)。见表3。
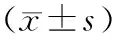
表3 2组MHD伴MIAS患者治疗前后炎症反应指标比较
2.42组治疗前后动脉粥样硬化指标比较 与治疗前比较,治疗后2组颈动脉分叉、颈总动脉IMT均明显降低(P均<0.05),且治疗后观察组上述指标均低于对照组(P均<0.05)。见表4。
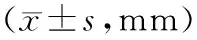
表4 2组MHD伴MIAS患者治疗前后颈动脉分叉、颈总动脉IMT比较
2.52组临床疗效比较 观察组治疗总有效率为87.5%(31/34),明显高于对照组的65.6%(24/34)(P<0.05)。见表5。
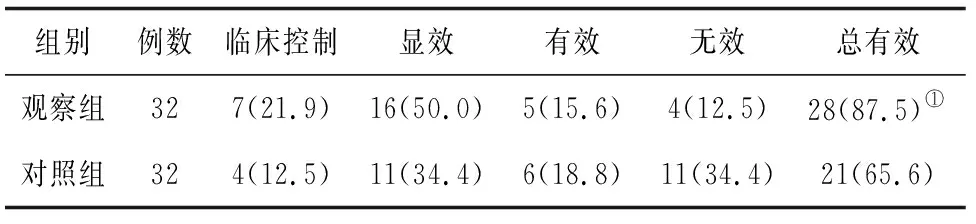
表5 2组MHD伴MIAS患者治疗12周后临床疗效比较 例(%)
3 讨 论
MIAS是血液透析患者常见的并发症之一,是造成患者生活质量低下和发生心血管事件发生的重要因素。血透中采用的透析器属于异物,生物相容性较低,可加速蛋白质的分解;代谢性酸中毒可增加脂肪与蛋白质的分解代谢速率;透析患者常伴有胃肠道功能紊乱如恶心呕吐、食欲减低等,导致营养物质摄入和吸收减少;MHD患者常伴有内分泌代谢紊乱,产生胰岛素抵抗和高胰岛素血症,对胰岛素样生长因子、生长激素的敏感性减低,从而导致蛋白质合成降低,分解加快,引起负氮平衡[9]。有研究表明,MHD患者中营养不良占40%~60%[3]。另外透析膜与血液接触后,可激活机体单核细胞、白细胞与补体系统,诱导炎症反应;且机体代谢毒性产物可激活核因子-κB(NF-κB),从而诱导TNF-α、IL-6、hs-CRP和细胞黏附分子释放,造成微炎症反应[10]。上述炎症细胞因子还能抑制胃肠道功能,降低食欲,导致营养成分摄入降低;还能促进骨骼肌蛋白分解,抑制白蛋白合成,从而诱发营养不良[11]。微炎症反应还能损伤血管内皮功能,促进细胞间黏附分子合成,并趋化单核巨噬细胞向内皮下聚集浸润,导致动脉粥样硬化的形成。有研究表明,动脉粥样硬化在MHD患者发生率高达65%[2-3]。MIAS中慢性炎症、营养不良与动脉硬化常相互影响,形成叠加效应,不断使患者病情恶化。
阿托伐他汀是一种HMG-CoA还原酶抑制剂,是常见的冠心病、脑梗死二级预防类药物,在调节血脂,抑制粥样斑块形成,降低心脑血管事件中具有重要价值。除了常规的调脂效应外,该药还能通过抑制NF-κB 65介导的炎症反应,下调IL-1、IL-6和单核细胞趋化因子-1 (MCP-1)等细胞炎症因子表达,减轻炎症对血管内皮的损伤,发挥减轻炎症、保护血管内皮功能、降低心血管并发症风险的功能[12]。另有临床研究证实,在MHD患者中加用阿托伐他汀可增强抗炎症效果,从而抑制与炎症相关的促红细胞生成素(EPO)合成不足与骨骼肌蛋白分解,有利于间接改善患者肾性贫血与营养不良状况[13]。
中医学认为接受MHD治疗的慢性肾衰竭属于“关格”“溺毒”“虚劳”范畴。本病主要病机以本虚标实为主,其中本虚为脾肾气虚,瘀血、湿热、痰浊毒等为标实。饮食不节、劳倦内伤、内卫不固、感受外邪等导致脾胃受损,加之长期透析,引起脾肾气虚,脾失健运,水液化生及转输功能失调,湿瘀内阻于中焦而发恶心呕吐、腹胀痞满和纳差食少。脾肾亏虚日久,气血化生乏源,导致新血不生、瘀血内阻,五脏六腑失去气血的濡养而引发营养不良。气虚无力祛逐邪毒,加之气血运行乏力,血瘀阻滞脉络,进一步加重气虚之证,邪毒留恋日久而发生微炎症反应。脾肾气虚,气血运行不畅,瘀血阻滞于经络脉管,失濡养后而发动脉硬化。本研究采用的肾衰六君子方剂是在经典名方香砂六君子汤的基础上化裁而来,方中人参可大补元气、健脾益肺;黄芪补肾益精、益气健脾、补气养血;山药固精止带、补脾肺肾;白术、党参、茯苓健脾益气祛湿;半夏、陈皮健脾理气;砂仁、木香疏通中焦气机,健脾和胃;桃仁、丹参活血化瘀,通利血脉;炙甘草益气复脉、补脾和胃,调和诸药。全方注重攻补并重、标本兼治,共奏健脾益肾、补中益气、调畅中焦气机、活血化瘀通络之功效。现代药理学研究表明,人参含有的人参皂甙、多种氨基酸、维生素、β-谷甾醇等具有调节免疫功能,刺激骨髓造血,提高血红蛋白,红细胞计数,促进蛋白质合成,具有改善贫血与营养不良的功效[14]。党参、白术、山药和茯苓相互配伍则能下调MHD患者的血清hs-CRP、TNF-α与IL-6表达水平,缓解微炎症状态,有利于改善预后[15]。丹参则能抑制血小板聚集,降低血液黏稠度,促进一氧化氮/内皮素表达平衡,保护血管内皮功能,抑制单核巨噬细胞向内皮下迁移,从而抑制脉粥样硬化斑块的形成[16]。
本研究结果显示,观察组加用中药干预后治疗总有效率及ALB、Hb、TRF、MAC、TSF均明显高于对照组,MIS评分、颈动脉分叉IMT、颈总动脉IMT及血清hs-CRP、TNF-α、IL-6水平均明显低于对照组。显示肾衰六君子方联合阿托伐他汀治疗MHD伴MIAS不仅可改善机体营养状况,缓解机体微炎症反应,还能抑制或逆转动脉粥样硬化。
利益冲突:所有作者均声明不存在利益冲突。
