术前超声造影和术中快速冰冻病理切片诊断VETC癌巢型肝细胞癌的价值及患者手术方式选择研究
2021-04-07杨建荣钟敬涛刘天奇杜阳春韦所苏唐耘天黄永塔董小锋
杨建荣,钟敬涛,刘天奇,杜阳春,韦所苏,殷 舞,凌 冰,唐耘天,黄永塔,董小锋
我国肝细胞癌(hepatocellular carcinoma,HCC)的新发患者及死亡患者均占全球的50.00%左右[1]。HCC患者5年的总体生存率为14.1%,由于HCC早期无明显症状,多数患者首诊时已处于中晚期,失去了外科手术机会,而手术患者术后5年的复发率、转移率亦高达50%~70%[2]。目前,尽管术后有分子靶向、免疫、化疗等多种治疗手段,但不同HCC患者因肿瘤亚型差异,对治疗反应不同,部分接受治疗的患者甚至出现进展加速现象[3]。因此,进行更加精细化的分型,制定个体化的诊疗方案,是减少HCC患者术后复发的关键[3]。有研究[4]发现,HCC中的内皮细胞除了在形态学上构成管状血管给肿瘤输送营养和氧气外,还可以将HCC细胞包绕成球形细胞团,形成血管包绕肿瘤细胞巢(vessels encapsulated tumor clusters,VETC)癌巢型HCC。VETC癌巢型HCC有其独特的生物学特征,且生存预后更差[4]。本研究将对VETC癌巢型HCC的形态学特点、术前超声诊断标准、术中冰冻诊断标准及手术方式选择进行探讨,现报告如下。
1 资料与方法
1.1资料来源 广西壮族自治区人民医院肝胆胰脾外科、山东省肿瘤防治研究院[山东省肿瘤医院/山东第一医科大学(山东省医学科学院)]肝胆外科2013-10~2018-10行手术切除且经常规病理证实为HCC的164例患者,其中男130例,女34例,年龄32~72(51±6.7)岁,肿瘤分期T1/T2期101例,T3/T4期63例。纳入标准:(1)超声造影检查资料完整;(2)首次外科手术患者;(3)常规病理免疫组化指标中包含CD34血管染色,资料完备。排除标准:(1)术前接受经肝动脉化疗栓塞(transarterial chemoembolization,TACE)介入治疗者;(2)术前接受射频、微波治疗者;(3)术前接受免疫及靶向治疗者。
1.2资料收集 通过医院病历系统收集患者的临床资料,包括年龄、性别、超声检查、术中快速冰冻病理切片(HE染色切片)结果、术后常规病理检查结果、手术记录等。手术方式分为解剖性肝切除(包括标准的肝段切除、肝叶切除)和非解剖性肝切除两种类型。全部患者均随访至术后2年,记录HCC复发情况。
1.3超声造影诊断标准 癌巢型HCC与非癌巢型HCC超声造影判读标准按照本课题组前期研究标准[4]:(1)VETC癌巢型HCC,超声造影动脉充盈期表现为肿瘤周边的环状高增强,后呈裂隙状、条索状逐渐向中央填充,直至造影剂达到峰值;(2)非VETC癌巢型HCC,超声造影动脉充盈期表现为肿瘤周边及内部多个点状造影剂的同时显示,后呈大片状、弥漫性快速充盈,造影剂达高峰后表现为更强的充盈相。超声造影结果由超声科2名副主任医师判断,遇到结果不一致时请第三名具有高级职称的超声科医师复核。所有参与研究的超声科医师对标本的CD34血管染色结果及是否为VETC癌巢型HCC患者均不知情。
1.4病理诊断标准
1.4.1 根据CD34血管染色结果,VETC癌巢型HCC最终诊断按照本课题组前期研究标准[4]:(1)VETC癌巢型HCC,CD34血管染色典型表现为球状血管内皮细胞包绕的HCC细胞团,形成血管包绕的肿瘤细胞簇(VETC癌巢结构);(2)非癌巢型HCC,CD34血管染色表现为内皮细胞未包绕HCC细胞,仅形成条索状的血管。
1.4.2 根据术中快速冰冻病理切片(HE染色切片)结果,VETC癌巢型HCC预测诊断按照本课题组前期研究标准[4]:(1)VETC癌巢型HCC,单层扁平细胞将肝癌细胞包裹成球体,球体最大径大小不一,球体内由HCC细胞聚集而成,球体内部无血管,球体之间的裂隙内含红细胞;(2)非VETC癌巢型HCC,肝癌细胞条索状、梁状、假腺样排列,癌细胞周围无扁平细胞包绕。HE染色切片(冰冻切片)的判读结果由病理科的2名副主任医师作出,遇到结果不一致时请第三名具有高级职称的病理科医师复核。所有参与研究的病理科医师对标本的CD34血管染色结果及是否为VETC癌巢型HCC患者均不知情。
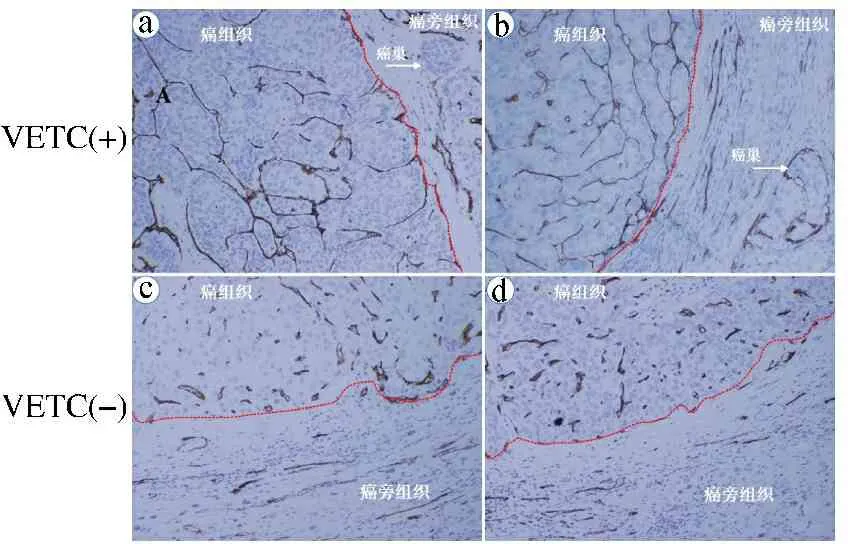
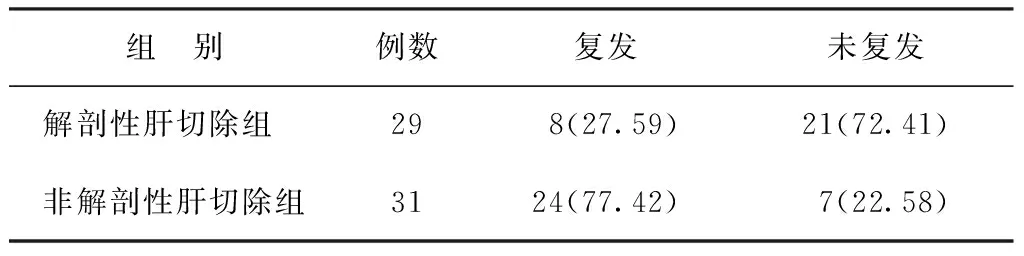
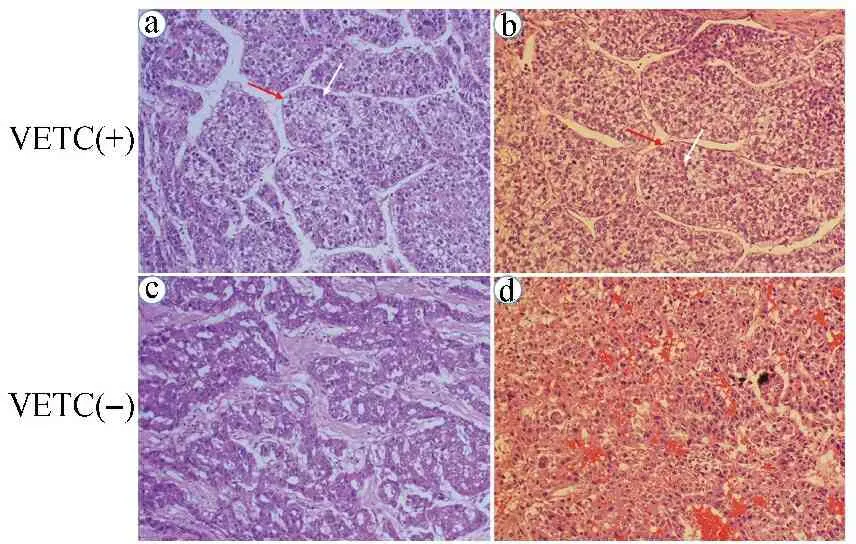
1.5统计学方法 应用SPSS18.0统计软件进行数据分析,计数资料以例数(百分率)[n(%)]表示,组间比较采用χ2检验。一致性分析采用Kappa检验,Kappa值>0.8表示一致性高,0.60 2.1164例HCC患者术后常规病理检查结果 164例HCC患者中,VETC癌巢型占40.24%(66/164),表现为球状血管内皮细胞包绕的HCC细胞团(见图1ⓐⓑ)。非癌巢型占59.76%(98/164),表现为内皮细胞未包绕HCC细胞,而仅形成传统的管状血管(见图1ⓒⓓ)。 ⓐⓑVETC癌巢型HCC CD34染色;ⓒⓓ非癌巢型HCC CD34染色。白箭头示VETC癌巢;红箭头示VETC癌巢间血流间隙;黑箭头示管状血管 2.2164例HCC患者术后标本CD34血管免疫组化检查结果 66例VETC癌巢型HCC患者中有30.30%(20/66)在癌旁组织中发现了癌巢(见图2ⓐⓑ)。98例非癌巢型HCC患者中仅10.20%(10/98)在癌旁组织中发现肿瘤细胞(见图2ⓒⓓ)。VETC癌巢型HCC患者癌旁转移率显著高于非癌巢型HCC患者(χ2=10.659,P=0.001),提示癌巢型HCC更易发生癌旁及远处转移。 ⓐⓑVETC癌巢型HCC及癌旁组织CD34血管染色;ⓒⓓ非癌巢型HCC及癌旁组织CD34血管染色。白箭头示癌旁癌巢;红色虚线示肿瘤边界 2.3164例HCC患者术后随访结果 经2年随访,VETC癌巢型HCC患者失访2例,死于其他疾病2例,肿瘤相关性死亡2例,纳入统计60例;非癌巢型HCC患者失访6例,死于其他疾病3例,肿瘤相关性死亡5例,纳入统计84例。VETC癌巢型HCC患者术后2年的复发率为53.33%(32/60),非癌巢型HCC患者术后2年的复发率为36.90%(31/84)。对于VETC癌巢型HCC患者,解剖性肝切除患者术后2年复发率显著低于非解剖性肝切除患者,差异有统计学意义(P<0.05)。见表1。 表1 VETC癌巢型HCC患者不同手术方式术后2年复发情况比较[n(%)] 2.4164例HCC患者术前超声造影检查与术后常规病理检查结果比较 以术后常规病理检查结果为金标准,术前超声造影诊断VETC癌巢型HCC的灵敏度为81.82%,特异度为91.84%,准确率为87.80%。Kappa一致性分析结果显示,术前超声造影检查与术后常规病理检查结果一致性较高(Kappa=0.744,P=0.000)。见表2。 表2 164例HCC患者术前超声造影检查与术后常规病理检查结果比较(n) 2.5164例HCC患者术中快速冰冻病理切片与术后常规病理检查结果比较 VETC癌巢型HCC术中冰冻病理表现为扁平细胞包绕的肝癌细胞团;非癌巢性HCC无扁平细胞包绕的肝癌细胞团(见图3)。以术后常规病理检查为金标准,术中快速冰冻病理切片诊断VETC癌巢型HCC的灵敏度为93.94%,特异度为91.84%,准确率为92.68%。Kappa一致性分析结果显示,术中快速冰冻病理切片结果与术后常规病理结果一致性高(Kappa=0.849,P=0.000)。见表3。 ⓐⓑVETC癌巢型HCC术中快速冰冻切片;ⓒⓓ非癌巢型HCC术中快速冰冻切片。红箭头示扁平细胞;白箭头示HCC细胞 表3 164例HCC患者术中快速冰冻病理切片与术后常规病理检查结果比较(n) 3.1本研究显示,术前超声造影检查和术中快速冰冻病理切片诊断VETC癌巢型HCC具有较高的灵敏度和特异度。超声造影是继实时二维超声、多普勒成像后超声领域的又一重大技术革命,随着超声造影剂的不断更新,其已经成为肝癌患者的重要影像学检查,与CT、MRI比较,具有操作方便、无辐射、费用低及可多次重复的优点[5,6]。本研究中超声造影诊断VETC癌巢型HCC的灵敏度为81.82%,特异度为91.84%,结果提示肝脏超声造影在肝癌精准分型中具有更加重要的意义。术中快速冰冻病理切片可在手术期间快速出片,是术中判断肝肿瘤良恶性的病理指标,课题组制定的VETC癌巢型肝癌冰冻切片诊断标准判断VETC癌巢型HCC,其灵敏度为93.94%,特异度为91.84%,可指导手术方式的选择,是对HE冰冻切片单纯诊断良恶性结果的进一步挖掘,达到更大限度为临床服务的目的[7]。 3.2VETC癌巢型HCC分型是以内皮细胞的形态学特点为基础的,既往认为内皮细胞的主要功能为形成血管,为肿瘤提供营养和氧气[8]。而深入的研究[9,10]认为内皮细胞可参与肿瘤多种功能的形成,包括通过自身收缩促进肿瘤转移,通过免疫抑制促进转移后肿瘤细胞的存活。内皮干细胞通过快速形成新生血管促进肿瘤转移等[9,11],而在VETC癌巢型HCC中,内皮细胞通过形成癌巢促进肿瘤转移,进一步丰富了内皮细胞的功能[4]。因有内皮细胞的包裹和保护,VETC癌巢型HCC更易发生癌旁转移及远处转移。 3.3HCC术后的复发转移严重影响了患者的预后,定期复查,对复发灶实现早发现、早治疗、早处理,是延长患者生存期及改善生活质量的关键[12]。VETC癌巢型HCC患者术后2年的复发率高达53.33%,而非癌巢型HCC患者术后2年的复发率为36.90%,提示癌巢型HCC患者术后需缩短复查间隔,尤其是术后2年内,建议每月复查超声,如有必要可追加CT和MRI检查[13,14]。 3.4本研究发现解剖性肝切除可有效降低VETC癌巢型HCC患者术后2年的复发率。术前或术中诊断患者是否为癌巢型HCC并行解剖性肝切除是降低此类患者复发的关键[3,14,15]。VETC癌巢型肝癌所在肝段的门脉小血管中可见大量由内皮细胞包裹的、整团的转移癌巢,且癌巢以团巢的形式侵入血管,其转移效率明显高于以单细胞转移为主的非癌巢型肝癌,这提示VETC癌巢型HCC行解剖性肝切除的必要性[16]。本研究制定的VETC癌巢型HCC术前超声造影、术中冰冻诊断标准,可有效对癌巢型HCC进行诊断。VETC癌巢型HCC对索拉菲尼、仑伐替尼等分子靶向药物敏感,对于不能手术的中晚期HCC患者,如超声造影提示为VETC癌巢型HCC,提示其为靶向药物的敏感人群,可考虑行药物靶向治疗,实现了对HCC人群的提前筛选,避免医疗资源的浪费,减轻患者负担,实现个体化诊疗[3,17]。 综上所述,依据术前超声造影、术中快速冰冻病理切片有助于VETC癌巢型HCC诊断,实现更加精细的分型,有利于个体化诊疗方案的选择,改善患者预后。2 结果



3 讨论
