基于配方均匀试验优化微弧氧化电解液浓度配比
2021-04-07杨登科马颖安凌云张睿峰吴雄飞孙乐王占营
杨登科,马颖,安凌云,张睿峰,吴雄飞,孙乐,王占营
(兰州理工大学 省部共建有色金属先进加工与再利用国家重点实验室,兰州 730050)
镁合金作为一种最轻的结构工程材料,具有较高的比强度、比刚度及良好的铸造性等各种优异性能,广泛应用于航空航天、军工及各类民用产品中[1]。然而,由于镁的标准电极电位极负,导致镁合金的耐蚀性极差,因此耐蚀性已成为严重制约镁合金发展的主要问题之一[2-4]。目前,提高镁合金耐蚀性的表面处理技术主要有化学氧化、阳极氧化、激光熔覆、气相沉积以及微弧氧化等[5-9]。微弧氧化技术由于工艺简单、无环境污染,日益受到研究者们的青睐,其主要是通过电化学、热化学、等离子化学等反应在基体金属表面原位生长陶瓷膜层[10-11]。近年来,关于微弧氧化的研究主要集中在专用工业电源的研发、电参数、处理时间、电解液对膜层的影响等方面[12-19],其中电解液成分在很大程度上决定了微弧氧化膜层的组成及性能。电解液领域的科研工作者大多数都在使用单因素法研究其成分对微弧氧化膜层微观结构及性能的影响[20-25],但电解液问题本身既属多因素影响的范畴,又需考虑不同成分电解质之间的配比,故而需要寻找针对性更强的实验设计方法。配方均匀试验方法是一种多因素的混料设计方法,适合解决试验因素间有比例搭配要求类型的问题,即遵循各因素的占比之和为100%的配方约束条件的基本要求。它利用均匀试验设计的优势,使试验点的分布更为均匀,加快寻找优化结果的收敛速度,提高优化结果的准确性。因此,本文基于配方均匀试验进行微弧氧化处理,研究电解液浓度配比对AM60B 镁合金微弧氧化膜微观组织和性能的影响,科学合理地对电解液配方进行优化,为微弧氧化技术在镁合金中的实际工业应用提供一定的实验数据和参考依据。
1 试验材料及研究方法
实验材料为AM60B 镁合金,其化学成分见表1。基体样品规格为30 mm×20 mm×10 mm。试样经过150#、400#、800#砂纸打磨后,用去离子水进行冲洗,最后吹干,用于下一步微弧氧化膜层的制备。电源设备为自制的双极性脉冲微弧氧化专用电源,其中以不锈钢片为阴极,基体样品作为阳极。电解液采用硅酸盐体系,并选择配方均匀试验设计方法[26],要求的配比如表2 所示。表2 中的每个数值代表某组分在相应配方中所占的比例,并且每个配方(A1—A13)必须遵循配方均匀试验的约束条件,即X1+X2+X3=1(其中,X1、X2、X3代表电解液中各组分的占比)。基于前期预研试验结果,当电解液总浓度过高时,试验均无法进行,故最终确定电解液的总质量浓度为40 g/L。选用恒压模式,终电压为400 V,频率为700 Hz,占空比为20%,氧化时间为15 min。在整个微弧氧化过程中,电解液温度通过冷却循环系统控制在20~30 ℃。

表1 AM60B 镁合金的名义化学成分Tab.1 Nominal chemical composition of AM60B magnesium alloy wt.%
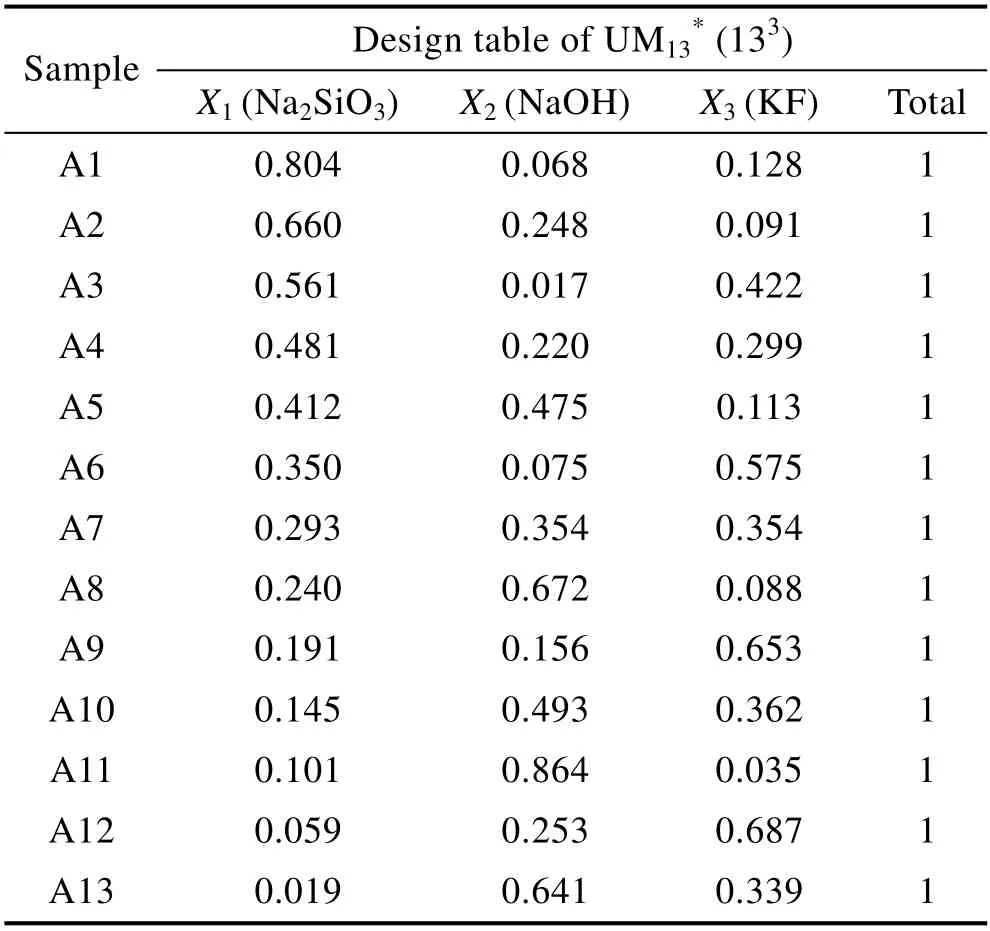
表2 配方均匀实验方案设计Tab.2 Formula uniform experimental design
使用SG-23 型多功能参数测试仪对各组电解液的电导率进行检测。采用TT260 数字式涡流测厚仪测量膜层厚度,每个试样选择20 个检测点,取其平均值作为膜层厚度。采用JSM-5600LV 型电子扫描显微镜(SEM)对膜层的微观形貌进行观察。采用EPMA-1600 型电子探针(EPMA)对膜层的截面元素分布进行检测分析。采用日本理学公司D/max-2400型X 射线衍射仪(XRD)对膜层的物相组成进行检测。
膜层的耐蚀性通过硝酸点滴实验、电化学实验进行检测,其中硝酸点滴实验参照HB 5061—77 进行,配方为90 mL/L 蒸馏水+10 mL/L(加倍)浓硝酸[27]+0.05 g/L 高锰酸钾。电化学实验采用辰华CHI660C 型电化学工作站进行测试,腐蚀介质为3.5%NaCl 溶液,以试样作为工作电极,其裸露面积为1 cm2,浸泡时间为30 min,饱和甘汞电极(SCE)为参比电极,铂电极为辅助电极,扫描速度为5 mV/s,扫描区间为–1.8~ –1.2 V。
需要说明的是,针对本实验设计的特性,本研究增加了2 个试验结果评价指标,即可行性和成膜性。前者是指微弧氧化反应的可行性,即在某浓度配比的电解液内,基体是否能够在规定的工艺条件下进行正常的微弧氧化反应,直观观察反应过程中试样是否出现局部烧蚀,电解液是否发生飞溅、沸腾等现象。利用微弧氧化反应的可行性这个评价指标,来判断某电解液配方的实际应用价值,其评定值规定为“1”(可行)和“0”(不可行)。后者是指在可行性为“1”的基础上,若基体表面所生成的膜层表观完整且色泽均匀,则规定其成膜性为“1”,否则为“0”,即利用微弧氧化膜层的成膜性,来评价在某个电解液配方下所制得膜层的合格程度。
2 结果及分析
2.1 配方均匀试验结果分析
表3 为配方均匀试验的检测结果。通过观察A1—A13 配方中微弧氧化的试验现象及膜层的外观质量可知,A1—A4、A6 和A9 配方中的微弧氧化过程正常,试样表面未出现局部烧蚀现象,氧化时间符合工艺条件,可达15 min,生成的微弧氧化膜层表面完整且光滑,色泽均匀;A5、A7、A8 和A10—A13 配方中的微弧氧化时间极短,约为2~3 min,试样表面出现局部烧蚀,并且随着氧化时间的延长,烧蚀现象愈加严重,试验无法继续进行而被迫提前结束。所以,A1—A4、A6 和A9 配方所对应的可行性、成膜性的等级评价均为“1”,A5、A7、A8 和A10—A13 配方所对应的可行性等级评价均为“0”。这说明在A1—A4、A6 和A9 配方中能够制备出完整且色泽均匀的微弧氧化膜层,具有一定的实际应用价值,其余配方下无法制备出完整的陶瓷膜层,无实际价值。另外,通过对表3 的直观分析可知,A9 配方中所制备的膜层最厚,A4 配方中所制备的膜层的点滴腐蚀时间最长,腐蚀电流密度最小,具有最佳的耐蚀性能。

表3 配方均匀试验结果Tab.3 Results of formula uniform experiments
图1 为电解液组成的直观分布。结合表3 可知,在总质量浓度为40 g/L 的硅酸盐电解液中,当NaOH的质量浓度小于10 g/L 时,电导率小于67.0 S/cm,在A1—A4、A6 和A9 配方(红色虚线右上侧区域内)的电解液内均可制备出完整且色泽均匀的微弧氧化膜层;当NaOH 的质量浓度超过10 g/L、电导率超过67.0 S/cm 时,即在A5、A7、A8 和A10—A13 配方(红色虚线左下侧区域内)的电解液内不能获得合格的膜层。以上结果表明,NaOH 对微弧氧化膜层的制备起决定性作用,这是因为NaOH 是决定电解液电导率的关键因素。随着NaOH 浓度的增大,溶液的电导率增大,离子迁移速率加快,溶液分压减小,试样表面分压增加,使得微弧氧化反应更加剧烈,溶液温度升高,放电火花变大。当试样表面分压远大于临界击穿电压时,放电火花彼此相连,持续时间较长,试样表面便呈现局部烧蚀的现象。另外,根据图1 中红色虚线的位置可以预判,当电解液中KF 的质量浓度接近30 g/L 时,微弧氧化反应也应该无法进行,而表3中A12 配方的情形印证了这一点。
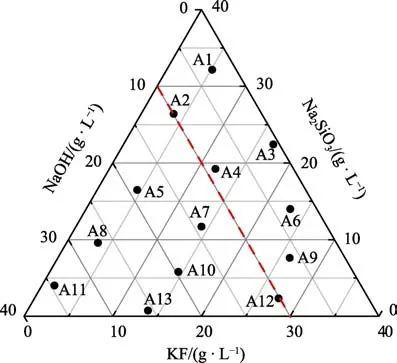
图1 电解液组成直观分布图Fig.1 Visual distribution of the electrolytes with different compositions
2.2 微弧氧化膜层的微观形貌

图2 不同配方微弧氧化膜层的表面形貌Fig.2 Surface morphologies of MAO coatings prepared with different electrolyte formulas of A1(a), A2(b), A3(c), A4(d), A6(e)and A9(f)
图2 为A1—A4、A6 和A9 配方中微弧氧化膜层的表面形貌。由图2 可知,不同配方制备的膜层表面呈现明显差异。当NaOH 和KF 的浓度都较低时,膜层表面光滑平整,微孔数量较少,孔径尺寸较小(如图2a)。当NaOH 的浓度再降低、KF 的浓度提高时,A3 膜层表面微孔数量多,孔径尺寸略大但分布不均(如图2c),若KF 的质量浓度再提高至23 g/L 时,A6 膜层表面呈现出熔融物质流动的痕迹,孔径尺寸两极分化严重,并具有明显的微裂纹(如图2e)。当KF 的浓度约为NaOH 的4 倍时,A9 膜层表面比较粗糙,微孔周围熔岩状凝固物凸起比较明显,呈圆饼状结构,同时有少量微裂纹和粉末状颗粒物存在(如图2f)。当NaOH 和KF 的配比相接近时,形成的A4 膜层表面微孔数量较多,微孔呈豆瓣状结构,出现大孔嵌套小孔的区域较多,这可以降低形成贯通孔的几率(如图2d)。当NaOH 的质量浓度达到可行范围的最高值(9.92 g/L)时,形成的A2 膜层表面大孔数量较多,孔径尺寸较大,最大孔径可达8 μm,并伴生有连续性微裂纹(如图2b)。由此可知,在微弧氧化过程中,随着NaOH 浓度的增加,溶液电导率增大,放电火花尺寸变大,数量减少,单个火花的放电能量增加,导致微孔数量减少,孔径变大,微裂纹出现。提高KF 的浓度可以减小微孔的尺寸,但过高也会使大孔产生,并增加微裂纹。微裂纹的形成是应力所致,即:一是放电通道能量过高(如高NaOH 的情形),瞬时热应力上升,由于熔融态氧化物受到电解液的快速冷淬,释放的热应力过大所造成的;二是膜层生长速度过快,导致机械应力产生,如KF 可以显著增加膜层的生长速率[23]。A9 膜层表面比较粗糙的状态表明,NaOH、KF 和Na2SiO3三者间还应具备适当的配比,A9 的情形与Na2SiO3浓度较低有关[28],而A4膜层的浓度配比及耐蚀性数据(如表3 所示)可以支持这一推断。
图3 为A1—A4、A6 和A9 配方中微弧氧化膜层的截面形貌。由图3 可知,A9 膜层最厚,为24.21 μm,但膜层整体最显疏松,膜层缺陷也最多(如图3f);A1 膜层最薄,厚度为8.82 μm,缺陷较少(如图3a);A4 膜层厚度为16.05 μm,缺陷最少,膜层最为致密(如图3d);其余配方下的膜层厚度相差不是很大,均存在不同程度的微孔(如图3b、图3c、图3e)。显然,KF 对膜层厚度的影响较大,NaOH 对膜层内部的大孔和微裂纹影响较大。适当配比的NaOH 与KF有利于提高膜层的致密度,减少膜层内部孔洞缺陷(如图3d)。而当NaOH、KF 和Na2SiO3三者间的配比失衡严重时,就出现了最为疏松的A9 膜层,其表面形貌(如图2f)也间接反映了这一点,并且从表3中可知,虽然A9 膜层最厚,但其硝酸点滴耐蚀性过低,这表明膜层的疏松结构削弱了抵挡腐蚀介质的能力。

图3 不同配方微弧氧化膜层的截面形貌Fig.3 Cross-sectional morphologies of MAO coatings prepared with different formulas of A1(a), A2(b), A3(c), A4(d), A6(e) and A9(f)
2.3 微弧氧化膜层的物相组成及元素分布
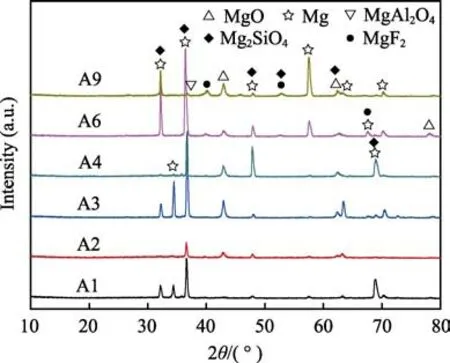
图4 不同配方中所制备的微弧氧化膜层的XRD 图谱Fig.4 XRD patterns of MAO coatings prepared with different formulas
图4 为A1—A4、A6 和A9 配方中微弧氧化膜层的XRD 图谱。由图4 可知,膜层主要由MgO、Mg2SiO4及少量的MgF2、MgAl2O4组成,同时还存在来自基体的Mg 衍射峰。究其原因,在微弧氧化过程中,溶液中的阴离子(SiO32–、OH–、F–)在强电场的作用下,进入放电通道,在通道内与熔融态的基体金属混合后发生一系列复杂的电化学、热化学以及等离子化学等反应,同时由于硅酸盐电解液中OH–的浓度较高,具有较强的选择吸附性,因而主成膜相为MgO和Mg2SiO4。其中,A4 膜层中Mg2SiO4的衍射峰相对较强,应是该配方中Na2SiO3、NaOH、KF 三者在合适配比下的交互作用会促进镁橄榄石Mg2SiO4生成,A4 膜层的高致密度也意味着更多的Mg2SiO4物相会沉积在膜层里,有利于增强膜层的耐蚀性。而A6、A9 膜层中包含MgF2略多是由所对应的配方中KF 浓度较高而造成的,同时根据文献[29]可知,少量MgF2的形成可能与Mg(OH)2、MgF2的溶度积Ksp有关。Mg 衍射峰的存在应该与微弧氧化膜层的疏松多孔有关,在A9 配方下获得的最疏松的膜层中出现较多的Mg 衍射峰就是典型的例证。
图5—7 为不同配方下所制备微弧氧化膜层的元素分布情况。由图5—7 可得,膜层主要由Mg、Al、O、Si、F 等元素组成。其中,Mg、Al 来源于AM60B镁合金基体,O、Si、F 来自于电解液,且Mg、Si、O 是膜层的主要组成元素,含量较高,F 元素的含量其次,而膜层中Al 元素的总体含量相对较低,这些现象在EPMA 面扫和线扫图上的表现是一致的。随着电解液中KF 浓度的增高,膜层中F 元素的含量也增加(如图7 中A6 和A9 的情形)。同样,随着电解液中Na2SiO3浓度的降低,膜层中Si 元素的含量减少(如图7 中A6 和A9 的情形),但并非在Na2SiO3浓度较高的A1 和A2 的情形下出现膜层中Si 元素含量也增加的状态,反而是在A3 和A4 的电解液配方下,膜层中Si 元素含量较高,这间接说明膜层中某种元素含量的高低,并非仅仅与电解液中包含此元素的电解质浓度呈正相关关系,而应该是各电解质之间有交互作用。结合图4 中XRD 的数据分析,A4 膜层中出现较强的Mg2SiO4衍射峰,就是该配方中Na2SiO3、NaOH、KF 三者在合适配比下发生交互作用的结果,又因A4 膜层的致密度高,也会使更多的Mg2SiO4物相沉积在膜层里,而较多镁橄榄石Mg2SiO4的存在,必然会对膜层耐蚀性的提高做出不可忽视的贡献。此外,从图4 中还可看出,仅在A9 配方下的膜层中出现少量MgAl2O4,可能意味着电解液中包含较少的时,基体中更多的Al 元素将会参与成膜反应。而图5—7 中的线扫数据表明,膜层中的Al 含量确实是随着浓度的减小呈现增加的趋势,且在Na2SiO3浓度最低的A9 配方下,膜层中Al 元素的含量最高。从图5—7 各膜层元素的分布图进一步可观察到,膜层中Si、O 元素的含量大体上呈现由膜层表面至基体方向逐渐减小的变化趋势,而F 元素的含量变化却与之相反。这表明在微弧氧化过程中,虽然溶液中的阴离子均参与膜层的形成,反应初期放电通道内的熔融态氧化物较少,所有阴离子均能够向内快速迁移和扩散,但由于离子半径不同[28],随着氧化时间的延长,放电通道内的熔融态氧化物增多,会阻碍半径较大的和OH–,使之迁移和扩散速率变慢,而F–凭借其较小的离子半径,以较大的迁移和扩散速率,优先吸附于膜基面,并与基体元素发生反应。因此,最终在膜层截面中Si、O 元素的含量变化与F元素的含量变化呈相反的趋势。
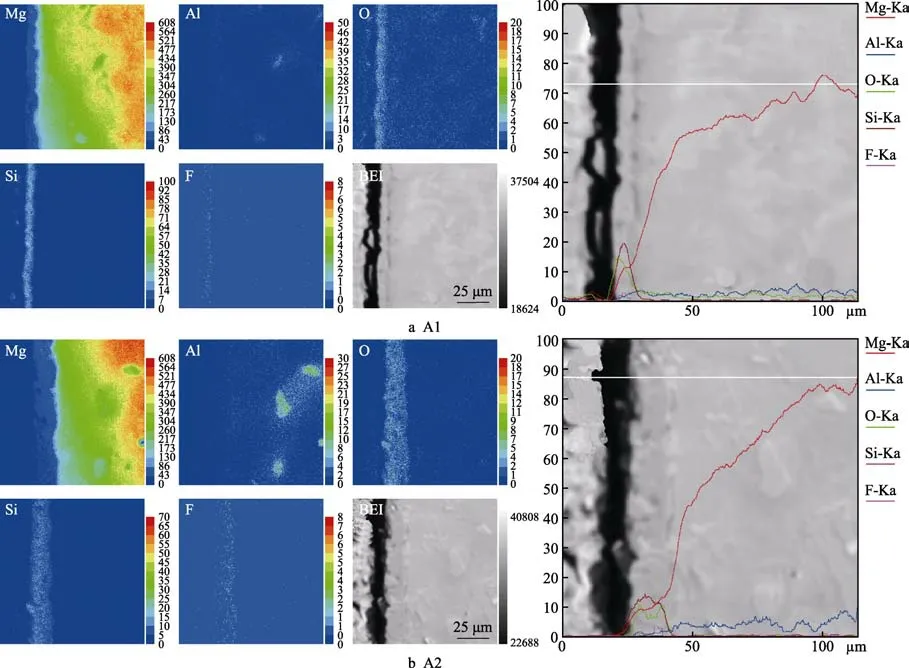
图5 A1、A2 膜层截面元素分布的EPMA 分析Fig.5 Elements distribution of cross-section of A1、A2 coatings by EPMA
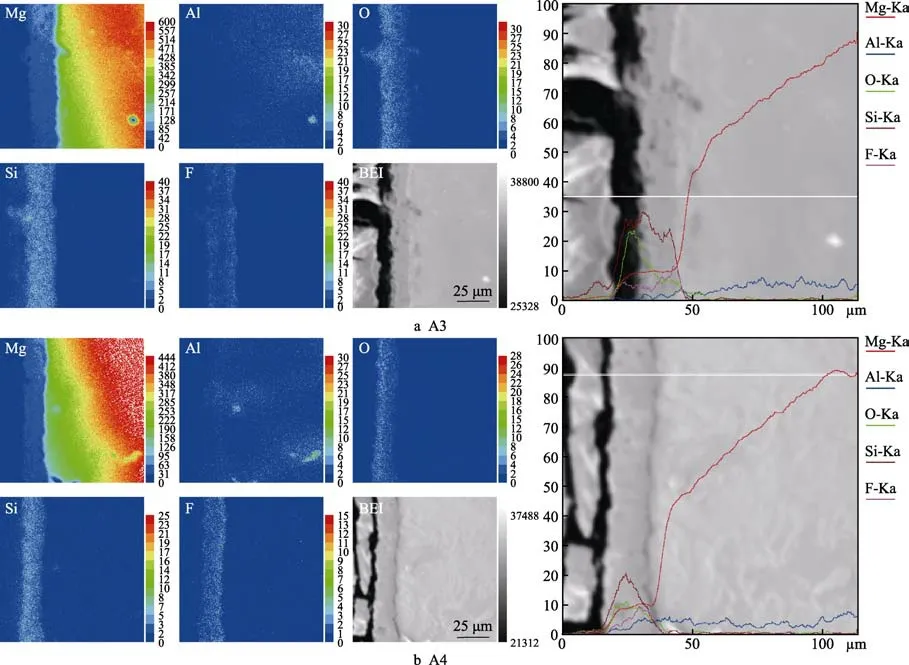
图6 A3、A4 膜层截面元素分布的EPMA 分析Fig.6 Elements distribution of cross-section of A3、A4 coatings by EPMA
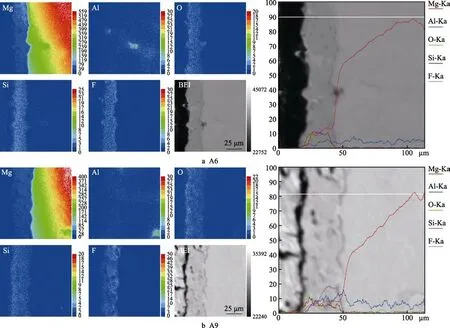
图7 A6、A9 膜层截面元素分布的EPMA 分析Fig.7 Elements distribution of cross-section of A6、A9 coatings by EPMA
2.4 微弧氧化膜层的耐蚀性
图8 为AM60B 镁合金基体与不同配方中微弧氧化膜层的点滴腐蚀时间。由图8 可知,与镁合金基体(A0)相比,经过微弧氧化处理后,试样的耐硝酸腐蚀能力明显增强。其中,A4 膜层的点滴完全腐蚀时间最长,可达156 s;A1 膜层的耐硝酸腐蚀时间最短,约为40 s;A9 膜层最厚但耐硝酸腐蚀时间较短,约为63 s;A2 膜层厚度虽小于A6 膜层,但其耐硝酸腐蚀能力却强于A6 膜层。这表明膜层的硝酸点滴耐蚀性受诸多因素的影响,如膜层厚度、膜层成分、致密度、微孔孔径等。同时,根据文献[30]的研究发现,膜层的硝酸点滴腐蚀呈现为以消耗性为主、渗透性为辅的均匀腐蚀特点,其耐蚀性主要与膜层厚度有关,如A1、A3 和A6 配方所对应的膜层,随着膜层厚度的增加,耐硝酸腐蚀能力随之增强。A4 膜层厚度居中但点滴耐蚀性最强,其主要原因为A4 膜层的致密度最高,膜层内部几乎无贯穿孔隙。A9 膜层最厚但其结构也最疏松,内部孔隙率最大,这是造成该膜层耐蚀性较差的主要原因。A2 和A6 膜层的厚度与硝酸点滴腐蚀时间未呈正相关,这应该与膜层的缺陷相关,从图3 中可观察到A2 膜层内部有延伸向膜基面的裂纹。
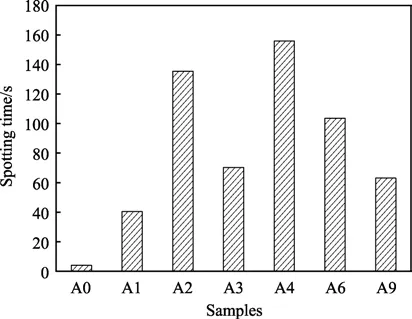
图8 AM60B 镁合金基体及其微弧氧化膜层的点滴腐蚀时间Fig.8 Corrosion resistance with spot test of AM60B matrix and its MAO coatings
图9 为AM60B 镁合金基体与不同配方中微弧氧化膜层的动电位极化曲线。结合动电位极化曲线拟合结果(表4)可知,经过微弧氧化处理后,试样的Jcorr比基体的降低了2~3 个数量级,表明经过氧化处理后试样的耐蚀性比基体有了显著提高。A4 膜层的Jcorr最小,Ecorr最正,呈现了最强的抗腐蚀能力和最弱的腐蚀倾向。这是因为微弧氧化膜层的电化学腐蚀呈现为以Cl–渗透为主的点腐蚀。腐蚀介质最早浸入膜层表面的微孔及微裂纹中,继而通过疏松层到达致密层,再渗透至膜层与基体的界面,与基体发生反应,导致基体的晶格发生畸变,从而使得膜层局部破裂凸起[31]。因此,膜层的电化学腐蚀性能受到膜层孔隙率、微孔孔径、微裂纹等这些膜层缺陷的影响更大。

图9 AM60B 镁合金基体及其微弧氧化膜层的动电位极化曲线Fig.9 Dynamic potential polarization curves of AM60B substrate and its MAO coatings
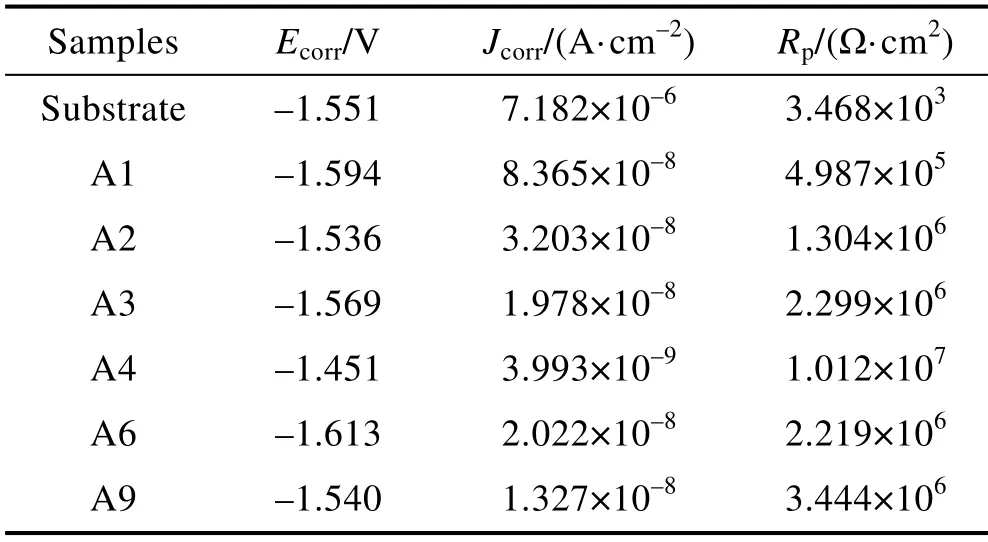
表4 基体及膜层的动电位极化曲线拟合结果Tab.4 Fitting results of dynamic potential polarization curves
综合上述两种情形下的数据分析,本实验A4 配方下所制备的膜层,在两种腐蚀介质中均呈现出较好的耐蚀性。
3 结论
1)本文实验设计方法的选择是保证研究结果有效性的核心和关键。
2)在电解液总质量浓度为40 g/L 时,若其中的NaOH 质量浓度超过10 g/L 时,微弧氧化反应将无法进行,而当NaOH 质量浓度小于10 g/L 时,便能获得表观完整且色泽均匀的微弧氧化膜层。
3)当NaOH 和KF 的配比相接近且两者之和约为Na2SiO3所占的比例时,膜层较厚,所含微孔孔径尺寸小,缺陷少,致密度高,膜层的耐蚀性更好。本实验中,A4 为最优配方,其组成为19.24 g/L Na2SiO3+8.80 g/L NaOH+11.96 g/L KF。
4)各电解液配方下所制得的膜层中包含的物相种类基本相同,主要由 MgO、Mg2SiO4及少量的MgF2、MgAl2O4组成,但其含量有所差别。A4 配方下的膜层中,镁橄榄石Mg2SiO4的含量相对较高,对膜层耐蚀性的提高也做出了不可忽视的贡献。
