某血液质控实验室参加CITIC血液成分细菌检测室间质评结果分析
2021-04-06樊璐
樊璐
(江西省血液中心,江西 南昌 330052)
输血传播性疾病(TTI)包括输血传播病毒感染(TTVI)、输血传播细菌感染(TTBI)、输血传播病原虫感染(TTPI)。血液制品细菌污染可导致TTBI,引发患者输血不良反应甚至死亡等严重后果,是输血安全领域的重要问题。《全血及成分血质量监测指南》[1]规定无菌试验是全血及各类成分血须开展的血液质量控制检查项目,血液制品质量抽检无菌试验符合性目标为符合率100%。针对采供血机构工作需求,自2013年起中国国际输血感染预防和控制(China International Transfusion Infection Control,CITIC)项目组建立血液成分细菌检测能力验证项目[2],客观评估参评实验室对血液成分中细菌的检测能力。本血液质控实验室于2015年起参加该项质评。现对近3年本室参评结果进行分析总结,报告如下。
1 材料与方法
1.1 样品来源 2019年3月至2021年6月CITIC项目组邮寄的细菌检测室间质量评价样品,由上海市血液中心质量与法规部质控科制备,样品批号为2019-04-17、2019-07-17、2019-10-23、2020-04-22、2020-07-15、2021-04-16、2021-07-14。质评项目代码BTBS4310。每次质评活动常温运输发放冻干状态样品10支,细菌阳性样品由商品化的标准菌株(生物梅里埃公司)经连续稀释而来,阴性样品采用无菌无热原的小牛血清。复溶用无菌检测用水、无菌生理盐水随同样品发放。本实验室检验人员接收质评物时进行外观检查,查看样品、试剂均无破损、无污染,核对数量无误,放置于2~8℃冰箱保存并尽快接种。
1.2 仪器与试剂 仪器设备:BacT/ALERT 3D全自动细菌/分枝杆菌培养监测系统(生物梅里埃公司)、洁净度百级净化工作台(上海跃进医疗器械有限公司),仪器设备每年定期校准检定。试剂:需氧培养瓶BPA(生物梅里埃公司)、无菌检测用水、无菌生理盐水(0.9%氯化钠溶液)、5 ml/10 ml一次性使用无菌注射器、安尔碘消毒剂、医用棉签。
1.3 方法
1.3.1 检测方法 室间质评样品及配套试剂通过实验室内部传递窗传送至净化室,在净化台中进行无菌操作。使用医用棉签蘸取安尔碘消毒剂擦拭样品瓶和配套试剂外表面,消毒样品瓶胶垫上的进针部位。用注射器吸取2 ml无菌检测用水注入样品瓶复溶冻干粉,放置至充分溶解后,再加入2 ml生理盐水混匀。每支样品接种需氧培养瓶1瓶。接种后的需氧培养瓶在0.5 h内加载至实验室日常使用的微生物培养系统,37℃孵育7 d。
1.3.2 结果判定 培养过程中,若培养仪发出反应性信号,查看仪器中相应培养瓶的细菌生长曲线,记录报阳时间。培养结束后,观察阳性培养瓶浑浊、底部变色情况。连续监测7 d未产生反应性信号的培养瓶判为阴性。
1.4 统计分析 血液筛查细菌检测为定性检测。根据CITIC项目秘书处历次发布的《血液成分细菌检测室间质评结果报告》,将本室定性检测结果与样品阴性/阳性参考结果相比较,将本室阳性样品检出时间与相同检测系统参评实验室的检测时间均值及标准差(SD)进行比对。检测结果符合率=总检测数中符合参考结果数/总检测数×100%。阳性样品检出时间的标准差指数(SDI)值=(x-x)/SD,x为本室检出时间,x为具备相同检测系统(BioMerieux BacT/ALERT BPA)参评实验室的平均检出时间。
2 结果
2.1 2019年第1次参加CITIC细菌检测室间质评结果 本室9份室间质评样品检测结果与参考结果一致,样品F出现假阳性结果,检测结果符合率90%。见表1。
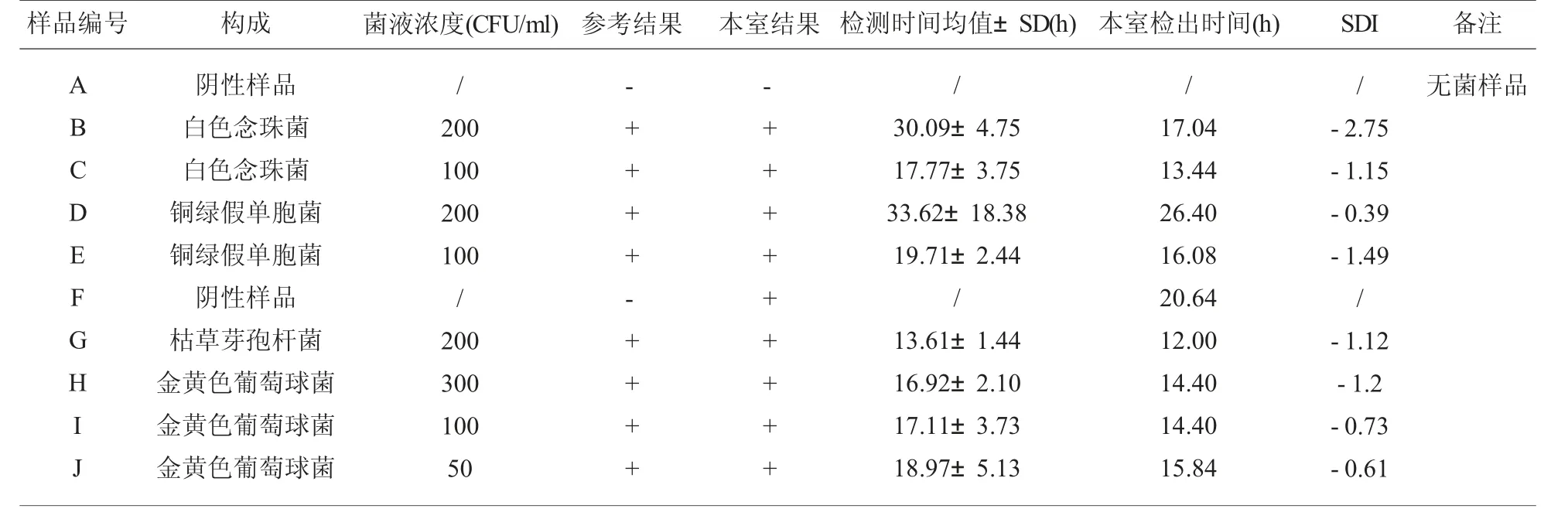
表1 2019年第1次参加CITIC细菌检测室间质评结果
2.2 2019年第2次参加CITIC细菌检测室间质评结果 本室10份室间质评样品检测结果与参考结果一致,检测结果符合率100%。见表2。
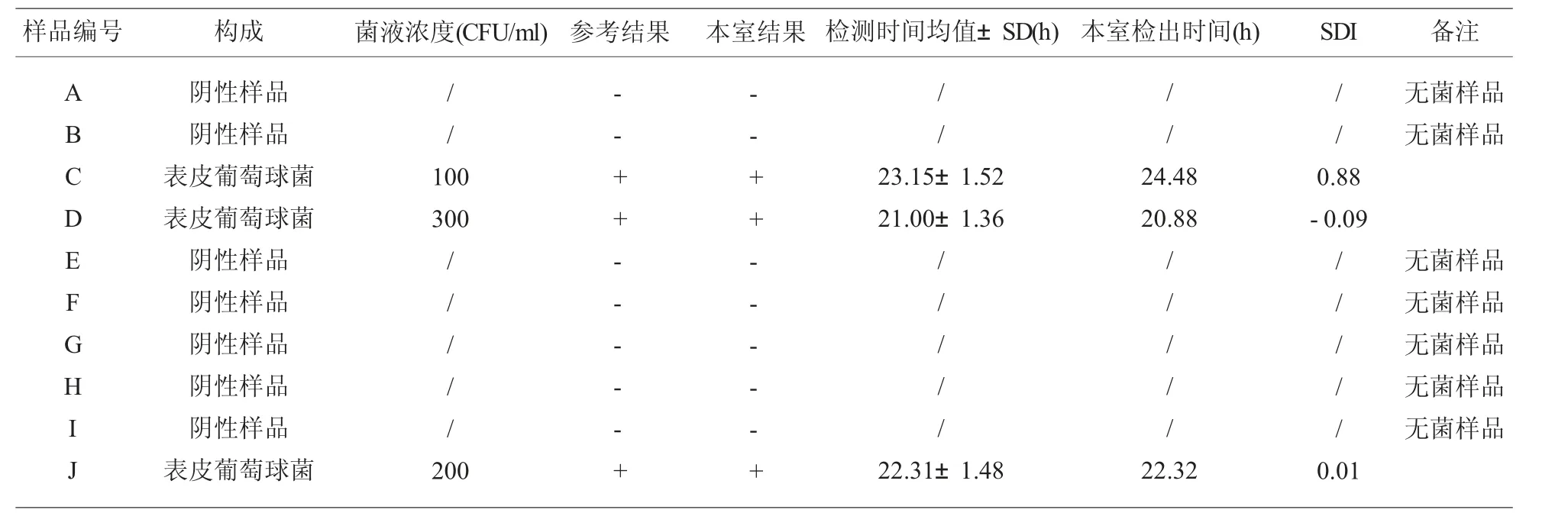
表2 2019年第2次参加CITIC细菌检测室间质评结果
2.3 2019年第3次参加CITIC细菌检测室间质评结果 除样品D和E被CITIC项目组撤回,不作分析评价,检测结果符合率100%。见表3。
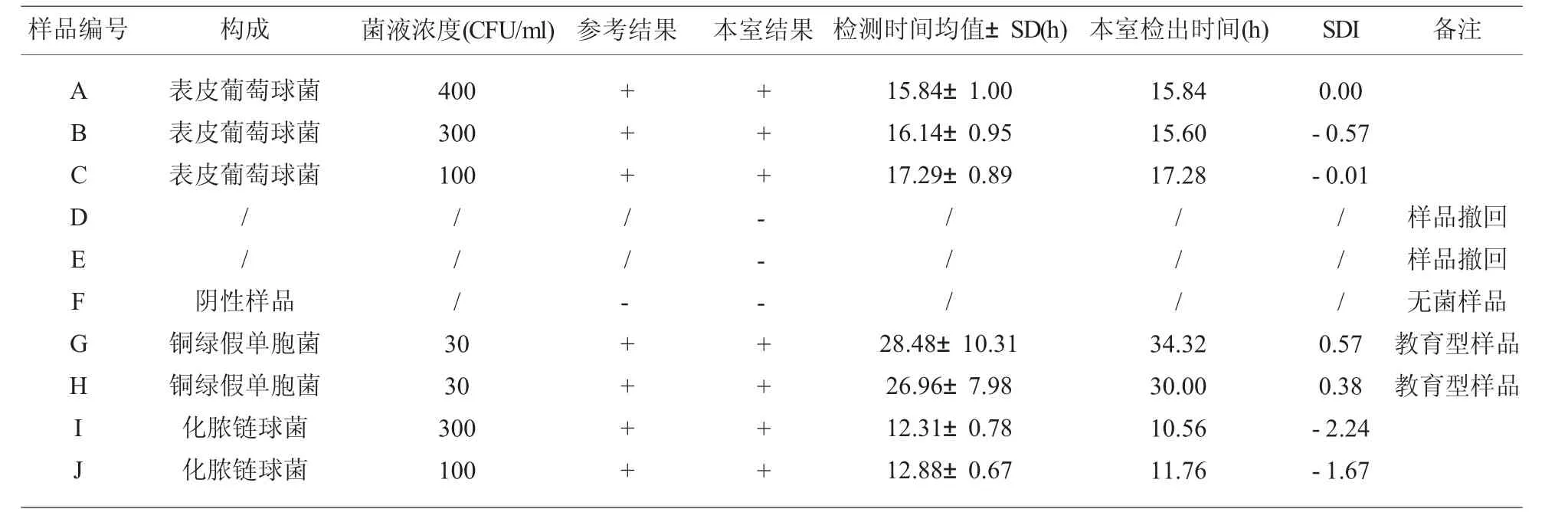
表3 2019年第3次参加CITIC细菌检测室间质评结果
2.4 2020年第1次参加CITIC细菌检测室间质评结果 除样品A和E因设备故障未完成培养,无法给出结果,CITIC项目组已将本室从样品A和E的统计分析中去除,检测结果符合率100%。见表4。

表4 2020年第1次参加CITIC细菌检测室间质评结果
2.5 2020年第2次参加CITIC细菌检测室间质评结果 教育型样品E菌液浓度较低,本室未检出,检测结果符合率90%。见表5。

表5 2020年第2次参加CITIC细菌检测室间质评结果
2.6 2021年第1次参加CITIC细菌检测室间质评结果 教育型样品E菌液浓度较低,本室未检出,检测结果符合率90%。见表6。

表6 2021年第1次参加CITIC细菌检测室间质评结果
2.7 2021年第2次参加CITIC细菌检测室间质评结果 样品H出现假阴性结果,检测结果符合率90%。见表7。
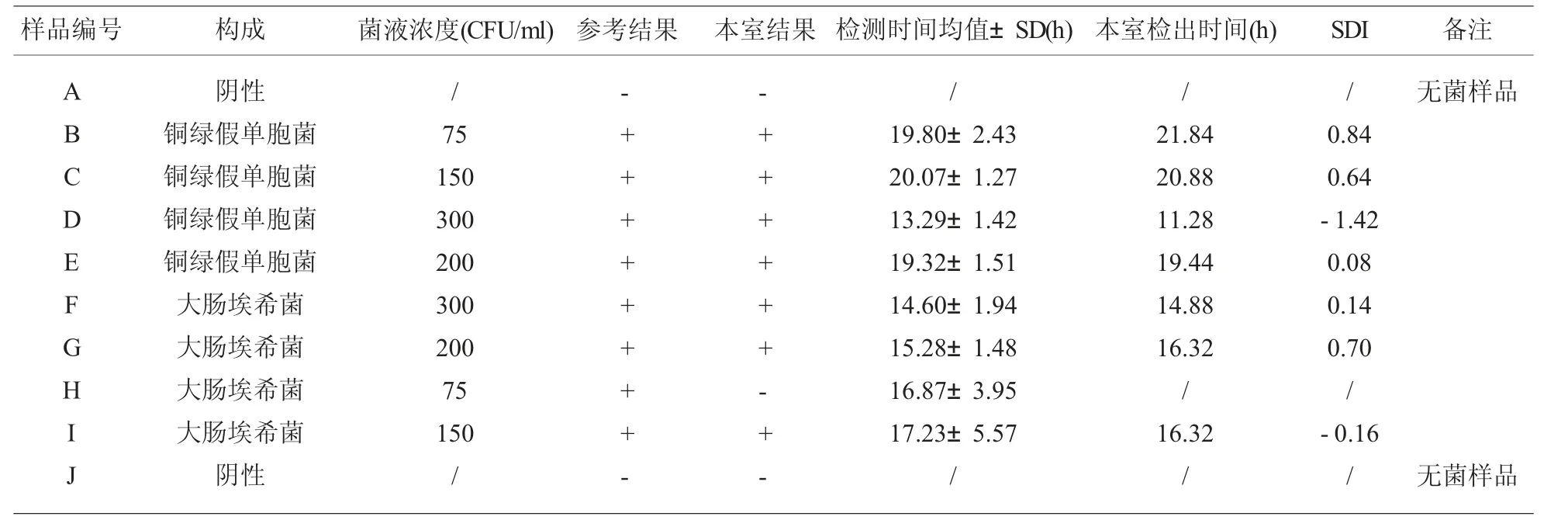
表7 2021年第2次参加CITIC细菌检测室间质评结果
2.8 阴性/阳性符合率 2019年3月至2021年7月本室检测CITIC血液成分细菌检测室间质评样品的阴性符合率为94.12%(16/17);阳性符合率为93.88%(46/49),其中教育型样品未检出2例。
2.9 阳性样品检出时间的标准差指数评价 2019年3月至2021年7月本室检出CITIC血液成分细菌检测室间质评阳性样品46份,阳性样品细菌检出时间优良率91.30%(42/46);2020年第1次质评教育型样品J本室检出时间(22.32 h)显著低于参评实验室平均检出时间(75.32h),SDI<-3。见表8。
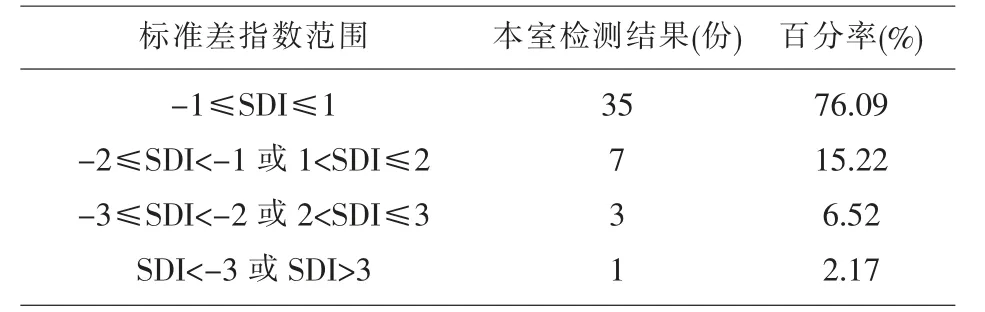
表8 46份阳性样品细菌检出时间SDI值分布情况
3 讨论
血液成分的细菌污染是输血后感染的主要风险之一,尤其是单采血小板保存温度为20~24℃,为细菌生长提供有利条件。细菌污染及脓毒性输血反应是血小板输注面临的重要风险[3]。何华庆等[4]报道血小板细菌筛检可有效预防和控制血小板制品细菌污染。《中国药典》[5]规定作为验证无菌检查所用培养基灵敏度的标准菌种包含白色念珠菌、铜绿假单胞菌、金黄色葡萄球菌、黑曲霉、枯草芽孢杆菌等。CITIC项目组样本设计方案对菌种选择、浓度匹配均有考量。选取上述代表性菌种作为血液成分细菌检测室间质评样品的标准菌种,能够有效监测采供血机构全自动微生物检测系统性能。
2019年第1次室间质评本室出现1例样品F假阳性检测结果,本次质评样品A和F为同一批制备的无菌样品,样品A本室检测为阴性。无菌样品F假阳性原因推测是接种过程中发生交叉污染。邱颖婕等[2]经研究提示操作人员应注意在接种时勿将标本液体打向空气中或残留于接种环境,尤其是残留在操作人员手部,以避免交叉污染造成假阳性结果。
2020年第2次、2021年第1次室间质评本室未检出浓度20CFU/ml白色念珠菌、30 CFU/ml表皮葡萄球菌教育型样品。此2次质评活动中,BioMerieux BacT/ALERT BPA检测系统参评实验室对于教育型样品的检测结果符合率分别为56.76%(21/37)、76.32%(29/38),出现不同程度漏检。参评实验室对低浓度的微生物样品检出能力存在一定差异,CITIC项目组不予评价教育型样品检测结果。教育型样品浓度接近检测范围下限,对监测系统设备和检测系统的性能要求更加严格[6]。徐蓓等[7]报道BacT/ALERT 3D和BD系列检测系统较Thermo REDOX 1系统发生不符合结果的比例小。许清[8]报道不同检测系统对不同菌种的检测能力有所差异,BacT/ALERT 3D系统对于某些品种的教育型样品检出率偏低。
2021年第2次室间质评本室出现1例样品H假阴性结果,相同检测系统参评实验室对此份样品的检测结果符合率为70.27%(26/37)。本室查找检测和样品保存过程中存在的异常情况,分析原因如下:⑴在抽取样品H菌液的实验过程中,样品瓶中负压较大,反复吸样操作使注射器中的菌液重返样品瓶中,生成大量气泡,导致接种吸取量不足。⑵朱立苇等[9]报道保存运输不当会造成室间质评样品中部分细菌死亡。此次质评时间为夏季,样品在室外高温环境下保存运输数天,可能发生细菌活性降低、细菌死亡现象。CITIC项目组提示冻干状态样品检测前的复溶过程很重要,注入复溶液后,放置数分钟至冻干粉完全溶解,避免气泡产生,再加入稀释液,充分混匀后接种。为确保阳性样品检出率,接种时应将样品液体全部注入培养瓶。
从质评阳性样品反应性信号出现的时间分析,超过90%检测值处于参考检测时间均值±2SD范围之内,表明本室检测系统受控。2020年第1次室间质评教育型样品J(20CFU/ml黑曲霉菌)是低浓度的真菌样品,全国参评实验室样品J中微生物的平均检出时间延长、变异较大,本室检出时间显著低于相同检测系统平均检出时间。此份样品本室检测结果与朱立苇等[9]报道其实验室2013年第2次室间质评样品B(50CFU/ml黑曲霉菌)的检出时间(19.8 h)比平均检出时间(53.1 h)明显偏短的情况相似,推测可能与样品中微生物的活性或浓度的均匀性相关。
2020年第1次室间质评本室有2份样品因设备发生电路故障未完成培养,提示我们设备硬件和软件的定期维护保养十分必要。CITIC血液成分细菌检测室间质评项目是实验室评估自身检测能力的方式之一,通过检测结果比对,了解参评实验室之间、不同检测系统之间的水平差异,从而持续监控和改进实验室检测水平[7]。本质控实验室细菌检测水平达标,满足日常血液成分无菌试验工作需求,对于低浓度细菌教育型样品的检出能力有待进一步提升。通过分析不符合结果产生的原因,总结经验、发现不足,进而采取改进措施,提高检测能力。采供血机构应加强“人、机、料、法、环、测”血站实验室管理要素[10]监控,确保质量管理体系有效运行,保障血液制品临床输注安全。
