miR-588表达水平与乳腺癌化疗疗效的关联研究
2021-04-06朱晓静栾文强董利王聪
朱晓静,栾文强,董利,王聪
(濮阳市人民医院肿瘤一科,河南 濮阳 457000)
乳腺癌是常见的女性恶性肿瘤,是威胁女性健康的重大疾病之一。化疗是乳腺癌常见的治疗方式,提高乳腺癌化疗疗效一直是临床治疗的重点和难点[1]。MicroRNA(miRNA)通过碱基与mRNA特异性结合,调节mRNA的降解以及蛋白质的表达[2],更重要的是对致癌基因、抑癌基因也具有一定联系,同时miRNA的表达水平对化疗药物的敏感度也有一定影响[3-4]。microRNA-588(miR-588)是乳腺癌相关的miRNA,但是临床中关于miR-588水平与乳腺癌化疗疗效的研究较少。本研究对126例乳腺癌患者的疗效以及miR-588表达水平进行比较分析,了解miR-588对化疗疗效的影响,以为临床提供参考。
1 对象与方法
1.1 研究对象 选取2019年3月至2021年1月在本院接受乳腺癌化疗患者126例,根据患者的疗效分为两组,显效组(87例)和无效组(39例)。收集两组患者临床就诊资料,进行回顾性分析。
1.2 纳入和排除标准 纳入标准:⑴患者为首次接受乳腺癌化疗治疗;⑵患者乳腺癌病理分期为Ⅰ~Ⅲ期;⑶患者或其家属对此次研究的内容和方法知情,并已签署知情同意书。
排除标准:⑴患者合并有其他恶性肿瘤;⑵患者合并有免疫系统疾病;⑶患者患有严重凝血疾病、神经系统或其他重要器官衰竭症。
1.3 方法
1.3.1 根据所有患者的就诊记录,统计等级其年龄、身体质量指数(Body mass index,BMI)、肿瘤直径、肿瘤类型、临床病理分期,有无吸烟、饮酒史、化疗方案。
1.3.2 分组标准 所有患者化疗结束后,根据实体瘤疗效评价标准 (Response Evaluation Criteria in Solid Tumors,RECIST)[5]对两组患者的近期疗效进行评估。完全缓解(Complete remission,CR):肿瘤体积肉眼完全消失持续1个月以上;部分缓解(Partial response,PR):肿瘤大直径*最大垂直直径减小50%以上,且无新发病灶,持续至少1个月;肿瘤稳定(Stable disease,SD):病灶最大双径乘积增大范围小于25%,同时减小不超过50%,,无新发病灶,持续至少1个月;肿瘤进展(Progression disease,PD):病灶最大双径乘积增大超过25%,并伴随新病灶出现。CR、PR纳入显效组,SD、PD纳入无效组。
1.3.3 miR-588表达检测:取患者乳腺癌组织以及距离肿瘤边缘5 cm的正常组织,采用RNA提取试剂盒(苏州阿尔法生物实验器材有限公司)、反转录试剂盒(上海翊圣生物科技有限公司)进行总RNA提取、逆转录合成cDNA后,在荧光定量仪中进行实时荧光定量PCR (Quantitative Real-time PCR)扩增。扩增条件:95℃预变性3min,95℃变性12 s、62℃退火40 s,共进行40个循环,最后表达量采用2-△△Ct法进行检测,内参照为U6。miR-588正向引物:CGTAGCTTCAGCTAGCCTC;反向引物:CCTTCATCACGCAGCGCA。U6正向引物:GGCATCGATCAGCTAGC;反向引物:TCGATCGGATCAGTAAGTTAGC。
1.3.4 血清指标检测 抽取患者外周静脉血5.0 ml,,经离心、抽取上层清液、冷置于后采用全自动生化分析仪检测其半乳糖凝集素-9(Galectin,Gal-9)、肿瘤坏死因子-α(Tumor necrosis factor,TNF-ɑ)血清浓度,分别采用卡迈舒(上海)生物科技有限公司Gal-9检测(双抗体夹心ABC-ELISA)试剂盒、武汉菲恩生物科技有限公司TNF-ɑ检测(ELISA)试剂盒。
1.4 统计学分析 采用SPSS20.0软件处理数据。计数资料以n(%)表示,行χ2检验;计量资料以(±s)表示,两组间行独立t检验。miR-588表达水平、血清Gal-9、TNF--α水平与化疗疗效的相关性采用Kendall相关性分析,对乳腺癌患者化疗疗效的预测价值采用受试者工作特征曲线(The receiver operating characteristic curve,ROC)分析。检验水准为α=0.05。
2 结果
2.1 乳腺癌患者化疗疗效情况 本研究纳入的126例乳腺癌患者,经4个化疗疗效后,CR患者30例、PR患者57例、SD患者29例、PD患者10例,因此无效组39共例、显效组患者87例。其中无效组患者的乳腺癌患者癌症组织中miR-588的相对表达水平为2.89±0.24,癌旁正常组织为5.39±0.49,显效组患者为3.70±0.51,三者间差异有统计学意义(t=312.246,P<0.001)。
2.2 两组患者基线资料以及相关指标对比 无效组患者的病变组织miR-588表达水平以及血清Gal-9浓度低于显效组(P<0.05),TNF--α血清水平高于显效组(P<0.05)。见表1。
表1 两组患者基线资料以及相关指标对比[n/(%),±s]

表1 两组患者基线资料以及相关指标对比[n/(%),±s]
?
2.3 Kendall相关性分析 Kendall分析显示,肿瘤组织中miR-588表达水平以及血清Gal-9均与化疗疗效为正相关关系(P<0.05),TNF--α浓度为负相关关系(P<0.05)。见表2。

表2 乳腺癌化疗患者相关参数的Kendall分析
2.4 相关指标预测乳腺癌患者化疗疗效的ROC分析ROC分析显示,肿瘤组织中miR-588表达水平、Gal-9、TNF--α均具有一定的化疗疗效预测价值(P<0.05),其中miR-588表达水平>3.626、血清Gal-9浓度>18.372 ng/L或TNF--α<29.250 ng/L的患者,化疗疗效更佳。见表3、图1。

图1 相关指标预测乳腺癌患者化疗疗效的ROC曲线
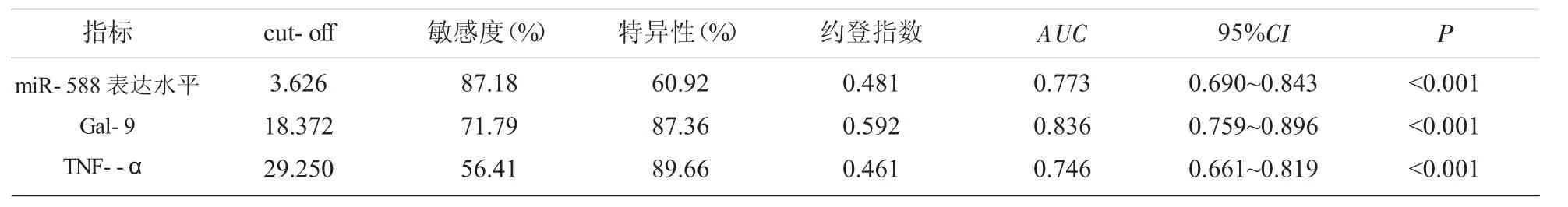
表3 相关指标预测乳腺癌患者化疗疗效的ROC分析
3 讨论
miRNA在细胞内具有多种调节作用,参与分化、发育、组织生长等多种生理过程。哺乳动物70%的miRNA是位于TUs区,不仅在基因位置上保守,序列上也呈现出高度的同源性[6-8]。研究表明,miR-588的表达水平与癌症组织的迁移过程有关,通过了解乳腺癌患者组织中miR-588的表达差异与化疗疗效的影响[9],对于控制乳腺癌发展具有重要意义。
本研究结果显示,乳腺癌患者癌症组织中miR-588相对表达水平显著低于癌旁正常组织。这可能是因为miR-588可靶向调控畸胎瘤细胞源性生长因子—颗粒体蛋白(Granulin,GRN)转化过程,从而抑制恶性肿瘤细胞的生长和转移。陶爽等人[10]的研究中也指出,miR-588在乳腺癌肿瘤细胞中的表达水平低于癌旁正常组织,且过表达会抑制肿瘤细胞的增殖。本研究结果还显示,无效组乳腺癌患者病变组织中miR-588表达水平低于显效组,Kendall分析显示miR-588表达水平与化疗效果具有一定相关性,说明miR-588表达不仅与乳腺癌的发生有关,同时还影响患者的化疗疗效。乳腺癌终末期通常伴有远处转移,威胁患者生命,而乳腺癌上皮间质转化是其肿瘤转移密切相关。miR-588可与靶基因酸腺苷结合转运蛋白G超家族成员2(Adenosine triphosphate binding cassette superfamily G member 2,ABCG2)的3’UTR的非翻译区结合,可介导其转录和修饰[11-12],ABCG2是跨膜运转蛋白,可促使肿瘤上皮间质转化,降低上皮细胞间的黏附能力,给予肿瘤细胞更大的活动、侵袭能力[13],因此miR-588参与肿瘤细胞的凋亡、转移过程,与乳腺癌疗效、肿瘤转移密切相关。陈元元等人[14]的研究中指出,GRN为miR-588的下游通路,miR-588高表达可降低GRN水平,从而实现抑制乳腺癌肿瘤细胞迁移、侵袭,本研究结果与其一致。
在Yu Miao等人[15]关于miR-588的研究中指出,miR-588下调会降低乳腺癌患者在接受顺铂化疗后的敏感性,其发生预后不良、淋巴转移、雌激素受体功能损害发生率升高;且miR-588低表达患者的生存期更短。此外,He C等人[16]也表示,SNHG8在前列腺、乳腺癌、肿瘤癌等多种癌症中充当癌基因,可促进癌细胞的增殖和发展,而miR-588/ATG7与小核仁RNA宿主基因8对肿瘤细胞的自噬作用有密切关系。本研究结果还显示,Gal-9也与乳腺癌化疗疗效具有一定相关性,这是因为Gal-9作为凝集素成员,与肿瘤、免疫信号的传导有密切关系。与T细胞黏蛋白-3结合后可诱导免疫耐受,促使T细胞免疫系统的激活,细胞凋亡从而提高化疗效果。TNF-α在ROC分析中的敏感度较低,同时TNF-α受多种感染性疾病等因素的影响,因此并不具有代表性。
综上所述,miR-588在乳腺癌肿瘤细胞中的表达水平高于正常组织,同时miR-588水平高表达也是乳腺癌患者化疗效果显著的保护因子。临床中可根据患者miR-588组织表达水平以预测化疗效果,可为临床乳腺癌化疗计划的制订提供参考。
