浓度梯度型锂离子电池富镍氧化物正极材料
2021-03-30张珊王珊陈卫晓高鹏朱永明
张珊,王珊,陈卫晓,高鹏,朱永明,2
(1 哈尔滨工业大学(威海)应用化学系,山东威海264209;2 松山湖材料实验室,广东东莞523808)
锂离子电池(LIBs)自1991年问世到现在经历了二十多年的发展,已经在便携式电子产品中得到了广泛的应用,在商业化上所取得的成功是任何一种二次电池无法比拟的。锂离子电池具有比能量高、质量轻、循环寿命长等优点,在纯电力汽车(EVs)、混合动力汽车(HEVs)和插电式汽车(PHEVs)中极具应用潜能[1]。其中提高能量密度和安全性是锂离子电池在汽车商业化应用中的关键,而这些性能在很大程度上取决于电极活性材料,特别是正极材料[2-4]。近年来,富镍三元氧化物正极材料LiNixCoyM1-x-yO2(M=Mn、Al,x≥0.6)由于具有高比容量、低成本、环保和无需高电压电解质等优点,受到越来越多的关注[5]。其中,LiNi0.8Co0.15Al0.05O2(NCA)和LiNi0.8Co0.1Mn0.1O2(NCM811) 被认为是最有前途的材料[6]。但是,三元材料中镍含量增高,会产生Li/Ni 阳离子混排、表面反应和导致结构不稳定的裂纹扩展等缺点,导致富镍正极材料的循环寿命差、热稳定性差[7-9]。三元材料中的镍含量越高,材料的稳定性越差,安全性也越差,尤其是材料表面与电解液接触时,表面镍含量的高低直接影响着材料的性能。由于Ni 含量增高导致高镍三元材料的表面呈碱性,因此易与空气中的CO2和水分反应生成LiCO3和LiOH,或与电解液反应生成HF 等副反应产物,从而导致其不易储存、电池性能不稳定及不利于商业化生产等诸多问题。针对这些问题,研究者通常的解决办法是进行材料改性,例如离子掺杂和表面包覆等。此外,有研究者发现,通过材料的结构设计,比如采用单晶结构、核-壳结构和浓度梯度结构,也能够有效地改善富镍三元正极材料的电化学性能,尤其是浓度梯度材料,为近年来广受关注的结构改性方法。本文将对以上改性手段进行介绍,重点对浓度梯度结构富镍正极材料的制备与应用进行分析。
1 掺杂与包覆改性
1.1 掺杂改性
研究表明,富镍正极在充电过程中由于各向异性的体积变化会产生微裂纹,这些微裂纹损害了正极的力学稳定性,并加剧了电解液腐蚀引起的化学降解[10-12]。当镍含量>0.85 时,微裂纹实际上是NCM 正极容量衰减的主要因素,随着镍含量接近1.0 时,微裂纹变得越来越严重。这种高荷电状态下固有的结构不稳定性无法避免,但可以通过合理布置一次粒子来减轻这种影响[13]。
通过在三元材料晶格中掺杂一些金属离子和非金属离子不仅可以提高电子电导率、离子电导率,而且可以提高三元材料结构的稳定性。可供掺杂的离 子 种 类 很 多,如Sn4+[14]、Mg2+[15]、Al3+[15]、Nb5+[16]、Zr4+[17]、Mo6+[18]等,离子掺杂被证明可以减少Li/Ni阳离子的混排并稳定层状结构,其掺杂方式及效果总结见表1。
通过改变表面能可以在锂化过程中调控一次粒子的定向生长,以实现微观结构的改变。在这方面,硼是较好的掺杂材料,因为它可以比较容易地掺入到晶格中。摩尔分数低至1%的硼掺杂会改变表面能,从而产生高度织构的微观结构,可以部分缓解Li[Ni0.90Co0.05Mn0.05]O2深充过程中产生的固有内部应变[13]。因此,摩尔分数为1%硼掺杂的B-Li[Ni0.90Co0.05Mn0.05]O2正极在4.3V 时放电容量可达237mA·h/g。在55℃下,100 个循环后仍具有91%的容量保持率,比未掺杂的Li[Ni0.90Co0.05Mn0.05]O2高15%。该合成策略证明了循环稳定性不佳的富镍Li[Ni1-x-yCoxMny]O2正极存在延长循环寿命的改性微观结构,并且通过表面能改性可以获得最佳的微观结构。但是随着硼掺杂水平的提高,正极的电子电导率逐渐降低,进而导致正极的倍率性能略有下降。
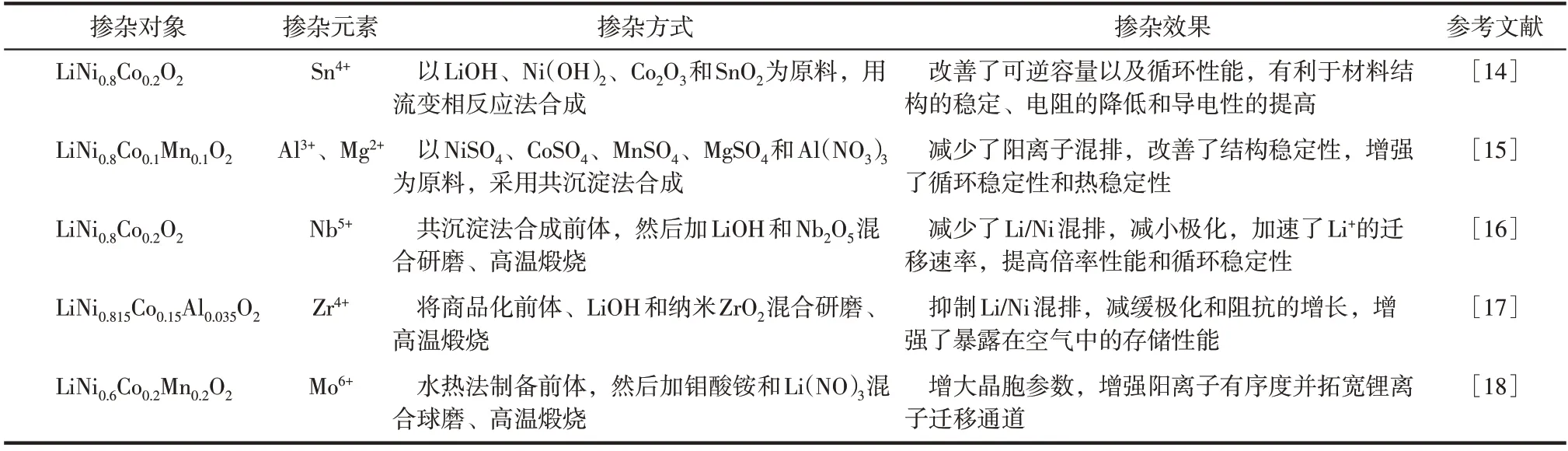
表1 掺杂元素与掺杂效果
1.2 包覆改性
富镍的锂过渡金属氧化物在循环过程中可提供高容量,但是,这种化合物在长期循环过程中显示出快速的容量衰减以及较快的阻抗上升。因此,在高荷电状态下(SOC),包覆保护层可以延长其循环寿命并改善这些富镍材料的热稳定性。另外,包覆层能够减少材料与电解液的直接接触,阻止电解液对主体材料的腐蚀,减少副反应的发生。目前在富镍锂离子正极材料上进行包覆改性的材料有Al2O3[19]、Ag[20]、ZrO2[21],Li3PO4[22]、MoS2[23]、SnO2[24]等,这些包覆材料均能改善循环稳定性和倍率性能,其包覆方式及效果总结见表2。
Jo等[25]用H3PO4对富镍的Li[Ni0.6Co0.2Mn0.2]O2进行改性。包覆的H3PO4与在表面上残留的LiOH和Li2CO3反应后,H3PO4转化为Li3PO4。由于减少了残留的LiOH 和Li2CO3,包 覆Li3PO4的Li[Ni0.6Co0.2Mn0.2]O2的容量保持率和倍率性能得到了显著的改善。通过X 射线衍射(XRD)、透射电子显微镜(TEM)和飞行时间二次离子质谱仪(TOF-SIMS)等物化测试对循环电极的进一步研究表明,Li3PO4包覆层具有多种功能:吸收电解质中的水、降低HF 含量、保护活性物质在循环过程中免受与电解质的有害副反应,从而在1000个循环后仍可保持高容量。
然而,掺杂和包覆也有一些固有的缺点。对材料进行掺杂并不能从根本上解决结构恶化的问题,同时掺杂也会降低材料比容量。包覆能够将材料颗粒包裹起来而不受电解液的侵蚀,保护了正极结构免受电解液中HF的侵蚀,因此稳定了正极界面的电荷转移电阻。然而,包覆层一般较薄(<10nm)且不均匀,如果受到HF持续的侵蚀,在长期循环过程中仍可能会损害正极表面,导致容量缓慢衰减。
2 单晶结构材料
多晶三元正极材料通常是由一次颗粒团聚形成的二次颗粒,一次颗粒的大小一般为几百纳米。随着循环次数的增加,由于二次球中的一次颗粒有着不同的晶面取向和滑移面,晶粒间晶格膨胀和收缩的各向异性导致其在循环后期可能会出现二次颗粒的破碎,并在一次颗粒间产生微裂纹,这将使材料与电解液的接触面积增大,加剧与电解液的副反应,发生严重的容量衰减[26-28]。而单晶材料的颗粒均为尺寸较大的一次颗粒,在反复循环过程中,这种结构可避免裂纹的产生,保持结构的完整性,从而提升循环稳定性。

表2 包覆材料与包覆效果
Qian等[29]通过熔融盐法合成了微米尺寸的单晶LiNi0.6Mn0.2Co0.2O2材料。结果表明,该材料通过消除内部晶界和晶间断裂,可以显著改善循环性能。此外,单晶LiNi0.6Mn0.2Co0.2O2颗粒在正常工作条件下可以保持晶粒结构的稳定,但如果过度充电则会破裂。Wang 等[30]采用水热法合成了单晶LiNi0.6Co0.2Mn0.2O2,在850℃退火后,样品结晶均匀,粒径约为800nm。样品在0.2C 条件下显示出183.7mA·h/g 的高容量,且在不同倍率下具有优异的循环稳定性,这主要可归因于单晶结构有利于Li+沿晶体的传输。Li等[31]使用两步锂化法合成单晶LiNi0.88Co0.09Al0.03O2正极材料,两步法可以抑制Li5AlO4杂质的形成而不影响颗粒的生长,适用于NCA 等含铝单晶正极材料的合成。
不过,单晶材料仍有许多缺点,因为单晶材料单个颗粒较大,使得Li+扩散更加困难,因此在相同的电压区间内充放电时,单晶材料的放电比容量通常较低,容量发挥不如多晶材料,倍率性能也较差。
3 核壳型结构改性
为了改善高镍材料的性能,对材料进行结构设计,在颗粒表面形成一层功能性壳层,引起了人们极大的兴趣。所谓的核壳材料,即富镍材料作为核提供高容量,外壳采用低镍材料在电化学循环过程中提供结构稳定性和热稳定性。研究表明,核壳结构能够有效地改善富镍材料的结构劣化问题,由低镍外壳和富镍核心组成的核-壳结构既可以规避掺杂元素的影响,还可以免去包覆的异相影响,能够实现良好的改性效果。目前合成核壳材料的方法有逐层沉积法、水热法、模板法和共沉淀法等。由于电池内部空间有限,因此需要高密度的活性材料来实现高能量密度,共沉淀法是制备高密度球形核壳结构材料的最佳方法之一[32]。
Li[Ni0.5Mn0.5]O2中Mn 的平均价态是四价,因此电化学惰性的四价Mn提供了显著的结构稳定,即使在4.6V 的高截止电压下,也能进行简单的立体定向反应,在电化学循环过程中保持六方相。由于其结构稳定性的改善,Li1-δ[Ni0.5Mn0.5]O2的放热起始温度通常高达280℃,并且在该温度下产生的热量较小。Li[Ni0.5Mn0.5]O2在结构和热稳定性方面是一种很有吸引力的材料,但容量较低(2.8~4.3V 下约150mA·h/g),限制了它在锂离子电池上的使用[32]。Sun 等[33]将富镍材料与Li[Ni0.5Mn0.5]O2结合,采用共沉淀的方法制备了富Mn 外壳包裹富Ni 核的正极材料,如图1 所示。虽然正极的容量略微降低,但电池的热稳定性和循环稳定性及容量保持率都得到了很好的改善。在3.0~4.3V 以1C 倍率进行500 次充放电循环,C/Li[Ni0.8Co0.1Mn0.1]O2电池的容量保持率为81%,循环后放电平台下降高达0.2V,这是由于活性材料的结构不稳定而降低了长期循环的稳定性。如使用Li[Ni0.8Co0.1Mn0.1]O2作为核, Li[Ni0.5Mn0.5]O2作为壳, 制得核壳材料Li[(Ni0.8Co0.1Mn0.1)0.8(Ni0.5Mn0.5)0.2]O2,则在500 次循环后的容量保持率为98%,循环过程中的电压降也更小,这是因为Li[Ni0.8Co0.1Mn0.1]O2核几乎完全被Li[Ni0.5Mn0.5]O2壳层所包围, 可以防止Li[Ni0.8Co0.1Mn0.1]O2在长期循环过程中被电解液中潜在的HF侵蚀,从而保持了循环稳定性。
Maeng 等[34]通过共沉淀法制备了以LiNi0.9Mn0.05Co0.05O2为核、LiNi0.33Mn0.33Co0.33O2为壳的核壳结构NMC811(标称成分为LiNi0.8Mn0.1Co0.1O2),并研究了一次颗粒形貌和二次颗粒结构的非均质性对颗粒力学强度的影响。随着煅烧温度从700℃升高到800℃,核壳结构NMC811 材料的初级颗粒变得更厚,在纳米压痕测试中,所有次级颗粒的破碎力都与商用均质NMC811 相似,核壳结构的NMC811的刚度和压缩应力-应变高于商用均质的NMC811。在纳米压痕测试中,所有次级颗粒的破碎力都与均质NMC811 相似,核壳结构的NMC811 的刚度和压缩应力-应变高于均质的NMC811。在200次循环的水平上,核-壳结构的NMC811 的非均质性不会削弱次级颗粒的机械强度,并且核与壳之间的结合力足够强,可以防止内部形成微裂纹。核壳结构NMC811 的初始放电容量低于均质NMC811,但与均质NMC811(39.6%的容量保持率)相比,经过200 次循环后NMC811 的循环稳定性(76.6%的容量保持率) 有了显著提高。差示扫描量热法(DSC)结果还表明,核壳结构的NMC811 的放热起始温度比均质NMC811高23℃,并且发热量减少了22.8%。这些结果表明,核壳结构NMC811 颗粒表现出良好的热稳定性、足够强的机械强度和高的容量保持率。

图1 核壳材料Li[(Ni0.8Co0.1Mn0.1)0(.8Ni0.5Mn0.5)0.2]O2[33]
4 浓度梯度型结构改性
4.1 浓度梯度壳加富镍核
尽管核壳材料有自身的优点,但核-壳结构也存在内部元素浓度梯度骤变的缺点,经过长时间的充放电循环后,由于核、壳材料体积变化的差异会引起结构失配,核与壳界面处形成了较大的空洞层,核-壳很容易剥离和破裂,导致容量突然下降,阻碍了Li+的扩散,进而损害了材料的电化学性能[35-36]。
浓度梯度壳(粒子浓度连续增加或减少)使得核壳之间浓度可以形成一个过渡,Li+得以平滑扩散,不会因为核壳界面处的体积变化而导致核壳结构失配,同时可以产生一个稳定的表面层。在电池测试中,这种材料在长时间循环中表现出高容量和优异的稳定性能,并且安全性大大提高。
Sun等[36-38]采用具有浓度梯度的壳层包裹住富镍的核,该壳层使得Li+能够平滑扩散并产生富Mn的表面层。在浓度梯度壳中,镍含量线性下降而Mn含量线性上升。相对于核壳材料,这种材料在倍率性能、容量保持率、安全性上都有所提高。Sun等[36]采 用 共 沉 淀 法,以NiSO4·6H2O、CoSO4·7H2O 和MnSO4·5H2O 为 原 料,制 备 了Li[Ni0.67Co0.15Mn0.18]O2材料,该材料由Li[Ni0.8Co0.15Mn0.05]O2核和浓度梯度壳组成,Ni、Co、Mn 的含量变化如图2 所示。首先在连续搅拌反应釜(CSTR)中通过共沉淀法合成球形核[Ni0.8Co0.15Mn0.05](OH)2颗粒。接着,将贫镍溶液(Ni∶Co∶Mn=0.05∶0.02∶0.93,摩尔比)连 续 泵 入 富 镍 溶 液(Ni∶Co∶Mn=0.8∶0.15∶0.05,摩尔比)中,同时将混合溶液泵入CSTR。控制反应釜中pH、温度和搅拌速度分别为11.0、50℃和1000r/min。在此过程中,混合溶液中金属离子的浓度随时间的变化而逐渐变化,从而在核心[Ni0.8Co0.15Mn0.05](OH)2颗粒上堆积了浓度梯度壳。将得到的浓度梯度[Ni0.67Co0.15Mn0.18](OH)2前体与适量的LiOH·H2O 充分混合,750℃下在空气中煅烧20h 得到最终材料。在55℃条件下循环至4.4V,浓度梯度Li[Ni0.67Co0.15Mn0.18]O2电极的初始容量为207mA·h/g,而常规Li[Ni0.8Co0.15Mn0.05]O2电极的初始容量为216mA·h/g,这是由于浓度梯度材料中镍含量的降低所致。在相同的循环周期内,常规Li[Ni0.8Co0.15Mn0.05]O2的容量保持率仅为79%,而浓度梯度Li[Ni0.67Co0.15Mn0.18]O2达到90%。DSC分析表明,浓度梯度Li[Ni0.67Co0.15Mn0.18]O2的热稳定性也有明显的提高。与常规Li[Ni0.8Co0.15Mn0.05]O2相比,浓度梯度Li[Ni0.67Co0.15Mn0.18]O2的电化学性能和热稳定性的提高可归因于充电后颗粒表面Mn4+含量的增加和Ni4+含量的减少。

图2 L[iNi0.67Co0.15Mn0.18]O2的电子探针显微分析(EPMA)线扫结果[36]
4.2 线性浓度梯度材料
鉴于浓度梯度壳加富镍核带来的优势,在此基础上,Sun 等[39]进一步提出了全浓度梯度材料(从粒子的中心到外层镍浓度线性下降,而锰浓度线性上升)的概念,如图3 所示。在设计合成的前体Ni0.75Co0.10Mn0.15(OH)2和终产品LiNi0.75Co0.10Mn0.15O2中,Co 的原子分数保持在约10%的恒定值,而Ni 的浓度从颗粒中心向外层持续下降,Mn 的浓度持续增加。这种全梯度材料能够利用富镍核的高能量密度和富锰外层的高热稳定性及长寿命。由图4可看出前体中Ni 和Mn 的浓度梯度大于终产品的浓度梯度,这是由于金属元素在高温煅烧过程中的定向迁移造成的。
为了制备全浓度梯度前体,将NiSO4·6H2O、CoSO4·7H2O 和MnSO4·5H2O (0.9∶0.1∶0,摩 尔比)用作共沉淀过程的起始富镍溶液。在反应过程中,将富锰溶液(Ni∶Co∶Mn=0.64∶10∶26,摩尔比)连续泵入装有起始富镍溶液的储液罐中,然后将均匀混合的溶液连续泵入反应釜中。将获得的全浓度梯度氢氧化物前体与LiOH·H2O混合,并在750℃的空气中煅烧20h 制得终产品材料。该材料具有富镍材料的高比容量和富锰材料的高稳定性,可以提供高达215mA·h/g 的比容量。该材料与MCMB组装的软包电池具有出色的循环稳定性,在1000次循环后仍有90%的容量保持率。
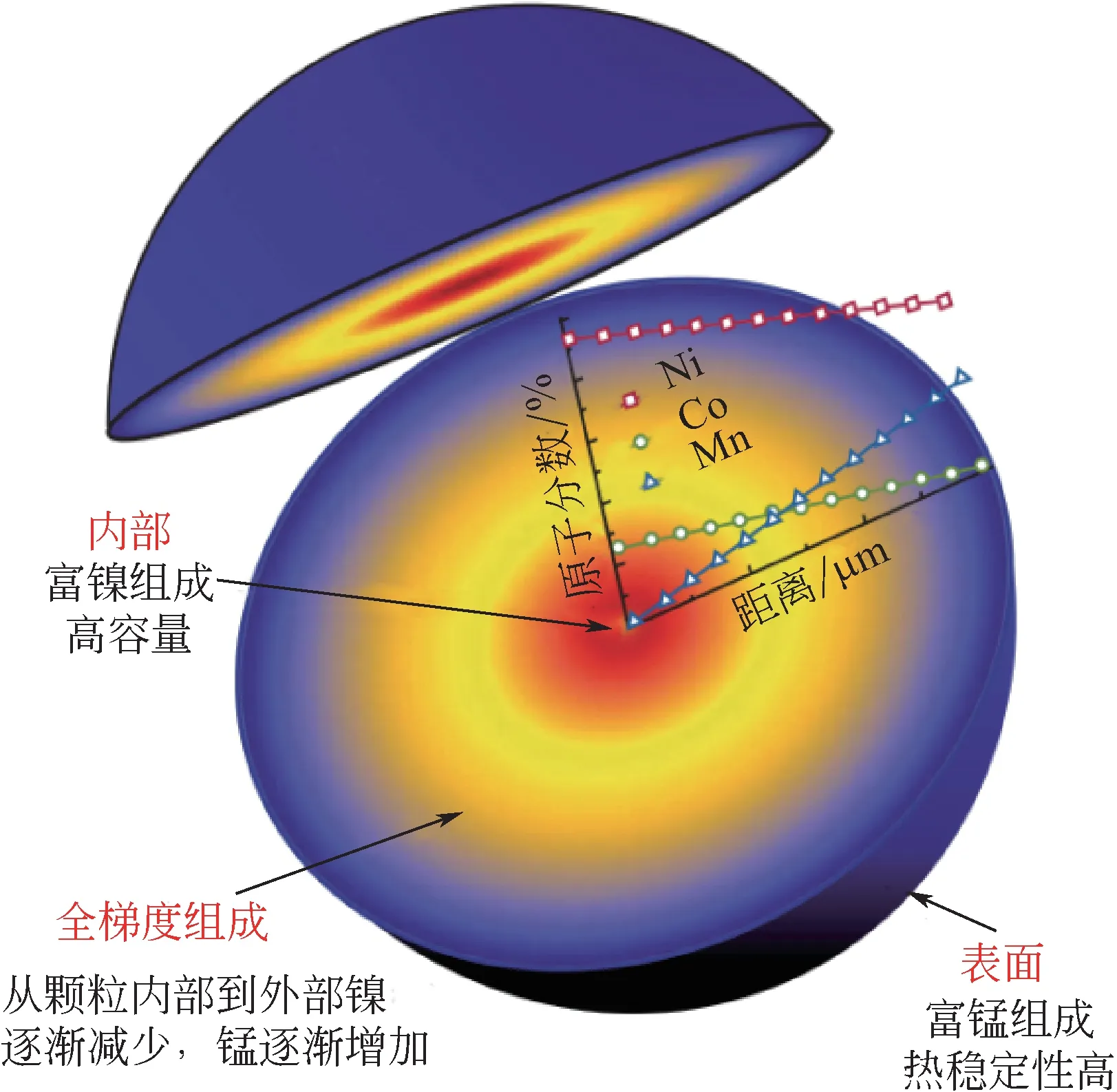
图3 LiNi0.75Co0.10Mn0.15O2颗粒的结构示意图[39]
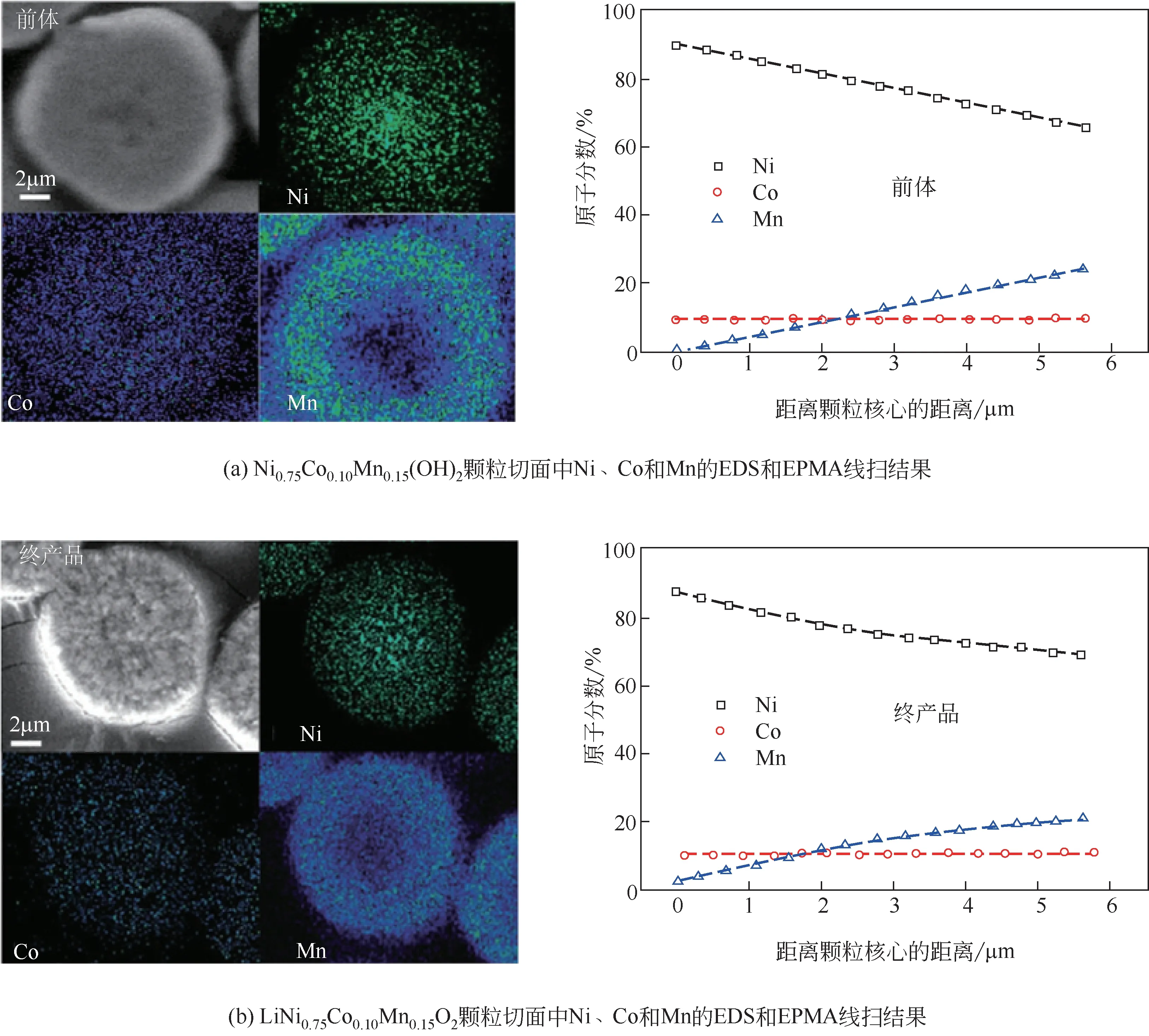
图4 LiNi0.75Co0.10Mn0.15O2的前体和终产品中各元素浓度梯度分布[39]
4.3 渐进式浓度梯度材料
线性浓度梯度材料中过渡金属的浓度从核到表面呈线性变化。与这种结构相伴而生的是,总体镍含量大幅降低到核心和表面的平均值。同时,这种结构不利于减轻Li+嵌入和脱出过程中晶格变化引起的内应力。因此,传统浓度梯度材料的可逆容量和结构稳定性还有提升的空间[40]。
由于传统浓度梯度材料存在提升的空间,研究人员[35,40-45]进一步提出了更为先进的渐进式浓度梯度材料(Ni的浓度从颗粒的中心向外层逐渐降低,而Mn 的浓度从中心向外层逐渐增加)。渐进式的浓度梯度可以显著缓解材料的内部应力,从而有效地提高微细颗粒在重复循环后的力学稳定性,最大限度地利用高容量富镍材料。

图5 浓度梯度材料LiNi0.8Co0.1Mn0.1O2合成示意图[41]
本文作者课题组[41]采用一种全新、便捷的方法来更准确地制备具有全梯度结构的LiNi0.8Co0.1Mn0.1O2,该方法将原始的三元材料盐溶液分成两股进料,这样可以准确地控制梯度合成比例。最终合成的材料是以高比容量的富镍材料为核心,并逐渐过渡到低镍富锰的外表面,而且随着不断增加的Mn含量和控制的精确度,Co 的含量也呈现缓慢的梯度变化。前体的制备过程如图5 所示。根据化学计量比称取镍、钴和锰的硫酸盐,将NiSO4·6H2O和CoSO4·7H2O溶解在去离子水中以制备盐溶液A,将MnSO4·H2O 溶解在去离子水中以制备盐溶液B。同时,分别制备氢氧化钠水溶液和氨水溶液作为沉淀剂和络合剂。在引入惰性气体的同时将A 溶液、氢氧化钠溶液和氨水通过蠕动泵加入到反应釜中,并将B溶液通过蠕动泵加入到A溶液中。通过调节氢氧化钠溶液的流速精确控制pH处于11.50,整个反应时间为36h。同时,将搅拌速度保持在800r/min。在该过程中,控制B 溶液的流速在约35h 内滴出。随着共沉淀反应的进行,进料中盐溶液中Mn2+的相对浓度逐渐增加,Ni2+和Co2+的相对浓度逐渐降低,合成了具有全梯度结构的前体。在镍和钴的盐溶液中加入锰盐溶液可以更方便、准确地调节梯度的平缓变化,使共沉淀更稳定。通过能量色散X射线光谱仪(EDX)结果可以清楚地观察到,应用这种方法制备的前体具有缓慢且平滑的梯度变化趋势。测试结果表明,前体具有88%镍含量的内核和镍含量为72%的外表面,终产品具有84%镍含量的内核和镍含量为76%的外表面,且二者之间过渡呈平滑过渡,如图6所示。电化学测试结果表明,全梯度材料能显著改善循环性能和高倍率性能,并且电流密度越大,改善越明显。在5C 倍率下经过100次循环的容量保持率高达90%,明显高于非梯度材料的71.8%。

图6 前体与终产品的浓度梯度对比[41]

图7 LiNi0.9Co0.07Mg0.03O2的设计与合成示意图[45]
Zhang 等[45]研 发 了 具 有Mg 浓 度 梯 度 的LiNi0.90Co0.07Mg0.03O2(CG-NCMg)正极材料。如图7所示,CG-NCMg 的特征是Ni 和Mg 的含量在整个微球上具有浓度梯度分布。富镍核心有助于提高容量,而富镁的外壳可增强表面稳定性。在制备Ni0.90Co0.07Mg0.03(OH)2前体过程中,贫镁、富镍核首先在氨的络合作用下形成,富镁壳随后在NaOH的作用下沉淀。由于Ni、Co 和Mg 的氢氧化物具有很大的平衡常数,因此可以通过精心调整试剂添加的顺序和反应物的浓度来实现梯度浓度。前体的具体制备过程为:在空气气氛下使用体积为10L 的连续搅拌釜式反应器(CSTR)。向CSTR 中加入2L 去离子水,温度保持在50℃。溶液A、B、C、D 和E 用于共沉淀反应。溶液A 和溶液B 分别为NaOH 水溶液(2.0mol/L)和氨水(2.0mol/L)。溶液C 是NiSO4·6H2O 和CoSO4·7H2O(摩尔比90∶7)的混合物,在去离子水中以2.0mol/L 的总浓度混合。溶液D 为去离子水,溶液E 为MgSO4溶液(0.247mol/L)。将总容积相等的B、C、D溶液以4v的最佳流量分别泵入CSTR。为保证MgSO4溶液的浓度变化,将溶液E 以v 的流速泵入D。通过控制溶液B 的流速,使CSTR 的pH 保持在10.7,反应过程中严格控制温度和搅拌速度。40h 后,通过过滤收集氢氧化物前体粉末并反复洗涤,直到滤液的pH 接近7,过滤后的粉末在110℃干燥12h。合成的浓度梯度CG-NCMg 具有均匀的粒径分布、低阳离子混合度和扩大的层间间距。与常规LiNi0.90Co0.07Mg0.03O2样品(CC-NCMg)相比,经过300 次循环后,CG-NCMg 在1C 倍率下容量保持率为93.5%,显著高于CC-NCMg(73.2%)。在5C倍率下,300 次循环后仍保留了90%以上的容量,这表明CG-NCMg 在高电流密度下具有出色的循环稳定性。DSC 分析结果表明,CG-NCMg 能明显改善热稳定性,这可以归因于表面富含的Mg 抑制了电极-电解质副反应。
蒋文全等[46]用“两步”进料方式实现进料口浓度的连续梯度变换,并根据微积分公式完成材料的浓度梯度设计。浓度梯度前体的合成采用“管道式合成”新技术,其核心装置反应釜和流量配比控制系统如图8 所示,具有3 个进料口和1 个温度计插口。制备浓度梯度前体时,确定反应体系中过渡金属离子浓度的连续性改变是整个合成过程的关键。在“管道式合成”技术基础上,对两种特定Ni/Co/Mn 摩尔比的溶液(Ni-rich 溶液和Mn-rich 溶液)进行“两步”进料:将Mn-rich溶液通过计量泵泵入到Ni-rich 溶液中,同时将Mn-rich 溶液和Ni-rich溶液的混合溶液泵入到反应釜中,以此进料方式实现进入反应釜的溶液浓度发生连续性改变(泵入反应釜中的过渡金属浓度可由微积分推导求得)。通过配制Ni-rich 和Mn-rich 溶液及控制流量和反应时间即可实现进料口过渡金属浓度大小的变换,达到目标材料所设计的梯度变化。用这种方式实现浓度梯度前体从粒子中心到表面过渡金属元素的浓度梯度变化:Ni 含量逐渐减少,Mn含量逐渐增多。

图8 通过“管道合成”氢氧化物前体的示意图[46]
“管道式合成”技术的优点在于:①通过引入副反应控制反应体系局部过饱和度,使成核与晶体生长过程彻底分开;②通过调节pH 与配位剂的配比控制副反应,抑制微小晶粒堆积,同时控制晶粒生长速率,实现晶体堆垛生长;③调整反应釜结构和搅拌电机转速营造适当的反应体系的流态,以借助离心力或向心力来控制M(OH)2(M=Ni、Co、Mn)颗粒在反应体系中足够的停留时间。用该方法合成的浓度梯度正极材料LiNi0.643Co0.055Mn0.302O2初始放电容量为187.68mA·h/g,略小于LiNi0.8Co0.1Mn0.1O2,但容量保持率明显提高,以1C倍率充放电循环200周后,LiNi0.643Co0.055Mn0.302O2的容量保持率为86.90%,而LiNi0.8Co0.1Mn0.1O2只有77.24%,循环性能的提高可归因于全浓度梯度正极材料中的富锰表面。
表3总结了以上提到的浓度梯度型结构改性的三种策略的主要控制方式及其优缺点。通过实践发现在实际生产过程中,渐进式浓度梯度方案具有工艺简单、浓度梯度可控性强的特点,在不同批次的生产中得到的材料稳定性和一致性很好,具有很好的推广应用价值。
5 结语与展望
锂离子电池正极材料是锂离子电池能量密度提高的瓶颈所在,富镍三元正极材料由于具有高比容量、性价比高等优点成为当前研究热点。如何得到高比容量的同时且能解决富镍三元材料本身稳定性差的问题是关键。掺杂有效元素能使材料的稳定性和倍率性能有所改善,但不能从根本上解决结构劣化的问题,同时掺杂也会降低材料比容量;包覆材料能短期提高材料的稳定性,但是包覆层非常薄(<10nm)且不均匀,长期受到电解液侵蚀也会溶解和脱落,同样不能从根本上解决问题;单晶材料的循环稳定性较好,但放电比容量通常较低,容量发挥不如多晶材料,倍率性能较差;核壳材料可有效改善富镍三元材料与电解液的接触问题,但在充放电过程中由于核壳材料体积变化的差异会造成核壳分离。浓度梯度材料既能很好地保持富镍材料的高容量优势,又可以通过富锰外壳在电解液中稳定存在,并且不会出现核壳分离的问题,但是如何进一步提高比容量同时保持稳定性仍将是下一步的研究重点。目前的改性材料都各有利弊,但各种制备方法都为能获得更大容量、更安全、更稳定的锂离子正极材料提供了新的思路,这将使得锂离子电池在电动汽车电动化、智能化、网联化等方面的应用能够更快地实现。

表3 浓度梯度结构材料的制备及优缺点
