重型新型冠状病毒肺炎118例临床特征分析
2021-03-25谢丹陈俊春邱婷赵川
谢丹,陈俊春,邱婷,赵川
(1.南京中医药大学附属昆山市中医医院急诊科,江苏 昆山 215300; 2.华中科技大学同济医学院附属同济医院综合医疗科,湖北 武汉 430030)
2019冠状病毒病(coronavirus disease 2019, COVID-19)仍在全球蔓延,可引起呼吸衰竭等严重呼吸道症状[1]。已证实COVID-19由一种新型冠状病毒引起,现称为重症急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2, SARS-CoV-2),最有可能来源于人畜共患病冠状病毒,如2002年出现的SARS-CoV。在第一次报告后的几个月内,SARS-CoV-2在我国和世界范围内蔓延,达到了大流行水平[2]。本科室相关医务人员在2020年2月至3月前往武汉参与救治新型COVID-19患者,在重症监护室抢救重型COVID-19患者时发现,同样是重型患者部分最终死亡,部分经治愈出院。因此,本研究拟通过回顾性分析死亡和非死亡COVID-19患者在临床特点和检验指标等方面的差异,为今后收治同样患者提供预判的可能。
1 对象与方法
1.1 研究对象
选择2020年2月至3月武汉同济医院光谷院区重症监护室COVID-19 确诊死亡患者51例作为死亡组;同时,选择同期重症监护室出院未死亡患者67例作为未死亡组。确诊病例依据国家卫健委印发《新型冠状病毒肺炎诊疗方案(试行第七版)》诊断标准执行: ① 通过采集咽拭子或痰液等分泌物标本进行SARS-CoV-2 核酸检测;② 胸部CT提示早期肺外带多发小斑片影,进行性发展为多发磨玻璃影或肺实变。本回顾性研究分析遵照赫尔辛基宣言原则进行并通过医院伦理委员会审查(批件号:KZY2020-41)。
1.2 纳入标准
1.2.1 入选标准 符合《新型冠状病毒肺炎诊疗方案(试行第七版)》临床分型为重型标准中的任何一条的成人患者,具体标准:静息状态下指氧饱和度≤93%;氧合指数PaO2/FiO2≤300 mmHg;呼吸急促(>30次/min);肺部影像显示24~48 h病灶明显进展>50%。
1.2.2 排除标准 非重型COVID-19;合并恶性肿瘤、肺结核等慢性消耗性疾病;合并新近心肌梗死和脑卒中;合并血液病或肝功能、肾功能等重要脏器功能衰竭病史;年龄<18岁;因药物过敏等原因出现意外死亡。
1.3 数据收集
1.3.1 临床基本特征 记录患者年龄、性别、吸烟史、高血压、心功能不全、糖尿病和慢性阻塞性肺疾病(COPD)等。
1.3.2 临床结局 记录患者是否发生呼吸衰竭、心力衰竭、脓毒血症、肾功能衰竭、多器官功能衰竭(MODS)、50%以上肺受累破坏等。
1.3.3 实验室检查 记录两组患者进重症监护室第1天外周血白细胞计数、中性粒细胞计数、谷草转氨酶(AST)、尿素氮、乳酸脱氢酶(LDH)、估算肾小球滤过率(eGFR)、心衰标志物N-末端B型利钠肽原(NT-proBNP)等。
1.4 统计学方法
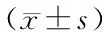
2 结果
2.1 COVID-19重症死亡患者的临床特征
死亡组和非死亡组年龄、吸烟史(>10年)和合并COPD比较差异有统计学意义(P均<0.05);性别,合并症(高血压、心功能不全、糖尿病)比较,差异无统计学意义(P均>0.05)。见表1。

表1 COVID-19死亡组和非死亡组临床病理特征差异
2.2 两组患者临床结局差异
死亡组呼吸衰竭、心力衰竭、肾功能衰竭和MODS合并症发生率明显高于非死亡组(P均<0.05);而两组患者合并脓毒血症无显著差异(P>0.05)。影像学提示,死亡组50%以上肺受累破坏(胸部CT)患者数明显高于非死亡组(P<0.05)。见表2。
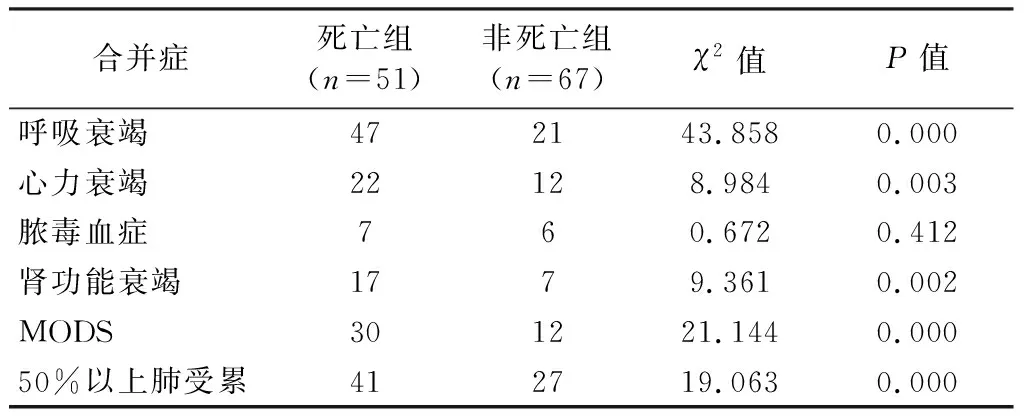
表2 COVID-19重症患者的疾病进程差异
2.3 两组患者外周血指标的差异
如表3,死亡组和非死亡组患者进重症监护室第1天外周血白细胞计数、中性粒细胞计数、AST、尿素氮、LDH、eGFR、NT-proBNP水平均存在显著差异(P<0.05)
2.4 多因素logistic回归分析
进一步采用多因素logistic回归分析显示,年龄、吸烟史>10年、呼吸衰竭、MODS、尿素氮和eGFR可作为COVID-19患者死亡预后的独立因素(P<0.05)。见表4。

表3 两组患者外周血指标差异
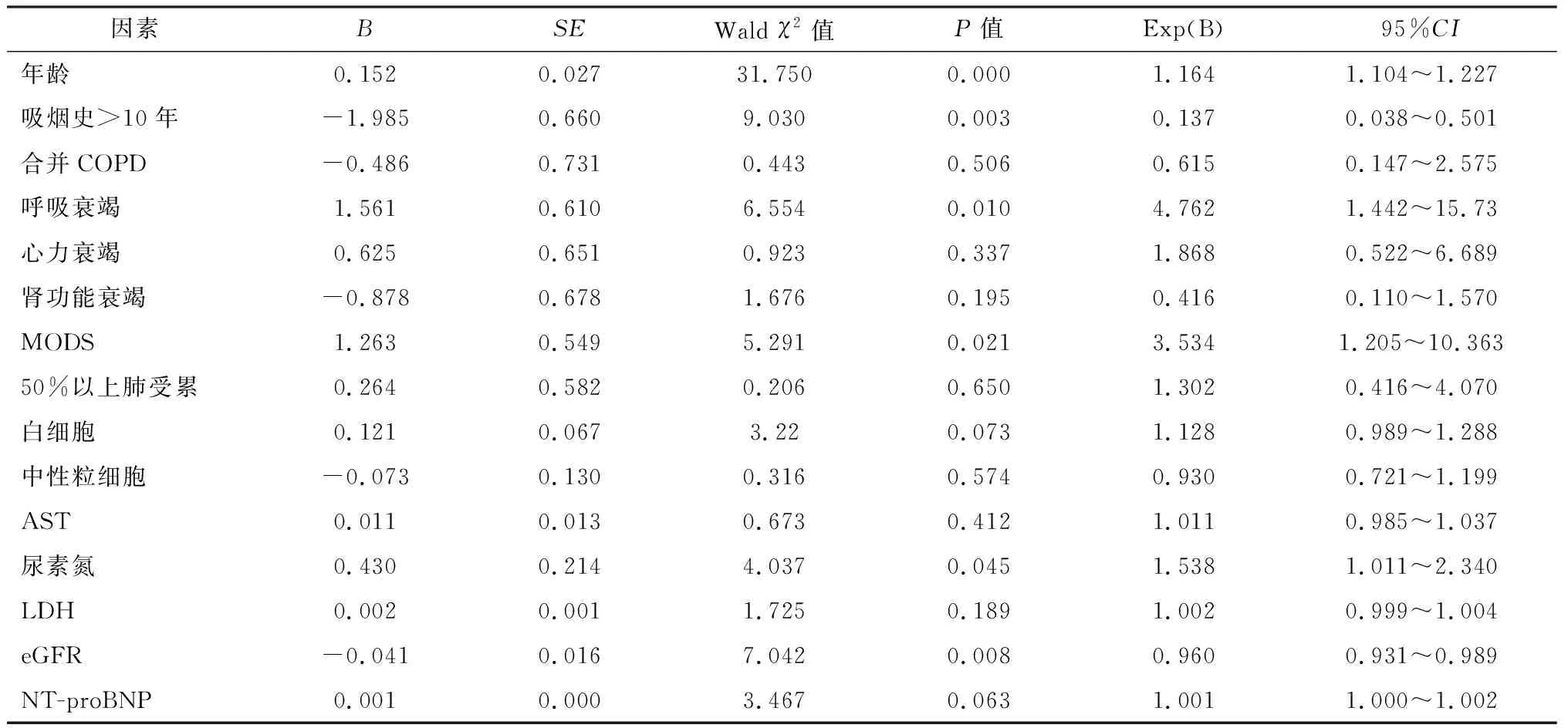
表4 多因素logistic回归分析结果
3 讨论
据报道,大多数SARS-CoV-2感染患者出现轻度症状,如干咳、喉咙痛和发烧,且大多数情况都可自行缓解[3-4]。然而,有部分患者出现各种致命的并发症,如器官衰竭、败血性休克、肺水肿、严重的肺炎和急性呼吸窘迫综合征,需要进一步的重症监护支持[5-7]。重症监护支持的重型COVID-19患者中相当一部分病情持续恶化后死亡,目前并没有明确的指标和参数能支持早期预警重症患者出现死亡的风险[8]。多项报道提示,年龄>80岁患者易出现病情加重而发展成重型COVID-19[9-10]。本研究发现,>67岁患者死亡风险增加,且与性别无关,其往往合并吸烟史、高血压、心功能不全、糖尿病和COPD;最终分析提示,合并有吸烟史>10年和COPD的重型COVID-19患者更易发生死亡。
死亡组外周血白细胞和中性粒细胞计数明显高于非死亡组,这提示外周血白细胞和中性粒细胞计数增高预示患者病情恶化,有死亡风险。同时,两组外周血AST、尿素氮、LDH、eGFR和NT-proBNP含量存在统计学差异。AST主要存在心肌、肝脏、骨骼肌和肾脏等,其上升往往提示心肌受损,或多器官功能受损;尿素氮是判断肾小球滤过功能的指标,其增高提示肾功能不全;LDH主要存在心肌、肾脏和骨骼肌中,其升高也提示相关脏器细胞受损;eGFR是用来评价肾小球滤过率的一个指标,下降提示肾功能不全;NT-proBNP是目前心衰诊疗中应用最广泛的生物标志物,其升高提示心力衰竭[11-13]。上述指标主要围绕心脏和肾两大器官,表明COVID-19死亡患者除肺部严重损害外,往往伴随显著的心、肾损害,同时,预警患者有死亡风险。
此外,并发呼吸衰竭、心功能衰竭、肾功能衰竭和MODS患者死亡风险增加,而病程中合并脓毒血症则无显著差异,推测这可能与敏感抗生素应用有关。并且,发生死亡的患者往往伴随双肺的严重损害。进一步发现,仅年龄、吸烟史>10年、呼吸衰竭、MODS、尿素氮和eGFR可作为COVID-19患者预后的独立因素。
综上所述,对重型COVID-19患者入住重症监护病房后应及时进行死亡风险评估,对于67岁以上合并有吸烟史>10年患者更要密切关注。同时,动态监测尿素氮和eGFR等指标,及时发现患者出现呼吸衰竭和MODS,对预测COVID-19死亡风险有预警意义。
